Минералокортикоиды

Минералокортико́иды, или минералокортикостеро́иды — общее собирательное название подкласса кортикостероидных гормонов коры надпочечников и их синтетических аналогов, общим свойством которых является более сильное и избирательное действие на водно-солевой, чем на углеводный обмен.
Классификация минералокортикоидов[править | править код]
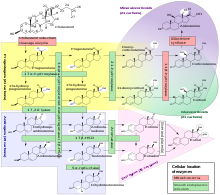
- 11-Дезоксикортикостерон → Кортикостерон → 5α-Дигидрокортикостерон1 → 3α,5α-Тетрагидрокортикостерон1
- Альдостерон → 5α-Дигидроальдостерон1 → 3α,5α-Тетрагидроальдостерон1
- 5α-Дигидродеоксикортикостерон1 → 3α,5α-Тетрагидродеоксикортикостерон1
Физиологическая роль[править | править код]
Естественные минералокортикоиды — альдостерон и дезоксикортикостерон практически не обладают глюкокортикоидной активностью. У человека альдостерон является основным, наиболее физиологически важным и наиболее активным минералокортикоидом. Но это верно не для всех видов животных — у некоторых видов роль основного минералокортикоида играет дезоксикортикостерон.
Основным глюкокортикоидом является кортизол. Без секреции кортизола при стрессе человек не смог бы выжить[1]. Он помогает поддерживать концентрацию глюкозы в крови за счёт усиления глюконеогенеза и блокирования поглощения глюкозы тканями, отличными от центральной нервной системы[2].
Синтетический аналог минералокортикоидных гормонов — флудрокортизон в отличие от естественных минералокортикоидов обладает сильной глюкокортикоидной активностью, но ещё более сильной минералокортикоидной. Поэтому в дозах, замещающих минералокортикоидную недостаточность, он практически не оказывает глюкокортикоидного действия и обычно не даёт характерных «глюкокортикоидных» побочных эффектов. Поэтому флудрокортизон, по крайней мере в рекомендуемых дозах, правомерно рассматривать именно как минералокортикоид.
Минералокортикоиды вызывают усиление канальцевой реабсорбции катионов натрия, анионов хлора и воды и одновременно усиливают канальцевую экскрецию катионов калия и повышают осмолярность тканей (способность тканей удерживать воду), способствуют переходу жидкости и натрия из сосудистого русла в ткани.
Конечным результатом действия минералокортикоидов является увеличение объёма циркулирующей крови и повышение системного артериального давления[3]. В патологических случаях гиперальдостеронизма это приводит к развитию отёков, гипернатриемии, гипокалиемии, гиперволемии, артериальной гипертензии и иногда застойной сердечной недостаточности.
Эпифиз регулирует выработку минералкортикоидов.
Механизм действия[править | править код]
Эффекты минералокортикоидов опосредованы медленными геномными механизмами через ядерные рецепторы, а также быстрыми негеномными механизмами через мембраносвязанные рецепторы и сигнальные каскады.
Геномные механизмы[править | править код]
Минералокортикоиды связываются с минералокортикоидным рецептором в клеточном цитозоле и способны свободно проникать через липидный бислой клетки. Этот тип рецептора активируется при связывании с лигандом. После того, как гормон связывается с соответствующим рецептором, новообразованный комплекс рецептор-лиганд перемещается в клеточное ядро, где он связывается со многими элементами гормонального ответа (HRE) в промоторной области генов-мишеней в ДНК.
Противоположный механизм называется трансрепрессией. Гормональный рецептор без связывания с лигандом взаимодействует с белками теплового шока и предотвращает транскрипцию целевых генов.
Альдостерон и кортизол (глюкостероид) обладают сходным сродством к минералокортикоидному рецептору; однако уровень циркулирующих глюкокортикоидов примерно в 100 раз превышает уровень минералокортикоидов. В тканях-мишенях минералокортикоидов существует фермент, предотвращающий чрезмерную стимуляцию глюкокортикоидами. Этот фермент, 11-бета-гидроксистероиддегидрогеназа II типа (белок: HSD11B2), катализирует дезактивацию глюкокортикоидов до 11-дегидрометаболитов. Известно, что лакрица является ингибитором этого фермента, и хроническое потребление может привести к состоянию, известному как псевдогиперальдостеронизм[5].
Патофизиология[править | править код]
Гиперальдостеронизм (синдром, вызванный повышенным уровнем альдостерона) обычно вызывается либо идиопатической гиперплазией надпочечников, либо аденомой надпочечников. Две основные возникающие проблемы:
- Гипертония и отеки из-за избыточного содержания Na+ и задержки воды.
- Ускоренное выведение ионов калия (K+). При крайней потере K+ возникает мышечная слабость и, в конечном итоге, паралич.
Гипоальдостеронизм (синдром, вызванный недостаточной выработкой альдостерона) приводит к солевому истощению, связанному с болезнью Аддисона, хотя классическая врожденная гиперплазия надпочечников и другие болезненные состояния также могут вызывать эту ситуацию. Острая недостаточная выработка (геморрагический адреналит) часто опасна для жизни.
Фармакология[править | править код]
Примером синтетического минералокортикоида является флудрокортизон (Флоринеф).
Важными антиминералокортикоидами являются спиронолактон и эплеренон.
Примечания[править | править код]
- ↑ Anthony W. Norman, Helen L. Henry. Chapter 10 - Adrenal Corticoids (англ.) // Hormones (Third Edition) / Anthony W. Norman, Helen L. Henry. — San Diego: Academic Press, 2015-01-01. — P. 223–238. — ISBN 978-0-12-369444-7.
- ↑ Cortisol | Definition & Function | Britannica (англ.). www.britannica.com (19 мая 2023). Дата обращения: 7 июня 2023. Архивировано 18 марта 2023 года.
- ↑ Elise P. Gómez Sánchez. 30 - Adrenocorticosteroids and Cardiovascular Regulation: Methods for Surgery and Blood Pressure Measurements (англ.) // Methods in Neurosciences / E. Ronald de Kloet, Win Sutanto. — Academic Press, 1994-01-01. — Vol. 22. — P. 496–509.
- ↑ Mikael Häggström, David Richfield. Diagram of the pathways of human steroidogenesis // WikiJournal of Medicine. — 2014. — Т. 1, вып. 1. — doi:10.15347/wjm/2014.005.
- ↑ Hesham R. Omar, Irina Komarova, Mohamed El-Ghonemi, Ahmed Fathy, Rania Rashad, Hany D. Abdelmalak, Muralidhar Reddy Yerramadha, Yaseen Ali, Engy Helal, Enrico M. Camporesi. Licorice abuse: time to send a warning message // Therapeutic Advances in Endocrinology and Metabolism. — 2012-08. — Т. 3, вып. 4. — С. 125–138. — ISSN 2042-0196. — doi:10.1177/2042018812454322.
Это заготовка статьи по медицине. Помогите Википедии, дополнив её. |
В статье не хватает ссылок на источники (см. рекомендации по поиску). |
Дальнейшее чтение[править | править код]
- Stewart P (2008): "The Adrenal Cortex " In: Kronenberg, Melmed, Polonsky, Larsen (eds.) Williams Textbook of Endocrinology (11 ed)., Saunders Elsevier, Philadelphia, pp. 445—504.
- Bennett PN and Brown MJ (2008) «Adrenal corticosteroids, antagonists, corticotropin», in Clinical Pharmacology (10ed), Churchill Livingstone Elsevier, Publ. pp. 593—607.
- Hu X, Funder JW (2006) The evolution of mineralocorticoid receptors. Mol Endocrinol. 20(7):1471-8.
- McKay L, Renoir JM, Weigel NL, Wilson EM, McDonnell DP, Cidlowski JA. (2006) International Union of Pharmacology. LXV. The pharmacology and classification of the nuclear receptor superfamily: glucocorticoid, mineralocorticoid, progesterone, and androgen receptors. Pharmacol Rev. Dec;58(4):782-97.
- Pippal JB, Fuller PJ. (2008) Structure-function relationships in the mineralocorticoid receptor. J Mol Endocrinol. 41(6):405-13.