Полимеризация

Полимериза́ция (др.-греч. πολυμερής — состоящий из многих частей) — процесс образования высокомолекулярного вещества (полимера) путём многократного присоединения молекул низкомолекулярного вещества (мономера, олигомера) к активным центрам в растущей молекуле полимера. Молекула мономера, входящая в состав полимера, образует так называемое мономерное (структурное) звено. Элементный состав (молекулярные формулы) мономера и полимера приблизительно одинаков.
Обычно мономерами являются соединения, содержащие кратные связи либо циклические фрагменты, способные раскрываться и образовывать новые связи с другими молекулами, обеспечивая рост цепей[1].
Вероятность образования молекулы полимера[2][править | править код]
Процесс полимеризации состоит в том, что к звену-мономеру присоединяется такой же мономер, к этому звену — ещё один такой же мономер и так далее. Можно рассматривать данный процесс как случайное событие: присоединение происходит с некоторой вероятностью и, следовательно, не происходит с вероятностью , так как сумма вероятностей противоположных событий равна единице [следствие теоремы сложения вероятностей двух несовместных событий]. Поскольку каждое следующее присоединение происходит независимо от предыдущих, то вероятность образования молекулы, содержащей мономеров, вычисляется по формуле
Классификация[править | править код]
В основу классификации полимеризации могут быть положены различные признаки. Если в полимеризации участвует только один мономер, то такая полимеризация называется гомополимеризацией; если же в реакции участвуют два и более мономеров, то это сополимеризация[1].
Рост полимерной цепи в ходе полимеризации осуществляется благодаря присоединению молекул мономера к активному центру на растущей цепи. Если этот центр является радикальным, то это радикальная полимеризация. В ионной полимеризации активными центрами являются ионы или поляризованные молекулы. Ионная полимеризация дополнительно подразделяется на катионную и анионную. Дополнительно выделяют стереоспецифическую полимеризацию, при которой происходит образование полимеров с упорядоченной пространственной структурой[1].
Полимеризация может осуществляться в системах с разным агрегатным состоянием. По этому признаку выделяют блочную полимеризацию, полимеризацию в растворе, эмульсионную или суспензионную полимеризацию (в дисперсных системах), газофазную полимеризацию и твердофазную полимеризацию[1].
С точки зрения структуры области, в которой сосредоточены активные центры, различают объемную полимеризацию (полимеризация протекает во всем объёме мономера); фронтальную полимеризацию (происходит в узком фронте, распространяющемся в среде мономера); эмульсионную полимеризацию (происходит на поверхности высоко-диспергированных частиц мономера в эмульсии).
Ступенчатая и цепная полимеризация[править | править код]

Различают два механизма полимеризации: ступенчатую полимеризацию и цепную полимеризацию. Отличие состоит в том, что при ступенчатой полимеризации реакция происходит между любыми двумя молекулами мономера, а макроцепь, соответственно, строится через стадии образования устойчивых димеров, тримеров и т. д. В цепной же полимеризации рост цепи происходит только в результате реакции мономера с активным центром на конце растущей цепи. Полимеризация одного и того же мономера может протекать по обоим механизмам, но, как правило, полимеры, полученные в результате цепной полимеризации, имеют более высокую молекулярную массу[3].
В ступенчатой полимеризации макроцепь на протяжении долгого времени растёт медленно. Вначале мономеры превращаются в димеры, димеры — в тримеры, тримеры — в тетрамеры и т. д., пока крупные олигомеры не начнут реагировать между собой — на этой стадии начинается быстрый рост макроцепи. Ступенчатые полимеризации протекают на протяжении часов. В цепной полимеризации отдельные молекулы мономера быстро друг за другом присоединяются к активному центру на макроцепи, поэтому, как только активный центр образовался, рост цепи происходит быстро. Когда рост цепи останавливается в результате какой-либо реакции обрыва цепи, эта цепь перестаёт участвовать в полимеризации. При таком механизме образование полимера происходит гораздо быстрее[3].
Ещё одним отличием ступенчатого и цепного механизма является учёт молекул мономера при расчёте средней молекулярной массы полимера. В цепной полимеризации молекулы мономера сильно отличаются от полимера и не учитываются в расчётах. В ступенчатой полимеризации большинство молекул мономера находится в составе олигомеров, а олигомеры сложнее отличить от полимеров, поэтому они учитываются при определении средней молекулярной массы[3].
В русскоязычной литературе под полимеризацией имеют в виду, как правило, именно цепную полимеризацию[1]. ИЮПАК же рекомендует выделять четыре вида полимеризации:
- цепную полимеризацию;
- конденсационную цепную полимеризацию;
- поликонденсацию;
- и полиприсоединение[3].
Механизм цепной полимеризации[править | править код]
В общем виде цепную полимеризацию можно представить как реакцию разложения инициатора (I) и дальнейший рост цепи путём присоединения молекул мономера (М) к растущей цепи[4].
Активный центр на растущей цепи может быть радикальным, катионным и анионным. Соответственно, цепная полимеризация делится на радикальную, катионную и анионную. Обычно мономеры, содержащие двойную С=С-связь, легко полимеризуются в ходе радикальной полимеризации. Применение катионной и анионной полимеризации зависит от структуры мономера. Если он содержит электронодонорную группу при двойной связи, то он может образовывать устойчивые карбокатионы и, соответственно, может полимеризоваться под действием катионного инициатора. Напротив, мономеры, содержащие акцепторные группы, способны образовывать устойчивые анионы и полимеризоваться в условиях анионной полимеризации[4].
Механизм цепной полимеризации обычно включает в себя четыре основные стадии:
- инициирование — зарождение активных центров полимеризации;
- рост (продолжение) цепи — процесс последовательного присоединения молекул мономеров к центрам;
- обрыв цепи — гибель активных центров;
- передача цепи — переход активного центра на другую молекулу[1].
Инициирование[править | править код]

В случае радикальной полимеризации выделяют несколько способов генерирования радикалов в среде мономера. Наиболее часто применяется термическое разложение инициатора: в смесь в количестве < 1 мас. % добавляют азосоединение либо пероксид. Это соединение при нагревании разлагается и образует радикалы, которые служат активными центрами[5].
Иногда радикалы генерируют в ходе окислительно-восстановительной реакции, что позволяет проводить инициирование при более низкой температуре (0-50 °С). Облучение смеси ультрафиолетовым светом, бомбардировка электронами либо использование γ-излучения позволяет создавать радикалы в смеси и без инициаторов. Так, например, радиационный процесс инициирования имеет нулевую энергию активации, поэтому его можно применять как при высоких, так и при низких температурах. Некоторые мономеры при нагревании сами дают радикалы. Например, стирол или метилметакрилат можно полимеризовать без использования инициатора[5].

Завершается стадия инициирования присоединением первичного радикала по двойной связи. В большинстве реакций полимеризации это более быстрая стадия, чем процесс разложения инициатора. Иногда наблюдается низкая эффективность инициатора. Это связано с рекомбинацией образовавшихся первичных радикалов: в течение 10-10-10-9 с после образования они находятся близко друг к другу в окружении молекул растворителя и мономера (эффект клетки). Поскольку радикалы вступают в реакции очень быстро и не всегда успевают диффундировать друг от друга, есть определённая вероятность того, что они прореагируют друг с другом. Такой процесс уменьшает число радикалов в смеси и не приводит к образованию растущих цепей полимера. Такие инициаторы, как азосоединения, разлагаются с выделением азота, поэтому рекомбинация радикалов приводит не к тому же инициатору, а к другой, более устойчивой молекуле, которая не может генерировать радикалы. Также эффективность инициатора уменьшается при повышении вязкости реакционной смеси. Поскольку в ходе полимеризации вязкость увеличивается, диффузия радикалов может значительно усложниться, из-за чего реакция не дойдёт до полной конверсии[5].
Рост цепи[править | править код]

В ходе роста цепи происходит реакция молекул мономера с радикальным центром на конце растущей цепи полимера. Обычно такими мономерами являются монозамещённые либо 1,1-дизамещённые этилены. Желательно, чтобы у 1,1-дизамещённых этиленов вида CH2=CXY заместители X и Y были не очень объёмными, поскольку в таком случае рост цепи становится пространственно затруднительным. Также сложными для полимеризации считаются 1,2-дизамещённые этилены, так как их подход к макроцепи также пространственно затруднён (хотя они хорошо вводятся в состав сополимеров)[6].
Обычно влияние стерических и электронных эффектов приводит к тому, что мономеры винильного типа присоединяются, как голова к хвосту. Исключение составляют небольшие заместители, которые не имеют сильных электронных эффектов: в этом случае может наблюдаться полимеризация голова к голове. Например, для поливинилфторида доля диад голова к голове составляет около 16 %[6].
Полимеры, получаемые радикальной полимеризацией, чаще всего являются атактическими, хотя может наблюдаться небольшое преобладание синдиотактического расположения боковых групп над изотактическим, что объясняется стерическим или электронным отталкиванием этих групп. В случае поливинилхлорида доля синдиотактических диад при −78 °С составляет 0,67, а при увеличении температуры полимеризации до 120 °С их доля уменьшается до 0,51. Для полиметилметакрилата эта доля равна 0,86 при −40 °С и 0,64 при 250 °С. Этот эффект связывают с тепловым движением[6].
В обычных условиях синтеза полимера рост цепи можно считать необратимым, однако при определённой высокой температуре существенную скорость приобретает обратный процесс деполимеризации. Эта температура не является постоянной величиной: она является функцией концентрации мономера[6].
Теоретически константа скорости роста цепи должна уменьшаться с ростом цепи, однако экспериментальные данные показывают, что после того, как цепь наросла более чем на 5 звеньев, скорость роста цепи практически не зависит от её длины. Эти результаты наблюдаются для многих полимеров различных типов. Следовательно, при получении полимеров с высокой степенью полимеризации длиной цепи в кинетических расчётах можно пренебречь[6].
Обрыв цепи[править | править код]

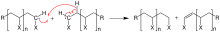
Обрыв цепи в радикальной полимеризации может происходить либо путём рекомбинации, либо путём диспропорционирования. Во втором случае на конце макроцепи образуется двойная связь. Однако эта связь неактивна в полимеризации, поскольку доля двойных связей в молекулах мономера существенно выше, чем доля концевых связей в оборванных макроцепях. Соотношение этих двух путей обрыва цепи зависит от типа мономера и температуры полимеризации. Например, в случае метилметакрилата при низкой температуре существенную роль играют оба процесса, а при высокой температуре основным путём является диспропорционирование[7].
Передача цепи[править | править код]
В процессе цепной полимеризации может произойти перенос активного центра на низкомолекулярное вещество: инициатор, мономер, растворитель, примесь и т. д. Такие процессы останавливают рост макроцепи, однако суммарное число радикалов в системе не уменьшается, поэтому скорость полимеризации или скорость расходования мономера остаются на том же уровне[8].
Вторая реакция представляет собой присоединение молекулы мономера к перенесённому радикалу. Если скорость этой реакции практически равна нулю, это означает, что радикал X* устойчив. В этом случае Х называют ингибитором полимеризации. Если константа скорости этой реакции ниже, чем константа скорости роста цепи, то Х является замедлителем[8].
Термодинамика и кинетика полимеризации[править | править код]
Реакции полимеризации протекают с уменьшением энтропии (ΔS° < 0), поскольку молекулы мономера, объединяясь в макроцепь, теряют степени свободы. Также в большинстве случаев реакции полимеризации экзотермические. Поскольку теплота выделяется, энергия системы понижается, а энтальпия реакции является отрицательной (ΔH° < 0). В этом случае свободная энергия Гиббса в ходе реакции убывает[1].
В соответствии с этим уравнением, выше некоторой предельной температуры изменение энергии Гиббса приобретает положительное значение. Следовательно, реакция полимеризации становится термодинамически запрещённой, и начинается обратный процесс деполимеризации. Например, для стирола эта температура равна 330 °С, однако для некоторых других полимеров она довольна низкая[1].
Кинетические уравнения различаются в зависимости от конкретных процессов. Сложность с их выведением заключается в том, что необходимо учитывать множество реакций, протекающих одновременно. Упростить ситуацию помогают некоторые допущения, которые обычно принимаются при расчётах[9].
- Все константы скорости считаются независящими от длины цепи.
- Считается, что количество мономера убывает только за счёт реакций роста цепи. Соответственно, скорость расходования мономера приравнивается к скорости роста цепи.
- Радикалы, образующиеся в результате переноса цепи, быстро удлиняются за счёт реакции с мономером и не влияют на скорость полимеризации.
- Для поиска концентрации радикалов применяют принцип стационарности, полагая, что эта концентрация постоянна, а скорости образования и расходования радикалов одинаковы[9].
Технологические процессы[править | править код]
В промышленности полимеризацию проводят четырьмя основными методами: выделяют объёмную полимеризацию, полимеризацию в растворе, суспензионную полимеризацию и эмульсионную полимеризацию[10].
Наиболее широко используется объёмная полимеризация (особенно, если конечный полимер представляет собой твёрдую массу). Это связано с тем, что такой метод позволяет получить полимер с минимальным количеством примесей. К его недостаткам можно отнести проблемы с перемешиванием реакционной массы, теплоотводом, прокачкой по коммуникациям и т. д., которые возникают из-за высокой вязкости. Стенки реактора и приборы для перемешивания загрязняются из-за высокой адгезии смеси к ним[10].
Остальные методы позволяют избежать указанных проблем либо применяются в тех случаях, когда конечный продукт имеет вид раствора, суспензии или эмульсии. Так, при полимеризации в растворе реакционная смесь имеет более низкую вязкость, из-за чего реактор меньше загрязняется и исчезают проблемы с перемешиванием. С другой стороны, такой процесс имеет более низкую эффективность, требует дополнительной стадии выделения полимера. Также могут существовать проблемы с огнеопасностью и токсичностью используемого растворителя[10].
В суспензионной полимеризации также используется реакционная смесь с низкой вязкостью, в которой теплоперенос осуществляется более эффективно, чем в объёмной полимеризации. Однако этот процесс также менее эффективен; его нельзя провести в непрерывном режиме (крупнотоннажных непрерывных суспензионных полимеризаций пока не разработано). Также требуются дополнительные затраты на обработку отходов воды[10].
Эмульсионная полимеризация позволяет получать продукты, имеющие конечную форму эмульсии (латекс). Она имеет те же преимущества (низкую вязкость смеси и хороший теплоперенос), а её недостатки связаны с дорогостоящим процессом выделения полимера и присутствием дополнительной примеси — эмульгатора[10].
Исторические данные[править | править код]
Полимеризация была открыта ещё в середине XIX века, практически одновременно с выделением первых способных к полимеризации мономеров (стирола, изопрена, винилхлорида, метакриловой кислоты и др.). Однако суть полимеризации как цепного процесса образования истинных химических связей между молекулами мономера была понята лишь в 20—30-е гг. XX века благодаря работам Г. Штаудингера, С. В. Лебедева, Б. В. Бызова, К. Циглера. В 1922 году химик Штаудингер доказал, что полимеры представляют собой соединения, состоящие из больших молекул, атомы которых связаны между собой ковалентными связями.
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 8 Химическая энциклопедия, 1992.
- ↑ Баврин И. И. Глава I. Случайные события и вероятности: §1.4. Случайные события в физике, химии, биологии // Теория вероятностей и математическая статистика: Учебник / И. И. Баврин. — М.: Высшая школа, 2005. — С. 24. — 160 с. — 3000 экз. — ISBN 5-06-005322-9, ББК 22.17, УДК 519.2.
- ↑ 1 2 3 4 Ullmann, 2015, p. 2–3.
- ↑ 1 2 Ullmann, 2015, p. 7–8.
- ↑ 1 2 3 Ullmann, 2015, p. 9–10.
- ↑ 1 2 3 4 5 Ullmann, 2015, p. 10–11.
- ↑ Ullmann, 2015, p. 11–12.
- ↑ 1 2 Ullmann, 2015, p. 8, 13.
- ↑ 1 2 Ullmann, 2015, p. 13–15.
- ↑ 1 2 3 4 5 Ullmann2, 2015, p. 12–13.
Литература[править | править код]
- Арест-Якубович А. А. Галогензамещенные углеводородов // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди — Полимерные. — С. 637–638. — 639 с. — 48 000 экз. — ISBN 5-85270-039-8.
- Tobita H. Polymerization Processes, 1. Fundamentals (англ.) // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2015. — doi:10.1002/14356007.a21_305.pub3.
- Tobita H., Hamielec A. E. Polymerization Processes, 2. Modeling of Processes and Reactors (англ.) // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2015. — doi:10.1002/14356007.o21_o01.pub2.




![{\displaystyle {\mathsf {R_{in}^{*}{\xrightarrow[{}]{+M}}R_{1}^{*}{\xrightarrow[{}]{+M}}R_{2}^{*}{\xrightarrow[{}]{+M}}R_{3}^{*}{\xrightarrow[{}]{+M}}...}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1b30d761400ceb2c7bce8ec891c08e318592acd7)



