Правило Каши
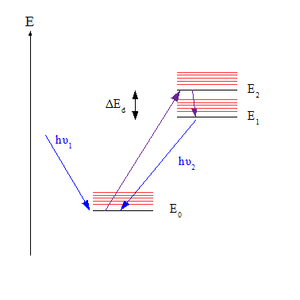
Правило Каши — эмпирическое правило в фотохимии, согласно которому для органических молекул в конденсированной фазе (в кристалле, стекле или жидкости, а также в растворе) излучение фотона (люминесценция) всегда происходит с низшего возбуждённого уровня данной мультиплетности. Названо в честь американского спектроскописта и химика Майкла Каши, который предложил это правило в 1950 году[1][2].
Суть и механизм действия[править | править код]
Данное правило применимо к спектрам излучения молекул, находящихся в возбуждённом состоянии. Поглощая фотон, электрон, находящийся на основном энергетическом уровне (обозначается как S0 в случае синглетного состояния) может, в зависимости от длины волны поглощённого кванта света, возбудиться и перейти на один из более высоких энергетических уровней (обозначаются как Sn, где n>0). Однако, согласно правилу Каши, испускание фотона (в случае S уровня обозначаемое как флуоресценция) может происходить только с самого низкого возбуждённого энергетического уровня S1. Поскольку в процессе флуоресценции участвует всего один энергетический уровень, то данное правило может быть переформулировано в эквивалентное утверждение, что форма спектра флуоресценции не зависит от длины волны возбуждающего света[3].
Таким образом, при излучении без изменения мультиплетности (флуоресценция) можно наблюдать только переход S1 → S0, а при излучении с изменением мультиплетности (фосфоресценция) — лишь T1 → S0 (квинтеты, септеты и высшие состояния, как правило, не рассматриваются, так как существует очень мало случаев, где их вообще можно наблюдать в конденсированной фазе, в отличие от газовой[К 1]). При этом обратный процесс — поглощение света — может происходить как переход к любому возбужденному состоянию. Это правило не имеет теоретического обоснования и просто отображает тот факт, что скорость безызлучательных переходов с высоких энергетических уровней (S2, S3 T2, T3) на самый низкий колебательный подуровень (колебательное квантовое число v = 0) состояний S1 или T1 настолько велика по сравнению со скоростью излучательных переходов из этих верхних состояний, что излучение происходит только с нижнего колебательного подуровня электронных энергетических уровней S1 или T1.
Механизм правила объясняется принципом Франка — Кондона для колебательных переходов. Для пары энергетических уровней с разными колебательным и электронным квантовыми числами фактор Франка-Кондона определяет степень перекрывания волновых функций. Чем больше степень перекрывания, тем быстрее молекула может перейти из возбуждённого в не возбуждённое состояние. Перекрывание между парой уровней максимально, когда колебательные уровни близки по своим энергиям. Такое происходит при переходе между двумя бесколебательными уровнями (их квантовое колебательное число v равно нулю). В большинстве молекул, бесколебательные подуровни энергетических уровней расположены близко друг к другу, так что возбуждённая молекула быстро переходит на самый низкий возбуждённый уровень S1, теряя энергию путём внутренней конверсии, до того как у него появится возможность осуществить флуоресценцию. Однако, разность энергий между S1 и S0 значительно больше, так что у молекулы появляется время на осуществление флуоресценции[4][5].
Из правила Каши существуют несколько исключений. Нарушения правила наблюдается, когда между двумя уровнями есть большой энергетический зазор. В качестве примера можно привести азулен: в классической версии объяснения этого феномена говорится о том, что уровни S1 и S2 расположены достаточно далеко друг от друга, так что здесь оказывается возможной флуоресценция. В результате большая часть флуоресценции происходит с S2 уровня[4][5]. Однако, новые исследования ставят под сомнение такое объяснение. Согласно новым данным, большая часть флуоресценции происходит с S2 потому, что структура S1 и S0 уровней отличается от таковой в обычных молекулах, в результате чего электрон может быстро переходить с S1 на S0 уровень, теряя энергию безызлучательным способом через внутреннюю конверсию.
Закон Вавилова[править | править код]
Как следствие из правила Каши можно рассматривать закон Вавилова, который гласит, что квантовый выход люминесценции в целом не зависит от длины волны возбуждающего света вплоть до некоторой предельной длины волны[4][6]. Такое поведение есть следствие указываемой правилом Каши тенденции для возбуждённых молекул переходить в исходное состояние преимущественно безызлучательным способом. Из этого правила также есть исключения, например, пары бензола[4].
См. также[править | править код]
Примечания[править | править код]
- ↑ Characterization of Electronic Transitions in Complex Molecules Архивировано 23 июля 2008 года.. Kasha, M. Discussions of the Faraday Society, 1950, 9: p.14-19.
- ↑ IUPAC. Kasha rule — Compendium of Chemical Terminology, 2nd ed. (the «Gold Book») Архивная копия от 25 мая 2015 на Wayback Machine. Compiled by McNaught, A.D. and Wilkinson, A. Blackwell Scientific Publications, Oxford, 1997.
- ↑ «Unusual autofluorescence characteristic of cultured red-rain cells» Архивная копия от 3 марта 2016 на Wayback Machine. Louis, J. and Kumar, A.S. Presented in SPIE Conference 7097, Aug 2008.
- ↑ 1 2 3 4 Photochemistry of Organic Compounds: From Concepts to Practice Архивная копия от 19 января 2018 на Wayback Machine. Klán, P. and Wirz, J. Wiley-Blackwell, 2009. p.40. ISBN 1-4051-6173-6.
- ↑ 1 2 Chemistry and Light. Suppan, P. Royal Society of Chemistry, 1994. p.56. ISBN 0-85186-814-2.
- ↑ IUPAC. Kasha–Vavilov rule – Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") Архивная копия от 21 марта 2012 на Wayback Machine. Compiled by McNaught, A.D. and Wilkinson, A. Blackwell Scientific Publications, Oxford, 1997.
Литература[править | править код]
- Н. Турро. Молекулярная фотохимия. Москва: Мир, 1967, с. 66.
- С. Мак-Глинн, Т. Адзуми, М. Киносита. Молекулярная спектроскопия триплетного состояния. Москва: Мир, 1972, с. 17–19.
Комментарии[править | править код]
- ↑ Последовательность мультиплетов для обычных молекул — нечетная (синглет, триплет, квинтет), для молекул с неспаренным электроном (радикалов) — парная (дуплет, квартет, секстет).





