Углеводный обмен
Углеводный обмен, или метаболизм углеводов в организмах животных и человека. Метаболизм углеводов в организме человека состоит из следующих процессов:
- Расщепление в пищеварительном тракте поступающих с пищей поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов из кишечника в кровь.
- Синтез и распад гликогена в тканях (гликогенез и гликогенолиз), прежде всего в печени.
- Гликолиз — распад глюкозы. Первоначально под этим термином обозначали только анаэробное брожение, которое завершается образованием молочной кислоты (лактата) или этанола и углекислого газа. В настоящее время понятие «гликолиз» используется более широко для описания распада глюкозы, проходящего через образование глюкозо-6-фосфата, фруктозо-1,6-дифосфата и пирувата как в отсутствие, так и в присутствии кислорода. В последнем случае употребляется термин «аэробный гликолиз», в отличие от «анаэробного гликолиза», завершающегося образованием молочной кислоты или лактата.
- Анаэробный путь прямого окисления глюкозы или, как его называют, пентозофосфатный путь (пентозный цикл).
- Взаимопревращение гексоз.
- Анаэробный метаболизм пирувата. Этот процесс выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза — пирувата.
- Глюконеогенез — образование углеводов из неуглеводных продуктов (пирувата, лактата, глицерина, аминокислот, липидов, белков и т. д.).
Краткие сведения об углеводах[править | править код]
Углеводы входят в состав живых организмов и вместе с белками, липидами и нуклеиновыми кислотами определяют специфичность их строения и функционирования. К углеводам относят соединения, обладающие разнообразными и зачастую сильно отличающимися функциями. Углеводы участвуют во многих метаболических процессах, но прежде всего они являются основными поставщиками энергии. На долю углеводов приходится примерно 75 % массы пищевого суточного рациона и более 50 % от суточного количества необходимых калорий. Однако неправильно сводить функцию углеводов только к энергетическому обеспечению процессов жизнедеятельности организма. Также углеводы играют и структурную роль. Так, в виде гликозаминогликанов углеводы входят в состав межклеточного матрикса. Большое число белков (ферменты, белки-транспортёры, белки-рецепторы, гормоны) — гликопротеины, углеводная составляющая которых повышает их специфичность. Например, различия в строении олигосахаридных фрагментов клеточной оболочки эритроцитов обеспечивают групповую принадлежность крови. Из углеводов в процессе метаболизма образуется большое число органических соединений, которые служат исходными субстратами для синтеза липидов, аминокислот, нуклеотидов. Производные углеводов — глюкурониды — участвуют в детоксикации ксенобиотиков и инактивации веществ эндогенного происхождения[1]. Углеводы могут быть синтезированы в организме с использованием других метаболитов: некоторых аминокислот, глицерина, молочной кислоты. Углеводы нельзя считать незаменимыми компонентами пищи. Однако если исключить углеводы из диеты, то следствием может быть гипогликемия, для компенсации которой будут расходоваться белки и липиды. Таким образом, углеводы — обязательные пищевые компоненты, потому что помимо их основной энергетической функции (клеточные «дрова») углеводы участвуют во многих метаболических клеточных процессах[2].
- Углеводы, потребляемые с пищей
-
Лактоза или молочный сахар, впервые была обнаружена в коровьем молоке, откуда и получила своё название.
-
Глюкоза, наиболее распространённый моносахарид, источник энергии в организме человека.
-
Амилопектин — разветвлённая форма крахмала.
-
Мальтоза или солодовый сахар, входит в состав семян зерновых культур (ячменя, ржи, пшеницы итд.).
-
Фруктоза или плодовый сахар.
-
Сахароза — один из самых потребляемых углеводов в мире.
Переваривание и всасывание углеводов[править | править код]
Пищеварение углеводов можно разделить на несколько этапов:
- Пищеварение, происходящее в полости рта
- Пищеварение в желудке
- Пищеварение и всасывание в тонком кишечнике.
Эпителиальные клетки кишечника способны всасывать только моносахариды. Поэтому процесс переваривания заключается в ферментативном гидролизе гликозидных связей в углеводах, имеющее олиго- или полисахаридное строение.
Переваривание углеводов в полости рта[править | править код]
В полости рта начинается расщепление крахмала (и гликогена) под действием фермента слюны — амилазы. Известны 3 вида амилаз, которые различаются главным образом по конечным продуктам их ферментативного действия:
- α-амилаза
- β-амилаза
- γ-амилаза
α-Амилаза (КФ 3.2.1.1) расщепляет в полисахаридах внутренние α-1,4-связи, поэтому её иногда называют эндоамилазой. Молекула α-амилазы содержит в своих активных центрах ионы Ca2+ необходимые для ферментативной активности. Кроме того, характерной особенностью α-амилазы животного происхождения является способность активироваться одновалентными анионами. Прежде всего Сl-.

Слюнная α-амилаза представляет собой смесь близких электрофоретически разделяемых изоферментов. Каждый из них — одноцепочечный полипептид (мол. масса 56000 Да), к которому присоединён олигосахарид. Структура этого олигосахарида, а также число его молекул на одну молекулу белка и способ прикрепления к белку неизвестны. Удивительно, что не существует соответствующих ферментов в слюне некоторых приматов, например у бабуинов или резусов.
В ротовой полости не может происходить полное расщепление крахмала, так как действие фермента на крахмал кратковременно. Кроме того, амилаза слюны не расщепляет α-1,6-гликозидные связи (связи в местах разветвлений), поэтому крахмал переваривается лишь частично с образованием крупных фрагментов — декстринов и небольшого количества мальтозы. Амилаза слюны не гидролизует гликозидные связи в дисахаридах.
Под действием β-амилазы от крахмала отщепляется дисахарид мальтоза, то есть β-амилаза является экзоамилазой. Она обнаружена у высших растений где играет важную роль в мобилизации резервного (запасного) крахмала.
γ-Амилаза отщепляет один за другим глюкозные остатки от конца полигликозидной цепочки. Различают 2 вида γ-амилаз: кислые и нейтральные, в зависимости от того в какой области pH они проявляют максимальную активность. В органах и тканях человека и млекопитающих кислая γ-амилаза локализована в лизосомах, а нейтральная — в микросомах и гиалоплазме. Амилаза слюны является α-амилазой. Под влиянием этого фермента происходят первые фазы распада крахмала (или гликогена) с образованием декстринов (в небольшом количестве образуется и мальтоза). Затем пища смешанная со слюной попадает в желудок.
Желудочный сок не содержит ферментов расщепляющие сложные углеводы (например целлюлозу). В желудке действие α-амилазы слюны прекращается так как желудочное содержимое имеет очень кислую среду (pH 1,5 — 2,5). Однако в более глубоких слоях пищевого комка, куда не сразу проникает желудочный сок, действие амилазы некоторое время продолжается и происходит расщепление полисахаридов с образованием декстринов и мальтозы. Наиболее важная фаза распада крахмала (или гликогена) протекает в двенадцатиперстной кишке под действием α-амилазы поджелудочного сока. Здесь pH возрастает до нейтральных значений, при этих условиях α-амилаза панкреатического сока обладает почти максимальной активностью. Этот фермент завершает превращение крахмала и гликогена в мальтозу, начатое амилазой слюны.
Переваривание углеводов в кишечнике[править | править код]
Расщепление крахмала и гликогена до мальтозы в кишечнике происходит под действием 3 ферментов:
- панкреатической α-амилазы
- амило-1,6-глюкозидазы
- олиго-1,6-глюкозидазы
Образующаяся мальтоза оказывается только временным продуктом, так как она быстро гидролизуется под влиянием фермента мальтазы (α-глюкозидазы) на 2 молекулы глюкозы. Кишечный сок также содержит активную сахаразу, под действием которой образуются глюкоза и фруктоза.
Панкреатическая α-амилаза[править | править код]
В двенадцатиперстной кишке рН среды желудочного содержимого нейтрализуется, так как секрет поджелудочной железы имеет рН 7,5-8,0 и содержит гидрокарбонаты (НСО3-). С секретом поджелудочной железы в кишечник поступает панкреатическая α-амилаза. Этот фермент гидролизует α-1,4-гликозидные связи в крахмале и декстринах.
Продукты переваривания крахмала на этом этапе — дисахарид мальтоза, содержащая 2 остатка глюкозы, связанные α-1,4-связью. Из тех остатков глюкозы, которые в молекуле крахмала находятся в местах разветвления и соединены α-1,6-гликозидной связью, образуется дисахарид изомальтоза. Кроме того, образуются олигосахариды, содержащие 3-8 остатков глюкозы, связанные α-1,4- и α-1,6-связями
α-Амилаза поджелудочной железы, так же, как α-амилаза слюны, действует как эндогликозидаза. Панкреатическая α-амилаза не расщепляет α-1,6-гликозидные связи в крахмале. Этот фермент также не гидролизует β-1,4-гликозидные связи, которыми соединены остатки глюкозы в молекуле целлюлозы. Целлюлоза, таким образом, проходит через кишечник неизменённой. Тем не менее непереваренная целлюлоза выполняет важную функцию балластного вещества, придавая пище дополнительный объём и положительно влияя на процесс переваривания. Кроме того, в толстом кишечнике целлюлоза может подвергаться действию бактериальных ферментов и частично расщепляться с образованием спиртов, органических кислот и СО2. Продукты бактериального расщепления целлюлозы важны как стимуляторы перистальтики кишечника.
Мальтоза, изомальтоза и триозосахариды, образующиеся в верхних отделах кишечника из крахмала, — промежуточные продукты. Дальнейшее их переваривание происходит под действием специфических ферментов в тонком кишечнике. Дисахариды пищи сахароза и лактоза также гидролизуются специфическими дисахаридазами в тонком кишечнике.
Особенность переваривания углеводов в тонком кишечнике заключается в том, что активность специфических олиго- и дисахаридаз в просвете кишечника низкая. Но ферменты активно действуют на поверхности эпителиальных клеток кишечника.
Тонкий кишечник изнутри имеет форму пальцеобразных выростов — ворсинок, покрытых эпителиальными клетками. Эпителиальные клетки, в свою очередь, покрыты микроворсинками, обращёнными в просвет кишечника. Эти клетки вместе с ворсинками образуют щёточную каёмку, благодаря которой увеличивается поверхность контакта гидролитических ферментов и их субстратов в содержимом кишечника. На 1 мм2 поверхности тонкой кишки у человека приходится 80-140 млн ворсинок.
Ферменты, расщепляющие гликозидные связи в дисахаридах (дисахаридазы), образуют ферментативные комплексы, локализованные на наружной поверхности цитоплазматической мембраны энтероцитов.
Сахаразо-изомальтазный комплекс[править | править код]
Этот ферментативный комплекс состоит из двух полипептидных цепей и имеет доменное строение. Сахаразо-изомальтазный комплекс прикрепляется к мембране микроворсинок кишечника с помощью гидрофобного (трансмембранного) домена, образованного N-концевой частью полипептида. Каталитический центр выступает в просвет кишечника. Связь этого пищеварительного фермента с мембраной способствует эффективному поглощению продуктов гидролиза клеткой.
Сахаразо-изомальтазный комплекс гидролизует сахарозу и изомальтозу, расщепляя α-1,2- и α-1,6-гликозидные связи. Кроме того, оба ферментных домена имеют мальтазную и мальтотриазную активности, гидролизуя α-1,4-гликозидные связи в мальтозе и мальтотриозе (трисахарид, образующийся из крахмала). На долю сахаразо-изомальтазного комплекса приходится 80 % от всей мальтазной активности кишечника. Но несмотря на присущую ему высокую мальтазную активность, этот ферментативный комплекс назван в соответствии с основной специфичностью. К тому же сахаразная субъединица — единственный фермент в кишечнике, гидролизующий сахарозу. Изомальтазная субъединица с большей скоростью гидролизует гликозидные связи в изомальтозе, чем в мальтозе и мальтотриозе.
В тощей кишке содержание сахаразо-изомальтазного ферментативного комплекса достаточно высокое, но оно снижается в проксимальной и дистальной частях кишечника.
Гликоамилазный комплекс[править | править код]
Этот ферментативный комплекс катализирует гидролиз α-1,4-связи между глюкозными остатками в олигосахаридах, действуя с восстанавливающего конца. По механизму действия этот фермент относят к экзогликозидазам. Комплекс расщепляет также связи в мальтозе, действуя как мальтаза. В гликоамилазный комплекс входят две разные каталитические субъединицы, имеющие небольшие различия в субстратной специфичности. Гликоамилазная активность комплекса наибольшая в нижних отделах тонкого кишечника.
β-Гликозидазный комплекс (лактаза)[править | править код]
Лактаза расщепляет β-1,4-гликозидные связи между глюкозой и галактозой в лактозе.
Этот ферментативный комплекс по химическому составу является гликопротеином. Лактаза, как и другие гликозидазные комплексы, связана с щёточной каёмкой и распределена неравномерно по всему тонкому кишечнику. Активность лактазы колеблется в зависимости от возраста. Так, активность лактазы у плода особенно повышена в более поздние сроки беременности и сохраняется на высоком уровне до 5-7 летнего возраста. Затем активность фермента снижается, составляя у взрослых 10 % от уровня активности, характерного для детей.
Трегалаза[править | править код]
Трегалаза (КФ 3.2.1.28) — также гликозидазный комплекс, гидролизующий связи между мономерами в трегалозе — дисахариде, содержащемся в грибах.
Совместное действие всех перечисленных ферментов завершает переваривание пищевых олиго- и полисахаридов с образованием моносахаридов, основной из которых — глюкоза. Кроме глюкозы, из углеводов пищи также образуются фруктоза и галактоза, в меньшем количестве — манноза, ксилоза, арабиноза.
Всасывание моносахаридов в кишечнике[править | править код]
Моносахариды образовавшиеся в результате переваривания, всасываются эпителиальными клетками тощей и подвздошной кишок с помощью специальных механизмов транспорта через мембраны клеток.
Транспорт моносахаридов в клетки слизистой оболочки кишечника может осуществляться разными способами: путём облегчённой диффузии и активного транспорта. В случае активного транспорта глюкоза и Na+ проходят через мембраны с люминальной стороны, связываясь с разными участками белка-переносчика. При этом Na+ поступает в клетку по градиенту концентрации, и одновременно глюкоза транспортируется против градиента концентрации (вторично-активный транспорт). Следовательно, чем больше градиент Na+, тем больше поступление глюкозы в энтероциты. Если концентрация Na+ во внеклеточной жидкости уменьшается, транспорт глюкозы снижается. Градиент концентрации Na+, являющийся движущей силой активного сим-порта, создаётся работой Nа+, К+-АТФ-азы. Перенос в клетки слизистой оболочки кишечника по механизму вторично-активного транспорта характерен также для галактозы.
При разной концентрации глюкозы в просвете кишечника «работают» различные механизмы транспорта. Благодаря активному транспорту эпителиальные клетки кишечника могут поглощать глюкозу при её очень низкой концентрации в просвете кишечника. Если же концентрация глюкозы в просвете кишечника велика, то она может транспортироваться в клетку путём облегчённой диффузии. Таким же способом может всасываться и фруктоза. Скорость всасывания глюкозы и галактозы гораздо выше, чем других моносахаридов.
После всасывания моносахариды (главным образом, глюкоза) покидают клетки слизистой оболочки кишечника через мембрану, обращённую к кровеносному капилляру, с помощью облегчённой диффузии. Часть глюкозы (более половины) через капилляры кишечных ворсинок попадает в кровеносную систему и по воротной вене доставляется в печень. Остальное количество глюкозы поступает в клетки других тканей.
Транспорт глюкозы из крови в клетки[править | править код]
Потребление глюкозы клетками из кровотока происходит также путём облегчённой диффузии. Следовательно, скорость трансмембранного потока глюкозы зависит только от градиента её концентрации. Исключение составляют клетки мышц и жировой ткани, где облегчённая диффузия регулируется инсулином (гормон поджелудочной железы). В отсутствие инсулина плазматическая мембрана этих клеток непроницаема для глюкозы, так как она не содержит белки-переносчики (транспортёры) глюкозы. Транспортёры глюкозы называют также рецепторами глюкозы. Например, описан транспортёр глюкозы, выделенный из эритроцитов. Это трансмембранный белок, полипептидная цепь которого построена из 492 аминокислотных остатков и имеет доменную структуру. Полярные домены белка расположены по разные стороны мембраны, гидрофобные располагаются в мембране, пересекая её несколько раз. Транспортёр имеет участок связывания глюкозы на внешней стороне мембраны. После присоединения глюкозы конформация белка изменяется, в результате чего глюкоза оказывается связанной с белком в участке, обращённом внутрь клетки. Затем глюкоза отделяется от транспортёра, переходя внутрь клетки. Считают, что способ облегчённой диффузии по сравнению с активным транспортом предотвращает транспорт ионов вместе с глюкозой, если она транспортируется по градиенту концентрации.
Глюкозные транспортёры[править | править код]
Глюкозные транспортёры или ГЛЮТ представляют собой несколько семейств мембранных белков, обнаруженных во всех тканях организма млекопитающих. На данный момент существуют несколько десятков разновидностей ГЛЮТ, они пронумерованы в соответствии с порядком их обнаружения[3].
Структура белков семейства ГЛЮТ (GLUT) отличается от белков, транспортирующих глюкозу через мембрану в кишечнике и почках против градиента концентрации. Описанные 4 типа ГЛЮТ имеют сходные первичную структуру и доменную организацию (все 4 типа относятся к I классу переносчиков глюкозы). ГЛЮТ-5 имеет несколько иную структуру и относится ко II классу переносчиков глюкозы.
Распределение белков-транспортёров глюкозы (ГЛЮТ)
| Типы ГЛЮТ | Локализация в органах | Сродство к глюкозе |
|---|---|---|
| ГЛЮТ-1 | Преимущественно в мозге, плаценте, почках, толстом кишечнике. | Высокое, низкое значение KM. |
| ГЛЮТ-2 | Преимущественно в печени, почках, β-клетках островков Лангерганса, эритроцитах. | Hизкое, высокое значение KM. |
| ГЛЮТ-3 | Во многих тканях, включая мозг, плаценту, почки. | Высокое, низкое значение KM. |
| ГЛЮТ-4(инсулинзависимый) | В мышцах (скелетных и сердечной), жировой ткани. Содержится в отсутствии инсулина почти полностью в цитоплазме. | Зависит от концентрации инсулина. |
| ГЛЮТ-5 | В апикальном отделе энтероцитов тонкого кишечника. Является переносчиком фруктозы[4]. | Очень низкое. |
Все типы ГЛЮТ могут находиться как в плазматической мембране, так и в цитозольных везикулах. ГЛЮТ-4 (и в меньшей мере ГЛЮТ-1) почти полностью находятся в цитоплазме клеток. Влияние инсулина на такие клетки приводит к перемещению везикул, содержащих ГЛЮТ, к плазматической мембране, слиянию с ней и встраиванию транспортёров в мембрану. После чего возможен облегчённый транспорт глюкозы в эти клетки. После снижения концентрации инсулина в крови транспортёры глюкозы снова перемещаются в цитоплазму, и поступление глюкозы в клетку прекращается.
Перемещение глюкозы из первичной мочи в клетки почечных канальцев происходит вторично-активным транспортом, подобно тому, как это осуществляется при всасывании глюкозы из просвета кишечника в энтероциты. Благодаря этому глюкоза может поступать в клетки даже в том случае, если её концентрация в первичной моче меньше, чем в клетках. При этом глюкоза реабсорбируется из первичной мочи почти полностью (99 %).
Известны различные нарушения в работе транспортёров глюкозы. Наследственный дефект этих белков может лежать в основе инсулинонезависимого сахарного диабета В то же время причиной нарушения работы транспортёра глюкозы может быть не только дефект самого белка. Нарушения функции ГЛЮТ-4 возможны на следующих этапах:
- передача сигнала инсулина о перемещении этого транспортёра к мембране;
- перемещение транспортёра в цитоплазме;
- включение в состав мембраны;
- отшнуровывание от мембраны и т. д.
Нарушения переваривания и всасывания углеводов[править | править код]
В основе патологии переваривания и всасывания углеводов могут быть причины двух типов:
- дефекты ферментов, участвующих в гидролизе углеводов в кишечнике;
- нарушение всасывания продуктов переваривания углеводов в клетки слизистой оболочки кишечника.
В обоих случаях возникает осмотическая диарея, которую вызывают нерасщеплённые дисахариды или невсосавшиеся моносахариды. Эти невостребованные углеводы поступают в дистальные отделы кишечника, изменяя осмотическое давление содержимого кишечника. Кроме того, оставшиеся в просвете кишечника углеводы частично подвергаются ферментативному расщеплению микроорганизмами с образованием органических кислот и газов. Всё вместе приводит к притоку воды в кишечник, увеличению объёма кишечного содержимого, усилению перистальтики, спазмам и болям, а также метеоризму.
Термином «мальабсорбция» называют недостаточное всасывание переваренных продуктов углеводов. Но поскольку клинические проявления при недостаточном переваривании и всасывании сходны, то термином «мальабсорбция» называют оба вида нарушений.
Нарушение переваривания углеводов в кишечнике[править | править код]
Нарушения переваривания могут быть связаны как с недостаточной активностью отдельных дисахаридаз, так и с недостаточностью всего ферментативного комплекса, например сахаразо-изомальтазного.
Известны наследственные и приобретённые формы недостаточности активности ферментов. Симптомы врождённых форм проявляются достаточно рано, например после первых кормлений грудным молоком (при дефиците лактазы), после перехода на искусственное вскармливание или при добавлении в рацион сахара и крахмала (при дефиците ос-амилазы или специфических дисахаридаз). В случае недостаточного лечения врождённые формы патологии сопровождаются хроническим дисбактериозом и нарушениями физического развития ребёнка.
Приобретённые формы патологии могут наблюдаться при кишечных заболеваниях, например гастритах, колитах, энтеритах. В этих случаях особенно заметно снижение активности лактазы. Как уже говорилось, активность лактазы в кишечнике ниже, чем других дисахаридаз, поэтому уменьшение её активности становится заметным для организма в первую очередь.
Дефицит лактазы у взрослых людей может иметь и другую причину. Возможно снижение экспрессии гена лактазы возрастного характера. Уже упоминалось, что активность лактазы у взрослых людей в норме значительно ниже, чем у детей. Поэтому снижение активности лактазы относительно уже имеющегося низкого уровня у отдельных людей может проявляться непереносимостью молока. Носителями патологии, связанной с дефицитом лактазы, являются чаще всего лица африканского и азиатского происхождения. Средняя частота данной формы патологии в странах Европы составляет 7-12 %, в Китае — 80 %, в отдельных районах Африки — до 97 %. Подобные наблюдения распространения лактазной недостаточности связывают с исторически сложившимся рационом питания и отсутствием молочного скотоводства в упомянутых регионах. Примеры и причины нарушения переваривания дисахаридов перечислены в таблице.
Существуют редкие формы нарушения переваривания углеводов. Например, известна наследственная недостаточность трегалазы, которая проявляется диспепсией после употребления грибов, содержащих трегалозу.
В отдельных случаях мальабсорбция может быть вызвана несколькими причинами. Например, после операции на желудке возможны ухудшение смешивания пищи с пищеварительными соками, снижение их секреции, ускорение прохождения пищи через кишечник, колонизация бактериями слепой и приводящей петель.
Нарушения всасывания моносахаридов[править | править код]
Для диагностики различных нарушений переваривания используют пробы с нагрузкой определёнными углеводами. Нарушения всасывания могут быть следствием дефекта какого-либо компонента (белка или фермента), участвующего в системе транспорта моносахаридов через мембрану. Описаны патологии, связанные с дефектом натрийзависимого белка-переносчика глюкозы. Недостаточность кишечных дисахаридаз можно диагностировать с помощью введения дисахарида и последующего определения концентрации глюкозы в крови. Для большей чувствительности этот тест проводят, вводя сначала дисахарид (50 г), а затем эквивалентное количество составляющих его моносахаридов (по 25 г каждого). После нагрузки концентрация глюкозы в крови увеличивается примерно на 50 % относительно нормы. При патологии отмечают незначительную гипергликемию.
Нарушения переваривания дисахаридов
| Причина заболевания | Клинические проявления и лабораторные данные |
|---|---|
| Наследственный дефицит лактазы | Встречается относительно редко.
После приёма молока наблюдаются рвота, диарея, спазмы и боли в животе, метеоризм. Симптомы развиваются сразу после рождения. |
| Недостаточность лактазы вследствие снижения экспрессии гена фермента в онтогенезе | Характерна для взрослых и детей старшего возраста.
Является следствием возрастного снижения количества лактазы. Симптомы непереносимости молока аналогичны наследственной форме дефицита лактозы. |
| Недостаточность лактазы вторичного характера | Это временная, приобретённая форма. Непереносимость молока может быть следствием кишечных заболеваний, например, колитов, гастритов. Кроме того, временный дефицит лактазы может быть следствием операций на ЖКТ. |
| Наследственная недостаточность сахаразо-изомальтазного комплекса | Проявляется, когда в рацион детей добавляют сахарозу и крахмал. Больные дети обычно неохотно едят сладкое. После нагрузки сахарозой отмечается незначительная гипергликемия. Другие сахара (глюкоза, фруктоза, лактоза) переносятся хорошо. |
| Приобретённая недостаточность сахаразо-изомальтазного комплекса | Может возникать вследствие кишечных заболеваний. Проявляется диспепсией, провоцируемой крупами, крахмалом, а также пивом и другими напитками на основе солода. |
Если тест при нагрузке моносахаридом сопровождается адекватным повышением его концентрации в крови, а нагрузка дисахаридом не даёт нормальной реакции, то это, скорее всего, указывает на дефект кишечной дисахаридазы, а не системы транспорта.
О недостаточности лактазы можно судить, определяя водород в выдыхаемом воздухе (водородный тест). Водород образуется в результате действия бактериальных ферментов на лактозу.
Анаболизм и катаболизм гликогена[править | править код]
Многие ткани синтезируют в качестве резервной формы глюкозы гликоген. Синтез и распад гликогена обеспечивают постоянство концентрации глюкозы в крови и создают депо для её использования тканями по мере необходимости.
Гликоген — одна из самых главных форм запасания углеводов у грибов, животных и человека.

Гликоген — разветвлённый гомополимер глюкозы, в котором остатки глюкозы соединены в линейных участках α-1,4-гликозидной связью. В точках ветвления мономеры соединены α-1,6-гликозидными связями. Эти связи образуются примерно с каждым десятым остатком глюкозы. Следовательно, точки ветвления в гликогене встречаются примерно через каждые десять остатков глюкозы. Так возникает древообразная структура с молекулярной массой >107Д, что соответствует приблизительно 50 000 остатков глюкозы. Таким образом, в молекуле гликогена имеется только одна свободная аномерная ОН-группа и, следовательно, только один восстанавливающий (редуцирующий) конец.
При полимеризации глюкозы снижается растворимость образующейся молекулы гликогена и, следовательно, её влияние на осмотическое давление в клетке. Это обстоятельство объясняет, почему в клетке депонируется гликоген, а не свободная глюкоза.
После приёма пищи, богатой углеводами, запас гликогена в печени может составлять примерно 4 %-5 % от её массы. В мышцах запасается около 1 % гликогена, однако масса мышечной ткани значительно больше и поэтому общее количество гликогена в мышцах в 2 раза больше, чем в печени. Гликоген может синтезироваться во многих клетках, например в нейронах, макрофагах, клетках жировой ткани, но содержание его в этих тканях незначительно. В организме может содержаться до 450 г гликогена.
Запасы углеводов в организме нормального человека (массой 70 кг) после приёма пищи. В таблице приведены средние показатели.
| Углевод | Процентное содержание и масса |
|---|---|
| Гликоген печени | 4 % = 72 г |
| Мышечный гликоген | 0,7 % = 245 г |
| Внеклеточная глюкоза | 0,1 % = 10 г |
| Итого | 327 г |
Следует подчеркнуть, что синтез и распад гликогена в клетке осуществляется разными метаболическими путями. В частности считалось, что гликогенфосфорилаза (фосфорилаза а) катализирует как распад, так и синтез гликогена потому что в опытах in vitro, было доказано что гликогенфосфорилазная реакция обратима. Однако в дальнейшем было установлено, что в клетке (in vivo) фосфорилаза а катализирует только распад гликогена, синтез гликогена осуществляется совершенно другим ферментом. Оба эти процесса (синтез и распад) регулируют содержание глюкозы в крови и создают резерв глюкозы для интенсивной мышечной работы.
Распад гликогена печени служит в основном для поддержания уровня глюкозы в крови в постабсорбтивном периоде. Поэтому содержание гликогена в печени изменяется в зависимости от ритма питания. При длительном голодании оно снижается почти до нуля. Гликоген мышц служит резервом глюкозы — источника энергии при мышечном сокращении. Мышечный гликоген не используется для поддержания уровня глюкозы в крови. Как уже упоминалось ранее, в клетках мышц нет фермента глюкозо-6-фосфатазы, и образование свободной глюкозы невозможно. Расход гликогена в мышцах зависит в основном от физической нагрузки.
Гликогеногенез[править | править код]
Гликоген синтезируется в период пищеварения (через 1-2 ч после приёма углеводной пищи). Синтез гликогена из глюкозы, как и любой анаболический процесс, является эндергоническим, то есть требующим затрат энергии.

Глюкоза, поступающая в клетку, фосфорилируется при участии АТФ. Затем глюкозо-6-фосфат в ходе обратимой реакции превращается в глюкозо-1-фосфат под действием фермента фосфоглюкомутазы. Глюкозо-1-фосфат по термодинамическому состоянию мог бы служить субстратом для синтеза гликогена. Но в силу обратимости реакции глюкозо-6-фосфат ↔ глюкозо-1-фосфат синтез гликогена из глюкозо-1-фосфата и его распад оказались бы также обратимыми и поэтому неконтролируемыми. Чтобы синтез гликогена был термодинамически необратимым, необходима дополнительная стадия образования УДФ-глюкозы из УТФ и глюкозо-1-фосфата. Фермент, катализирующий эту реакцию, назван по обратной реакции: УДФ-глюкопирофосфорилаза. Однако в клетке обратная реакция не протекает, потому что образовавшийся в ходе прямой реакции пирофосфат очень быстро расщепляется пирофосфатазой на 2 молекулы фосфата.
Реакция образования УДФ-глюкозы обусловливает необратимость всей серии реакций, протекающих при синтезе гликогена. Этим же объясняется невозможность протекания распада гликогена путём простого обращения процесса его синтеза.
Образованная УДФ-глюкоза далее используется как донор остатка глюкозы при синтезе гликогена. Эту реакцию катализирует фермент гликогенсинтаза (глюкозилтрансфераза). Поскольку в данной реакции не используется АТФ, фермент называют синтазой, а не синтетазой. Нуклеотидная часть УДФ-глюкозы играет существенную роль в действии гликоген синтазы, выполняя функцию «рукоятки», при помощи которой фермент располагает глюкозу в полисахаридной цепи в нужном положении. Кроме того, нуклеотидная часть УДФ-глюкозы, по-видимому, необходима для узнавания субстрата при катализе.
Так как гликоген в клетке никогда не расщепляется полностью, синтез гликогена осуществляется путём удлинения уже имеющейся молекулы полисахарида, называемой «затравка», или «праймер». К «затравке» последовательно присоединяются молекулы глюкозы. Строением молекулы «затравки» как бы предопределяется тип связи, который возникает в реакции трансгликозилирования. Таким образом, синтезируется полисахарид, аналогичный по строению с «затравочным». В состав «затравки» может входить белок гликогенин, в котором к ОН-группе одного из тирозиновых остатков присоединена олигосахаридная цепочка (примерно 8 остатков глюкозы). Глюкозные остатки переносятся гликогенсинтазой на нередуцирующий конец олигосахарида и связываются α-1,4-гликозидными связями. По окончании синтеза гликогенин остаётся включённым в гранулу гликогена.
Разветвлённая структура гликогена образуется при участии амило-1,4 → 1,6-глюкозилтрансферазы, называемой ферментом «ветвления» (от англ. branching enzyme). Как только гликогенсинтаза удлиняет линейный участок примерно до 11 глюкозных остатков, фермент ветвления переносит её концевой блок, содержащий 6-7 остатков, на внутренний остаток глюкозы этой или другой цепи. В точке ветвления концевой остаток глюкозы олигосахарида соединяется с гидроксильной группой в С6 положении с образованием α-1,6-гликозидной связи. Новая точка ветвления может быть образована на расстоянии не менее 4 остатков от любой уже существующей. Таким образом, по мере синтеза гликогена многократно возрастает число ветвлений. Концы цепей служат точками роста молекулы при её синтезе и началом при её распаде.
Гликогенолиз[править | править код]

Распад гликогена или его мобилизация происходят в ответ на повышение потребности организма в глюкозе. Гликоген печени распадается в основном в интервалах между приёмами пищи, кроме того, этот процесс в печени и мышцах ускоряется во время физической работы. Распад гликогена происходит путём последовательного отщепления остатков глюкозы в виде глюкозо-1-фосфата. Гликозидная связь расщепляется с использованием неорганического фосфата, поэтому процесс называется фосфоролизом, а фермент гликогенфосфорилазой.
Так же как и синтез, расщепление гликогена начинается с нередуцирующего конца полисахаридной цепи. При этом наличие разветвлённой структуры гликогена облегчает быстрое высвобождение глюкозных остатков, так как чем больше концов имеет молекула гликогена, тем больше молекул гликогенфосфорилазы могут действовать одновременно.
Гликогенфосфорилаза расщепляет только α-1,4-гликозидные связи. Последовательное отщепление глюкозных остатков прекращается, когда до точки ветвления остаётся 4 мономера. Подобная особенность в действии гликогенфосфорилазы обусловлена размером и строением её активного центра.
Дальнейший распад гликогена требует участия двух других ферментов. Сначала три оставшихся до точки ветвлении глюкозных остатка переносятся при участии олигосахаридтрансферазы на нередуцирующий конец соседней цепи, удлиняя её и таким образом создавая условия для действия фосфорилазы. Оставшийся в точке ветвления глюкозный остаток гидролитически отщепляется с помощью α-1,6-глюкозидазы в виде свободной глюкозы, после чего неразветвлённый участок гликогена может вновь атаковаться фосфорилазой.
Считают, что перенос трёх остатков глюкозы и удаление мономера из точки ветвления катализирует один и тот же фермент, который обладает двумя разными ферментативными активностями — трансферазной и гликозидазной. Его называют «деветвящим» ферментом (от англ, debranching enzyme).
Продукт действия гликогенфосфорилазы — глюкозо-1-фосфат — затем изомеризуется в глюкозо-6-фосфат фосфоглюкомутазой. Далее глюкозо-6-фосфат включается в процесс катаболизма или другие метаболические пути. В печени (но не в мышцах) глюкозо-6-фосфат может гидролизоваться с образованием глюкозы, которая выделяется в кровь. Эту реакцию катализирует фермент глюкозо-6-фосфатаза. Реакция протекает в просвете ЭР (эндоплазматического ретикулума), куда с помощью специального белка транспортируется глюкозо-6-фосфат. Фермент локализован на мембране ЭР таким образом, что его активный центр обращён в просвет ЭР. Продукты гидролиза (глюкоза и неорганический фосфат) возвращаются в цитоплазму также с помощью транспортных систем.
Гликогенолиз в печени[править | править код]
Установлено, что при стимуляции гликогенолиза катехоламинами в печени в качестве главных посредников выступают α1-рецепторы. При этом происходит ЦАМФ-независимая мобилизация ионов Са2+ и переход их из митохондрий в цитозоль, где они стимулируют Са2+/кальмодулинчувствительную киназу фосфорилазы. Фосфорилаза скелетных мышц в отличие от фосфорилазы печени не активируется глюкагоном. Отметим, что фосфорилаза сердечной мышцы активируется этим гормоном. Другим важным отличием является ингибирование печеночной протеинфосфатазы-1 активной формой фосфорилазы.
Биологическое значение обмена гликогена в печени и мышцах[править | править код]
Сравнение этих процессов позволяет сделать следующие выводы:
- синтез и распад гликогена протекают по разным метаболическими путям;
- печень запасает глюкозу в виде гликогена не столько для собственных нужд, сколько для поддержания постоянной концентрации глюкозы в крови, и, следовательно, обеспечивает поступление глюкозы в другие ткани. Присутствие в печени глюкозо-6-фосфатазы обусловливает эту главную функцию печени в обмене гликогена;
- функция мышечного гликогена заключается в освобождении глюкозо-6-фосфата, потребляемого в самой мышце для окисления и использования энергии;
- синтез гликогена — процесс эндергонический. Так на включение одного остатка глюкозы в полисахаридную цепь используется 1 моль АТФ и 1 моль УТФ;
- распад гликогена до глюкозо-6-фосфата не требует энергии;
- необратимость процессов синтеза и распада гликогена обеспечивается их регуляцией.
Регуляция метаболизма гликогена[править | править код]
Процессы накопления глюкозы в виде гликогена и его распада должны быть согласованы с потребностями организма в глюкозе как источнике энергии. Одновременное протекание этих метаболических путей невозможно, так как в этом случае образуется «холостой» цикл, существование которого приводит только к бесполезной трате АТФ.
Изменение направления процессов в метаболизме гликогена обеспечивают регуляторные механизмы, в которых участвуют гормоны. Переключение процессов синтеза и мобилизации гликогена происходит при смене абсорбтивного периода на постабсорбтивный или состояния покоя организма на режим физической работы. В переключении этих метаболических путей в печени участвуют гормоны инсулин, глюкагон и адреналин, а в мышцах — инсулин и адреналин.
Характеристика гормонов, регулирующих обмен гликогена[править | править код]
Первичным сигналом для синтеза и секреции инсулина и глюкагона является изменение уровня глюкозы в крови. В норме концентрация глюкозы в крови соответствует 3,3-5,5 ммоль/л (60- 100 мг/дл).
Инсулин — пептидный гормон, синтезируется и секретируется в кровь β-клетками островков Лангерганса поджелудочной железы, которые чувствительны к изменениям содержания глюкозы в крови и секретируют инсулин в ответ на повышение её содержания после приёма пищи. Транспортный белок (ГЛЮТ-2), обеспечивающий поступление глюкозы в β-клетки, отличается низким сродством к ней. Следовательно, этот белок транспортирует глюкозу в клетку поджелудочной железы лишь после того, как её содержание в крови будет выше нормального уровня (более 5,5 ммоль/л).
В β-клетках глюкоза фосфорилируется глюкокиназой, имеющей также высокую Кm для глюкозы — 12 ммоль/л. Скорость фосфорилирования глюкозы глюкокиназой в β-клетках прямо пропорциональна её концентрации в крови.
Синтез инсулина регулируется глюкозой. Глюкоза (или её метаболиты), по-видимому, непосредственно участвуют в регуляции экспрессии гена инсулина. Секреция инсулина и глюкагона также регулируется глюкозой, которая стимулирует секрецию инсулина из β-клеток и подавляет секрецию глюкагона из α-клеток. Кроме того, сам инсулин снижает секрецию глюкагона.
Глюкагон — «гормон голода», вырабатываемый α-клетками поджелудочной железы в ответ на снижение уровня глюкозы в крови. По химической природе глюкагон — пептид.
Адреналин выделяется из клеток мозгового вещества надпочечников в ответ на сигналы нервной системы, идущие из мозга при возникновении экстремальных ситуаций (например, бегство или борьба), требующих внезапной мышечной деятельности. Адреналин является сигналом «тревоги». Он должен мгновенно обеспечить мышцы и мозг источником энергии.
Регуляция активности гликогенфосфорилазы и гликогенсинтазы[править | править код]
Поскольку синтез и распад гликогена протекают по различным метаболическим путям, эти процессы могут контролироваться реципрокно (взаимно). Влияние гормонов на синтез и распад гликогена осуществляется путём изменения в противоположных направлениях активности двух ключевых ферментов: гликогенсинтазы и гликогенфосфорилазы с помощью их фосфорилирования и дефосфорилирования.
Гликогенфосфорилаза существует в 2 формах:
1) фосфорилированная — активная (форма а);
2) дефосфорилированная — неактивная (форма в).
Фосфорилирование осуществляется путём переноса фосфатного остатка с АТФ на гидроксильную группу одного из сериновых остатков фермента. Следствие этого — конформационные изменения молекулы фермента и его активация.
Взаимопревращения 2 форм гликогенфосфорилазы обеспечиваются действием ферментов киназы фосфорилазы и фосфопротеинфосфатазы (фермент, структурно связанный с молекулами гликогена). В свою очередь, активность киназы фосфорилазы и фосфопротеинфосфатазы также регулируется путём фосфорилирования и дефосфорилирования.
Активация киназы фосфорилазы происходит под действием протеинкиназы А — ПКА (цАМФ-зависимой). цАМФ сначала активирует протеинкиназу А, которая фосфорилирует киназу фосфорилазы, переводя её в активное состояние, а та, в свою очередь, фосфорилирует гликогенфосфорилазу. Синтез цАМФ стимулируется адреналином и глюкагоном.
Активация фосфопротеинфосфатазы происходит в результате реакции фосфорилирования, катализируемой специфической протеинкиназой, которая, в свою очередь, активируется инсулином посредством каскада реакций с участием Ras-белка, а также других белков и ферментов. Активируемая инсулином протеинкиназа фосфорилирует и тем самым активирует фосфопротеинфосфатазу. Активная фосфопротеинфосфатаза дефосфорилирует и, следовательно, инактивирует киназу фосфорилазы и гликогенфосфорилазу.
Активность гликогенсинтазы также изменяется в результате фосфорилирования и дефосфорилирования. Однако есть существенные различия в регуляции гликогенфосфорилазы и гликогенсинтазы:
- фосфорилирование гликогенсинтазы катализирует ПК А и вызывает её инактивацию;
- дефосфорилирование гликогенсинтазы под действием фосфопротеинфосфатазы, наоборот, её активирует.
Регуляция метаболизма гликогена в печени[править | править код]
Инсулин и глюкагон постоянно присутствуют в крови, но при смене абсорбтивного периода на постабсорбтивный изменяется их относительная концентрация, что является главным фактором, переключающим метаболизм гликогена в печени. Отношение концентрации инсулина в крови к концентрации глюкагона называют «инсулинглюкагоновый индекс». В постабсорбтивном периоде инсулинглюкагоновый индекс снижается, и решающее значение в регуляции концентрации глюкозы в крови приобретает концентрация глюкагона.
Глюкагон для гепатоцитов служит внешним сигналом о необходимости выделения в кровь глюкозы за счёт распада гликогена (гликогенолиза) или синтеза глюкозы из других веществ — глюконеогенеза (этот процесс будет изложен позднее). Гормон связывается с рецептором на плазматической мембране и активирует при посредничестве G-белка аденилатциклазу, которая катализирует образование цАМФ из АТФ. Далее следует каскад реакций, приводящий в печени к активации гликогенфосфорилазы и ингибированию гликогенсинтазы. Этот механизм приводит к высвобождению из гликогена глюкозо-1-фосфата, который превращается в глюкозо-6-фосфат. Затем под влиянием глюкозо-6-фосфатазы образуется свободная глюкоза, способная выйти из клетки в кровь. Таким образом, глюкагон в печени, стимулируя распад гликогена, способствует поддержанию глюкозы в крови на постоянном уровне.
Адреналин стимулирует выведение глюкозы из печени в кровь, для того чтобы снабдить ткани (в основном мозг и мышцы) «топливом» в экстремальной ситуации. Эффект адреналина в печени обусловлен фосфорилированием (и активацией) гликогенфосфорилазы. Адреналин имеет сходный с глюкагоном механизм действия.
Но возможно включение и другой эффекторной системы передачи сигнала в клетку печени.
Какая система передачи сигнала в клетку будет использована, зависит от типа рецепторов, с которыми взаимодействует адреналин. Так, взаимодействие адреналина с β2-рецепторами клеток печени приводит в действие аденилатциклазную систему. Взаимодействие же адреналина с α1-рецепторами «включают» инозитолфосфатный механизм трансмембранной передачи гормонального сигнала. Результат действия обеих систем — фосфорилирование ключевых ферментов и переключение процессов с синтеза гликогена на его распад. Тип рецепторов, который в наибольшей степени вовлекается в ответ клетки на адреналин, зависит от концентрации его в крови.
В период пищеварения преобладает влияние инсулина, так как инсулинглюкагоновый индекс в этом случае повышается. В целом инсулин влияет на обмен гликогена противоположно глюкагону. Инсулин снижает концентрацию глюкозы в крови в период пищеварения, действуя на метаболизм печени следующим образом:
- снижает уровень цАМФ в клетках, фосфорилируя (опосредованно через Ras-путь) и тем самым активируя протеинкиназу В (цАМФ-независимую). Протеинкиназа В, в свою очередь, фосфорилирует и активирует фосфодиэстеразу цАМФ — фермент, гидролизующий цАМФ с образованием АМФ.
- активирует (через Ras-путь) фосфопротеинфосфатазу гранул гликогена, которая дефосфорилирует гликогенсинтазу и таким образом её активирует. Кроме того, фосфопротеинфосфатаза дефосфорилирует и, следовательно, инактивирует киназу фосфорилазы и гликогенфосфорилазу;
- индуцирует синтез глюкокиназы, тем самым ускоряя фосфорилирование глюкозы в клетке. Следует напомнить, что регуляторным фактором в метаболизме гликогена является также величина Кm глюкокиназы, которая много выше, чем Кm гексокиназы. Смысл этих различий понятен: печень не должна потреблять глюкозу для синтеза гликогена, если её количество в крови в пределах нормы.
Всё это вместе приводит к тому, что инсулин одновременно активирует гликогенсинтазу и ингибирует гликогенфосфорилазу, переключая процесс мобилизации гликогена на его синтез.
В печени существует и аллостерическая регуляция гликогенфосфорилазы, обеспечивающая внутриклеточные потребности в глюкозе, но гормональные сигналы имеют приоритет над внутриклеточными и преследуют другие физиологические цели.
Регуляция метаболизма гликогена в мышцах[править | править код]
Регуляция обмена гликогена в скелетных мышцах обеспечивает энергетическим материалом как интенсивную работу мышц (например: бег или борьба), так и энергозатраты в состоянии покоя.
В экстремальных ситуациях в мышечных клетках мобилизация гликогена ускоряется адреналином. Связывание адреналина с β-рецепторами, ассоциированными с аденилатциклазной системой, приводит к образованию цАМФ в клетке, а затем фосфорилированию и активации киназы фосфорилазы и гликогенфосфорилазы.
Образование цАМФ, стимулированное адреналином, служит сигналом к увеличению производства энергии в результате ускорения расщепления гликогена. Именно в ходе распада, образованного из гликогена глюкозо-6-фосфата, синтезируется АТФ.
Инактивация гликогенсинтазы под влиянием адреналина в мышечных клетках проходит так же, как и в печени.
В состоянии покоя при низких концентрациях адреналина в крови гликогенфосфорилаза мышц находится в дефосфорилированном — неактивном состоянии (форма В), но распад гликогена всё-таки происходит. Это объясняется тем, что гликогенфосфорилаза активируется способом, не связанным с её фосфорилированием, так как уровень цАМФ в клетке низкий. В данной ситуации происходит аллостерическая активация гликогенфосфорилазы В. Активаторами фермента служат АМФ и Н3РО4, образующиеся в клетке при распаде АТФ.
При умеренных мышечных сокращениях, то есть в ситуации, не требующей участия в регуляции цАМФ, аллостерическим способом активируется киназа фосфорилазы. В данном случае аллостерическими эффекторами служат ионы Са2+, концентрация которых резко возрастает при сокращении мышц в ответ на сигнал от двигательного нерва. Активность фермента снижается сразу же, как только концентрация Са2+ в клетке уменьшается после поступления сигнала к расслаблению мышц. Таким образом, роль ионов Са2+ заключается не только в инициации мышечного сокращения, но также в обеспечении его энергозатрат.
Активация киназы фосфорилазы с помощью ионов Са2+ опосредована кальмодулином. Кальмодулин в данном случае — прочно связанная субъединица фермента. Мышечная киназа фосфорилазы состоит из субъединиц 4 типов: α, β, γ и δ, объединённых в комплекс. Фермент включает 4 таких комплекса. Каталитической активностью обладает γ-субъединица. Субъединицы α и β выполняют регуляторную функцию. Они содержат остатки серина, фосфорилируемые пируваткиназы А. δ-Субъединица связывает 4 иона кальция; она идентична белку кальмодулину. Связывание ионов кальция вызывает конформационные изменения, что приводит к активации каталитического центра γ-субъединицы, хотя молекула остаётся в дефосфорилированном состоянии.
В мышцах в период пищеварения, если он совпадает с состоянием покоя, происходит стимуляция синтеза гликогена. Мышечная работа во время пищеварения замедляет процесс синтеза гликогена, так как при этом мышцы используют для окисления глюкозу крови, поступающую из кишечника.

В переключении мобилизации гликогена на запасание глюкозы участвует инсулин. Как уже говорилось, глюкоза поступает в мышечные и жировые клетки с помощью глюкозного белка-транспортёра ГЛЮТ-4. Транспортёры в отсутствие инсулина находятся в цитоплазме клеток, и глюкоза клетками не используется, так как в мембране нет белков-переносчиков. Инсулин стимулирует перемещение ГЛЮТ-4 и встраивание их в мембрану клеток. Механизм подобного влияния инсулина изучен недостаточно, но определены его основные этапы. Цепь событий при стимуляции инсулином потребления глюкозы мышцами и жировыми клетками выглядит следующим образом:
- рецептор инсулина (IR) — инсулинстимулируемая тирозиновая протеинкиназа — обязательный посредник всех действий инсулина;
- активированный инсулином IR фосфорилирует специфические цитоплазматические белки — субстраты инсулина (IRS);
- фосфорилированный субстрат (в основном IRS-1) соединяется с фосфатидилинозитол-3-киназой (ФИ-3-киназа) и активирует этот фермент;
- активная ФИ-3-киназа катализирует фосфорилирование по позиции 3 ряд компонентов инозитолфосфатной сигнальной системы, приводящей к стимуляции транслокации (перемещению) ГЛЮТ из цитозоля в плазматическую мембрану;
- глюкоза с помощью ГЛЮТ-4 поступает в мышечные клетки и включается в синтез гликогена.
Влияние инсулина на скорость синтеза гликогена в мышцах осуществляется посредством изменения активности гликогенсинтазы и гликогенфосфорилазы — ключевых ферментов, о чём уже говорилось при обсуждении влияния инсулина на метаболизм гликогена в печени.
Катаболизм глюкозы[править | править код]
Под катаболизмом глюкозы подразумевается её расщепление в организме под действием ферментативных процессов, идущих с образованием запаса энергии в виде АТФ и выделением так называемых «отходов» ПВК, лактата, этанола, масляной кислоты и т. д. Катаболизм глюкозы — основной поставщик энергии для процессов жизнедеятельности организма.
Основные пути катаболизма глюкозы[править | править код]
Окисление глюкозы до СО2 и Н2О (аэробный распад). Аэробный распад глюкозы можно выразить суммарным уравнением:
Этот процесс включает несколько стадий:
- Аэробный гликолиз — процесс окисления глюкозы с образованием двух молекул пирувата;
- Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитратном цикле;
- ЦПЭ на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы
В определённых ситуациях обеспечение кислородом тканей может не соответствовать их потребностям. Например, на начальных стадиях интенсивной мышечной работы при стрессе сердечные сокращения могут не достигать нужной частоты, а потребности мышц в кислороде для аэробного распада глюкозы велики. В подобных случаях включается процесс, который протекает без кислорода и заканчивается образованием лактата из пировиноградной кислоты. Этот процесс называют анаэробным распадом, или анаэробным гликолизом. Анаэробный распад глюкозы энергетически мало эффективен, но именно этот процесс может стать единственным источником энергии для мышечной клетки в описанной ситуации. В дальнейшем, когда снабжение мышц кислородом будет достаточным в результате перехода сердца на ускоренный ритм, анаэробный распад переключается на аэробный.
Гликолиз[править | править код]

Гликолиз представляет собой один из сложных последовательных ферментативных процессов, в результате которых расщепляется глюкоза и одновременно синтезируется АТФ. Название «гликолиз» происходит от греч. γλυκός, glykos — сладкий и греч. λύσης, lysis — растворение.
Анаэробный гликолиз[править | править код]
В анаэробном процессе, не нуждающемся в митохондриальной дыхательной цепи, АТФ образуется за счёт двух реакций субстратного фосфорилирования.
При анаэробном гликолизе в цитозоле протекают все 10 реакций, идентичных аэробному гликолизу. Лишь 11-я реакция, где происходит восстановление пирувата цитозольным НАДН, является специфической для анаэробного гликолиза. Восстановление пирувата в лактат катализирует лактатдегидрогеназа (реакция обратимая, и фермент назван по обратной реакции). С помощью этой реакции обеспечивается регенерация НАД+ из НАДН без участия митохондриальной дыхательной цепи в ситуациях, связанных с недостаточным снабжением клеток кислородом. Роль акцептора водорода от НАДН (подобно кислороду в дыхательной цепи) выполняет пируват. Таким образом, значение реакции восстановления пирувата заключается не в образовании лактата, а в том, что данная цитозольная реакция обеспечивает регенерацию НАД+. К тому же лактат не является конечным продуктом метаболизма, удаляемым из организма. Это вещество выводится в кровь и утилизируется, превращаясь в печени в глюкозу, или при доступности кислорода превращается в пируват, который вступает в общий путь катаболизма, окисляясь до СО2 и Н2О.
Реакции анаэробного гликолиза[править | править код]
Фосфорилирование молекулы D-глюкозы[править | править код]
Первой реакцией гликолиза является фосфорилирование молекулы глюкозы, происходящее при участии тканеспецифичного фермента гексокиназы с затратой энергии 1 молекулы АТФ; образуется активная форма глюкозы — глюкозо-6-фосфат (Г-6-Ф):

Фосфорилирование глюкозы преследует две цели: во-первых, из-за того что плазматическая мембрана, проницаемая для нейтральной молекулы глюкозы, не пропускает отрицательно заряженные молекулы Г-6-Ф, фосфорилированная глюкоза оказывается запертой внутри клетки. Во-вторых, при фосфорилировании глюкоза переводится в активную форму, способную участвовать в биохимических реакциях и включаться в метаболические циклы.
Печёночный изофермент гексокиназы — глюкокиназа — имеет важное значение в регуляции уровня глюкозы в крови.
2. Изомеризация глюкозо-6-фосфата во фруктозо-6-фосфат[править | править код]
Во второй реакции ферментом фосфоглюкоизомеразой Г-6-Ф превращается во фруктозо-6-фосфат (Ф-6-Ф):

Энергия для этой реакции не требуется, и реакция является полностью обратимой. На данном этапе в процесс гликолиза может также включаться путём фосфорилирования и фруктоза.
3. Фосфолирование фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата[править | править код]
Фосфорилирование Ф-6-Ф осуществляется фосфофруктокиназой с затратой энергии ещё одной молекулы АТФ; это вторая ключевая реакция гликолиза, её регуляция определяет интенсивность гликолиза в целом. Данная реакция относится к необратимым.

4. Расщепление фруктозо-1,6-дифосфата на глицеральдегид-3-фосфат и диоксиацетонфосфат[править | править код]
Альдольное расщепление Ф-1,6-бФ происходит под действием альдолазы фруктозо-1,6-бисфосфата:

Реакция обратима. Равновесие сильно сдвинуто в сторону диоксиацетонфосфата: 95 % диоксиацетонфосфата и 5 % — глицеральдегид-3-фосфата. Образованием глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая стадия — наиболее сложная и важная она включает окислительно-восстановительную реакцию (реакция гликолитической оксиредукции), сопряжённую с субстратным фосфорилированием, в процессе которого образуется АТФ.
5. Взаимопревращение триозофосфатов[править | править код]
В результате четвёртой реакции образуются дигидроксиацетонфосфат и глицеральдегид-3-фосфат, причём первый почти сразу под действием фосфотриозоизомеразы переходит во второй, который и участвует в дальнейших превращениях:

6. Окисление глицеральдегид-3-фосфата до 1,3-бисфосфоглицерата[править | править код]
Каждая молекула глицеральдегидфосфата окисляется НАД+ в присутствии дегидрогеназы глицеральдегидфосфата до 1,3-бисфосфоглицерата:

7. Перенос фосфатной группы с 1,3-бисфосфоглицерата на АДФ[править | править код]
С образовавшегося 1,3-бисфосфоглицерата, содержащего макроэргическую связь в 1 положении, ферментом фосфоглицераткиназой на молекулу АДФ переносится остаток фосфорной кислоты — образуется молекула АТФ:

Это первая реакция субстратного фосфорилирования. С этого момента процесс расщепления глюкозы перестаёт быть убыточным в энергетическом плане, так как энергетические затраты первого этапа оказываются компенсированными: синтезируются 2 молекулы АТФ (по одной на каждый 1,3-бисфосфоглицерат) вместо двух потраченных в реакциях 1 и 3. Для протекания данной реакции требуется присутствие в цитозоле АДФ, то есть при избытке в клетке АТФ (и недостатке АДФ) её скорость снижается. Поскольку АТФ, не подвергающийся метаболизму, в клетке не депонируется, а просто разрушается, то эта реакция является важным регулятором гликолиза.
8. Изомеризация 3-фосфоглицерата в 2-фосфоглицерат[править | править код]
Данная реакция сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат):

Реакция легкообратима, протекает в присутствии ионов Mg2+. Кофактором фермента является 2,3-бисфосфоглицериновая кислота, аналогично тому, как в фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-дифосфат.
9. Дегидратация 2-фосфоглицерата с образованием фосфоенолпирувата[править | править код]
Эта реакция катализируется енолазой, при этом 2-фосфоглицерат в результате отщепления молекулы воды переходит в фосфоенолпируват (ФЕП), а фосфатная связь в положении 2 становится высокоэргической:
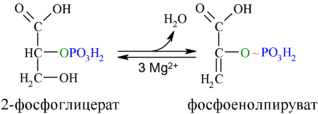
Енолаза активируется двухвалентными катионами Mg2+ или Mn2+ и ингибируется фторидом.
10. Перенос фосфатной группы с фосфоенолпирувата на АДФ[править | править код]
Десятая реакция характеризуется разрывом высокоэргической связи и переносом фосфатного остатка от ФЕП на АДФ (субстратное фосфорилирование). Катализируется ферментом пируваткиназой:

Для действия пируваткиназы необходимы ионы Mg2+, а также одновалентные катионы щелочных металлов (K+ или др.). Внутри клетки реакция является практически необратимой. Это последняя ключевая реакция гликолиза. Изомеризация енольной формы пирувата в пируват происходит неферментативно.
11. Восстановление пирувата до лактата[править | править код]
В результате данной реакции происходит восстановление пирувата до лактата под действием фермента ЛДГ и кофермента НАДН, который образуется в 6 реакции:

Баланс АТФ при анаэробном гликолизе[править | править код]
Анаэробный гликолиз по сравнению с аэробным менее эффективен (в аэробном из 1 моль глюкозы образуется 38 моль АТФ). В этом процессе катаболизм 1 моль глюкозы без участия митохондриальной дыхательной цепи сопровождается синтезом 2 моль АТФ и 2 моль лактата. АТФ образуется за счёт 2 реакций субстратного фосфорилирования. Поскольку глюкоза распадается на 2 фосфотриозы, то с учётом стехиометрического коэффициента, равного 2, количество моль синтезированного АТФ равно 4. Учитывая 2 моль АТФ, использованных на первом этапе гликолиза, получаем конечный энергетический эффект процесса, равный 2 моль АТФ. Таким образом, 10 цитозольных ферментов, катализирующих превращение глюкозы в пируват, вместе с лактатдегидрогеназой обеспечивают в анаэробном гликолизе синтез 2 моль АТФ (на 1 моль глюкозы) без участия кислорода.
Значение анаэробного гликолиза[править | править код]
Анаэробный гликолиз, несмотря на небольшой энергетический эффект, является основным источником энергии для скелетных мышц в начальном периоде интенсивной работы, то есть в условиях, когда снабжение кислородом ограничено. Кроме того, зрелые эритроциты извлекают энергию за счет анаэробного окисления глюкозы, потому что не имеют митохондрий[5].
Аэробный гликолиз[править | править код]
Аэробным гликолизом называют процесс окисления глюкозы до пировиноградной кислоты, протекающий в присутствии кислорода. Все ферменты, катализирующие реакции этого процесса, локализованы в цитозоле клетки.
Аэробный гликолиз — основной путь для образования энергии в клетках организма. Он может протекать как прямым (апотомическим, или, как его называют пентозофосфатным), так и непрямым (дихотомическим) путём. В результате непрямого окисления глюкоза полностью распадается на углекислый газ и воду, и при этом выделяется большое количество энергии (ΔQ = 2870 кДж/моль)
В аэробном гликолизе можно выделить 2 этапа:
- Подготовительный этап, в ходе которого глюкоза фосфорилируется и расщепляется на две молекулы фосфотриоз. Эта серия реакций протекает с использованием 2 молекул АТФ.
- Этап, сопряжённый с синтезом АТФ. В результате этой серии реакций фосфотриозы превращаются в пируват. Энергия, высвобождающаяся на этом этапе, используется для синтеза 10 моль АТФ.
Реакции аэробного гликолиза[править | править код]
Превращение глюкозо-6-фосфата в 2 молекулы глицеральдегид-3-фосфата[править | править код]
Глюкозо-6-фосфат, образованный в результате фосфорилирования глюкозы с участием АТФ, в ходе следующей реакции превращается в фруктозо-6-фосфат. Эта обратимая реакция изомеризации протекает под действием фермента глюкозофосфатизомеразы.
Затем следует ещё одна реакция фосфорилирования с использованием фосфатного остатка и энергии АТФ. В ходе этой реакции, катализируемой фосфофруктокиназой, фруктозо-6-фосфат превращается во фруктозо-1,6-дисфосфат. Данная реакция, так же, как гексокиназная, практически необратима, и, кроме того, она наиболее медленная из всех реакций гликолиза. Реакция, катализируемая фосфофруктокиназой, определяет скорость всего гликолиза, поэтому, регулируя активность фосфофруктокиназы, можно изменять скорость катаболизма глюкозы.
Фруктозо-1,6-дисфосфат далее расщепляется на 2 триозофосфата: глицеральдегид-3-фосфат и дигидроксиацетонфосфат. Реакцию катализирует фермент фруктозодисфосфатальдолаза, или просто альдолаза. Этот фермент катализирует как реакцию альдольного расщепления, так и альдольной конденсации, то есть обратимую реакцию. Продукты реакции альдольного расщепления — изомеры. В последующих реакциях гликолиза используется только глицеральдегид-3-фосфат, поэтому дигидроксиацетонфосфат превращается с участием фермента триозофосфатизомеразы в глицероальдегид-3-фосфат.
В описанной серии реакций дважды происходит фосфорилирование с использованием АТФ. Однако расходование двух молекул АТФ (на одну молекулу глюкозы) далее будет компенсировано синтезом большего количества АТФ.
Превращение глицеральдегид-3-фосфата в пируват[править | править код]
Эта часть аэробного гликолиза включает реакции, связанные с синтезом АТФ. Наиболее сложной в данной серии реакций является реакция превращения глицеральдегид-3-фосфата в 1,3-дисфосфоглицерат. Это превращение — первая реакция окисления в ходе гликолиза. Реакцию катализирует глицеральдегид-3-фосфатдегидрогеназа, которая является НАД-зависимым ферментом. Значение данной реакции заключается не только в том, что образуется восстановленный кофермент, окисление которого в дыхательной цепи сопряжено с синтезом АТФ, но также и в том, что свободная энергия окисления концентрируется в макроэргической связи продукта реакции. Глицеральдегид-3-фосфатдегидрогеназа содержит в активном центре остаток цистеина, сульфгидрильная группа которого принимает непосредственное участие в катализе. Окисление глицеральдегид-3-фосфата приводит к восстановлению НАД и образованию с участием Н3РО4 высокоэнергетической ангидридной связи в 1,3-дисфосфоглицерате в положении 1. В следующей реакции высокоэнергетический фосфат передаётся на АДФ с образованием АТФ. Фермент, катализирующий это превращение, назван по обратной реакции фосфоглицераткиназой (киназы называются по субстрату, находящемуся в уравнении реакции по одну сторону с АТФ).
Образование АТФ описанным способом не связано с дыхательной цепью, и его называют субстратным фосфорилированием АДФ. Образованный 3-фосфоглицерат уже не содержит макроэргической связи. В следующих реакциях происходят внутримолекулярные перестройки, смысл которых сводится к тому, что низкоэнергетический фосфоэфир переходит в соединение, содержащее высокоэнергетический фосфат. Внутримолекулярные преобразования заключаются в переносе фосфатного остатка из положения 3 в фосфоглицерате в положение 2. Затем от образовавшегося 2-фосфоглицерата отщепляется молекула воды при участии фермента енолазы. Название дегидратирующего фермента дано по обратной реакции. В результате реакции образуется замещённый енол — фосфоенолпируват. Образованный фосфоенолпируват — макроэргическое соединение, фосфатная группа которого переносится в следующей реакции на АДФ при участии пируваткиназы (фермент также назван по обратной реакции, в которой происходит фосфорилирование пирувата, хотя подобная реакция в таком виде не имеет места).
Превращение фосфоенолпирувата в пируват — необратимая реакция. Это вторая в ходе гликолиза реакция субстратного фосфорилирования. Образующаяся енольная форма пирувата затем неферментативно переходит в более термодинамически стабильную кетоформу.
Окисление цитоплазматического НАДН в митохондриальной дыхательной цепи, челночные системы[править | править код]
НАДН, образующийся при окислении глицеральдегид-3-фосфата в аэробном гликолизе, подвергается окислению путём переноса атомов водорода в митохондриальную дыхательную цепь. Однако цитозольный НАДН не способен передавать водород на дыхательную цепь, потому что митохондриальная мембрана для него непроницаема. Перенос водорода через мембрану происходит с помощью специальных систем, называемых «челночными». В этих системах водород транспортируется через мембрану при участии пар субстратов, связанных соответствующими дегидрогеназами, то есть с обеих сторон митохондриальной мембраны находится специфическая дегидрогеназа. Известны 2 челночные системы. В первой из этих систем водород от НАДН в цитозоле передаётся на дигидроксиацетонфосфат ферментом глицерол-3-фосфатдегидрогеназой (НАД-зависимый фермент, назван по обратной реакции). Образованный в ходе этой реакции глицерол-3-фосфат, окисляется далее ферментом внутренней мембраны митохондрий — глицерол-3-фосфатдегидрогеназой (ФАД — зависимым ферментом). Затем протоны и электроны с ФАДН2 переходят на убихинон и далее по ЦПЭ. Глицеролфосфатная челночная система работает в клетках белых мышц и гепатоцитов. Однако в клетках сердечных мышц митохондриальная глицерол-3-фосфатдегидрогеназа отсутствует. Вторая челночная система, в которой участвуют малат, цитозольная и митохондриальная малат-дегидрогеназы, является более универсальной. В цитоплазме НАДН восстанавливает оксалоацетат в малат (смотрите рисунок, реакция 1), который при участии переносчика проходит в митохондрии, где окисляется в оксалоацетат НАД-зависимой малатдегидрогеназой (реакция 2). Восстановленный в ходе этой реакции НАД отдаёт водород в митохонодриальную ЦПЭ. Однако образованный из малата оксалоацетат выйти самостоятельно из митохондрий в цитозоль не может, так как мембрана митохондрий для него непроницаема. Поэтому оксалоацетат превращается в аспартат, который и транспортируется в цитозоль, где снова превращается в оксалоацетат. Превращения оксалоацетата в аспартат и обратно связаны с присоединением и отщеплением аминогруппы. Эта челночная система называется малат-аспартатной (смотрите рисунок). Результат её работы — регенерация цитоплазматического НАД+ из НАДН.
Обе челночные системы существенно отличаются по количеству синтезированного АТФ. В первой системе соотношение Ф/О равно 2, так как водород вводится в ЦПЭ на уровне KoQ. Вторая система энергетически более эффективна, так как передаёт водород в ЦПЭ через митохондриальный НАД+ и соотношение Ф/О близко к 3.
Баланс АТФ при аэробном гликолизе[править | править код]
На образование фруктозо-1,6-бисфосфата из одной молекулы глюкозы требуется 2 молекулы АТФ. Реакции, связанные с синтезом АТФ, происходят после распада глюкозы на 2 молекулы фосфотриозы, то есть на втором этапе гликолиза. На этом этапе происходят 2 реакции субстратного фосфорилирования и синтезируются 2 молекулы АТФ (реакции 7 и 10). Кроме того, одна молекула глицеральдегид-3-фосфата дегидрируется, a НАДН передаёт водород в митохондриальную ЦПЭ, где синтезируется 3 молекулы АТФ путём окислительного фосфорилирования. В данном случае количество АТФ (3 или 2) зависит от типа челночной системы. Следовательно, окисление до пирувата одной молекулы глицеральдегид-3-фосфата сопряжено с синтезом 5 молекул АТФ. Учитывая, что из глюкозы образуются 2 молекулы фосфотриозы, полученную величину нужно умножить на 2 и затем вычесть 2 молекулы АТФ, затраченные на первом этапе. Таким образом, выход АТФ при аэробном гликолизе составляет (5×2) — 2 = 8 АТФ.
Выход АТФ при аэробном распаде глюкозы до конечных продуктов[править | править код]
В результате гликолиза образуется пируват, который далее окисляется до СО2 и Н2О в общем пути катаболизма. Теперь можно оценить энергетическую эффективность гликолиза и общего пути катаболизма, которые вместе составляют процесс аэробного распада глюкозы до конечных продуктов.
Таким образом, выход АТФ при окислении 1 моль глюкозы до СО2 и Н2О составляет 38 моль АТФ.
В процессе аэробного распада глюкозы происходят 6 реакций дегидрирования. Одна из них протекает в гликолизе и 5 в ОПК. Субстраты для специфических НАД-зависимых дегидрогеназ: глицеральдегид-3-фосфат, пируват, изоцитрат, α-кетоглутарат, малат. Одна реакция дегидрирования в цитратном цикле под действием сукцинатдегидрогеназы происходит с участием кофермента ФАД. Общее количество АТФ, синтезированное путём окислительного фосфорилирования, составляет 17 моль АТФ на 1 моль глицеральдегидфосфата. К этому необходимо прибавить 3 моль АТФ, синтезированных путём субстратного фосфорилирования (две реакции в гликолизе и одна в цитратном цикле). Учитывая, что глюкоза распадается на 2 фосфотриозы и что стехиометрический коэффициент дальнейших превращений равен 2, полученную величину надо умножить на 2, а из результата вычесть 2 моль АТФ, использованные на первом этапе гликолиза.
| Этапы аэробного распада глюкозы | Количество использованного АТФ, моль | Количество синтезированного АТФ, моль |
|---|---|---|
| I. Аэробный гликолиз | ||
| Глюкоза → 2 Пируват | -2 | +10 |
| II. Окислительное декарбоксилирование пирувата | - | |
| 2 (Пируват → Ацетил-КоА) | +6 | |
| III. Цитратный цикл | ||
| 2 (Ацетил-КоА → СО2 + Н2О) | +24 | |
| Суммарный выход АТФ при окислении 1 моль глюкозы | +38 |
Значение катаболизма глюкозы[править | править код]
Основное физиологическое назначение катаболизма глюкозы заключается в использовании энергии, освобождающейся в этом процессе для синтеза АТФ. Энергия, выделяющаяся в процессе полного распада глюкозы до СО2 и Н2О, составляет 2880 кДж/моль. Если эту величину сравнить с энергией гидролиза высокоэнергетических связей — 38 моль АТФ (50 кДж на моль АТФ), то получим: 50×38 = 1900 кДж, что составляет 65 % от всей энергии, выделяющейся при полном распаде глюкозы. Такова эффективность использования энергии распада глюкозы для синтеза АТФ. Необходимо учитывать, что реальная эффективность процесса может быть ниже. Точно оценить выход АТФ можно только при субстратном фосфорилировании, а соотношение между поступлением водорода в дыхательную цепь и синтезом АТФ является приблизительным.
Аэробный распад глюкозы происходит во многих органах и тканях и служит основным, хотя и не единственным, источником энергии для жизнедеятельности. Некоторые ткани находятся в наибольшей зависимости от катаболизма глюкозы как источника энергии. Например, клетки мозга расходуют до 100 г глюкозы в сутки, окисляя её аэробным путём. Поэтому недостаточное снабжение мозга глюкозой или гипоксия проявляются симптомами, свидетельствующими о нарушении функций мозга (головокружения, судороги, потеря сознания).
Анаэробный распад глюкозы происходит в мышцах, в первые минуты мышечной работы, в эритроцитах (в которых отсутствуют митохондрии), а также в разных органах в условиях ограниченного снабжении их кислородом, в том числе в клетках опухолей. Для метаболизма клеток опухолей характерно ускорение как аэробного, так и анаэробного гликолиза. Но преимущественный анаэробный гликолиз и увеличение синтеза лактата служит показателем повышенной скорости деления клеток при недостаточной обеспеченности их системой кровеносных сосудов.
Кроме энергетической функции, процесс катаболизма глюкозы может выполнять и анаболические функции. Метаболиты гликолиза используются для синтеза новых соединений. Так, фруктозо-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата — структурного компонента нуклеотидов; 3-фосфоглицерат может включаться в синтез аминокислот, таких как серин, глицин, цистеин. В печени и жировой ткани ацетил-КоА, образующийся из пирувата, используется как субстрат при биосинтезе жирных кислот, холестерина, а дигидроксиацетонфосфат как субстрат для синтеза глицерол-3-фосфата.
Регуляция катаболизма глюкозы[править | править код]
Поскольку основное значение гликолиза состоит в синтезе АТФ, его скорость должна коррелировать с затратами энергии в организме.
Большинство реакций гликолиза обратимы, за исключением трёх, катализируемых гексокиназой (или глюкокиназой), фосфофруктокиназой и пируваткиназой. Регуляторные факторы, изменяющие скорость гликолиза, а значит и образование АТФ, направлены на необратимые реакции. Показателем потребления АТФ является накопление АДФ и АМФ. Последний образуется в реакции, катализируемой аденилаткиназой: 2 АДФ ↔ АМФ + АТФ
Даже небольшой расход АТФ ведёт к заметному увеличению АМФ. Отношение уровня АТФ к АДФ и АМФ характеризует энергетический статус клетки, а его составляющие служат аллостерическими регуляторами скорости как общего пути катаболизма, так и гликолиза. На рисунке показана аллостерическая регуляция скорости катаболизма глюкозы в скелетных мышцах.
Существенное значение для регуляции гликолиза имеет изменение активности фосфофруктокиназы, потому что этот фермент, как упоминалось ранее, катализирует наиболее медленную реакцию процесса.
Фосфофруктокиназа активируется АМФ, но ингибируется АТФ. АМФ, связываясь с аллостерическим центром фосфофруктокиназы, увеличивает сродство фермента к фруктозо-6-фосфату и повышает скорость его фосфорилирования. Эффект АТФ на этот фермент — пример гомотропного ашюстеризма, поскольку АТФ может взаимодействовать как с аллостерическим, так и с активным центром, в последнем случае как субстрат.
При физиологических значениях АТФ активный центр фосфофруктокиназы всегда насыщен субстратами (в том числе АТФ). Повышение уровня АТФ относительно АДФ снижает скорость реакции, поскольку АТФ в этих условиях действует как ингибитор: связывается с аллостерическим центром фермента, вызывает конформационные изменения и уменьшает сродство к его субстратам.
Изменение активности фосфофруктокиназы способствует регуляции скорости фосфорилирования глюкозы гексокиназой. Снижение активности фосфофруктокиназы при высоком уровне АТФ ведёт к накоплению как фруктозо-6-фосфата, так и глюкозо-6-фосфата, а последний ингибирует гексокиназу. Следует напомнить, что гексокиназа во многих тканях (за исключением печени и β-клеток поджелудочной железы) ингибируется глюкозо-6-фосфатом.
При высоком уровне АТФ снижается скорость цикла лимонной кислоты и дыхательной цепи. В этих условиях процесс гликолиза также замедляется. Следует напомнить, что аллостерическая регуляция ферментов ОПК и дыхательной цепи также связана с изменением концентрации таких ключевых продуктов, как НАДН, АТФ и некоторых метаболитов. Так, НАДН накапливаясь в том случае, если не успевает окислиться в дыхательной цепи, ингибирует некоторые аллостерические ферменты цитратного цикла.
Физиологическая роль гликолиза в печени и жировой ткани несколько иная, чем в других тканях. В печени и жировой ткани гликолиз в период пищеварения функционирует в основном как источник субстратов для синтеза жиров. Регуляция гликолиза в печени имеет свои особенности и будет рассмотрена ниже.
Бисфосфоглицератный цикл[править | править код]
В эритроцитах многих млекопитающих имеется фермент, позволяющий направить процесс в обход стадии, катализируемой фосфоглицераткиназой; при этом свободная энергия, обусловленная присутствием высокоэнергетического фосфата в молекуле бисфосфоглицерата[1,3-], рассеивается в форме теплоты. В большинстве тканей 2,3-БФГ образуется в небольших количествах. Дополнительный фермент бисфосфоглицератмутаза катализирует превращение 1,3-бисфосфоглицерата в бисфосфоглицерат[2,3-], последний далее превращается в фосфоглицерат[3-] (принято считать, что этой активностью обладает фосфоглицератмутаза). Потеря на этой стадии высокоэнергетического фосфата означает, что процесс гликолиза более не сопровождается производством АТФ. В этом может заключаться определенное преимущество, поскольку даже в тех случаях, когда потребности в AТФ минимальны, гликолиз может продолжаться. Образующийся 2,3-бисфосфоглицерат связывается с гемоглобином, понижая сродство последнего к кислороду то есть сдвигает кривую диссоциации оксигемоглобина вправо. Таким образом, присутствие 2,3-бисфосфоглицерата в эритроцитах способствует диссоциации кислорода из оксигемоглобина и переходу его в ткани.
Брожения[править | править код]
Брожение (также сбраживание, ферментация) — «это такой метаболический процесс, при котором регенерируется АТФ, а продукты расщепления органического субстрата могут служить одновременно и донорами, и акцепторами водорода»[6]. Брожение — это анаэробный (происходящий без участия кислорода) метаболический распад молекул питательных веществ, например глюкозы. По выражению Луи Пастера, «брожение — это жизнь без кислорода». Большинство типов брожения осуществляют микроорганизмы — облигатные или факультативные анаэробы.

Брожение не высвобождает всю имеющуюся в молекуле энергию, поэтому промежуточные продукты брожения могут использоваться в ходе клеточного дыхания.
- Термин брожение также используется в более широком смысле, для обозначения бурного роста микроорганизмов в соответствующей среде. При использовании в этом смысле не делается различия между аэробным и анаэробным метаболизмом.
Брожение часто используется для приготовления или сохранения пищи. Говоря о брожении, обычно имеют в виду брожение сахара (превращение его в спирт) с использованием дрожжей, но, к примеру, при производстве йогурта используются другие виды брожения.
Использование брожения человеком обычно предполагает применение определенных видов и штаммов микроорганизмов. Вина иногда улучшают с использованием процесса взаимного брожения.
Брожение — это процесс, важный в анаэробных условиях, в отсутствие окислительного фосфорилирования. В ходе брожения, как и в ходе гликолиза, образуется АТФ. Во время брожения пируват преобразуется в различные вещества.
Хотя на последнем этапе брожения (превращения пирувата в конечные продукты брожения) не освобождается энергия, он крайне важен для анаэробной клетки, поскольку на этом этапе регенерируется никотинамидадениндинуклеотид (НАД+), который требуется для гликолиза. Это важно для нормальной жизнедеятельности клетки, поскольку гликолиз для многих организмов — единственный источник АТФ в анаэробных условиях.
В ходе брожения происходит частичное окисление субстратов, при котором водород переносится на НАД+ (никотинамидадениндинуклеотид). В ходе других этапов брожения его промежуточные продукты служат акцепторами водорода, входящего в состав НАДН; в ходе регенерации НАД+ они восстанавливаются, а продукты восстановления выводятся из клетки.
Конечные продукты брожения содержат химическую энергию (они не полностью окислены), но считаются отходами, поскольку не могут быть подвергнуты дальнейшему метаболизму в отсутствие кислорода (или других высоко-окисленных акцепторов электронов) и часто выводятся из клетки. Следствием этого является тот факт, что получение АТФ брожением менее эффективно, чем путём окислительного фосфорилирования, когда пируват полностью окисляется до диоксида углерода. В ходе разных типов брожения на одну молекулу глюкозы получается от двух до четырёх молекул АТФ (ср. около 36 молекул путём аэробного дыхания). Однако даже у позвоночных брожение (анаэробное окисление глюкозы) используется как эффективный способ получения энергии во время коротких периодов интенсивной мышечной работы, когда перенос кислорода к мышцам недостаточен для поддержания аэробного метаболизма. Брожение у позвоночных помогает во время коротких периодов интенсивной работы, но не предназначено для длительного использования. Например, у людей гликолиз с образованием молочной кислоты дает энергию на период от 30 секунд до 2 минут. Скорость генерации АТФ примерно в 100 раз больше, чем при окислительном фосфорилировании. Уровень pH в цитоплазме быстро падает, когда в мышце накапливается молочная кислота, в конечном итоге ингибируя ферменты, вовлеченные в процесс гликолиза.
Спиртовое брожение[править | править код]
Спиртовое брожение осуществляется за счёт так называемых дрожжеподобных организмов, а также некоторых плесневых грибов и бактерий. Суммарную реакцию спиртового брожения можно изобразить следующим образом:
в результате которой, одна молекула глюкозы преобразуется в 2 молекулы этанола и в 2 молекулы углекислого газа и сопровождается запасанием энергии в виде АТФ.
Механизм реакции спиртового брожения чрезвычайно близок к гликолизу. Расхождение начинается лишь после этапа образования пирувата. При гликолизе пируват при участии фермента ЛДГ и кофермента НАДН восстанавливается в лактат. При спиртовом брожении этот конечный этап заменен двумя другими ферментативными реакциями — пируватдекарбоксилазной и алкогольдегидрогеназной.
В дрожжевых клетках пируват вначале подвергается декарбоксилированию, в результате чего образуется ацетальдегид. Данная реакция катализируется ферментом пируваткарбоксилазой (последняя отсутствует в тканях животных), который требует наличие ионов Mg2+ и кофермента — триаминпирофосфата (ТПФ).
Реакция необратимая.
Образовавшийся ацетальдегид присоединяет к себе водород, отщепляемый от НАДН, восстанавливаясь при этом в этанол. Реакция катализируется ферментом алкогольдегидрогеназой:
Таким образом, конечным продуктом спиртового брожения являются этанол и CO2, а не молочная кислота, как при гликолизе.
Молочнокислое брожение[править | править код]
Молочнокислое брожение — процесс анаэробного окисления углеводов, конечным продуктом при котором выступает молочная кислота.
Гомоферментативные бактерии (например, Lactobacillus delbruekii) расщепляют моносахариды с образованием двух молекул молочной кислоты в соответствии с суммарным уравнением[7]:
Название получило по характерному продукту — молочной кислоте. Для молочнокислых бактерий является основным путём катаболизма углеводов и основным источником энергии в виде АТФ. Также молочнокислое брожение происходит в тканях животных в отсутствие кислорода при больших нагрузках.
Маслянокислое брожение[править | править код]
Маслянокислое брожение — брожение глюкозы, в ходе которого образуется масляная кислота C3H7COOH. Оно протекает по уравнению:
При этом водород и углекислота являются побочными продуктами. В качестве побочных продуктов при этом также получаются этиловый и бутиловый спирты, уксусная кислота и др[8]. Маслянокислое брожение — результат деятельности анаэробных бактерий, в том числе рода Клостридиум. Как следует из названия, такое брожение связано с прогорканием жиров.
Лимоннокислое брожение[править | править код]
Лимоннокислым брожением называется окисление глюкозы грибами-микромицетами (например, Aspergillus niger) в лимонную кислоту. Конечный результат брожения можно представить следующим суммарным уравнением:
Химизм образования лимонной кислоты из сахара до настоящего времени окончательно не установлен. Большинство исследователей считает, что это брожение до образования пировиноградной кислоты протекает, как и другие брожения. Далее превращение пировиноградной кислоты в лимонную через ряд кислот (уксусную, янтарную, фумаровую, яблочную, щавелево-уксусную) сходно с превращениями в цикле Кребса[9].
Ацетоно-бутиловое брожение[править | править код]
Ацетоно-бутиловое брожение близко к масляному, однако при этом брожении образуется значительно больше бутилового спирта и ацетона:
Кроме того, в процессе ацетоно-бутилового брожения накапливаются этиловый спирт, масляная и уксусная кислоты, выделяются углекислый газ и водород. Химизм ацетоно-бутилового брожения сходен с маслянокислым брожением. Первые стадии — до образования ацетальдоля — аналогичны стадиям маслянокислого брожения[10].
Фруктоза и другие углеводы в процессе гликолиза[править | править код]
Установлено, что фруктоза, присутствующая в свободном виде во многих фруктах и образующаяся в тонком кишечнике из сахарозы, всасываясь в тканях, может подвергаться фосфорилированию во фруктозо-6-фосфат при участии фермента гексокиназы и АТФ.
Эта реакция ингибируется глюкозой. Образовавшийся фруктозо-6-фосфат либо превращается в глюкозу через стадии образования глюкозо-6-фосфата и последующего отщепления фосфорной кислоты, либо подвергается дальнейшим преобразованиям. Из фруктозо-6-фосфата под влиянием 6-фосфофруктокиназы и АТФ образуется фруктозо-1,6-дифосфат:
Далее фруктозо-1,6-дифосфат может подвергаться дальнейшим превращениям по пути гликолиза. Таков главный путь включения фруктозы в метаболизм мышечной ткани, почек, жировой ткани.
В печени, однако, для этого существует другой путь. Присутствующая в ней фруктокиназа катализирует фосфорилирование фруктозы не по 6-му, а по 1-му атому углерода:
В отличие от 1-й реакции, эта реакция не блокируется глюкозой. Затем под действием кетозо-1-фосфатальдолазы (альдолазы B) образовавшийся фруктозо-1-фосфат расщепляется с образованием D-глицеральдегида и дигидроксиацетонфосфата.
Галактоза в процессе гликолиза[править | править код]
Основным источником галактозы является лактоза пищи, которая в пищеварительном тракте расщепляется до галактозы и глюкозы. Обмен галактозы начинается с превращения её в галактозо-1-фосфат. Эта реакция катализируется галактокиназой с участием АТФ:
В следующей реакции в присутствии УДФ-глюкозы фермент гексозо-1-фосфатуридилилтрансфераза катализирует превращение галактозо-1-фосфата в глюкозо-1-фосфат, одновременно образуется уридиндифосфатгалактоза (УДФ-галактоза).
Нарушения метаболизма фруктозы[править | править код]
Нарушения метаболизма фруктозы, причиной которых является дефект ферментов, отражены в таблице
| Неактивный фермент | Блокируемая реакция | Локализация фермента | Клинические проявления и лабораторные данные |
|---|---|---|---|
| Фруктокиназа | Фруктоза + АТФ → Фруктозо-1-фосфат + АДФ | Печень, почки, энтероциты | Фруктоземия, фруктозурия |
| Фруктозо-1-фосфатальдолаза (альдолаза B) | Фруктозо-1-фосфат → Дигидроксиацетон-3 -фосфат + Глицеральдегид | Печень | Рвота, боли в животе, диарея, гипогликемия, гипофосфатемия, фруктоземия, гиперурикемия, хроническая недостаточность функций печени, почек. |
Недостаточность фруктокиназы клинически не проявляется. Фруктоза накапливается в крови и выделяется с мочой, где её можно обнаружить лабораторными методами. Очень важно не перепутать эту безвредную аномалию с сахарным диабетом. Данное заболевание известно как доброкачественная эссенциальная фруктозурия и встречается с частотой 1:130 000.
Наследственная непереносимость фруктозы, возникающая при генетически обусловленном дефекте фруктозо-1-фосфатальдолазы (альдолазы В), не проявляется, пока ребёнок питается грудным молоком, то есть пока пища не содержит фруктозы. Симптомы возникают, когда в рацион добавляют фрукты, соки, сахарозу. Рвота, боли в животе, диарея, гипогликемия и даже кома и судороги возникают через 30 мин после приёма пищи, содержащей фруктозу. У маленьких детей и подростков, продолжающих принимать фруктозу, развиваются хронические нарушения функций печени и почек. Непереносимость фруктозы — достаточно частая аутосомно-рецессивная форма патологии.
Дефект альдолазы фруктозо-1-фосфата сопровождается накоплением фруктозо-1-фосфата, который ингибирует активность фосфоглюкомутазы, превращающей глюкозо-1-фосфат в глюкозо-6-фосфат и обеспечивающей включение продукта гликогенфосфорилазной реакции в метаболизм. Поэтому происходит торможение распада гликогена на стадии образования глюкозо-1-фосфата, в результате чего развивается гипогликемия. Как следствие, ускоряется мобилизация липидов и окисление жирных кислот. Следствием ускорения окисления жирных кислот и синтеза кетоновых тел, замещающих энергетическую функцию глюкозы, может быть метаболический ацидоз, так как кетоновые тела являются кислотами и при высоких концентрациях снижают рН крови.
Результатом торможения гликогенолиза и гликолиза является снижение синтеза АТФ. Кроме того, накопление фосфорилированной фруктозы ведёт к нарушению обмена неорганического фосфата и гипофосфатемии.
Для пополнения внутриклеточного фосфата ускоряется распад адениловых нуклеотидов. Продукты распада этих нуклеотидов включаются в катаболизм, проходя стадии образования гипоксантина, ксантина и, наконец, мочевой кислоты. Повышение количества мочевой кислоты и снижение экскреции уратов в условиях метаболического ацидоза проявляются в виде гиперурикемии. Следствием гиперурикемии может быть подагра даже в молодом возрасте.
Нарушения метаболизма галактозы[править | править код]
Обмен галактозы особенно интересен в связи с наследственным заболеванием — галактоземией.
Галактоземия возникает при нарушении обмена галактозы, обусловленном наследственным дефектом любого из трёх ферментов, включающих галактозу в метаболизм глюкозы.
Галактоземия, вызванная недостаточностью галактозо-1-фосфатуридилтрансферазы (ГАЛТ), наиболее хорошо изучена. Это заболевание проявляется очень рано, и особенно опасно для детей, так как основным источником углеводов для них служит материнское молоко, содержащее лактозу. Ранние симптомы дефекта ГАЛТ: рвота, диарея, дегидратация, уменьшение массы тела, желтуха. Они появляются вскоре после рождения, как только ребёнок начинает получать молоко. В крови, моче и тканях повышается концентрация галактозы и галактозо-1-фосфата. В тканях глаза (в хрусталике) галактоза восстанавливается альдоредуктазой с образованием галактитола (дульцита). В этой реакции в качестве донора водорода используется
НАДФН. Восстановление галактозы происходит и в ходе нормального метаболизма, но протекает с небольшой скоростью. При галактоземии галактитол накапливается в стекловидном теле и связывает большое количество воды. Вследствие этого нарушается баланс электролитов, а чрезмерная гидратация хрусталика приводит к развитию катаракты, которая наблюдается уже через несколько дней после рождения.
Тяжёлые последствия дефекта ГАЛТ наблюдают в печени. Это связано с накоплением галактозо-1-фосфата и его токсическим действием на гепатоциты. В результате возникают нарушения функции печени: гепатомегалия, жировая дистрофия. В почках таких больных также повышена концентрация галактитола и галактозо-1-фосфата, что влияет на их функции. Отмечают нарушения в клетках полушарий головного мозга и мозжечка, в тяжёлых случаях — отёк мозга, задержку умственного развития, возможен летальный исход.
Для галактоземии, вызванной дефектом галактокиназы, тоже характерна катаракта, но при этом заболевании, в отличие от дефекта ГАЛТ, не отмечают нарушений функций печени, почек, мозга. Наиболее тяжёлые последствия снижения активности ГАЛТ связывают с влиянием галактозо-1-фосфата на активность других ферментов, участвующих в углеводном обмене (фосфоглюкомутазы, глюкозо-6-фосфатдегидрогеназы).
Нарушения обмена галактозы
| Дефектный фермент (частота) | Блокируемая реакция | Клинические проявления и лабораторные данные |
|---|---|---|
| Галактокиназа (1:500 000) | Галактоза + АТФ → Галактозо-1-фосфат + АДФ | Галактоземия, галактозурия, катаракта. Активность фермента в эритроцитах нормальная. |
| Галактозо-1-фосфатуридилтрансфераза (1:40000) | Галактозо-1-фосфат + УДФ-глюкоза → УДФ-галактоза + Глюкозо-1-фосфат | Галактоземия, галактозурия, галактозо-1-фосфатемия, катаракта. Тенденция к гипогликемии, компенсаторная мобилизация жиров, цирроз печени, нарушения функции почек. Гепатомегалия, задержка психического развития. Активность фермента в эритроцитах снижена. |
| Уридилфосфат-4-эпимераза (1:1000000) | УДФ-глюкоза ↔ УДФ-галактоза | Галактоземия, галактозурия. Тяжёлых клинических проявлений нет. Описаны единичные случаи заболевания |
Известно несколько форм галактоземии, причиной которой является недостаточность ГАЛТ[2]:
Некоторые варианты генетического дефекта ГАЛТ
| Изменения в структуре ГАЛТ | Проявления |
|---|---|
| Асн → Асп | Признак Дюарта. У гетерозигот при этом варианте активность фермента составляет 75 % от нормальной. Гомозиготный фенотип Дюарта обычно связан с 50 % потерей активности. Пациенты с синдромом Дюарта могут быть здоровыми, несмотря на структурную аномалию ГАЛТ. |
| Глн → Арг | Проявляется как тяжёлая галактоземия. Причина — мутация типа замены нуклеотида 591 в гене фермента. Активность ГАЛТ составляет 10 % от нормы. Эта форма встречается в 70 % случаев заболевания галактоземией среди европеоидов, частота — 1 :338 886. |
| Сер → Лей | Заболевание описано у чернокожих пациентов и названо «чёрный признак». Галактоземия проявляется как результат недостаточной активности ГАЛТ в печени и эритроцитах. Активность ГАЛТ в печени составляет 10 % от нормы. Тем не менее отмечалась утилизация некоторого количества галактозы, что объяснялось развитием альтернативного пути. Причина — мутация типа замены 1 158-го нуклеотида в гене фермента. |
| Арг → Три | Тяжёлая форма галактоземии. Причина — миссенс-мутация нуклеотида 1025 в гене фермента. Активность ГАЛТ отсутствует. |
| Лиз → Асн | Широко распространённая мутация при галактоземии[2]. |
Некоторые дефекты в строении ГАЛТ приводят лишь к частичной потере активности фермента. Поскольку в норме ГАЛТ присутствует в организме в избытке, то снижение его активности до 50 %, а иногда и ниже может клинически не проявляться.
При диагностике галактоземии исследуют мочу на содержание галактозы, собранную после нескольких кормлений молоком. При обнаружении у ребёнка катаракты его обследуют на недостаточность галактокиназы и ГАЛТ. Наличие галактозы в моче при отсутствии нарушений функции печени указывает на дефект галактокиназы. При обследовании проведение теста с нагрузкой галактозой не рекомендуется, так как этот тест опасен для больных. Лечение заключается в удалении галактозы из рациона.
Пентозофосфатный путь[править | править код]
Открытие пути прямого окисления углеводов, или, как его называют, пентозофосфатного цикла, принадлежит О. Варбургу, Ф. Липману, Ф. Диккенсу и В. А. Энгельгардту. Расхождение путей окисления углеводов — классического (цикл трикарбоновых кислот, или цикл Кребса) и пентозофосфатного — начинается со стадии образования гексозомонофосфата. Если глюкозо-6-фосфат, который фосфолируется второй раз и превращается во фруктозо-1,6-дифосфат, то в этом случае дальнейший распад углеводов происходит по обычному гликолитическому пути с образованием ПВК, которая, окисляясь до ацетил-KoA, затем сгорает в цикле Кребса. Ключевую роль в реакциях этого цикла играют пентозофосфаты.
Пентозофосфатный путь является альтернативным путём окисления глюкозы. Он включает несколько циклов, в результате функционирования которых из трёх молекул глюкозо-6-фосфата образуются три молекулы СО2 и три молекулы пентоз. Последние используются для регенерации двух молекул глюкозо-6-фосфата и одной молекулы глицеральдегид-3-фосфата. Поскольку из двух молекул глицеральдегид-3-фосфата можно регенерировать молекулу глюкозо-6-фосфата, глюкоза может быть полностью окислена при превращении по пентозофосфатному пути:
Ферменты пентозофосфатного пути, так же, как и ферменты гликолиза, локализованы в цитозоле.
Наиболее активно пентозофосфатный путь протекает в жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации, семенниках.
Последовательность реакций[править | править код]
Ферменты пентозофосфатного пути локализованы во внемитохондриальном пространстве клетки — в цитозоле. Как и в процессе гликолиза, окисление осуществляется путём дегидрогенирования, однако акцептором водорода в этом случае служит не НАД, a НАДФ. Последовательность реакций пути можно разделить на две фазы: окислительную и неокислительную. В реакциях первой фазы глюкозо-6-фосфат дегидрогенируется и декарбоксилируется с образованием рибулозо-5-фосфата. В ходе второй фазы рибулозо-5-фосфат превращается снова в глюкозо-6-фосфат в результате серии реакций, в которых главную роль играют два фермента: транскетолаза и трансальдолаза.

Окислительная фаза[править | править код]
В окислительной части пентозофосфатного пути глюкозо-6-фосфат подвергается окислительному декарбоксилированию, в результате которого образуются пентозы. Этот этап включает 2 реакции дегидрирования.
Дегидрирование глюкозо-6-фосфата[править | править код]
Первая реакция дегидрирования — превращение глюкозо-6-фосфата в глюконолактон-6-фосфат — катализируется НАДФ+-зависимой глюкозо-6-фосфатдегидрогеназой и сопровождается окислением альдегидной группы у первого атома углерода и образованием одной молекулы восстановленного кофермента НАДФН.
Дегидрогеназа глюкозо-6-фосфата — димер с молекулярной массой около 135 000. Имеется 7-8 изоферментов этого фермента, разделяющихся при электрофорезе.
Дегидрирование 6-фосфоглюконата с образованием рибулозо-5-фосфата[править | править код]
Эта реакция катализируется ферментом — 6-фосфоглюконат-дегидрогеназой по уравнению:
Равновесие реакции сдвинуто вправо. 6-Фосфоглюконат-дегидрогеназа — димер с молекулярной массой около 100 тыс. Имеется несколько изоферментов этой дегидрогеназы. Особенность реакции заключается в том, что при дегидрировании образуется нестойкое промежуточное соединение, которое на поверхности этого же фермента декарбоксилируется. Это вторая реакция окисления в пентозофосфатном цикле, приводящая к образованию НАДФ·Н2.
Суммарное уравнение окислительного этапа пентозофосфатного пути можно представить в виде:
Глюкозо-6-фосфат + 2НАДФ+ + Н2О = Рибулозо-5-фосфат + 2НАДФН + Н+ + СО2.
Реакции окислительного этапа служат основным источником НАДФН в клетках. Гидрированные коферменты снабжают водородом биосинтетические процессы, окислительно-восстановительные реакции, включающие защиту клеток от активных форм кислорода. НАДФН как донор водорода участвует в анаболических процессах, например в синтезе холестерина. Это источник восстановительных эквивалентов для цитохрома Р450, катализирующего образование гидроксильных групп при синтезе стероидных гормонов, жёлчных кислот, при катаболизме лекарственных веществ и других чужеродных соединений. Высокая активность фермента глюкозо-6-фосфатдегидрогеназы обнаружена в фагоцитирующих лейкоцитах, где НАДФН-оксидаза использует восстановленный НАДФН для образования супероксидного иона из молекулярного кислорода. Супероксидный ион генерирует другие активные формы кислорода, под действием которых и повреждаются молекулы ДНК, белков, липидов бактериальньж клеток. Синтез жирных кислот из углеводов в печени является основным путём утилизации НАДФН и обеспечивает регенерацию окисленной формы НАДФ+. В печени глюкозо-6-фосфатдегидрогеназа, как и ключевые ферменты гликолиза и биосинтеза жирных кислот, индуцируется при увеличении соотношения инсулин/глюкагон после приёма богатой углеводами пищи.
Несмотря на то, что НАДФН образуется также при окислении малата до пирувата и диоксида углерода (при участии НАДФ+-зависимой малатдегидрогеназы) и дегидрировании изо-цитрата (при участии НАДФ+ -зависимой изоцитратдегидрогеназы), в большинстве случаев потребности клеток в восстановительных эквивалентах удовлетворяются за счёт пентозофосфатного пути.
Реакции окислительного пути протекают только в том случае, если восстановленный кофермент НАДФН возвращается в исходное окисленное состояние НАДФ+ при участии НАДФН-зависимых дегидрогеназ (то есть при условии использования гидрированного НАДФН в восстановительных процессах). Если потребности клетки в НАДФН незначительны, рибозо-5-фосфат образуется в результате обратимых реакций неокислительного этапа пентозофосфатного пути, используя в качестве исходных веществ метаболиты гликолиза — глицеральдегид-3-фосфат и фруктозо-6-фосфат.
Неокислительная фаза[править | править код]
Неокислительная фаза пентозофосфатного пути включает серию обратимых реакций, в результате которых рибулозо-5-фосфат превращается в рибозо-5-фосфат и ксилулозо-5-фосфат, и далее за счёт переноса углеродных фрагментов в метаболиты гликолиза — фруктозо-6-фосфат и глицеральдегид-3-фосфат. В этих превращениях принимают участие ферменты: эпимераза, изомераза, транскетолаза и трансальдолаза. Транскетолаза в качестве кофермента использует тиаминдифосфат. Неокислительный этап пентозофосфатного пути не включает реакции дегидрирования и поэтому используется только для синтеза пентоз.
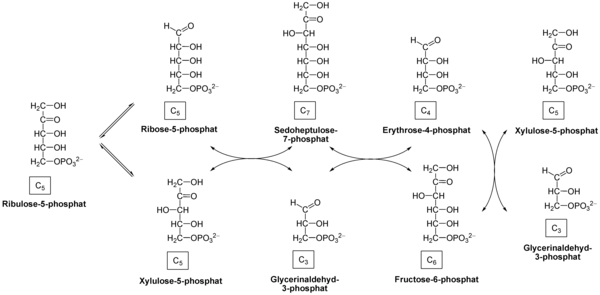
Гидролиз 6-фосфоглюконолактона с образованием 6-фосфоглюконата[править | править код]
Образовавшийся в результате 1-й реакции глюконолактон-6-фосфат быстро превращается в 6-фосфоглюконат при участии фермента глюконолактонгидратазы.
Взаимопревращение, или изомеризация, пентозофосфатов[править | править код]
Рибулозо-5-фосфат может обратимо изомеризоваться в другие пентозофосфаты — ксилулозо-5-фосфат и рибозо-5-фосфат. катализируют эти реакции два разных фермента: пентозофосфат-эпимераза и пентозофосфат-изомераза по уравнениям:
Образование из рибулозо-5-фосфата двух других пентозофосфатов — ксилулозо-5-фосфата и рибозо-5-фосфата необходимо для последующих реакций цикла. Причём требуется две молекулы ксилулозо-5-фосфата и одна молекула рибозо-5-фосфата.
Первая транскетолазная реакция[править | править код]
В этой реакции, катализируемой транскетолазой, используется образовавшиеся в предыдущей реакции пентозофосфаты:
Транскетолаза — димер с молекулярной массой 140 000. Реакция требует ионов Mg2+. Коферментом в транскетолазной реакции служит ТПФ, играющий роль промежуточного переносчика гликольальдегидной группы от ксилулозо-5-фосфата к рибозо-5-фосфату. В результате образуется семиуглеродный моносахарид седогептулозо-7-фосфат и глицеральдегид-3-фосфат. Оба продукта транскетолазной реакции используются на следующей стадии цикла в качестве субстратов.
Перенос дигидроксиацетонового фрагмента с седогептулозо-7-фосфата на глицеральдегид-3-фосфат[править | править код]
Фермент трансальдолаза катализирует перенос остатка диоксиацетона (но не свободного диоксиацетона) от седогептулозо-7-фосфата на глицеральдегид-3-фосфат. Эта обратимая реакция:
Трансальдолаза — димер с молекулярной массой около 70 000 Да. Молекула фруктозо-6-фосфата, образующаяся в этой реакции, подключается к гликолизу, а эритрозо-4-фосфат используется как субстрат для последующих стадий цикла.
Вторая транскетолазная реакция[править | править код]
Эта реакция сродни первой транскетолазной реакции и катализируется тем же ферментом. Отличие её в том, что акцептором гликолевого альдегида служит эритрозо-4-фосфат.
Фруктозо-6-фосфат и глицеральдегид-3-фосфат подключаются к гликолизу.
Так как все реакции неокислительного этапа обратимы, образование рибозо-5-фосфата может происходить не только в результате изомерного превращения продукта окислительной фазы пентозофосфатного пути рибулозо-5-фосфата в рибозо-5-фосфат под действием изомеразы, но также и из промежуточных продуктов гликолиза — фруктозо-6-фосфата и глицеральдегид-3-фосфата. Последовательность превращений, приводящих к образованию рибозо-5-фосфата из таких продуктов гликолитического пути, можно представить в виде:
2Фруктозо-6-фосфат + Глицеральдегид-3-фосфат = 2Ксилулозо-5-фосфат + Рибозо-5-фосфат + 2Ксилулозо-5-фосфат = 2Рибулозо-5-фосфат + 2Рибулозо-5-фосфат = 2Рибозо-5-фосфат.
Суммарный результат метаболизма 3 молекул рибулозо-5-фосфата в неокислительной фазе пентозофосфатного пути — образование 2 молекул фруктозо-6-фосфата и 1 молекулы глицеральдегид-3-фосфата. Далее фруктозо-6-фосфат и глицеральдегид-3-фосфат могут превратиться в глюкозу. С учётом стехиометрического коэффициента, равного 2, для образования 5 молекул глюкозы (содержащих 30 атомов углерода) потребуются 4 молекулы фруктозо-6-фосфата и 2 молекулы глицеральдегид-3-фосфата (в сумме содержащие также 30 атомов углерода) или, соответственно, 6 молекул рибулозо-5-фосфата. Таким образом, неокислительный путь можно представить как процесс возвращения пентоз в фонд гексоз.
Пентозофосфатный цикл[править | править код]
Окислительный этап образования пентоз и неокислительный этап (путь возвращения пентоз в гексозы) составляют вместе циклический процесс.
Такой процесс можно описать общим уравнением:
6Глюкозо-6-фосфат + 12НАДФ+ + 6Н2О = 5Глюкозо-6-фосфат + 12НАДФН + 12Н+ + 6СO2.
Шесть молекул глюкозо-6-фосфата, вступая в пентозофосфатный цикл, образуют 6 молекул рибулозо-5-фосфата и 6 молекул СО2, после чего из 6 молекул рибулозо-5-фосфата снова регенерируется 5 молекул глюкозо-6-фосфата. Однако это не означает, что молекула глюкозо-6-фосфата, вступающая в цикл, полностью окисляется. Все 6 молекул СО2 образуются из С1-атомов 6 молекул глюкозо-6-фосфата.
Протекание пентозофосфатного цикла позволяет клеткам продуцировать НАДФН, необходимый для синтеза жиров, не накапливая пентозы.
Энергия, выделяющаяся при распаде глюкозы, трансформируется в энергию высокоэнергетического донора водорода — НАДФН. Гидрированный НАДФН служит источником водорода для восстановительных синтезов, а энергия НАДФН преобразуется и сохраняется во вновь синтезированных веществах, например жирных кислотах, высвобождается при их катаболизме и используется клетками.
В последние годы появились работы, которые дают основание предполагать, что в некоторых тканях схема пентозофосфатного превращения углеводов сложнее, чем это представлено схемой (смотрите выше). Согласно этой более полной схеме пентозофосфатного пути, первые этапы превращения совпадают с прежней схемой, однако после первой транскетолазной реакции начинаются некоторые отклонения.
Считают, что пентозофосфатный путь и гликолиз, протекающие в цитозоле, взаимосвязаны и способны переключаться друг на друга в зависимости от соотношения концентраций промежуточных продуктов, образовавшихся в клетке.
Взаимосвязь пентозофосфатного цикла и гликолиза[править | править код]
Оба превращения углеводов тесно связаны. продукты пентозофосфатного пути — фруктозо-6-фосфата и глицеральдегид-3-фосфат — являются также метаболитами гликолиза, поэтому они вовлекаются в гликолизе и превращаются его ферментами. Две молекулы фруктозо-6-фосфата могут регенерироваться в две молекулы глюкозо-6-фосфата с помощью глюкофосфатизомеразы — фермента гликолиза. В этом случае пентозофосфатный путь выглядит как цикл. Другой продукт — глицеральдегид-3-фосфат, включившись в гликолиз, превращается в анаэробных условиях в лактат, а в аэробных сгорает до CO2 и H2O[11].
Сравнение с гликолизом[править | править код]
Пентозофосфатный путь существенно отличается от гликолиза. Окисление осуществляется на первой стадии, и в нём участвует не НАД, как в гликолизе, a НАДФ; одним из продуктов пентозофосфатного пути является СО2, который в реакциях гликолиза не образуется. Наконец, пентозофосфатный путь не генерирует АТФ.
Образование рибозы[править | править код]
Пентозофосфатный путь поставляет рибозу для синтеза нуклеотидов и нуклеиновых кислот. Источником рибозы является интермедиат рибозо-5-фосфат, который в реакции с АТФ образует PRPP — 5-фосфорибозил-1-пирофосфат, используемый в биосинтезе нуклеотидов. Мышечная ткань содержит очень малые количества глюкозо-6-фосфатдегидрогеназы и 6-фосфоглюконатдегидрогеназы. Тем не менее скелетная мышца способна синтезировать рибозу. Вероятно, это осуществляется при обращении неокислительной фазы пентозофосфатного пути, утилизирующей фруктозо-6-фосфат. Таким образом, синтез рибозы может осуществляться в ткани, если в ней протекает часть реакций пентозофосфатного пути.
Биологическая функция пентозофосфатного цикла[править | править код]
Пентозофосфатный цикл не приводит к синтезу АТФ, он выполняет две главные функции:
- образование НАДФН для восстановительных синтезов, таких, как синтез жирных кислот и стероидов;
- Обеспечение рибозой синтеза нуклеотидов и нуклеиновых кислот.
Регуляция[править | править код]
Судьба глюкозо-6-фосфата — вступит ли он в гликолиз или пентозофосфатный путь — определяется потребностями клетки в данный момент, а также концентрацией НАДФ+ в цитозоле. Без наличия акцептора электронов первая реакция пентозофосфатного пути (катализируемая глюкозо-6-фосфатдегидрогеназой) не будет идти. Когда клетка быстро переводит НАДФН в НАДФ+ в биосинтетических восстановительных реакциях, уровень НАДФ+ поднимается, аллостерически стимулируя глюкозо-6-фосфатдегидрогензазу и тем самым увеличивая ток глюкозо-6-фосфата через пентозофосфатный путь. Когда потребление НАДФН замедляется, уровень НАДФ+ снижается, и глюкозо-6-фосфат утилизируется гликолитически[12].
Метилглиоксалевый шунт[править | править код]
Метилглиоксалевый шунт — метаболический путь, встречающийся у некоторых бактерий и представляющий собой отличный от гликолитических реакций путь окисления дигидроксиацетонфосфата до пирувата[13]. Метилглиоксаль был обнаружен в тканевых автолизатах полвека назад. Позднее было убедительно доказано широкое распространение глиоксалазы, катализирующей превращение метилглиоксаля в лактат. Однако смысл этих данных оставался непонятным, поскольку источник метилглиоксаля не был выявлен. Это соединение приобрело новое значение в связи с описанием метилглиоксальсинтазы, изолированной из Е. coli и P. vulgaris.
Аэробный метаболизм пирувата[править | править код]
Клетки недостаточно снабжаемые кислородом, могут частично или полностью существовать за счет энергии гликолиза. Однако большинство животных и растительных клеток в норме в аэробных условиях и все своё «органическое топливо» окисляет до углекислого газа и воды. В этих условиях пируват, образовавшийся при расщеплении глюкозы, не восстанавливается до лактата, а постепенно окисляется до CO2 и H2O в аэробной стадии катаболизма, при этом первоначально происходит окислительное декарбоксилирование пирувата с образованием ацетил-КоА.
Окислительное декарбоксилирование пирувата[править | править код]
Пируватдегидрогеназный комплекс (PDH)
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединённых структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
На I стадии этого процесса пируват теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1-ТПФ-СНОН-СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидролипоилацетилтрансферазой (Е2). Этот фермент катализирует III стадию — перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид-Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидролипоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+.
Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нём принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, дигидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 коферментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, липоамид-Е2 и ФАД-Е3), а два — легко диссоциируют (HS-KoA и НАД).
Все эти ферменты, имеющие субъединичное строение, и коферменты организованы в единый комплекс. Поэтому промежуточные продукты способны быстро взаимодействовать друг с другом. Показано, что составляющие комплекс полипептидные цепи субъединиц дигидролипоил-ацетилтрансферазы составляют как бы ядро комплекса, вокруг которого расположены пируватдегидрогеназа и дигидролипоилдегидрогеназа. Принято считать, что нативный ферментный комплекс образуется путём самосборки.
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:
Пируват + НАД+ + HS-KoA = Ацетил-КоА + НАДН + Н+ + СO2.
Реакция сопровождается значительным уменьшением стандартной свободной энергии и практически необратима.
Образовавшийся в процессе окислительного декарбоксилирования ацетил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса). Этот процесс, так же как окислительное декарбоксилирование пирувата, происходит в митохондриях клеток.
Клинические аспекты метаболизма пирувата[править | править код]
Арсенат, а также ионы ртути образуют комплексы с —SH-группами липоевой кислоты и ингибируют пируватдегидрогеназу; при недостаточном содержании тиамина в диете активность пируватдегидрогеназы снижается и пируват может накапливаться. Недостаток тиамина возникает у алкоголиков с нарушенным режимом питания; при введении им глюкозы может происходить быстрое накопление пирувата и лактата, приводящее к лактатацидозу, нередко с летальным исходом. У больных с наследственной недостаточностью пируватдегидрогеназы также может развиваться лактатацидоз, особенно после глюкозной нагрузки. Зарегистрированы мутации практически всех ферментов углеводного метаболизма, и в каждом случае их следствием является заболевание человека.
Взаимопревращения гексоз[править | править код]
Процесс взаимопревращения или изомеризации является реакция, приводящая к обратимому равновесию между α-D и β-D-формами гексоз, например, глюкозы. Этот процесс аномеризации протекает при физиологических значениях pH очень большой скоростью. Тем не менее существуют целый ряд специфических ферментов (муторотазы, альдозоизомеразы) ещё более его ускоряющие.
Энергетика окисления углеводов[править | править код]
При сжигании в калориметре 1 моль глюкозы с образованием СО2 и Н2О выделяется приблизительно 2780 кДж теплоты. Когда окисление глюкозы происходит в тканях, часть высвобождаемой энергии не теряется в форме теплоты, а «улавливается» в виде высокоэнергетических фосфатных связей. На молекулу глюкозы, окисляющуюся до СО2 и Н2О, образуется примерно 38 высокоэнергетических фосфатных связей. Если принять, что энергия высокоэнергетической связи равна 30,5 кДж, то суммарная энергия, запасаемая в форме АТФ, составит 1159 кДж на 1 моль глюкозы (приблизительно 41,7 % от энергии сгорания). Большая часть АТФ образуется в процессе окислительного фосфорилирования при окислении восстановленных коферментов дыхательной цепью. Другая часть АТФ образуется в результате фосфорилирования, происходящего «на субстратном уровне».
Анаболизм глюкозы[править | править код]
Анаболизм глюкозы — образование глюкозы в организме, под действием ферментативных процессов, в основном из неуглеводных продуктов, таких как — ПВК, лактата и др.
Глюконеогенез[править | править код]

Глюконеогенез — синтез глюкозы из неуглеводных источников. Например: анаэробная фаза расщепления глюкозы — гликолиз — заканчивается образованием ПВК или лактата. Они при определённых условиях (при голоде и т. д.) могут вновь ресинтезироваться в глюкозу. Из двух молекул молочной кислоты образуется одна молекула глюкозы, то есть происходит как бы обращение гликолиза. Это означает, что глюконеогенез — процесс противоположный гликолизу. Однако у гликолиза существуют четыре необратимые стадии, протекающие с выделением значительного количества энергии, поэтому глюконеогенез идет в обход этих стадий.
Кребс отметил, что простому обращению гликолиза препятствуют энергетические барьеры на ряде стадий: 1) и 2) между пируватом и фосфоенолпируватом, 3) между фруктозо-1,6-дисфосфатом и фруктозо-6-фосфатом, 4) между глюкозо-6-фосфатом и глюкозой, а также между глюкозо-1-фосфатом и гликогеном. Эти барьеры обходятся с помощью специальных реакций.

- Первая необратимая стадия
Первой необратимой реакцией глюконеогенеза — является превращение пирувата в оксалоацетат под действием фермента пируваткарбоксилаза, CO2 и АТФ. Реакция протекает в митохондриях, куда проникает пируват, и катализируется пируваткарбоксилазой по уравнению:
Пируват + НСО3- + АТФ → оксалоацетат + AДФ + Фi
Этот фермент в качестве кофактора, как и ферменты, усваивающие CO2, содержит, биотин.
- Вторая необратимая стадия
На этой стадии образовавшийся в 1-й стадии оксалоацетат поступает из митохондрий в цитоплазму, где подвергается декарбоксилированию и фосфорилированию под влиянием фермента фосфоенолпируваткарбоксикиназы превращается в фосфоенолпируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат (ГТФ).
От фосфоенолпирувата до фруктозо-1,6-дифосфата все реакции гликолиза обратимы, поэтому молекулы образовавшегося фосфоенолпирувата используются для образования фруктозо-1,6-дифосфата теми же ферментами гликолиза.
- Третья необратимая стадия
Третья необратимая стадия глюконеогенеза это — превращение фруктозо-1,6-дисфосфата во фруктозо-6-фосфат, необходимое для обращения гликолиза на рассматриваемой стадии, катализируется специфическим ферментом фруктозо-1,6-дисфосфатазой. Это — ключевой фермент в том смысле, что именно его присутствием определяется, способна ли ткань ресинтезировать гликоген из пирувата и триозофосфатов. Этот фермент имеется в печени и почках, он был также обнаружен в поперечнополосатых мышцах. Считают, что в сердечной мышце и гладких мышцах он отсутствует.
Фруктозо-6-фосфат изомеризуется в глюкозо-6-фосфат глюкозофосфатизомеразой.
- Четвёртая необратимая стадия
Четвёртая и последняя необратимая стадия глюконеогенеза это — превращение глюкозо-6-фосфата в глюкозу. Реакция катализируется другой специфической фосфатазой — глюкозо-6-фосфатазой (реакция идет в обход гексокиназной реакции). Она присутствует в печени и почках, но отсутствует в мышцах и жировой ткани. Наличие этого фермента позволяет ткани поставлять глюкозу в кровь.
При распаде гликогена образуется глюкозо-1-фосфат[править | править код]
Распад гликогена с образованием глюкозо-1-фосфата осуществляется фосфорилазой. Синтез гликогена идет по совершенно другому пути, через образование уридиндифосфатглюкозы, и катализируется гликогенсинтазой.
На примере глюконеогенеза можно видеть экономичность организации путей обмена, поскольку помимо 4-х специальных ферментов глюконеогенеза: пируваткарбоксилазы, фосфоенолпируваткарбоксилазы, фруктозо-1,6-дифосфатазы и глюкозо-6-фосфатазы для новообразования глюкозы используются отдельные ферменты гликолиза.
Синтез глюкозы из лактата[править | править код]
Лактат, образованный в анаэробном гликолизе, не является конечным продуктом метаболизма. Использование лактата связано с его превращением в печени в пируват. Лактат как источник пирувата важен не столько при голодании, сколько при нормальной жизнедеятельности организма. Его превращение в пируват и дальнейшее использование последнего являются способом утилизации лактата.
Лактат, образовавшийся в интенсивно работающих мышцах или в клетках с преобладающим анаэробным способом катаболизма глюкозы, поступает в кровь, а затем в печень. В печени отношение НАДН/НАД+ ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в обратном направлении, то есть в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту последовательность событий называют «глюкозо-лактатным циклом», или «циклом Кори». Цикл Кори выполняет 2 важнейшие функции:
- — обеспечивает утилизацию лактата;
- — предотвращает накопление лактата и, как следствие этого, опасное снижение рН (лактоацидоз). Часть пирувата, образованного из лактата, окисляется печенью до СО2 и Н2О. Энергия окисления может использоваться для синтеза АТФ, необходимого для реакций глюконеогенеза.
Лактатацидоз[править | править код]
Термин «ацидоз» обозначает увеличение кислотности среды организма (снижение рН) до значений, выходящих за пределы нормы. При ацидозе либо увеличивается продукция протонов, либо происходит снижение их экскреции (в некоторых случаях и то и другое). Метаболический ацидоз возникает при увеличении концентрации промежуточных продуктов обмена (кислотного характера) вследствие увеличения их синтеза или уменьшения скорости распада или выведения. При нарушении кислотно-основного состояния организма быстро включаются буферные системы компенсации (через 10-15 мин). Лёгочная компенсация обеспечивает стабилизацию соотношения гидрокарбонатного буфера НСО3-/Н2СО3, которая в норме соответствует 1:20, а при ацидозе уменьшается. Лёгочная компенсация достигается увеличением объёма вентиляции и, следовательно, ускорением выведения СО2 из организма. Однако основную роль в компенсации ацидоза играют почечные механизмы с участием аммиачного буфера. Одной из причин метаболического ацидоза может быть накопление молочной кислоты. В норме лактат в печени превращается обратно в глюкозу путём глюконеогенеза либо окисляется. Кроме печени, другим потребителем лактата служат почки и сердечная мышца, где лактат может окисляться до СО2 и Н2О и использоваться как источник энергии, особенно при физической работе.
Уровень лактата в крови — результат равновесия между процессами его образования и утилизации. Кратковременный компенсированный лактатацидоз встречается довольно часто даже у здоровых людей при интенсивной мышечной работе. У нетренированных людей лактатацидоз при физической работе возникает как следствие относительного недостатка кислорода в мышцах и развивается достаточно быстро. Компенсация осуществляется путём гипервентиляции.
При некомпенсированном лактоацидозе содержание лактата в крови увеличивается до 5 ммоль/л (в норме до 2 ммоль/л). При этом рН крови может составлять 7,25 и менее (в норме 7,36-7,44)
Повышение содержания лактата в крови может быть следствием нарушения метаболизма пирувата.
Так, при гипоксии, возникающей вследствие нарушения снабжения тканей кислородом или кровью, уменьшается активность пируватдегидрогеназного комплекса и снижается окислительное декарбоксилирование пирувата. В этих условиях равновесие реакции пируват ↔ лактат сдвинуто в сторону образования лактата. Кроме того, при гипоксии уменьшается синтез АТФ, что следовательно, ведёт к снижению скорости глюконеогенеза — другого пути утилизации лактата. Повышение концентрации лактата и снижение внутриклеточного рН отрицательно влияют на активность всех ферментов, в том числе и пируваткарбоксилазы, катализирующей начальную реакцию глюконеогенеза.
Возникновению лактатацидоза также способствуют нарушения глюконеогенеза при печёночной недостаточности различного происхождения. Кроме того, лактоацидозом может сопровождаться гиповитаминоз В1, так как производное этого витамина тиаминдифосфат выполняет коферментную функцию в составе пируватдекарбоксилазы (ПДК) при окислительном декарбоксилировании пирувата. Дефицит тиамина может возникать, например, у алкоголиков с нарушенным режимом питания.
Итак, причинами накопления молочной кислоты и развития лактатацидоза могут быть:
- активация анаэробного гликолиза вследствие тканевой гипоксии различного происхождения;
- поражения печени (токсические дистрофии, цирроз и др.);
- нарушение использования лактата вследствие наследственных дефектов ферментов глюконеогенеза, недостаточности глюкозо-6-фосфатазы;
- нарушение работы ПДК вследствие дефектов ферментов или гиповитаминозов;
- применение ряда лекарственных препаратов, например бигуанидов (блокаторы глюконеогенеза, используемые при лечении сахарного диабета).
Глюконеогенез из других неуглеводных источников[править | править код]
Субстратами для синтеза глюкозы служат не только пируват или лактат, поступающие в печень и почки, но и другие неуглеводные соединения.
Синтез глюкозы из аминокислот[править | править код]
В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, оксалоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратного цикла, так и глюконеогенеза.
Из всех аминокислот, поступающих в печень, примерно 30 % приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюконеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в мышцах → аланин в печени → глюкоза в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
Синтез глюкозы из глицерина[править | править код]
Глицерин образуется при гидролизе триацилглицеринов (жиров), главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицерол киназа, например печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерина в α-глицерофосфат (глицерол-3-фосфат). При включении глицерол-3-фосфата в глюконеогенез происходит его дегидрирование НАД-зависимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.
Глюконеогенез требует значительных затрат энергии[править | править код]
В таблице представлены реакции, ведущие от пирувата к глюкозе крови. Суммарная реакция имеет вид:
2Пируват + 4АТФ + 2ГТФ + 2НАДН + 2Н+ + 4Н2О → Глюкоза + 2НАД+ + 4АДФ + 2ГДФ + 6Фi.
| Последовательные реакции глюконеогенеза, ведущие от пирувата к глюкозе | Количество повторенных реакций* |
|---|---|
| Пируват + СО2 + АТФ → Оксалоацетат + АДФ + Фi | х 2 |
| Оксалоацетат + ГТФ ↔ Фосфоенолпируват + СО2 + ГДФ | x 2 |
| Фосфоенолпируват + Н2О ↔ 2-фосфоглицерат | x 2 |
| 2-фосфоглицерат ↔ 3-фосфоглицерат | x 2 |
| 3-фосфоглицерат + АТФ ↔ 3-фосфоглицероилфосфат + АДФ | x 2 |
| 3-фосфоглицероилфосфат + НАДН + Н+ → Глицеральдегид-3-фосфат + НАД+Фi | x 2 |
| Глицеральдегид-3-фосфат ↔ Дигидроксиацетонфосфат | x 2 |
| Глицеральдегид-3-фосфат + Дигидроксиацетонфосфат ↔ Фруктозо-1,6-дифосфат | x 2 |
| Фруктозо-1,6-дифосфат + Н2О → Фруктозо-6-фосфат + Фi | x 2 |
| Фруктозо-6-фосфат ↔ Глюкозо-6-фосфат | x 2 |
| Глюкозо-6-фосфат + Н2О — Глюкоза + Фi | x 2 |
| Суммарная реакция:
2Пируват + 4АТФ + 2ГТФ + 2НАДН + 2Н+ + 4Н2О → Глюкоза + 2НАД+ + 4АДФ + 2ГДФ + 6Фi | |
| *Цифры справа указывают, что данная реакция должна быть повторена дважды, потому что для образования одной молекулы глюкозы
требуется два трёхуглеродных предшественника[14]. |
На каждую молекулу глюкозы, образующуюся из пирувата, расходуется шесть высокоэнергетических фосфатных групп — четыре от АТФ и две от ГТФ. Кроме того, для восстановительных этапов требуются ещё две молекулы НАДH. Ясно, что это уравнение не является простым обращением уравнения, описывающего превращение глюкозы в пируват в процессе гликолиза, поскольку такое превращение сопровождается образованием всего лишь двух молекул АТФ[14]: Глюкоза + 2АДФ + 2Фi + 2НАД+ → 2Пируват + 2АТФ + 2НАДН + 2Н+ + 2Н2О.
Таким образом, синтез глюкозы из пирувата обходится организму довольно дорого. Однако немалая часть этой платы расходуется лишь на то, чтобы обеспечить необратимость глюконеогенеза. В условиях, существующих в клетке, в которых величина ΔGP для АТФ может достигать 16 ккал/моль, общее изменение свободной энергии в процессе гликолиза составляет по меньшей мере — 15 ккал/моль. В тех же условиях общее изменение свободной энергии при глюконеогенезе (синтезе глюкозы из пирувата) выражается гораздо большей величиной. Поэтому в нормальных внутриклеточных условиях и гликолиз, и глюконеогенез представляют собой необратимые процессы[14].
«Холостые» циклы в метаболизме углеводов[править | править код]
В нормальных условиях холостые циклы, вероятно, не имеют места, так как их появлению препятствуют реципрокные регуляторные механизмы (механизмы обратного направления). Всякий раз, когда преобладает катаболизм, то есть когда суммарный поток направлен в сторону гликолиза, фруктозодифосфатазная активность выключается. И наоборот, когда суммарный поток направлен в сторону глюконеогенеза, выключается фосфофруктокиназа.
Недавние исследования показали, однако, что иногда холостые циклы могут происходить и в физиологических условиях, имея при этом вполне определенный биологический смысл — производство тепла. Любопытный пример подобного холостого цикла обнаружен у некоторых насекомых. В холодную погоду шмель не может летать до тех пор, пока он не прогреет свой «мотор»; температура мышц должна подняться у него примерно до 30 °С и поддерживаться на этом уровне за счет холостого цикла с участием фруктозо-6-фосфата и фруктозо-1,6-дифосфата и последующим гидролизом АТФ, который служит источником тепла. Полагают также, что холостые циклы, генерирующие тепло, имеют место, возможно, и у некоторых животных, пробуждающихся после зимней спячки, то есть в период, когда температура тела животного бывает гораздо ниже нормы.
Регуляция метаболизма углеводов[править | править код]
Пути регуляции метаболизма углеводов крайне разнообразны. На любых уровнях организации живых организма обмен углеводов регулируется факторами, влияющими на активность ферментов, участвующих в реакциях углеводного обмена. К этим факторам относятся концентрация субстратов, содержание продуктов (метаболитов) отдельных реакций, кислородный режим, проницаемость биологических мембран, концентрация коферментов, необходимых для отдельных реакций и т. д.
Регуляция содержания глюкозы в крови[править | править код]
Результат регуляции метаболических путей превращения глюкозы — постоянство концентрации глюкозы в крови.
Источники глюкозы крови[править | править код]
А.Углеводы, содержащиеся в пищевом рационе.
Большинство углеводов, поступающих в организм с пищей, гидролизуется с образованием глюкозы, галактозы или фруктозы, которые через воротную вену поступают в печень. Галактоза и фруктоза быстро превращаются в печени в глюкозу.
Б. Различные глюкозообразующие соединения, вступающие на путь глюконеогенеза. Эти соединения можно разделить на две группы:
- соединения, превращающиеся в глюкозу и не являющиеся продуктами её метаболизма, например аминокислоты и пропионат;
- соединения, которые являются продуктами частичного метаболизма глюкозы в ряде тканей; они переносятся в печень и почки, где из них ресинтезируется глюкоза.
Так, лактат, образующийся в скелетных мышцах и эритроцитах из глюкозы, транспортируется в печень и почки, где из него вновь образуется глюкоза, которая затем поступает в кровь и ткани. Этот процесс называется циклом Кори, глюколактатным или циклом молочной кислоты.

Источником глицерина, необходимого для синтеза триацилглицеридов (ТАГ) в жировой ткани, является глюкоза крови, поскольку использование свободного глицерола в этой ткани затруднено. Ацилглицериды (АГ) жировой ткани подвергаются постоянному гидролизу, в результате которого образуется свободный глицерин, который диффундирует из ткани в кровь. В печени и почках он вступает на путь глюконеогенеза и вновь превращается в глюкозу. Таким образом, постоянно функционирует цикл, в котором глюкоза из печени и почек транспортируется в жировую ткань, а глицерин из этой ткани поступает в печень и почки, где превращается в глюкозу. Среди аминокислот, транспортируемых при голодании из мышц в печень, преобладает аланин. Это позволило постулировать существование глюкозоаланинового цикла, по которому глюкоза поступает из печени в мышцы, а аланин — из мышц в печень, за счет чего обеспечивается перенос аминоазота из мышц в печень и «свободной энергии» из печени в мышцы. Энергия, необходимая для синтеза глюкозы из пирувата в печени, поступает за счет окисления жирных кислот.
В. Гликоген печени.
Регуляция содержания глюкозы в крови в абсорбтивном и постабсорбтивном периодах[править | править код]
Для предотвращения чрезмерного повышения концентрации глюкозы в крови при пищеварении основное значение имеет потребление глюкозы печенью и мышцами, в меньшей мере — жировой тканью. Следует напомнить, что более половины всей глюкозы (60 %), поступающей из кишечника в воротную вену, поглощается печенью. Около 2/3 этого количества откладывается в печени в форме гликогена, остальная часть превращается в жиры и окисляется, обеспечивая синтез АТФ. Ускорение этих процессов инициируется повышением инсулинглюкагонового индекса. Другая часть глюкозы, поступающей из кишечника, попадает в общий кровоток. Примерно 2/3 этого количества поглощается мышцами и жировой тканью. Это обусловлено увеличением проницаемости мембран мышечных и жировых клеток для глюкозы под влиянием высокой концентрации инсулина. Глюкоза в мышцах откладывается в форме гликогена, а в жировых клетках превращается в жиры. Остальная часть глюкозы общего кровотока поглощается другими клетками (инсулинонезависимыми).
При нормальном ритме питания и сбалансированном рационе концентрация глюкозы в крови и снабжение глюкозой всех органов поддерживается главным образом за счёт синтеза и распада гликогена. Лишь к концу ночного сна, то есть к концу самого большого перерыва между приёмами пищи, может несколько увеличиться роль глюконеогенеза, значение которого будет возрастать, если завтрак не состоится и голодание продолжится
Регуляция содержания глюкозы в крови при предельном голодании[править | править код]
При голодании в течение первых суток исчерпываются запасы гликогена в организме, и в дальнейшем источником глюкозы служит только глюконеогенез (из лактата, глицерина и аминокислот). Глюконеогенез при этом ускоряется, а гликолиз замедляется вследствие низкой концентрации инсулина и высокой концентрации глюкагона. Но, кроме того, через 1-2 сут существенно проявляется действие и другого механизма регуляции — индукции и репрессии синтеза некоторых ферментов: снижается количество гликолитических ферментов и, наоборот, повышается количество ферментов глюконеогенеза. Изменение синтеза ферментов также связано с влиянием инсулина и глюкагона.
Начиная со второго дня голодания достигается максимальная скорость глюконеогенеза из аминокислот и глицерина. Скорость глюконеогенеза из лактата остаётся постоянной. В результате синтезируется около 100 г глюкозы ежесуточно, главным образом в печени.
При голодании глюкоза не используется мышечными и жировыми клетками, поскольку в отсутствие инсулина не проникает в них и таким образом сберегается для снабжения мозга и других глюкозозависимых клеток; обеспечение энергетических потребностей мышц и других тканей происходит за счёт жирных кислот и кетоновых тел. Поскольку при других условиях мышцы — один из основных потребителей глюкозы, то прекращение потребления глюкозы мышцами при голодании имеет существенное значение для обеспечения глюкозой мозга. При достаточно продолжительном голодании (несколько дней и больше) мозг начинает использовать и другие источники энергии (например жиры).
Вариантом голодания является несбалансированное питание, в частности такое, когда по калорийности рацион содержит мало углеводов — углеводное голодание. В этом случае также активируется глюконеогенез, и для синтеза глюкозы используются аминокислоты и глицерол, образующиеся из пищевых белков и жиров.
Регуляция содержания глюкозы в крови в период покоя и во время физической нагрузки[править | править код]
Как в период покоя, так и во время продолжительной физической работы сначала источником глюкозы для мышц служит гликоген, запасённый в самих мышцах, а затем глюкоза крови. Известно, что 100 г гликогена расходуется на бег примерно в течение 15 мин, а запасы гликогена в мышцах после приёма углеводной пищи могут составлять 200—300 г.
На рисунке представлены значения гликогена печени и глюконеогенеза для обеспечения глюкозой работы мышц разной интенсивности и продолжительности.
Регуляция гликолиза и глюконеогенеза в печени[править | править код]
По сравнению с другими органами печень отличается наиболее сложным обменом глюкозы. Кроме пары противоположных процессов (синтеза и распада гликогена), в печени могут происходить ещё два противоположно направленных процесса — гликолиз и глюконеогенез. В большинстве других органов происходит только гликолиз. Переключение печени с гликолиза на глюконеогенез и обратно происходит с участием инсулина и глюкагона и осуществляется с помощью:
- аллостерической регуляции активности ферментов;
- ковалентной модификации ферментов путём фосфорилирования/дефосфорилирования;
- индукции/репрессии синтеза ключевых ферментов.
Регуляторные воздействия направлены на ферменты, катализирующие необратимые стадии гликолиза и глюконеогенеза, сочетание которых называют «субстратными», или «холостыми» циклами.
Регуляция скорости реакции гликолиза и глюконеогенеза, составляющих субстратные циклы[править | править код]
«Субстратные» циклы — парные комбинации процессов синтеза и распада метаболитов. Как уже упоминалось, сочетание процессов синтеза и распада гликогена или необратимых реакций гликолиза и соответствующих им необратимых реакций глюконеогенеза может составить подобный цикл. Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата. Название «холостой» отражает результат работы подобного цикла, заключающийся в бесполезном расходовании АТФ. Хотя существование «холостых» циклов нелогично, тем не менее они могут функционировать. Более того, эти циклы могут быть мишенью регуляторных воздействий, так как составляющие их реакции катализируют разные ферменты. Реципрокное изменение активности этих ферментов предотвращает одновременное протекание противоположных процессов.
Изменение в печени гликолитического направления на глюконеогенез и обратно при смене абсорбтивного состояния на постабсорбтивное или при голодании происходит главным образом в результате регуляции активности ферментов, катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II, III на рисунке, представляющем общую картину регуляции гликолиза и глюконеогенеза в печени.
Направление реакции первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается (до 8-10 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакция образования глюкозо-6-фосфата. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена и по гликолитическому пути.
Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. Активность этих ферментов зависит от концентрации фруктозо-2,6-бисфосфата. Фруктозо-2,6-бисфосфат — метаболит, образующийся в незначительных количествах из фруктозо-6-фосфата и выполняющий только регуляторные функции. Образование фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата катализирует бифункциональный фермент (БИФ), который катализирует также и обратную реакцию. Однако превращение фруктозо-2,6-бисфосфата во фруктозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
В реакции фосфорилирования фруктозо-6-фосфата фермент проявляет киназную активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата — фосфатазную. Это обстоятельство и определило название фермента «бифункциональный».
Киназная активность БИФ проявляется, когда фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий. В этот период количество фруктозо-2,6-бисфосфата увеличивается.
Киназную и фосфатазную реакции катализируют разные активные центры БИФ, но в каждом из двух состояний фермента (фосфорилированном и дефосфорилированном) один из активных центров ингибирован. Регуляторное влияние фруктозо-2,6-бисфосфата заключается в том, что он аллостерически активирует фосфофруктокиназу (фермент гликолиза). При этом фруктозо-2,6-бисфосфат снижает ингибирующее действие АТФ на этот фермент в абсорбтивном периоде и повышает его сродство к фруктозо-6-фосфату. В то же время фруктозо-2,6-бисфосфат ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза). Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что приводит к активации фосфофруктокиназы и ускорению гликолиза.
Результатом уменьшения количества фруктозо-2,6-бисфосфата в постабсорбтивном периодебудет снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез. Регуляторное влияние фруктозо-2,6-бисфосфата представлено на рисунке:
В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная — активна.
период пищеварения инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя её в активное состояние. Кроме того, инсулин в печени влияет на количество ферментов, индуцируя синтез пируваткиназы и репрессируя синтез фосфоенолпируваткарбоксикиназы. Следовательно, гликолитическая реакция фосфоенолпируват → пируват ускоряется при пищеварении. Эта же реакция замедляется в постабсорбтивном состоянии под влиянием глюкагона, который опосредованно через цАМФ-зависимую протеинкиназу фосфорилирует и инактивирует пируваткиназу.
При длительном голодании глюкагон ускоряет глюконеогенез. Это достигается не только путём фосфорилирования пируваткиназы и снижением скорости гликолиза, но и путём индукции синтеза ферментов глюконеогенеза: фосфоенолпируваткарбоксикиназы, фруктозо-1,6-бисфосфатазы и глюкозо-6-фосфатазы. Известно, что глюкагон, фосфорилируя опосредованно транскрипционные факторы, влияет на их активность и таким образом индуцирует синтез этих ферментов глюконеогенеза. Кроме того, синтез фосфоенолпируваткарбоксикиназы при длительном голодании индуцируется кортизолом, однако это происходит в результате включения другого механизма действия, характерного для стероидных гормонов.
Координация скорости реакции II и III субстратных циклов достигается с помощью фруктозо-1,6-бисфосфата — продукта II субстратного цикла (гликолитическое направление), который является аллостерическим активатором пируваткиназы. В период пищеварения вследствие ускорения начальных стадий гликолиза концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
Противоположные реакции каждого из субстратных циклов могут протекать одновременно. Соответственно, гликолиз и глюконеогенез в печени в какой-то мере тоже могут происходить одновременно, хотя их относительные скорости изменяются. Так, при пищеварении преобладает гликолитическое направление, а в постабсорбтивном состоянии — направление глюконеогенеза. Например, реакция глюконеогенеза пируват → оксалоацетат может протекать при любых состояниях организма. Это объясняется необходимостью поддерживать концентрацию оксалоацетата на определенном уровне, потому что оксалоацетат используется не только в глюконеогенезе, но и в других процессах, таких как цитратный цикл, трансмембранный перенос веществ, синтез аминокислот.
Значение гликолиза в печени для синтеза жиров[править | править код]
Основным значением ускорения гликолиза в печени в период пищеварения является образование дигидроксиацетонфосфата и ацетил-КоА — исходных веществ для синтеза жира. Образование ацетил-КоА из пирувата в ходе реакции, катализируемой пируватдегидрогеназным комплексом (ПДК), регулируется разными способами.
В абсорбтивном периоде ПДК (пируватдикарбоксилаза) находится в дефосфорилированной (активной) форме, следовательно, декарбоксилирование пирувата ускоряется. Образуемый ацетил-КоА используется в основном двумя путями: для синтеза жирных кислот и в цитратном цикле. В период пищеварения ускоряются образование ацетил-КоА и его использование для синтеза жирных кислот. Необходимый для синтеза жира α-глицерофосфат образуется в реакции восстановления из дигидроксиацетонфосфата.
Аллостерическая регуляция аэробного распада глюкозы и глюкогенеза в печени энергетическим статусом клетки[править | править код]
Аллостерическая регуляция скорости гликолиза, зависимая от изменения соотношения АТФ/АДФ, направлена на изменение скорости использования глюкозы непосредственно клетками печени. Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но также и как источник энергии для синтеза АТФ. Основными потребителями АТФ в гепатоцитах являются процессы трансмембранного переноса веществ, синтез белков, гликогена, жиров, глюконеогенез. От скорости утилизации АТФ в этих процессах зависит скорость его синтеза. АТФ, АДФ и АМФ, а также НАД+ и НАДН служат аллостерическими эффекторами некоторых гликолитических ферментов и ферментов глюконеогенеза. В частности, АМФ активирует фосфофруктокиназу и ингибирует фруктозо-1,6-бисфосфатазу. АТФ и НАДН ингибируют пируваткиназу, а АДФ активирует пируваткарбоксилазу.
Следовательно, при усилении расходования АТФ и снижении его концентрации с одновременным увеличением концентрации АМФ, активируется гликолиз и образование АТФ, а глюконеогенез при этом замедляется. Кроме того, от соотношения АТФ/АДФ, АМФ и НАД/НАДН зависит скорость реакций общего пути катаболизма.
Влияние алкоголя на углеводный обмен[править | править код]
Алкоголь снижает активность ферментов гликолиза, глюконеогенеза[14], пентозофосфатного цикла, цикла Кребса. В результате чего в тканях печени, крови, ликворе и, в особенности, в мозге, накапливаются промежуточные продукты метаболизма углеводов, которые приводят к «глюкозному голоду» клеток — то есть нарушению утилизации глюкозы клетками тканей[15].
Алкоголь вызывает дегенерацию клеток поджелудочной железы, что приводит к дефициту выделения многих ферментов, гормонов влияющих на углеводный обмен — инсулина и глюкагона. Вследствие чего, повышается риск возникновения хронического панкреатита[16].
Особенно опасно принимать алкоголь лицам страдающим сахарным диабетом[16] ибо действие алкоголя лишь усугубляет те изменения, которые уже имеют место у лиц с сахарным диабетом в результате нарушенного метаболизма и сосудистых поражений (хронические дистрофические процессы с трагическим финалом развиваются быстрее).
Нарушения метаболизма углеводов[править | править код]
Многочисленные расстройства метаболизма углеводов условно объединяют в несколько групп: гипогликемии, гипергликемии, гликогенозы, гексоз- и пентоземии, агликогенозы. Перечисленные расстройства рассматривают как типовые формы нарушений углеводного обмена.
Гипогликемия[править | править код]
Гипогликемия (от др.-греч. ὑπό — снизу, под + γλυκύς — сладкий + αἷμα — кровь)[17] — патологическое состояние, характеризующееся снижением концентрации глюкозы в крови ниже 3,5 ммоль/л периферической крови ниже нормы (3,3 ммоль/л), вследствие чего возникает гипогликемический синдром.
Механизм развития гипогликемии может значительно отличаться в зависимости от этиологии. Так, например, при употреблении этанола, наблюдается следующая картина.
Метаболизм этанола в печени катализируется алкогольдегидрогеназой. Кофактором этого фермента служит НАД — вещество, необходимое для глюконеогенеза. Приём этанола приводит к быстрому расходованию НАД и резкому торможению глюконеогенеза в печени. Поэтому алкогольная гипогликемия возникает при истощении запасов гликогена, когда для поддержания нормогликемии особенно необходим глюконеогенез. Такая ситуация наиболее вероятна при недостаточном питании. Чаще всего алкогольная гипогликемия наблюдается у истощенных больных алкоголизмом, но бывает и у здоровых людей после эпизодических приёмов большого количества алкоголя или даже небольшой дозы алкоголя, но натощак. Необходимо подчеркнуть, что алкоголь снижает концентрацию глюкозы в плазме больных с нормальной функцией печени. Особенно чувствительны к алкоголю дети.
Сахарный диабет[править | править код]
Среди заболеваний, имеющих в основе нарушения углеводного обмена, сахарный диабет занимает особое место. Это связано с частотой его распространения и относительно изученной биохимической характеристикой. Основными биохимическими симптомами сахарного диабета являются гипергликемия, глюкозурия, кетонимия и некоторые другие.

Пищевые продукты содержат различные типы углеводов. Некоторые из них, такие как глюкоза, состоят из одного шестичленного гетероциклического углеводного кольца и всасываются в кишечнике без изменений. Другие, такие как сахароза (дисахарид) или крахмал (полисахарид), состоят из двух или более связанных между собой пятичленных или шестичленных гетероциклов. Эти вещества подвергаются расщеплению под действием различных ферментов желудочно-кишечного тракта до молекул глюкозы и других простых сахаров, и, в конечном счёте, также всасываются в кровь. Помимо глюкозы в кровь поступают и такие простые молекулы, как фруктоза, которые в печени превращаются в глюкозу. Таким образом, глюкоза является основным углеводом крови и всего организма. Ей принадлежит исключительная роль в обмене веществ организма человека: она является основным и универсальным источником энергии для всего организма. Многие органы и ткани (например, мозг) могут использовать в качестве источника энергии только глюкозу[18].
Основную роль в регуляции углеводного обмена организма играет гормон поджелудочной железы — инсулин. Он представляет собой белок, синтезируемый в β-клетках островков Лангерганса (скопление эндокринных клеток в ткани поджелудочной железы) и призван стимулировать переработку глюкозы клетками. Почти все ткани и органы (например, печень, мышцы, жировая ткань) способны перерабатывать глюкозу только в его присутствии. Эти ткани и органы называются инсулинзависимыми. Другие ткани и органы, например мозг, не нуждаются в инсулине для того, чтобы утилизовать (перерабатывать) глюкозу, и потому называются инсулиннезависимыми[19].
Непереработанная (неутилизированная) глюкоза депонируется (запасается) в печени и мышцах в виде полисахарида гликогена, который в дальнейшем может быть снова превращён в глюкозу. Но для того, чтобы превратить глюкозу в гликоген, тоже нужен инсулин.
В норме содержание глюкозы в крови колеблется в достаточно узких пределах: от 70 до 110 мг/дл (миллиграмм на децилитр) (3,3—5,5 ммоль/л) утром после сна и от 120 до 140 мг/дл после еды. Это происходит благодаря тому, что поджелудочная железа производит тем больше инсулина, чем выше уровень глюкозы в крови.
При недостаточности инсулина (сахарный диабет 1-го типа) или нарушении механизма взаимодействия инсулина с клетками организма (сахарный диабет 2-го типа) глюкоза накапливается в крови в больших количествах (гипергликемия), а клетки организма (за исключением инсулиннезависимых органов) лишаются основного источника энергии.
Толерантность к глюкозе[править | править код]
Способность животного и человека использовать вводимую глюкозу обозначают как толерантность к глюкозе. Когда глюкоза вводится (либо через рот, либо в вену), её концентрация в крови быстро возрастает. В оральном тесте на толерантность к глюкозе при обычной дозе 1 г глюкозы на килограмм массы тела концентрация глюкозы в крови в течение ~ 1 ч может возрасти от ~90 мг на 100 мл при голодании до максимального уровня, достигающего величины 140 мг на 100 мл. К этому времени скорость поступления глюкозы в кровь начинает снижаться, в то время как скорость её потребления тканями возрастает, так что наступает снижение концентрации в крови. При этих условиях возросшая скорость удаления глюкозы из крови определяется следующими причинами: во-первых, скорость поступления глюкозы в клетки прямо пропорциональна концентрации глюкозы во внеклеточной жидкости и, во-вторых, повышение уровня глюкозы в крови стимулирует нормальную поджелудочную железу к выделению инсулина в кровь с повышенной скоростью. В связи с увеличением притока глюкозы в клетки наблюдается ускорение гликогенеза, особенно в мышце, а также усиление гликолиза, как об этом свидетельствует увеличение содержания лактата в крови; дыхательный коэффициент растет, увеличиваясь в сторону единицы, что указывает на большую интенсивность окисления углеводов, и содержание глюкозы в крови быстро падает. Обычно в конце второго часа концентрация глюкозы в крови становится приблизительно нормальной и часто продолжает уменьшаться, опускаясь ниже исходного уровня, вероятно, в результате продолжающегося влияния секреции инсулина. По мере исчезновения гипергликемии, стимулирующей островки Лангерганса, секреция инсулина возвращается к более низкому уровню. В ходе орального теста на толерантность к глюкозе в норме у человека концентрация глюкозы в крови никогда не превышает значения, при котором сахар начинает выводиться с мочой и не возникает глюкозурии. У людей, страдающих диабетом, испытывающих недостаточность инсулина, содержание глюкозы в крови в периоды голодания повышено. После орального введения глюкозы уровень сахара в крови становится даже более высоким, зачастую превышая почечный порог и вызывая глюкозурию. Инсулиновый ответ в этом случае будет недостаточным или совсем не проявится, и в результате падение концентрации глюкозы в крови будет происходить медленно. Человеку с таким типом ответа, как принято говорить, свойственна пониженная толерантность к глюкозе или повышенная кривая глюкозной толерантности.
Гипергликемия[править | править код]
Гипергликемия (от др.-греч. υπερ — сверху, над; γλυκύς — сладкий; αἷμα — кровь)[20] — клинический симптом, обозначающий увеличение содержания глюкозы в сыворотке крови по сравнению с нормой в 3,3—5,5 ммоль/л[21].
Глюкозурия[править | править код]
Гликозурия, или глюкозурия — наличие глюкозы в моче. В норме моча не содержит глюкозы, поскольку почки способны реабсорбировать (возвращать в кровоток) весь объём глюкозы, прошедший через почечный клубочек в просвет канальцев нефрона. В подавляющем большинстве случаев гликозурия является симптомом декомпенсированного сахарного диабета как результат патологического увеличения концентрации глюкозы в крови. Редким исключением является нарушение реабсорбции в самой почке, — т. н. ренальная (почечная) гликозурия. Гликозурия ведёт к избыточной потере воды с мочой — дегидратации организма, развивающейся из-за усиления осмотического компонента диуреза.
Наследственные нарушения метаболизма углеводов[править | править код]
Развитие большинства из них является следствием дефекта единичных генов, кодирующих индивидуальные ферменты, которые обеспечивают превращение одних веществ (субстраты) в другие (продукты). В большинстве случаев таких расстройств патогенным является накопление веществ, обладающих токсическим действием или нарушающих способность синтеза других жизненно важных соединений.
Гликогенозы[править | править код]
Гликогенозы — это ряд наследственных заболеваний, обусловленные дефектом ферментов, участвующих в распаде гликогена. Они проявляются или необычной структурой гликогена, или его избыточным накоплением в печени, сердечной или скелетных мышцах, почках, лёгких и других органах. В таблице описаны некоторые типы гликогенозов, различающихся характером и локализацией ферментного дефекта.
| Форма гликогеноза | Дефектный фермент | Проявления болезни | Тип, название болезни |
|---|---|---|---|
| Печёночная | Глюкозо-6-фосфатаза | Гипогликемия, гиперацилглицеролемия, гиперурикемия, ацидоз (вследствие накопления лактата), характерное выражение лица («лицо китайской куклы»). | I Болезнь Гирке |
| Амило-1,6-глюкозидаза («деветвящий» фермент) | Накопление гликогена с короткими внешними ветвями (лимито-декстрин). Остальные проявления менее выражены, чем при типе I. | III Болезнь Форбса-Кори, лимитодекстриноз | |
| Амило- 1,4 → 1,6 глюкозилтрансфераза («ветвящий» фермент) | Накопление структурно изменённого гликогена с очень длинными наружными ветвями и редкими точками ветвления. | IV Болезнь Андерсена | |
| Фосфорилаза | Накопление гликогена нормальной структуры. Умеренная гипогликемия, гепатомегалия, клинические проявления похожи, но менее выражены, чем при гликогенозах I и III типов. | VI Болезнь Херса | |
| Киназа фосфорилазы | Аналогичны VI типу | IX | |
| Протеинкиназа А | Аналогичны VI типу | X | |
| Мышечные | Гликогенфосфорилаза | Боли в мышцах, судороги при физической нагрузке (даже умеренной). Накопление в мышцах гликогена нормальной структуры. | V Болезнь Мак-Ардла |
| Фосфофруктокиназа | Аналогичны V типу | VII | |
| Фосфоглицеромутаза | Аналогичны V типу | ||
| Лактатдегидрогеназа (М-протомер) | Аналогичны V типу | ||
| Смешанные | Лизосомная α-1,4-гликозидаза | Генерализованное накопление гликогена в лизосомах, а затем в цитозоле | II Болезнь Помпе |
Термин «гликогеноз» был впервые предложен К. Ф. Кори и Г. Т. Кори. Они же предложили систему нумерации этих болезней. Однако в настоящее время преобладает деление гликогенозов на 2 группы: печёночные и мышечные. Печёночные формы гликогенозов ведут к нарушению использования гликогена для поддержания уровня глюкозы в крови. Поэтому общий симптом для этих форм — гипогликемия в постабсорбтивный период.
Болезнь Гирке (тип I) — отмечают наиболее часто. Описание основных симптомов этого типа гликогеноза и их причин может служить основанием для понимания симптомов всех остальных типов. Причина этого заболевания — наследственный дефект глюкозо-6-фосфатазы — фермента, обеспечивающего выход глюкозы в кровоток после её высвобождения из гликогена клеток печени. Болезнь Гирке проявляется гипогликемией, гипертриацилглицеролемией (повышением содержания триацилглицеролов), гиперурикемией (повышением содержания мочевой кислоты).
Болезнь Кори, болезнь Форбса, лимитодекстриноз (тип III) весьма распространена. Она составляет 1/4 всех случаев печёночных гликогенозов. Накапливаемый гликоген аномален по структуре, так как дефектен фермент амило-1,6-глюкозидаза, гидролизующий гликозидные связи в местах разветвлений («деветвящий фермент», от англ. debranching enzyme). Недостаток глюкозы в крови проявляется быстро, поскольку гликогенолиз возможен, но в незначительном объёме. В отличие от гликогеноза I типа, лактоацидоз и гиперурикемия не отмечаются. Болезнь отличается более лёгким течением.
Болезнь Андерсена (тип IV) — крайне редкое аутосомно-рецессивное заболевание, возникающее вследствие дефекта ветвящего фермента — амило-1,4-1,6-глюкозилтрансферазы. Содержание гликогена в печени не сильно увеличено, но структура его изменена, и это препятствует его распаду. Молекула гликогена имеет мало точек ветвления, а также очень длинные и редкие боковые ветви. В то же время гипогликемия выражена умеренно. Болезнь развивается быстро, отягощается ранним циррозом печени и практически не поддаётся лечению. Дефект фермента ветвления обнаруживается не только в печени, но также в лейкоцитах, мышцах, фибробластах, на ранние и преобладающие проявления болезни обусловлены нарушением функции печени.
Болезнь Херса (тип VI) (гепатофосфорилазная недостаточность) также проявляется симптомами, обусловленными поражением печени. Данный гликогеноз — следствие дефекта гликогенфосфорилазы. Б гепатоцитах накапливается гликоген нормальной структуры. Течение болезни сходно с гликогенозом I типа, но симптомы выражены в меньшей степени. Сниженная активность гликогенфосфорилазы обнаруживается также в лейкоцитах. Болезнь Херса — редкий тип гликогеноза; наследуется по аутосомнорецессивному типу.
Дефект киназы фосфорилазы (тип IX)(болезнь Хага) — встречается только у мальчиков, так как этот признак сцеплен с Х-хромосомой. У больных наблюдается гепатомегалия.
Дефект протеинкиназы А (тип X), так же как и дефект киназы фосфорилазы, проявляется симптомами, сходными с болезнью Херса. Известен случай у единственного больного, наследование не установлено.
Мышечные формы гликогенозов характеризуются нарушением в энергоснабжении скелетных мышц. Эти болезни проявляются при физических нагрузках и сопровождаются болями и судорогами в мышцах, слабостью и быстрой утомляемостью.
Болезнь Мак-Ардла (тип V) — аутосомнорецессивная патология, при которой полностью отсутствует в скелетных мышцах активность гликогенфосфорилазы. Поскольку активность этого фермента в гепатоцитах нормальная, то гипогликемия не наблюдается (строение фермента в печени и мышцах кодируются разными генами). Тяжёлые физические нагрузки плохо переносятся и могут сопровождаться судорогами, однако при физических нагрузках гиперпродукция лактата не наблюдается, что подчёркивает значение внемышечных источников энергии для сокращения мышц, например, таких как жирные кислоты, замещающие при данной патологии глюкозу (см. раздел 8). Хотя болезнь не сцеплена с полом, большая частота заболевания характерна для мужчин[2].
Дефект фосфофруктокиназы (болезнь Таруи, миофосфофруктокиназная недостаточность) характерен для гликогеноза VII типа. Больные могут выполнять умеренные физические нагрузки. Течение болезни сходно с гликогенозом V типа, но основные проявления менее выражены.
Дефект фосфоглицеромутазы и дефект М-субъединицы ЛДГ (ненумерованные по классификации Кори) характерны для мышечных форм гликогенозов. Проявления этих патологий аналогичны болезни МакАрдла. Дефект фосфоглицеромутазы в мышцах описан только у одного больного.
Смешанные формы гликогенозов. Эти заболевания характеризуются нарушениями метаболизма гликогена, как в мышцах, так и в печени, могут затрагивать и другие органы[2].
Болезнь Помпе (тип II) — наследуется по аутосомно-рецессивному типу. Симптомы проявляются в первые недели жизни — до шести месяцев после рождения. Дефект фермента найден в печени, почках, селезенке, мышцах, нервной ткани, лейкоцитах. Наблюдается расстройство дыхания, беспокойство или адинамия. Отмечаются отсутствие аппетита, задержка роста, мышечная гипотония. Увеличиваются размеры сердца, печени, почек, селезенки. Сердце приобретает шаровидную форму, в связи с гипертрофией миокарда появляются изменения ЭКГ. Часто возникают гипостатические пневмонии, бронхиты, ателектазы лёгких, наблюдаются миодистрофия, гипорефлексия, спастические параличи. Мышечная форма гликогеноза II типа возникает только в мышцах при дефиците кислой α-1,4-глюкозидазы. Болезнь проявляется в более поздние сроки и по клинической картине напоминает миопатию[2].
Агликогенозы[править | править код]
Агликогеноз (гликогеноз 0 по классификации) — заболевание, возникающее в результате дефекта гликогенсинтазы. В печени и других тканях больных наблюдают очень низкое содержание гликогена. Это проявляется резко выраженной гипогликемией в постабсорбтивном периоде. Характерный симптом — судороги, проявляющиеся особенно по утрам. Болезнь совместима с жизнью, но больные дети нуждаются в частом кормлении.
Мукополисахаридозы[править | править код]
Мукополисахаридозы (МПС) — гетерогенная группа заболеваний, отнесенных к наследственным болезням обмена сложных сахаров. МПС сопровождаются избыточным накоплением в тканях и повышенной экскрецией гликоз-аминогликанов (ГАГ) — кислых мукополисахаридов, соединенных с белком и состоящих из уроновых кислот, аминосахароз и нейтральных сахаров. Указанные комплексы существуют в форме протеогликанов, являющихся важнейшими компонентами основного структурного белка волос (0-кератина) и структурного белка соединительной ткани (коллагена)[22].
Для большинства МПС характерен аутосомно-рецессивный тип наследования, кроме синдрома Хантера (Х-сцепленный рецессивный).
Некоторые наследственные нарушения метаболизма углеводов были описаны выше.
См. также[править | править код]
- Углеводы
- Глюкоза
- Гликоген
- Обмен веществ
- Гликолиз
- Спиртовое брожение
- Глюконеогенез
- Липолиз
- Цикл Кребса
- Цикл Калвина
- Сахар крови
- Инсулин
- Глюкагон
- Сахарный диабет
- Ферментопатии
Примечания[править | править код]
- ↑ Соединения глюкуроновой кислоты, образующиеся в организме при обезвреживании и выделении токсических веществ (билирубина, фенолов и др.).
- ↑ 1 2 3 4 5 6 Северин Е. С. . Биология. — М.: ГЭОТАР-МЕД, 2004. — 779 с. — ISBN 5-9231-0254-4.
- ↑ Joost H., Thorens B. The extended GLUT-family of sugar/polyol transport facilitators: nomenclature, sequence characteristics, and potential function of its novel members (review) // Mol. Membr. Biol.. — 2001. — Vol. 18, no. 4. — P. 247—256. — doi:10.1080/09687680110090456. — PMID 11780753.
- ↑ Uldry M., Thorens B. The SLC2 family of facilitated hexose and polyol transporters // Pflügers Archiv: European Journal of Physiology. — 2004. — Vol. 447, no. 5. — P. 480—489. — doi:10.1007/s00424-003-1085-0. — PMID 12750891.
- ↑ 6. Значение анаэробного гликолиза - Лекция 3. Метаболизм углеводов - Биохимия - Лекции 2 курс - Medkurs.ru - медицинский сервер. Дата обращения: 21 марта 2013. Архивировано 22 марта 2013 года.
- ↑ Шлегель Г. . Общая микробиология. — М.: Мир, 1987. — С. 263.
- ↑ Молочнокислое брожение. Дата обращения: 8 марта 2013. Архивировано из оригинала 11 января 2013 года.
- ↑ Маслянокислое брожение. Дата обращения: 8 марта 2013. Архивировано из оригинала 12 ноября 2016 года.
- ↑ Лимоннокислое брожение | Микробиология. Дата обращения: 8 марта 2013. Архивировано из оригинала 15 января 2013 года.
- ↑ Ацетоно-бутиловое брожение | Объекты живой природы. Дата обращения: 8 марта 2013. Архивировано 15 марта 2013 года.
- ↑ Строев Е. А. Биологическая химия: Учебник для фармац. ин-тов и фармац. фак. мед. ин-тов. — М.: Высшая школа, 1986. — 479 с.
- ↑ Nelson & Cox, 2008, p. 563.
- ↑ Современная микробиология, 2005, с. 267.
- ↑ 1 2 3 4 Ленинджер, 1985.
- ↑ Влияние алкоголя на организм. Дата обращения: 8 марта 2013. Архивировано 10 февраля 2013 года.
- ↑ 1 2 Касаткина Э. П. . Сахарный диабет у детей. 1-е изд. — М.: Медицина, 1990. — 272 с. — ISBN 5-225-01165-9. — С. 41—90.
- ↑ См. ὑπό, γλυκύς, αἷμα в «Древнегреческо-русском словаре» Архивная копия от 28 ноября 2011 на Wayback Machine Дворецкого И. Х. (под ред. Соболевского С. И.), 1958).
- ↑ Клиническая эндокринология. Руководство. 3-е изд / Под ред. Н. Т. Старковой. — СПб.: Питер, 2002. — 576 с. — (Спутник Врача). — ISBN 5-272-00314-4. — С. 209—213.
- ↑ Михайлов В. В. . Основы патологической физиологии: Руководство для врачей / Под ред. Б. М. Сагаловича. — М.: Медицина, 2001. — 704 с. — ISBN 5-225-04458-1. — С. 117—124.
- ↑ См. υπερ, γλυκύς, αἷμα в «Древнегреческо-русском словаре» Архивная копия от 28 ноября 2011 на Wayback Machine Дворецкого И. Х. (под ред. Соболевского С. И.), 1958.
- ↑ Ефимов А. С., Скробонская Н. А. . Клиническая диабетология. 1-е изд. — Киев: Здоров’я, 1998. — 320 с. — ISBN 5-311-00917-9. — С. 273—277.
- ↑ Наследственные нарушения углеводного обмена, ведущие к поражению печени | Интернет-издание «Новости медицины и фармации». Дата обращения: 8 марта 2013. Архивировано 15 марта 2013 года.
Литература[править | править код]
- Берёзов Т. Т., Коровкин Б. Ф. . Биологическая химия. 3-е изд. — М.: Медицина, 1998. — 704 с. — ISBN 5-225-02709-1.
- Кольман Я., Рём К. Г. . Наглядная биохимия / Пер. с нем.. — М.: Мир, 2000. — 469 с. — ISBN 5-03-003304-1.
- Ленинджер А. . Основы биохимии: В 3-х тт. Т. 2 / Пер. с англ.. — М.: Мир, 1985. — 368 с.
- Марри Р., Греннер Д., Мейес П., Родуэлл В. . Биохимия человека: В 2-х тт. Т. 1 / Пер. с англ.. — М.: Мир, 1993. — 384 с. — ISBN 5-03-001774-7.
- Мецлер Д. . Химические реакции в клетках: В 3-х тт. Т. 2 / Пер. с англ.. — М.: Мир, 1980. — 608 с.
- Николаев А. Я. . Биологическая химия. 3-е изд. — М.: Мед. информ. агентство, 2004. — 565 с. — ISBN 5-89481-219-4.
- Основы биохимии: В 3-х тт. Т. 2 / Пер. с англ. В. П. Скулачёва, Э. И. Будовского, Л. М. Гинодмана; под ред. Ю. А. Овчинникова. — М.: Мир, 1981. — 617 с.
- Современная микробиология. Прокариоты. Т. 1 / Под ред. Й. Ленгелера, Г. Древса, Г. Шлегеля. — М.: Мир, 2005. — 654 с. — (Лучший зарубежный учебник). — ISBN 5-03-003707-1.
- Nelson D. L., Cox M. M. . Lehninger Principles of biochemistry. 5th ed. — New York: W. H. Freeman and Company, 2008. — 1158 p. — ISBN 978-0-7167-7108-1.