Фторид ниобия(V)
Перейти к навигации
Перейти к поиску
| Фторид ниобия(V) | |
|---|---|
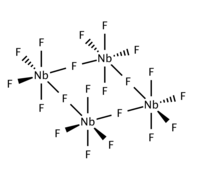 | |
| Общие | |
| Систематическое наименование |
Фторид ниобия(V) |
| Традиционные названия | фтористый ниобий |
| Хим. формула | NbF5 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 187,90 г/моль |
| Плотность | 3,293; 3,29 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 79,0; 79,5 °C |
| • кипения | 233; 234,5; 236 °C |
| Мол. теплоёмк. | 134,8 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1813,8 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7783-68-8 |
| PubChem | 82217 |
| Рег. номер EINECS | 232-020-2 |
| SMILES | |
| InChI | |
| ChemSpider | 74197 и 7969865 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Фторид ниобия(V) — неорганическое соединение, соль металла ниобия и фтористоводородной кислоты с формулой NbF5, бесцветные кристаллы, реагирует с водой.
Получение[править | править код]
- Действие фтора на ниобий или оксид ниобия(V):
- Действие фторида водорода на ниобий или хлорид ниобия(V):
Физические свойства[править | править код]
Фторид ниобия(V) образует бесцветные кристаллы моноклинной сингонии, пространственная группа C 2/m, параметры ячейки a = 0,962 нм, b = 1,443 нм, c = 0,512 нм, β = 96,1°, Z = 8.
Растворяется в этаноле, слабо растворим в хлороформе, сероуглероде.
Химические свойства[править | править код]
- Реагирует с влагой из воздуха:
- Реагирует с водой:
- Реагирует с концентрированной плавиковой кислотой:
- С фторидами щелочных металлов образует комплексные соли:
- Реагирует с щелочами:
Литература[править | править код]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |






![{\displaystyle {\mathsf {NbF_{5}+2HF\ {\xrightarrow {}}\ H_{2}[NbF_{7}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ea1941f5945fe4023bfda8b4ad9769b80e8f1f3)
![{\displaystyle {\mathsf {NbF_{5}+RbF\ {\xrightarrow {}}\ Rb[NbF_{6}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8b6d30873a4e4f428f4d4afaea02b0e18de8c8e3)
![{\displaystyle {\mathsf {NbF_{5}+2KF\ {\xrightarrow {}}\ K_{2}[NbF_{7}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e71a126f293228740ef416ceb0c0ec63ca46d17a)
![{\displaystyle {\mathsf {NbF_{5}+3NaF\ {\xrightarrow {}}\ Na_{3}[NbF_{8}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f9d95955214dd75c6b4fde344adddcd12de5144c)
![{\displaystyle {\mathsf {NbF_{5}+2KOH\ {\xrightarrow {}}\ K_{2}[NbOF_{5}]+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/285b08dfc2c10f5e91768d74e83a53342e6c1597)