Хиноны
Хиноны — полностью сопряжённые циклогексадиеноны и их аннелированные аналоги. Существуют два класса хинонов: пара-хиноны с пара-расположением карбонильных групп (1,4-хиноны) и орто-хиноны с орто-расположением карбонильных групп (1,2-хиноны). Благодаря способности к обратимому восстановлению до двухатомных фенолов некоторые производные пара-хинонов участвуют в процессах биологического окисления в качестве коферментов ряда оксидоредуктаз.
История исследований[править | править код]
Открытие хинонов было следствием исследований состава и свойств веществ, выделяемых из коры хинного дерева Cinchona L., использовавшейся как антималярийное средство. Первый представитель хинонов был описан А. А. Воскресенским в его докторской работе «Рассуждение о хинной кислоте и открытом в ней новом теле хиноиле» (1839 г.), выполненной в лаборатории Юстуса Либиха[1] под названием «хиноил» как продукт окисления хинной кислоты диоксидом марганца в присутствии серной кислоты:
Берцелиус установил, что «хиноил» имеет свойства, схожие со свойствами кетонов и дал ему используемое поныне название хинон (от «хин-» — хинная кислота и «-он» — кетон). Работы Воскресенского по химии p-бензохинона были продолжены Фридрихом Вёлером, который в 1844 г. восстановлением p-бензохинона сероводородом получил гидрохинон[2]: эта работа раскрыла фундаментальное отличие химии хинонов от химии ненасыщенных кетонов — возможность обратимого восстановления хинонов. Одновременно Вёлером был открыт хингидрон — молекулярный комплекс p-бензохинона и гидрохинона, первый описанный в химической литературе молекулярный комплекс. Дальнейшие работы по химии хинонов были стимулированы развитием химии красителей и исследованиями ализарина — производного антрахинона.
В течение шести десятилетий после синтезов p-бензохинона и гидрохинона попытки получить o-бензохинон окислением пирокатехина оканчивались неудачей, до тех пор, пока Вильштеттер не предположил, что o-бензохинон чувствителен к влаге и не провёл его синтез окислением оксидом серебра в среде абсолютного эфира и в присутствии безводного сульфата натрия в качестве водопоглощающего агента:
Строение и физические свойства[править | править код]
Ядро хинонов не является ароматическим, вклад резонансных структур ароматического типа в свойства хинонов невелик. Спектроскопические свойства близки к свойствам 1,2-ненасыщенных кетонов, при этом свойства 1,4-хинонов ближе к перекрестно-сопряжённых ненасыщенным 1,4-дикетонов, в то время как 1,2-хиноны ближе к диендионам.
Так, например, простейший 1,4-хинон — пара-бензохинон — имеет жёлтую окраску, тогда как 1,2-бензохинон окрашен в ярко-красный цвет за счёт более длинной цепи сопряжения, обуславливающей батохромный сдвиг.
В инфракрасных спектрах для 1,4-хинонов типичны две полосы поглощения карбонила, обусловленные резонансом Ферми при 5.98 и 6.06 мкм, в случае 1,2-хинонов присутствует слабая полоса при 5.95 мкм и более сильная при 6.02 мкм. В спектрах 1H ЯМР сигналы протонов хиноидного ядра лежат в области δ ~6.7, что близко к химическим сдвигам протонов при двойной связи α,β-ненасыщенных кетонов (δ 6.63 для α-протона метилвинилкетона[3]) и указывает на отсутствие эффекта кольцевого тока ароматической π-системы, то есть на неароматичность хиноидного ядра.
Хиноны — кристаллические вещества с высокими температурами плавления, низшие хиноны окрашены, так как молекула имеет протяжённую цепь сопряжения.
Некоторые представители хинонов:
-
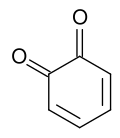
о-бензохинон
Методы синтеза[править | править код]
Общий метод синтеза хинонов — как моноциклических бензохинонов и их производных, так и полициклических конденсированных хинонов, причём если для окисления производных бензола требуется, как правило, наличие электродонорных заместителей, активирующих ароматическое кольцо (например, гидрокси- или аминогрупп), то в случае полициклических ароматических углеводородов возможно и прямое окисление до соответствующих хинонов.
Окисление активированных ароматических соединений может проводиться с использованием различных окислителей (CrO3/H2CrO4 в кислой среде, Ag2O, Fe3+), однако для синтеза пара-бензохинонов наиболее широко используется реакция Тойбера — окисление активированных производных бензола (фенолов, ароматических аминов, аминофенолов) солью Фреми (нитрозодисульфонатом калия):
Соль Фреми (KO3S)2NO. является стабильным нитроксильным свободным радикалом и окисление с её участием идёт по одноэлектронному механизму в мягких условиях: так, например, одноатомные фенолы и ароматические амины со свободным пара- положением в водном спирте или ацетоне в присутствии ацетатного или фосфатного буфера быстро окисляются двумя эквивалентами соли Фреми с выходами, близкими к количественным. Если пара-положение занято, реакция Тойбера ведёт к орто-хинону, однако может происходить и элиминирование p-заместителя (галогена или трет-бутильной группы)
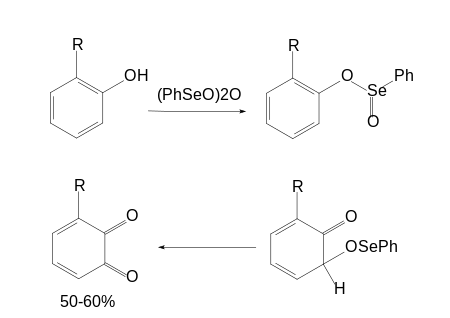
Синтез орто-хинонов из ароматических соединений со свободным пара-положением, являющийся проблемой при использовании большинства окисляющих агентов, может быть осуществлён исходя из одноатомных фенолов с использованием окислителя дифенилселенинового ангидрида: в этом случае за счёт промежуточной этерификации гидроксильной группы фенола происходит внутримолекулярное окисление в орто-положение образующегося интермедиата, пара-окисления при этом практически не происходит:
- Окисление конденсированных углеводородов:
Химические свойства[править | править код]
Молекула хинона многоцентровая, поэтому для хинонов характерны реакции:
- по карбонильной группе (идут под действием сильных нуклеофильных реагентов): реакции нуклеофильного замещения и нуклеофильного присоединения.
- по сопряжённой системе связи: неароматический первичный продукт присоединения перегрупировывается в замещённый гидрохинон(1,4 — гидроксибензол), в результате возникает термодинамически более выгодный ароматический продукт. Например, при реакции парабензохинина (1,4 — бензохинон) с HCl образуется 1,4-гидрокси,3-хлорбензол.
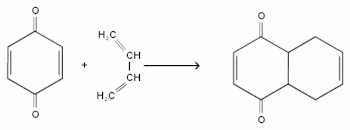
- по двойной связи(с образованием циклопродуктов):
- восстановление сопровождается переносом одного электрона. Присоединение одного электрона приводит к образованию семихинона (анион-радикала), после присоединения второго электрона образуется дианион двухатомного фенола, конечный продукт восстановления — гидрохинон:

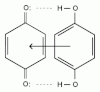
В процессе восстановления хинонов образуется окрашенный в темно-зелёный цвет промежуточный комплекс с переносом заряда — хингидрон, в котором образуется водородная и донорно-акцепторная связь:
Восстановление хинонов до двухатомных фенолов проводят с помощью самых разнообразных восстановителей, среди которых в лабораторных условиях предпочтение отдаётся дитиониту натрия Na2S2O4 в щелочной среде.[4]
Применение[править | править код]
Хиноны являются структурной основой пигментов. Важнейший краситель — ализарин (1,2-диоксиантрахинон). Ализариновые красители светоустойчивы, применяются в лакокрасочной промышленности, полиграфии. Но из-за большой стоимости используются реже, чем азокрасители. Окислительные свойства хинонов проявляются в биохимических реакциях. Убихиноны (коферменты Q) распространены в животном и растительном мире, участвуют в переносе электронов и протонов в дыхательной цепи.
Примечания[править | править код]
- ↑ И. С. Дмитриев. Взгляд на формирование химических школ Петербурга. Природа, № 9, 2003. Дата обращения: 18 мая 2014. Архивировано 5 марта 2016 года.
- ↑ Wöhler, F. Untersuchungen über des Chinons. Ann. 1844, 51, 152
- ↑ Х. Гюнтер. Введение в курс спектроскопии ЯМР, М., 1984 (стр. 92)
- ↑ [1] Архивная копия от 23 мая 2012 на Wayback Machine "Органическая химия.В 4-х частях.Ч.3/О.А.Реутов, А.Л.Курц, К.П.Бутин - М, БИНОМ.Лаборатория знаний, 2004. - 544 с., ил."
Литература[править | править код]
- Л. Физер, М. Физер. Органическая химия. Углублённый курс. М.: Химия, 1996. т.2, гл. 26 Хиноны и ареноны.
- Е. В. Федоренко, И. В. Богомолова «Органическая химия», ISBN 978-5-369-00143-1