Остеоартроз
| Остеоартроз | |
|---|---|
 | |
| МКБ-10 | M15-M19, M47 |
| МКБ-9 | 715 |
| МКБ-9-КМ | 715.3[1] |
| OMIM | 165720 |
| DiseasesDB | 9313 |
| MedlinePlus | 000423 |
| eMedicine | med/1682 orthoped/427 pmr/93 radio/492 |
| MeSH | D010003 |
Остеоартро́з (новолат. osteoarthrosis, от др.-греч. ὀστέον «кость» + ἄρθρον «сустав»), деформирующий остеоартроз (ДОА), артроз, деформирующий артроз — дегенеративно-дистрофическое заболевание суставов, причиной которого является поражение хрящевой ткани суставных поверхностей[2].
В зарубежной литературе для обозначения того же заболевания используется другой термин — osteoarthritis (рус. остеоартрит).
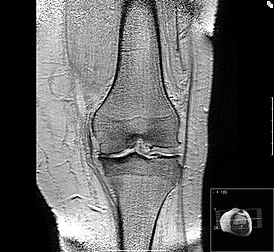
Симптомами заболевания являются боль в суставе, скованность сустава по утрам или после периода покоя, ухудшение подвижности сустава, хруст/треск/скрип при движении и припухлость/увеличение/изменение внешнего вида сустава[3][4]. Инструментально оно диагностируется при рентгенологическом исследовании[5].
Остеоартрит (остеоартроз) часто начинается в возрасте 40−50 лет. Подавляющее большинство 80-летних людей поражены этим заболеванием в той или иной степени. У людей моложе 40 лет заболевание чаще всего обнаруживается случайно при проведении рентгенологического обследования и протекает без симптомов, за исключением ситуаций, когда остеоартроз является последствием травмы[источник не указан 86 дней]. В возрасте от 40 до 70 лет эта болезнь чаще поражает женщин, чем мужчин. После 70 лет заболевание поражает представителей любого пола с одинаковой частотой[5].
Определение[править | править код]
Остеоартроз (остеоартрит) представляет собой хроническую артропатию, характеризующуюся поражением и разрушением суставного хряща, сочетающуюся с другими суставными изменениями, в том числе гипертрофией костной ткани (развитие остеофитов). Это наиболее распространённое заболевание суставов[4].
Остеоартрит — хроническое заболевание, вызывающее повреждение хрящей и окружающих их тканей. Для заболевания характерна боль, скованность и утрата функции[5].
Симптомы заболевания[4]:
- постепенно развивающаяся боль, усиливающаяся или начинающаяся при физической нагрузке;
- периодическая припухлость сустава.
В основе дегенеративных дистрофических изменений при артрозе лежит первичное повреждение хряща с последующей воспалительной реакцией, поэтому часто артроз называют артрозо-артритом. Артроз всегда связан с деформацией костной ткани, в связи с чем его также называют остеоартритом или деформирующим артрозом.[источник не указан 1155 дней]
Терминологические определения «остеоартроз», «остеоартрит», «деформирующий артроз» в Международной классификации болезней десятой редакции представлены как синонимы[6].
Чаще всего термин «остеоартроз» применяется для обозначения хронического прогрессирующего заболевания синовиальных суставов[7].
Выделяют локализованную (с поражением одного сустава) и генерализованную формы остеоартроза (полиостеартроз). Некоторые распространённые виды остеоартроза получили отдельные названия. В частности, термин «гонартро́з» (от др.-греч. γόνυ «колено») используют для обозначения артроза коленного сустава, «коксартро́з» (от лат. coxae «тазовая кость») — для обозначения артроза тазобедренного сустава.[источник не указан 1155 дней]
Различают первичный (иначе — идиопатический) и вторичный остеоартрит. В подавляющем числе случаев причина первичного остеоартрита не ясна. При этом обычно поражён один коленный сустав, реже несколько суставов, ещё реже — многие или почти все суставы в организме[5].
Вторичный остеоартрит вызван другим заболеванием или нарушением, чаще всего это инфекция, порок развития сустава, травма или нарушение обмена веществ[5].
Эпидемиология[править | править код]
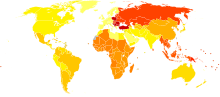

Остеоартроз — самая распространённая форма поражения суставов[4][5] и одна из главных причин нетрудоспособности, вызывающая ухудшение качества жизни и значительные финансовые затраты, особенно у пожилых людей.
Встречается остеоартроз повсеместно. В США им болеет 21 млн человек (примерно 7 % населения). Широкомасштабное исследование в 7 городах бывшего СССР выявило манифестный (сопровождающийся клиническими симптомами) остеоартроз у 6,43 % обследованных (41 348 человек старше 15 лет)[9].
В целом, в различных странах мира распространённость и заболеваемость остеоартрозом широко разнится. Например, распространённость остеоартроза на Украине составляет 2515,7 на 100 тыс. населения, заболеваемость — 497,0 на 100 тыс. населения. Как установлено популяционными исследованиями, эти показатели несколько ниже, чем в США, и значительно выше, чем в Великобритании[7][10].
Заболеваемость остеоартрозом резко увеличивается с возрастом, достигая трети населения в пожилом и старческом возрастах. Среди больных остеоартрозом в молодом возрасте преобладают мужчины, а в пожилом возрасте — женщины. В США остеоартроз встречается у 2 % населения моложе 45 лет, у 30 % в возрасте 45−64 лет и у 63−85 % старше 65 лет.[11]
В то же время в Швеции манифестный остеоартроз периферических суставов обнаружен только у 5,8 % населения в возрасте 50−70 лет.
Чаще всего при остеоартрозе поражаются суставы кисти, первый плюснефаланговый сустав стопы, суставы шейного и поясничного отделов позвоночника, коленных и тазобедренных суставов. Однако по тяжести нарушения функции опорно-двигательного аппарата первое место занимают тазобедренный, коленный и голеностопный суставы, а также плечевой сустав[12].
Этиология[править | править код]

По современным представлениям, остеоартрит (остеоартроз) возникает в результате взаимодействия различных внутренних и внешних факторов. Среди них возраст, женский пол, дефекты развития, наследственная предрасположенность, избыточный вес, чрезмерные спортивные и профессиональные нагрузки, травма[13].
Среди всех факторов риска избыточная масса тела имеет особое значение. Она способствует как возникновению остеоартрита, так и более быстрому прогрессированию этого заболевания[13].
Остеоартроз поражает все ткани суставов. Заболевание проявляется морфологическими, биохимическими, молекулярными и биомеханическими изменениями в клетках и матриксе, которые приводят к размягчению, разволокнению, изъязвлению и уменьшению толщины суставного хряща, а также к остеосклерозу с резким утолщением и уплотнением кортикального слоя субхондральной кости, формированию остеофитов и развитию субхондральных кист[7].
Клинически остеоартроз проявляется артралгиями, болезненностью и ограничением движений, рецидивирующим синовитом, местным воспалением в различных тканях сустава.
Первичный и вторичный остеоартроз[править | править код]
Остеоартроз бывает первичным и вторичным.
Если причина развития заболевания не установлена, то такой артроз принято называть первичным, или идиопатическим (от др.-греч. ἴδιος «своеобразный, особый, необычный» + πάθος «болезнь»).
Вторичный остеоартроз имеет явную причину: он развивается после травмы, при нарушениях метаболизма, эндокринных заболеваниях, как исход дегенеративно-некротического процесса (асептический некроз головки бедренной кости, рассекающий остеохондрит (болезнь Кёнига), болезнь Пертеса), как исход воспалительного процесса (гнойное воспаление сустава, ревматоидный артрит, артрит при системной красной волчанке, при туберкулёзе).
Основные причины[править | править код]
Остеоартроз является мультифакториальным полиэтиологическим заболеванием. Три основные причины развития дегенеративно-дистрофического процесса в суставе: травма, дисплазия и воспаление.
Травма сустава — самая частая причина артроза. На втором месте стоит дисплазия сустава — врождённые особенности, которые сопровождаются плохой биомеханикой сустава.
Воспаление также достаточно часто приводит к повреждениям тканей сустава и развитию вторичного артроза. Чаще всего это является результатом аутоиммунных заболеваний (например, ревматоидный артрит), реже — инфекционного процесса (к примеру, острое гнойное воспаление сустава, вызванное стафилококком или другой специфической инфекцией (при гонорее, сифилисе, клещевом энцефалите)). Это также очень распространённое осложнение при хронических гемартрозах (гемофилия).
Факторы риска[править | править код]
Факторами риска первичного остеоартроза являются: наследственная предрасположенность, избыточная масса тела, пожилой возраст, специфические профессии. Кроме этого, заболеваемость остеоартрозом зависит от пола и расовой/этнической принадлежности.
К генетическим факторам относятся: наследственные нарушения и мутации коллагена II типа, другие наследственные заболевания костей и суставов, врождённые нарушения развития сустава (дисплазии)[7].
Накладывают отпечаток на развитие и прогрессирование остеоартроза негенетические (ненаследуемые) множественные факторы, такие как:
- возраст, остеопороз;
- избыточная масса тела;
- нарушение эндокринного баланса организма, в том числе снижение секреции эстрогенов (постменопаузальный период);
- метаболические нарушения в организме;
- дефицит в организме микроэлементов;
- нарушение развития (дисплазия) и приобретённые заболевания костей и суставов;
- нейродистрофические проявления патологического процесса в пояснично-крестцовом (синдром пояснично-подвздошной мышцы), или в шейном отделе позвоночника (плече-лопаточный периартрит);
- воспалительный процесс в суставе.
Следующие факторы риска остеоартроза — факторы окружающей среды:
- переохлаждение;
- нарушение экологического равновесия[источник не указан 1361 день];
- действие химических токсинов;
- травма сустава, повторяющиеся микротравмы;
- операции на суставах (например, менискэктомия);
- род занятий и физическая активность на работе.
Стадии заболевания[править | править код]
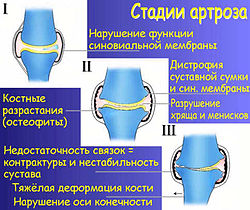
Вне зависимости от причины, различают 3 стадии артроза[14]. При первой или начальной стадии артроза нет выраженных морфологических нарушений тканей сустава. Изменения относятся только к функции синовиальной оболочки, к биохимическому составу синовиальной жидкости, которая за счёт диффузии питает хрящ и мениски сустава. Сустав теряет способность противостоять привычной для него нагрузке, и перегрузка сустава сопровождается воспалением и болевым синдромом.
Во второй стадии заболевания мы видим начинающееся разрушение суставного хряща и менисков. Кость реагирует на нагрузку суставной площадки краевыми разрастаниями — остеофитами.
Вторая стадия неизбежно переходит в третью — стадия тяжёлого артроза. Её признаки — выраженная костная деформация опорной площадки сустава, которая изменяет ось конечности. Несостоятельность, укорочение связок сустава приводит к патологической подвижности сустава или в сочетании с жёсткостью суставной сумки — к резкому ограничению естественных движений — контрактур. Хроническое воспаление и хронический болевой синдром обычно сопровождают 2 и 3 стадию.
В начальной стадии заболевания мышцы, которые осуществляют движения в суставе, ослаблены, но, в общем, не изменены. Во второй стадии наблюдается нарушение функции мышц за счёт нарушения рефлекторной нейро-трофической регуляции. В третьей стадии заболевания нагружение сустава и двигательная активность резко нарушается, в связи с контрактурами и нарушением оси конечности изменяется амплитуда сокращения мышцы, изменяются нормальные точки прикрепления мышечно-сухожильного комплекса. Это сопровождается укорочением или растяжением мышцы, снижением способности к полноценному сокращению. Трофические нарушения при заболевании сустава касаются не только мышц, но и всех тканей конечности.
Патогенез[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |

В основе патогенеза этого заболевания лежит нарушение функции и структуры хряща сустава. Суставной хрящ — высокоспециализированная ткань, состоящая из матрикса и погружённых в него хондроцитов. Матрикс содержит две главные макромолекулы, гликозамины (протеогликаны) и коллаген. Высокая концентрация протеогликанов в хряще держит коллагеновую сеть под напряжением, способствуя таким образом равномерному распределению нагрузки, которая воздействует на хрящ, и обеспечивая восстановление формы после прекращения действия нагрузки. При потере даже небольшого количества гликозаминов сопротивление матрикса хряща к воздействию физической нагрузки уменьшается, и поверхность хряща становится чувствительной к повреждению. На самых ранних стадиях артроза хрящ становится толще, чем в норме, но при прогрессировании — истончается. Хрящ становится мягким и рыхлым, на нём появляются глубокие язвы, обычно только в наиболее нагружаемой части сустава.
В норме, при периодических нагрузках, например при ходьбе, хрящевая пластинка деформируется и возвращает прежнюю форму, выполняя функцию своеобразного насоса, который обеспечивает выталкивание продуктов распада и «всасывание» питательных веществ и строительного материала. Сжатие и восстановление формы при нагружении — это основное условие регенерации повреждённой хрящевой ткани. Однако чрезмерное или длительное нагружение сустава неблагоприятно влияет на функцию суставного хряща и утяжеляет течение артроза.
Питание хряща и менисков сустава осуществляется только за счёт синовиальной жидкости. От того, в каком количестве и какого качества жидкость секретирует синовиальная оболочка, зависит «здоровье» скользящих и амортизирующих структур сустава.
Синовиальная мембрана выполняет важную функцию фильтрации строительного материала хряща — гиалуроновой кислоты, она предохраняет вымывание последней из полости сустава. Нарушение биохимического состава синовиальной жидкости при травме или воспалении сустава собственно и приводит к развитию болезни, именуемой остеоартрозом.
Эффективность циркуляции и диффузии синовиальной жидкости напрямую связана с движением в суставе и нагружением сустава. Движение в суставе необходимо для обмена веществ в хряще. Само по себе длительное ограничение движений в суставе приводит к ухудшению питания хряща.
При артрозе нарушается равновесие между образованием нового строительного материала для восстановления хряща и его разрушением. Хрящ из прочной, эластичной структуры превращается в сухую, мутную, тонкую с шероховатой поверхностью. Подлежащая кость становится толще и разрастается в стороны от хряща, что ограничивает движение и является причиной деформации суставов. Суставная капсула уплотняется — фиброзируется, а также воспаляется. Сустав наполняется воспалительной жидкостью, которая растягивает капсулу и связки сустава. Боль, а в дальнейшем и деформация суставных поверхностей при артрозе ведёт к тугоподвижности сустава и к контрактурам сустава. Утренняя и стартовая боль, а также скованность в суставе у больных с деформирующим артрозом собственно и обусловлена низкой эластичностью хряща и необходимостью стартовых движений для восстановления достаточной эластичности хряща. Это создаёт ощущение боли и скованности.
При воспалении сустав принимает положение покоя или физиологическое положение. При этом положении обеспечивается максимальное расправление связок и капсулы сустава. В этом положении боль в суставе минимальна. Большое влияние на течение патологического процесса оказывает состояние так называемого мышечного корсета сустава, то есть системы мышц, которая не только осуществляет движение в суставе, но и является стабилизаторами сустава, поглощая мощные инерционные импульсы при движении. Так, внутренняя широкая мышца в составе квадрицепса бедра предохраняет коленный сустав от боковой нестабильности в момент приземления на пятку при ходьбе, а средняя ягодичная мышца на стороне опорной ноги ограничивает наклон таза в момент переноса, что предохраняет тазобедренный сустав от перегрузки.
В более тяжёлых случаях заболевания обнаруживается некроз тканей, а также вторичные артрозы[15].
Исход заболевания[править | править код]

Исход артроза — полное разрушение сустава с формированием анкилоза — полной неподвижности сустава или неоартроза с неестественной подвижностью. Это сопровождается тяжёлым нарушением функции конечности. В последнее время, не дожидаясь исхода заболевания, всё чаще применяют специальные операции по замене сустава протезом — эндопротезирование сустава. На рисунке изображена типичная для терминальной стадии артроза коленного сустава варусная деформация колена в сочетании с боковой патологической нестабильностью коленного сустава. Артроз блоковидного или шаровидного сустава, такого как тазобедренный, завершается анкилозированием. При этом замыкание сустава обычно происходит в нефизиологическом (порочном) положении конечности. В данном случае мы видим бедро в положении сгибания и приведения, при котором нога укорачивается, а ось конечности и биомеханика опорно-двигательной системы существенно нарушается.
Клиническое течение и диагностика[править | править код]
Если в начале болезни боль возникает лишь периодически, после значительной физической нагрузки, и быстро проходит в покое, то по мере прогрессирования заболевания интенсивность боли увеличивается, она не исчезает после отдыха и появляется в ночные часы.
В условиях доказательной медицины разработан целый ряд стандартных тестов для оценки остеоартроза. Для оценки болей в суставах и утренней скованности используется десятибалльная визуальная аналоговая шкала. Для характеристики гонартроза и коксартроза широко применяют индекс Лекена[16].
| Баллы для расчёта суммарного индекса | |||||||
|---|---|---|---|---|---|---|---|
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | |
| Боль в течение ночи | нет | только при движении | без движения | ||||
| Боль при ходьбе | нет | при прохождении определённого расстояния | в начале движения | ||||
| Боль в положении сидя после 2 ч | нет | да | |||||
| Утренняя скованность | нет | меньше 15 мин | больше 15 мин | ||||
| Усиление боли в положении стоя в течение 30 мин | нет | да | |||||
| Ограничение дистанции ходьбы | нет | больше 1 км, но трудно | 1 км | 500—900 м | 300—500 м | 100—300 м | меньше 100 м |
Для оценки тяжести нарушения функции нижних конечностей используют интегральный показатель, который вычисляется как среднее арифметическое значение от величины 6 экспертных признаков в %. НФНК более 20 % расценивается как тяжёлое и соответствует III и более группам инвалидности (в соответствии с экспертными оценками ВТЭК). Показатель НФНК используется как основной критерий оценки эффективности реабилитационных мероприятий в амбулаторных условиях[12].
| Экспертный признак | Оценка нарушения функции нижних конечностей в % | ||||
|---|---|---|---|---|---|
| 0−20 | 21−40 | 41−60 | 61−80 | 81−100 | |
| Передвижение | хромота незначительна | хромота выражена | хромота резко выражена | патологический тип передвижения | ходьба невозможна |
| Дополнительная опора | отсутствует | трость | две трости | костыли | специальные средства |
| Выполнение бытовых функций | не ограничено | ограничено незначительно | ограничено | резко затруднено | невозможно |
| Самообслуживание | не ограничено | ограничено незначительно | ограничено | резко затруднено | невозможно |
| Пользование общественным транспортом | не ограничено | ограничено незначительно | ограничено | резко затруднено | невозможно |
| Выполнение профессиональных обязанностей | не ограничено | ограничено незначительно | ограничено | резко затруднено | невозможно |
Клиническая картина остеоартроза включает основные симптомы: «механический» характер боли, утренняя скованность не более 30 мин, ограничение объёма движений, снижение функциональных возможностей сустава.
Основные признаки клинической картины остеоартроза — это болезненные точки и плотные утолщения по краю суставной щели, крепитация, умеренные признаки воспаления, ограниченные болезненные движения, ощущения напряжённости в суставе, нестабильность.
Клинические критерии, позволяющие поставить диагноз «остеоартроз»:
- боль в суставах, возникающая в конце дня и/или в первой половине ночи, а также после механической нагрузки, уменьшающаяся в покое.
- наличие деформации сустава за счёт костных разрастаний.
Рентгенодиагностика остеоартроза[править | править код]

Рентгенологическая семиотика остеоартроза складывается из признаков, отражающих дистрофические изменения в суставных хрящах (сужение суставной щели) и в костной ткани (уплощение и деформация суставных поверхностей, кистовидные образования), нестабильность суставов (подвывихи, искривления оси конечностей), реактивные компенсаторно-приспособительные процессы (краевые костные разрастания, субхондральный остеосклероз).

Ранним рентгенологическим симптомом являются краевые костные разрастания — остеофиты — следствие активной пролиферации периферических отделов суставного хряща. Они проявляются вначале заострением краёв суставных поверхностей, а затем, нарастая, образуют массивные костные шипы и губы. Краевые остеофиты, как правило, раньше обнаруживаются со стороны суставных впадин.
Сужение суставной щели свидетельствует о значительных изменениях суставных хрящей. Суставная щель может стать клиновидной, суживаясь с одной стороны и нередко расширяясь при этом с противоположной, что указывает на недостаточность связочного аппарата и нестабильность сустава.
При остеоартрозе утрачивается амортизационная функция суставных хрящей, предохраняющих костную ткань от механических перегрузок. Как компенсация развивается остеосклероз субхондральной губчатой кости. Особенно он выражен при коксартрозе в крыше вертлужной впадины, распространяясь иногда почти на всё тело подвздошной кости. Однако рано или поздно этот механизм компенсации становится недостаточным. Механические силы, передающиеся непосредственно с одной суставной поверхности на другую, вызывают атрофию от давления их наиболее нагружаемых участков и прежде всего центральных отделов суставных головок. Вследствие этого они уплощаются и одновременно расширяются.

Результатом поражения суставных хрящей являются очаговые дистрофические и некротические процессы в субхондральной губчатой кости, соответствующие локальным пикам механических напряжений. В результате этих процессов формируются кистовидные образования. Последние наиболее характерны для коксартроза, при котором они часто множественны и достигают больших размеров (эрозивный артроз).
В России ранее использовалась рентгенологическая классификация остеоартроза по стадиям развития, разработанная Н. С. Косинской.
- Остеоартроз на I стадии характеризуется главным образом краевыми костными разрастаниями при незначительном сужении суставной щели.
- На II стадии она сужена более отчётливо, возникает субхондральный остеосклероз.
- Резкое сужение суставной щели на III стадии сопровождается уплощением суставных поверхностей и развитием кистовидных образований.
В настоящее время используется рентгенологическая классификация остеоартроза по Kellgren-Lawrence[18][19]:
- I стадия (сомнительный) — сомнительное сужение суставной щели, возможны остеофиты
- II стадия (мягкий) — определённые остеофиты и сомнительное сужение суставной щели
- III стадия (умеренный) — умеренные остеофиты, определённое сужение суставного пространства, возможная деформация костей
- IV стадия (тяжёлый) — большие остеофиты, сужение суставного пространства, тяжёлый остеосклероз, определённая деформация костей
Рентгенологическое исследование играет важную роль в распознавании этиологических факторов при вторичных остеоартритах. Так, при посттравматическом остеоартрозе оно даёт возможность обнаружить костные деформации после внутрисуставных переломов, установить характерные признаки диспластических артрозов, особенно в тазобедренном суставе, на рентгенограммах можно выявить краевые дефекты суставных поверхностей, остеопороз и атрофию костей при постартритических артрозах. С помощью рентгенографии можно установить связь между отдалёнными от суставов деформациями костей диспластической, посттравматической или иной природы. Например, угловое искривление оси длинной трубчатой кости, сопровождающимися изменениями условий нагрузки на суставы, и вторичным (статическим) остеоартрозом. Рентгенологическое исследование даёт возможность выявить такие причины артроза, как внутрисуставное тело при хондроматозе сустава[20].
Лечение[править | править код]
Целями лечения остеоартрита (остеоартроза) являются обезболивание, сохранение подвижности сустава и оптимизация его функций. Для этого используются, в порядке приоритета: лечебная физкультура (ЛФК) и изменение образа жизни, медикаментозное лечение, в последнюю очередь, если предыдущие методы не дали результата — протезирование[5].
Физические мероприятия (ЛФК) — это упражнения на растяжку, укрепление мышц и осанку. Наиболее важная цель упражнений — укрепить близлежащие к суставу мышцы для лучшей амортизации ударных нагрузок (например, при ходьбе)[5].
Медикаментозное лечение направлено на снижение боли, для этого применяются анальгетики. Пищевые добавки не имеют заметного эффекта на протекание болезни[5]. Также для снижения боли эффективна внутрисуставная инъекция кортикостероидов[21]. Другие лекарственные методы, в том числе приём хондропротекторов (препараты на основе хондроитина и глюкозамина) и внутрисуставные инъекции гиалуроновой кислоты, не имеют клинической эффективности. Из-за отсутствия доказательств пользы от применения хондопротекторов и гиалуроновой кислоты профильные научные сообщества (Американская академия хирургов-ортопедов — англ. American Academy of Orthopaedic Surgeons, AAOS, Американская коллегия ревматологов — ACR, Европейская лига против ревматизма — EULAR и Международное общество исследований остеоартрита — OARSI) рекомендуют избегать их применения. Внутрисуставное введение стволовых клеток также не имеет научного обоснования[22].
Хирургическое протезирование сустава применяется тогда, когда остальные методы лечения не в силах снять боль или улучшить функции сустава[5]. Протезирование имеет существенно больший уровень осложнений и является последним выбором среди методов лечения[23]. При этом полная артропластика тазобедренного сустава не приводит к улучшению качества жизни пациентов[24].
Двигательный режим и ЛФК[править | править код]

По мере того, как поверхность кости теряет хрящевую защиту, пациент начинает ощущать боль при физической нагрузке на сустав, в частности при ходьбе или в положении стоя. Это приводит к гиподинамии, поскольку пациент щадит сустав, стараясь избежать боли. В свою очередь, гиподинамия может явиться причиной локальной атрофии мышц и слабости связок. В период обострения больному суставу придают нейтральное положение для создания покоя и максимальной разгрузки. К движениям в суставе приступают сразу же после снятия воспаления и боли не позднее чем через 3-5 дней.
Задачи ЛФК при комплексном лечении артроза можно представить в виде пирамиды, в основании которой лежит восстановление подвижности и необходимой амплитуды движений в суставе; увеличения силы и выносливости мышц; аэробная тренировка. На этой основе собственно и располагаются все остальные методы восстановительного лечения.
Многочисленные исследования показывают, что на благоприятный прогноз в лечении суставов влияет образование больного и уровень его интеллекта. Понимание того, что с больным суставом надо жить, работать, что с заболеванием надо считаться, должно привести к изменению образа жизни больного, в котором высокая двигательная активность должна разумно сочетаться со строгим режимом разгрузки сустава. Пробуждение мотивации к двигательной активности, к здоровому образу жизни, воспитание необходимых двигательных качеств, обучение пациента методикам ЛФК для самостоятельного применения, — всё это также является важнейшей задачей ЛФК при лечении артрозов[25].
Дозирование нагрузки — самая трудная задача ЛФК. С одной стороны, достижение лечебного эффекта физической нагрузки при коротком воздействии просто невозможно. С другой стороны, перегрузка сустава, обострение болезни, необходимость постельного режима перечеркнёт все усилия проделанной работы.
Двигательный режим (объём эффективной, но безопасной нагрузки, необходимость дополнительной опоры) и конкретные формы, средства и методики ЛФК зависят от стадии, локализации, особенности течения заболевания и определяются индивидуально врачом после обследования и оценки функционального состояния пациента.
Фармакотерапия[править | править код]
Поскольку поводом для обращения больного к врачу является боль, то на первом месте в фармакотерапии стоят нестероидные противовоспалительные препараты, назначаемые для снятия боли и воспаления. В фазе острой боли, когда остеоартроз может быть осложнён синовитом, используется внутрисуставное введение кортикостероидов (дипроспан, триамцинолон, гидрокортизон) для снятия боли и воспаления[26].
Хондропротекторы (хондроитин сульфат и глюкозамин) до сих пор применяют на территории бывшего СССР в виде курсового лечения внутрь (см.: диета и пищевые добавки), внутримышечно, внутрисуставно в I и II стадии заболевания. Однако результаты ряда современных научных исследований показывают отсутствие эффекта у данных препаратов по сравнению с плацебо[27]. Тем не менее результаты других современных научных исследований показывают наличие эффекта у данных препаратов по сравнению с плацебо[28]. Для внутрисуставного введения применяют также препараты гиалуроновой кислоты[12] и полиакриламидного геля.
Применяются растительные препараты — неомыляемые соединения авокадо и сои (Пиаскледин 300)[29][30][31]. Восстанавливается баланс анаболических (созидательных) и катаболических (разрушительных) процессов в хрящевой ткани. Это происходит путём снижения выработки различных медиаторов воспаления (IL-1,6,8, PGE2, MMP-3, NO), способствующих появлению боли и скованности, а также дальнейшему разрушению сустава[32][33]. И за счёт продукции веществ, составляющих основу хрящевого матрикса (коллагена II типа, аггрекана), что позволяет замедлять разрушение сустава. Действия применение неомыляемых соединений авокадо и сои позволяет облегчить симптомы заболевания и замедлить его прогрессирование[34].
| Рекомендации по лечению остеоартрита Международного общества по изучению ОА (OARSI):[35] | |||||
|---|---|---|---|---|---|
| Рекомендация | Уровень[36] | ES для боли (95 % доверительный интервал) | Частота встречаемости в других рекомендациях | Уровень консенсуса экспертов (%) | Сила рекомендации (%) (95 % доверительный интервал) |
| Парацетамол в дозе до 4 г/сут может служить эффективным начальным анальгетиком для лечения слабого и умеренного болевого синдрома при ОА ТС или КС. Если адекватного ответа не получено, или имеется выраженный болевой синдром и/или признаки воспаления, следует рассмотреть альтернативную фармакотерапию с учётом относительной эффективности и безопасности, а также приёма других медикаментов и наличия сопутствующих заболеваний | Ia (КС)IV (ТС) | 0,21 (0,02 до 0,41) | 16/16 | 77 | 92 (88-99) |
| У больных с симптомами ОА КС или ТС следует использовать НПВС в минимальных эффективных дозах, а их длительное применение по возможности следует избегать. При высоком риске осложнений со стороны желудочно-кишечного тракта можно рассмотреть возможность назначения либо селективного ингибитора циклооксигеназы-2, либо неселективного НПВС в сочетании с ингибитором протонной помпы или мизопростолом, но при наличии кардиоваскулярных факторов риска как циклооксигеназа-2-селективные, так и неселективные НПВС должны использоваться с осторожностью | Ia (КС) Ia (ТС) | 0,32 (0,24 до 0,39) | НПВС+ИПП 8/8 НПВС + мизопростол 8/8 ЦОГ-2 ингибиторы 11/11 |
100 | 93 (88-99) |
| Местные НПВС и капсаицин могут быть эффективными дополнительными или альтернативными пероральным анальгетикам/противовоспалительным средствам при ОА КС | Ia (НПВС) Ia (капсаицин) | 0,41 (0,22 до 0,59) | 7/9 8/9 |
100 | 85 (75-95) |
| Внутрисуставное введение кортикостероидов может быть использовано в лечении ОА КС или ТС и должно быть рассмотрено в тех случаях, когда выраженный болевой синдром не отвечает удовлетворительно на пероральные анальгетические/ противовоспалительные средства и у больных с симптомным ОА КС при наличии выпота или других признаков местного воспаления | Ib (ТС) Ia (КС) |
0,72 (0,42 до 1,02) | 11/13 | 69 | 78 (61-95) |
| Лечение глюкозамина сульфатом и/или хондроитина сульфатом может обеспечить симптоматический эффект у больных ОА КС. При отсутствии ответа в течение 6 месяцев приём этих препаратов следует прекратить | Ia (глюкозамин) Ia (хондроитин) |
0,45 (0,04 до 0,86) 0,30 (-0,1 до 0,70) |
6/10 2/7 |
92 | 63 (44-82) |
| У больных с симптомным ОА КС глюкозамина сульфат и хондроитин сульфат могут обладать структурно-модифицирующими эффектами, а диацереин может обладать структурно-модифицирующими эффектами при симптомном ОА ТС | Ib (КС) Ib (ТС) |
69 | 41 (20-62) | ||
| Использование слабых опиоидов и наркотических анальгетиков может быть рассмотрено для лечения рефрактерного болевого синдрома при ОА КС и ТС в тех случаях, когда другие средства оказались неэффективными или противопоказаны. Сильные опиоиды должны использоваться только в исключительных случаях при выраженной боли. У таких пациентов следует использовать нефармакологические методы лечения и рассмотреть необходимость хирургического вмешательства | Ia (слабые опиоиды) IV (сильные опиоиды) IV (другие) |
9/9 | 92 | 82 (74-90) | |
Внутрисуставные инъекции[править | править код]
Для внутрисуставного введения используют препараты гиалуроновой кислоты: Ферматрон, Остенил, Синвиск, Ортовиск, Гиалган, Артрум и др. Эти препараты получили широкое распространение, но они обладают кратким сроком действия, аллергическими и даже инфекционными осложнениями на их внутрисуставное введение[37][38][39]. По данным систематического обзора и метаанализа, опубликованного в 2012 году в Annals of Internal Medicine, внутрисуставные инъекции гиалуроновой кислоты приносят небольшую, клинически несущественную пользу и обусловливают значительный риск серьёзных побочных явлений[40]. Согласно кокрановскому обзору 2015 года, не существует доказательств эффективности гиалуроновой кислоты при остеоартрите голеностопного сустава: имеющиеся клинические испытания применения гиалуроновой кислоты при этом заболевании низкокачественные (малое число участников)[41].
Кроме препаратов гиалуроновой кислоты, существуют синтетические препараты, полностью исключающие осложнения и обладающие долгим сроком действия: Нолтрекс, Артрамид, Нолтрексин. Проведённые клинические исследования показали, что лечебный эффект лечения пациентов с гоноартрозом уже после первого же введения синтетического препарата в коленный сустав был связан с восстановлением вязкоэластических свойств синовиальной жидкости, нормализацией синтеза эндогенного протеогликана хондроцитами, замедлением или остановкой процесса разрушения гиалинового хряща. Выраженный лечебный эффект пациенты ощущали независимо от стадии и давности существования у них гонартроза. Благодаря наличию в своём составе ионов серебра, обладают бактериостатическим действием на внутреннюю среду сустава и улучшает биологические функции синовиальной оболочки. Синтетические препараты обладают также анальгетическим, противовоспалительным, антиоксидантным и хондропротекторным действием[42].
Внутрисуставная оксигенотерапия[править | править код]

Ранее предлагалось выполнение внутрисуставной оксигенотерапии и озонотерапии. Считалось, что внутрисуставная оксигенотерапия патогенетически обоснована, так как в условиях кислородной недостаточности усиливается гликолиз в тканях сустава, в результате чего накапливаются недоокисленные продукты обмена: молочная, пировиноградные кислоты. Для их окисления требуется усиленная доставка кислорода в ткани сустава. Кроме того, кислород растягивает капсулу сустава и создаёт разгружающую «газовую» подушку[43]. В настоящее время этот метод не используется и не содержится в рекомендациях по данному вопросу[44].
Лазеротерапия[править | править код]
Лазеротерапия применяется как основной метод лечения (противовоспалительный, анальгезирующий, стимулирующий эффекты) в ранней стадии заболевания, так и в качестве фактора, снижающего риск применения кортикостероидов и манипуляций на костях и суставах на более поздних стадиях[45].
Декомпрессия метаэпифиза и внутрикостные блокады[править | править код]
Патогенетически обоснованной и достаточно эффективной является методика декомпрессии зоны метаэпифиза бедра. Устранение повышенного внутрикостного давления способно «сломать» ишемический цикл заболевания. Успех от применения этой методики колеблется от 50 до 90 %. Эффективность лечения повышается при применении малотравматичного и доступного в амбулаторных условиях метода туннелизации зоны метаэпифиза с декомпрессией кости и проведением внутрикостных блокад. Декомпрессия осуществляется в области большого вертела, мыщелков бедра, голени, внутренней лодыжки и пяточной кости.
Многоканальная электромиостимуляция[править | править код]

Многоканальная электромиостимуляция (МЭСМ) применяется у больных, в том числе старших возрастных групп, с выраженными нарушениями функции мышц и двигательного стереотипа с применением 6-канального стационарного электростимулятора под клинико-биомехано-электромиографическим контролем. Этот метод сочетается с мышечными, проводниковыми, внутрикостными блокадами, со внутрисуставной инъекционной терапией и электромиостимуляцией в покое. Положительный эффект лечения возможен, если при мануальном тестировании сила мышц составляет не менее 2 баллов. Кроме того, непременным условием проведения процедуры является возможность самостоятельного передвижения больного с дополнительной опорой или без неё на расстояние не менее 10 метров, а также отсутствие резко выраженного болевого синдрома[46].
Ортопедический электрет[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Метод лечении артроза с применением имплантируемых электретных стимуляторов остеорепарации - ортопедических электретов основан на непрерывном воздействии электрического поля электрета на сустав (костную и хрящевую ткань).
В конце 70-х годов XX века в Военно-Медицинской Академии им. С. М. Кирова под руководством профессора В.В. Руцкого начались исследования влияния электрического поля электретов на остеорепарацию. Более 40 лет исследований позитивного воздействия электрического поля показали высокую эффективность электретов при лечении артрозов суставов человека подтвердили возможность продуктивного применения электретов в клинической практике[47].
Многочисленные исследования показали, что электрическое поле способствует восстановлению костной и хрящевой ткани, благоприятно воздействует на микроциркуляцию в поражённом суставе, способствует купированию болевого синдрома и увеличению объёма движения в суставе[48].
Эндопротезирование суставов[править | править код]

При наличии показаний к операции методом выбора может быть эндопротезирование суставов. В настоящее время разработаны и успешно применяются эндопротезы тазобедренного и коленного суставов. При остеопорозе эндопротезирование осуществляется конструкциями с цементным креплением. Дальнейшее консервативное лечение способствует снижению сроков реабилитации оперированных больных и повышению эффективности лечения.
Диета и пищевые добавки при остеоартрозе[править | править код]
При остеоартрозе страдает хрящевая ткань. Для того, чтобы её укрепить, следует употреблять продукты, богатые коллагеном (желе, холодец), а также рыбий жир, ягоды, фрукты[источник не указан 2985 дней].
Медики не рекомендуют употреблять в пищу алкоголь, «пустые углеводы», которые содержатся в сахаре, газированных напитках, кондитерских изделиях[источник не указан 2985 дней].
Широкое применение в последнее время получили специально выпускаемые фармацевтической промышленностью препараты под название хондопротекторы. Включают в себя два основных компонента, очень важных для сохранения здоровья хряща - хондроитин и глюкозамин. Лечение хондопротекторами длительное (от полугода до нескольких лет) и эффект проявляется не сразу, носит накопительный характер. Эффективны только на начальных стадиях артроза[49].
Какой-либо специальной диеты или необходимости применения биологически активных добавок (БАД) при остеоартрозе не существует. Диета при остеоартрозе может определяться сопутствующей патологией или избыточной массой тела[44].
Санаторно-курортное лечение[править | править код]
Санаторно-курортное лечение позволяет проводить комплексную реабилитацию, включающую положительное воздействие лечебных грязей, ванн, сауны, физиопроцедур, массажа, занятий лечебной физкультурой. Немаловажную роль играет смена обстановки, снятие стрессорных воздействий, нахождение на свежем воздухе. Санаторно-курортное лечение можно проводить только вне обострения болезни.
Эффективность методов лечения[править | править код]
В 2006—2012 годах американское правительственное Агентство по исследованиям и качеству здравоохранения (англ. Agency for Healthcare Research and Quality, U.S. Department of Health and Human Services) провело по заданию правительства и Конгресса США ряд крупномасштабных исследований в области эффективности методов лечения остеоартроза, в ходе которых были обобщены и проанализированы результаты тысяч клинических испытаний.
Физиотерапевтическое лечение[править | править код]
В ходе крупномасштабного исследования, проведённого Агентством в 2012 году[50], было проанализировано сравнительное влияние разных методов физиотерапии на боль и физические ограничения, вызванные остеоартрозом коленного сустава. В ходе исследования было проанализировано 4266 статей и отчётов о клинических испытаниях (все, доступные на английском языке, с 1970 года), из которых были отобраны 422 наиболее релевантных и достоверных, результаты которых легли в основу исследования. В ходе исследования было произведено сравнение следующих методов лечения и реабилитации:
- аэробные упражнения;
- упражнения в воде;
- упражнения для развития силы мышц ног;
- упражнения для развития проприоцепции;
- образовательные программы;
- оздоровительная гимнастика тайчи;
- массаж;
- мобилизация сустава;
- мобилизация сустава с упражнениями;
- применение ортопедических приспособлений;
- тейпирование;
- пульсовая магнитотерапия (PEMF);
- ультразвуковая терапия;
- электромиостимуляция;
- диатермия;
- прогревание[51];
- криотерапия.
В результате исследования были сделаны следующие выводы:
- Аэробные и водные упражнения уменьшают физические ограничения у пациентов. Существенной разницы между результатами аэробных и водных упражнений установлено не было.
- Аэробные упражнения и упражнения для развитие силы мышц ног уменьшают боль и улучшают функциональные показатели.
- Упражнения для развития проприоцепции уменьшают боль.
- Ультразвуковая терапия уменьшает боль и улучшает функциональные показатели.
- Занятия гимнастикой цигун краткосрочно улучшают функциональные показатели, но эффект непродолжителен.
- Электромиостимуляция уменьшает боль на короткий период, но затем боль значительно усиливается.
- Следующие методы продемонстрировали эффективность, но исследований было недостаточно для точных утверждений: прогревание, массаж, мобилизация сустава.
- Следующие методы не продемонстрировали эффективность: пульсовая магнитотерапия, диатермия, криотерапия, тейпирование, образовательные программы, применение ортопедических приспособлений (речь идёт об измерениях, проведённых без ортопедических приспособлений, после окончания периода их ношения).
Обезболивающие препараты[править | править код]
В 2006 и 2011 годах Агентством были проанализированы результаты 273 исследований и клинических испытаний, касающихся применения обезболивающих препаратов при остеоартрозе[52][53]. Были собраны данные о применении различных нестероидных противовоспалительных препаратов (НПВП), ацетаминофена и хондроитина/глюкозамина. В результате исследований были сделаны следующие выводы:
- Между различными НПВП нет разницы в эффективности снятия болевого синдрома, но есть разница в опасности побочных эффектов. (Эффективность аспирина и других салицилатов не сравнивалась с эффективностью других НПВП, но при сравнении салицилатов между собой разницы в эффективности обнаружено не было.)
- Все селективные НПВП, а также частично селективные мелоксикам и этодолак, реже вызывают язвенную болезнь ЖКТ, чем неселективные НПВП. Вероятность язвенной болезни снижает одновременный с НПВП приём мизопростола, ингибиторов протонного насоса, и блокаторов H2-гистаминовых рецепторов (последние более эффективны в удвоенной дозе). Среди неселективных НПВП также было установлено, что напроксен чаще вызывает побочные эффекты со стороны ЖКТ, чем ибупрофен. Применение НПВП вместе с антикоагулянтами многократно увеличивает риск желудочно-кишечных кровотечений.
- Целекоксиб и большинство неселективных НПВП, за исключением аспирина, связаны с риском развития тяжёлых заболеваний сердечно-сосудистой системы. Более высокие дозы этих препаратов повышают риск, но связь между риском этих заболеваний и более продолжительным приёмом препаратов не была установлена.
- Все НПВП негативно влияют на артериальное давление, эдему и функцию почек.
- Между местным и внутренним применением НПВП, за исключением салицилатов, нет значительной разницы в эффективности снятия болевого синдрома при локализованном остеоартрозе. При этом местное применение НПВП уменьшает риск побочных эффектов со стороны ЖКТ, но увеличивает риск дерматологических побочных эффектов. Риск серьёзных заболеваний ЖКТ и сердечно-сосудистой системы не изучался для местного применения НПВП. Местное применение салицилатов было признано неэффективным и опасным.
- Бутадион. Может назначаться в виде таблеток или мази. Приём препарата направлен на купирование болевого синдрома, снижение температуры тела, которая сопровождает воспалительный процесс[54].
- Между хондроитином, глюкозамином и НПВП нет значительной разницы в эффективности снятия болевого синдрома. При этом в большинстве исследований, показавших эффективность глюкозамина, использовался глюкозамин высокого медикаментозного качества, недоступный в США из-за отсутствия разрешения FDA. Эффективность же распространённых ныне пищевых биологических добавок с хондроитином и глюкозамином вызывает большие сомнения.
- Ацетаминофен менее эффективен для снятия болевого синдрома, чем НПВП. Он более безопасен для ЖКТ, но может вызвать повышение энзимов печени в крови.
- Есть данные об эффективности местного применения капсаицина, но их недостаточно для точных утверждений.
Профилактика[править | править код]
Среди многочисленных путей профилактики остеоартроза можно выделить следующие, наиболее значимые:
- Профилактика и эффективное лечение травмы сустава
- Достаточная двигательная активность на протяжении всей жизни
- Снижение избыточного веса тела
- Своевременная коррекция приобретённого или врождённого нарушения биомеханики сустава (например, коррекция плоскостопия, исправление травматической деформации оси конечности, лечение врождённого вывиха бедра и т. п.)
- Соблюдение диеты. Употребление большого количества молочных продуктов, фруктов, ягод, овощей и зелени.[55]
Физические нагрузки[править | править код]
Мнение о том, что физическая нагрузка может привести к преждевременному «изнашиванию сустава», ошибочно. Исследования показывают, что само по себе занятие спортом не приводит к остеоартрозу[56]. Напротив, любая двигательная активность, направленная на сохранение подвижности суставов, на укрепление мышц, на координацию движений позволяет длительное время поддерживать хорошую функцию сустава и противостоять болезням[57].
Для пациентов, относящихся к «группе риска» заболевания артрозом (травма или дисплазия сустава, избыточный вес, низкая физическая подготовленность), рекомендуется упражнения с дозированной нагрузкой на сустав (дозированная ходьба, восхождения, велосипед, плавание).
Ходьба — это основная естественная локомоция человека. Повседневной ходьбой человек занят несколько часов в день. Это в любом случае больше, чем время специальных ежедневных занятий физической культурой. Поэтому важно, чтобы ходьба стала основным средством профилактики остеоартроза. Именно поэтому при последствиях травм и артрозах суставов нижних конечностей рекомендуют дозированную ходьбу как основной метод профилактики и лечения. Рекомендуя увеличить двигательную активность, прежде всего имеют в виду пройденные километры в течение дня (до 7 км). Дозирование ходьбы — это ограничение времени непрерывного (без отдыха) пребывания «на ногах» не более 30-40 минут, но не пройденного расстояния за день.
Контроль массы тела[править | править код]
Избыточная масса тела — важный фактор развития и прогрессирования остеоартроза. Снижение массы тела уменьшает риск развития заболевания и сопровождается улучшением функции суставов, поэтому в программу лечения обязательно включают диетотерапию[58].
Принято считать, что уменьшение веса тела на 1 кг снижает нагрузку при ходьбе на каждый коленный или тазобедренный сустав на 4 кг[59]. Именно поэтому при лечении артроза применяют программы ЛФК для снижения массы тела больного, в основе которых лежит аэробная тренировка.
Профилактика диспластического коксартроза[править | править код]
Своевременно не устранённая дисплазия сустава (неправильное лечение врождённого вывиха бедра) приводит к нарушению биомеханики тазобедренного сустава и к развитию тяжёлого заболевания, именуемого «диспластический коксартроз», нередко двустороннего[60][61].
Профилактика диспластических коксартрозов заключается в соблюдении ортопедического режима (избегать травм, физических упражнений или работы, связанных с инерционными нагрузками на сустав: бег, прыжки, поднятие тяжестей), а также в активном занятии физической культурой, направленной на укрепление мышц, стабилизирующих тазобедренный сустав (группа ягодичных мышц, четырёхглавая мышца бедра, разгибатели спины и мышцы брюшного пресса): плавание, ходьба на лыжах и т. п. Для женщин важны соблюдение ортопедического режима и ЛФК в до и послеродовом периоде.
Примечания[править | править код]
- ↑ Disease Ontology (англ.) — 2016.
- ↑ Покровский В. И. Малая медицинская энциклопедия. — Советская энциклопедия, 1996. — Т. 4. — 577 с. — ISBN 5-225-02819-5. Архивировано 7 июня 2012 года.Архивированная копия. Дата обращения: 9 мая 2007. Архивировано 7 июня 2012 года.
- ↑ Рубрикатор КР. cr.minzdrav.gov.ru. Дата обращения: 19 июня 2023. Архивировано 19 июня 2023 года.
- ↑ 1 2 3 4 Kontzias, 2018.
- ↑ 1 2 3 4 5 6 7 8 9 10 Kontzias, 2020.
- ↑ МКБ-10 : Международная статистическая классификация болезней и проблем, связанных со здоровьем : в 3 т.. — 10-е изд. — Казань : Медицина, 2003. — 2438 с. — ISBN 5-225-03268-0.
- ↑ 1 2 3 4 Корж H. А., Филиппенко В. А., Дедух Н. В. Остеоартроз — подходы к лечению— // Вісник ортопедії травматології та протезування. — 2004. — № 3. — С. 75—79. (недоступная ссылка)
- ↑ WHO Disease and injury country estimates. World Health Organization. Дата обращения: 11 ноября 2009. Архивировано 19 августа 2011 года.
- ↑ Беневоленская Л. И., Бржезовский М. М. Эпидемиология ревматических болезней. — М.: Медицина, 1988. — 237 с. — ISBN 5-225-01653-7.
- ↑ Коваленко В. Н., Борткевич О. П. Остеопороз. Практическое руководство. — К.: Морион, 2003. — 448 с.
- ↑ Rebecca J. Frey. Osteoarthritis: Encyclopedia of Medicine (англ.). CNET. Дата обращения: 25 ноября 2007. Архивировано 22 мая 2008 года.
- ↑ 1 2 3 Берглезов М. А., Угнивенко В. И., Надгериев В. М. Комплексное лечение больных с тяжёлыми нарушениями функции нижних конечностей в амбулаторных условиях. Пособие для врачей. — М.: ЦИТО, 1999. — 28 с. Архивировано 12 октября 2007 года.
- ↑ 1 2 НИИ Ревматологии.
- ↑ Косинская Н. С. Дегенеративно-дистрофические поражения костно-суставного аппарата. — Л.: Медгиз. — 1961. — 196 с.
- ↑ В. Х. Василенко. Пропедевтика внутренних болезней / под ред. В. Х. Василенко, А. Л. Гребнева. — М.: Медицина, 1989. — С. 498. — 512 с.
- ↑ Lequesne M. et al. // Scand. J. Rheumatol. — 1987. — Suppl. 65. — P. 85-89.
- ↑ Бурмакова Г. М., Нацвлишвили З. Г. Применение препарата Реписан при лечении больных остеоартрозом коленных суставов // Вестник травматологии и ортопедии им. Н. Н. Приорова. 2005, № 3. С. 52—53
- ↑ Definition of the Kellgren-Lawrence radiographic grades. Дата обращения: 31 марта 2013. Архивировано 7 февраля 2015 года.
- ↑ J. H. Kellgren and J. S. Lawrence. "Radiological Assessment of Osteo-Arthrosis", Ann Rheum Dis. 1957 Dec; 16(4): 494–502.
- ↑ Рейнберг С. А. Рентгенодиагностика заболеваний костей и суставов Архивная копия от 13 июля 2007 на Wayback Machine. Медицина, 1958. Т 1. С. 366
- ↑ AAOS, 2017, p. 7.
- ↑ Katz et al., 2021.
- ↑ AAOS, 2017.
- ↑ AAOS, 2017, p. 582.
- ↑ Епифанов В. А. Лечебная физическая культура и спортивная медицина. Учебник. М.: Медицина, 1999. 304 с.
- ↑ Калягин А. Н., Казанцева Н. Ю. Остеоартроз: современные подходы к терапии (сообщение 2). // Сибирский медицинский журнал. — 2005. — Т. 51. № 2. — С. 93-97.|issn=1815-7572|
- ↑ Wandel S., Jüni P., Tendal B. et al. Effects of glucosamine, chondroitin, or placebo in patients with osteoarthritis of hip or knee: network meta-analysis. Сетевой мета-анализ 10 крупных РКИ, проведённых у 3803 пациентов ОА коленного и тазобедренного суставов, не смог выявить какого-либо клинически значимого эффекта Г, Х или их комбинации в отношении уменьшения суставной боли или замедления сужения суставной щели в сравнении с плацебо. British Medical Journal. BMJ (5 июля 2010). Дата обращения: 28 февраля 2015. Архивировано 23 февраля 2015 года.
- ↑ Алексеева Л. И., Шарапова Л. П. Хондроитин сульфат в лечении остеоартроза. // Ревматология. № 21, 2009. - НИИ Ревматологии РАМН, Москва
- ↑ Bahare Salehi, Antonio Rescigno, Tinuccia Dettori, Daniela Calina, Anca Oana Docea, Laxman Singh, Fatma Cebeci, Beraat Özçelik, Mohammed Bhia, Amirreza Dowlati Beirami, Javad Sharifi-Rad, Farukh Sharopov, William C. Cho, Natália Martins. Avocado-Soybean Unsaponifiables: A Panoply of Potentialities to Be Exploited // Biomolecules. — 2020-01-13. — Т. 10, вып. 1. — С. 130. — ISSN 2218-273X. — doi:10.3390/biom10010130. Архивировано 19 июня 2023 года.
- ↑ Лила А.м, Алексеева Л.и, Таскина Е.а, Кашеварова Н.г. ОСТЕОАРТРИТ КАК МЕЖДИСЦИПЛИНАРНАЯ ПРОБЛЕМА: АЛГОРИТМ ЛЕЧЕНИЯ ДЛЯ ТЕРАПЕВТОВ И ВРАЧЕЙ ОБЩЕЙ ПРАКТИКИ // Современная ревматология. — 2021. — Т. 15, вып. 5. — С. 68–75. — ISSN 1996-7012. Архивировано 19 июня 2023 года.
- ↑ D. M. Merkulova, A. A. Onsin, Yu A. Merkulov. [Piascledin in the treatment of chronic dorsalgia] // Zhurnal Nevrologii I Psikhiatrii Imeni S.S. Korsakova. — 2013. — Т. 113, вып. 9. — С. 18–22. — ISSN 1997-7298. Архивировано 19 июня 2023 года.
- ↑ Yves E. Henrotin, Michelle A. Deberg, Jean-Michel Crielaard, Nathalie Piccardi, Philippe Msika, Christelle Sanchez. Avocado/soybean unsaponifiables prevent the inhibitory effect of osteoarthritic subchondral osteoblasts on aggrecan and type II collagen synthesis by chondrocytes // The Journal of Rheumatology. — 2006-08. — Т. 33, вып. 8. — С. 1668–1678. — ISSN 0315-162X. Архивировано 19 июня 2023 года.
- ↑ Yves Edgard Henrotin. Avocado/Soybean Unsaponifiables (Piacledine®300) show beneficial effect on the metabolism of osteoarthritic cartilage, synovium and subchondral bone: An overview of the mechanisms (англ.) // AIMS Medical Science. — 2018. — Vol. 5, iss. 1. — P. 33–52. — ISSN 2375-1576. — doi:10.3934/medsci.2018.1.33.
- ↑ Piotr Głuszko, Małgorzata Stasiek. Symptom-modifying effects of oral avocado/soybean unsaponifiables in routine treatment of knee osteoarthritis in Poland. An open, prospective observational study of patients adherent to a 6-month treatment // Reumatologia. — 2016. — Т. 54, вып. 5. — С. 217–226. — ISSN 0034-6233. — doi:10.5114/reum.2016.63661. Архивировано 19 июня 2023 года.
- ↑ Zhang W, Moskowitz RW, Nuki G, et al. OARSI recommendations for the management of hip and knee osteoarthritis, Part II: OARSI evidence-based, expert consensus guidelines.// Osteoarthritis Cartilage. 2008 Feb;16(2):137-162.
- ↑ Уровень доказательных данных: Ia — мета-анализ рандомизированных контролируемых испытаний, Ib — рандомизированные контролируемые испытания, IV — мнение экспертов; ES — величина терапевтического эффекта, представляет собой стандартизованную разность средних, то есть средняя разность между основной и контрольной группой, делённая на величину стандартного отклонения разности; ES=0,2 — маленькая величина эффекта, ES=0,5 — умеренная, ES>0,8 — большая. ОА — остеоартрит, КС — коленные суставы, ТС — тазобедренные суставы, НПВС — нестероидные противовоспалительные средства
- ↑ Bagga H., Burkhardt D., Sambrook P., March L. L. Longterm effects of intraarticular hyaluronan on synovial fluid in osteoarthritis of the knee (англ.) // J Rheumatol. — 2006. — № 33(5). — С. 946-950.
- ↑ Бадокин В.В. Локальная терапия остеоартроза (рус.) // Лечащий врач. — 2007. — № 10.
- ↑ Беленький А.Г. Локальная инъекционная терапия при дегенеративных заболеваниях опорно-двигательного аппарата: учебное пособие. — учебное пособие. — 2003. — С. 40.
- ↑ Rutjes A. W., Jüni P., da Costa B. R., Trelle S., Nüesch E., Reichenbach S. Viscosupplementation for osteoarthritis of the knee: a systematic review and meta-analysis. (англ.) // Annals Of Internal Medicine. — 2012. — 7 August (vol. 157, no. 3). — P. 180—191. — doi:10.7326/0003-4819-157-3-201208070-00473. — PMID 22868835.
- ↑ Witteveen AGH, Hofstad CJ, Kerkhoffs GMMJ. Гиалуроновая кислота и другие варианты не-хирургического лечения остеоартрита голеностопного сустава : [арх. 21 апреля 2021] // Cochrane. — 17 октября 2015.
- ↑ Н.В. Загородний, Н.И. Карпович, М.А. Абдулхабиров, В.А. Дирин, О.А. Тихонов, Ф.А. Таруходжаев, В.А. Малков, РУДН, Москва. Применение нового биополимерного материала «Нолтрекс» в комплексном лечении пациентов с гонартрозом (рус.) // Земский Врач : Журнал. — 2012. — № 6(17). — С. 49-52.
- ↑ Голикова Н М, Вялько В. В., Угнивенко В. И. Лазерная и внутрисуставная инъекционная терапия в комплексном лечении больных с деформирующим артрозом. // Профилактическая и лечебная работа поликлиник на новом этапе Перестройки: Тез. докл. V-й Межполиклинической конференции. М.: 1988. С. 60-62.
- ↑ 1 2 Клинические рекомендации. Остеоартрит: Диагностика и ведение больных остеоартритом коленных и тазобедренных суставов./ Под ред. О. М. Лесняк. — М.: ГЭОТАР-Медиа, 2006. — 176 с.
- ↑ Вялько В. В., Берглезов М. А., Угнивенко В. И. Низкоэнергетические лазеры в травматологии и ортопедии Архивная копия от 8 февраля 2009 на Wayback Machine М.: 1998. 83 с.
- ↑ Угнивенко В. И., Паршикова М. В., Жиляев А. А. Восстановление стереотипа ходьбы методом многоканальной электростимуляции мышц у больных с тяжёлыми дистрофическими поражениями нижних конечностей // Тез. докл. VI съезда травматологов и ортопедов России. Нижний Новгород, 1997. С. 880
- ↑ Руцкий В.В., Хомутов В.П., Моргунов М.С. Особенности остеорепарации при накостном остеосинтезе с использованием электретов. Ортопедия, травматология, протезирование // М.Медицина. — 1988. — № 12. — С. 1-5.
- ↑ Александрова С. А., Александрова О. И., Хомутов В. П., Моргунов М. С., Блинова М. И. Влияние электрического поля электрета на основе анодного оксида тантала на дифференцировочные свойства стромальных клеток костного мозга больного остеоартрозом // Цитология. — 2018. — № 60(12). — С. 987-995.
- ↑ Эффективность современных хондопротекторов при остеоартрозе. Дата обращения: 19 июля 2019. Архивировано 19 июля 2019 года.
- ↑ Physical Therapy Interventions for Knee Pain Secondary to Osteoarthritis | Effective Health Care (EHC) Program. effectivehealthcare.ahrq.gov. Дата обращения: 26 декабря 2021. Архивировано 26 декабря 2021 года.
- ↑ * Источники теплового излучения не принимались в расчёт.
- ↑ Analgesics for Osteoarthritis: An Update of the 2006 Comparative Effectiveness Review. Дата обращения: 12 июля 2014. Архивировано из оригинала 12 марта 2013 года.
- ↑ Analgesics for Osteoarthritis. Дата обращения: 12 июля 2014. Архивировано из оригинала 14 июля 2014 года.
- ↑ Анальгетики и противовоспалительные препараты при лечении артроза. Дата обращения: 28 августа 2018. Архивировано 29 августа 2018 года.
- ↑ Остеоартроз суставов – причины, симптомы и лечение остеоартроза, профилактика. www.ayzdorov.ru. Дата обращения: 16 января 2021. Архивировано 4 декабря 2020 года.
- ↑ Lane N. E., Michel B., Bjorkengren A., et al. The risk of osteoarthritis with running and aging: A 5-year longitudinal study. J Rheumatol, март 1993; 20(3):461-8.
- ↑ Sandmeier R.H. Osteoarthritis and Exercise: Does Increased Activity Wear Out Joints? Архивная копия от 8 октября 2007 на Wayback Machine The Permanente Journal / Fall 2000 / Vol. 4, № 4
- ↑ «Также при беременности возникают болевые ощущения при естественном наборе веса. Сильную боль, отекание, опухание, воспаление сустава может вызвать поднятие тяжести. Больным уже с первой стадии не рекомендуется поднимать груз более 2 кг» // Алексеева Л. И. Основные достижения в лечении остеоартроза. Качество жизни. Медицина, № 3, 2003 С. 34-38
- ↑ Остеоартроз угрожает. Статьи на тему здоровья и медицины: «Остеоартроз угрожает». Дата обращения: 14 октября 2007. Архивировано из оригинала 20 мая 2008 года.
- ↑ Гурьев В. Н. Двусторонний коксартроз и его оперативное лечение. Таллин: Валгус, 1975, 275 с.
- ↑ Берглезов М. А., Угнивенко В. И., Надгериев В. М. Диагностика и лечение диспластического коксартроза в амбулаторных условиях Архивная копия от 26 февраля 2008 на Wayback Machine Заболевание и повреждение тазобедренного сустава. Научно-практическая конференция. Рязань, 2000.
Литература[править | править код]
- Игнатьев В. К. Остеоартроз. — Петрозаводск, 2003 (в соавторстве)
- Фёдоров В. Г. Синовиальный сустав и принципы лечения остеоартроза и других дегенеративных заболеваний синовиального сустава Архивная копия от 24 января 2019 на Wayback Machine
- Management of Osteoarthritis of the Hipevidence-based Clinical Practive Guideline : Adopted by the American Academy of Orthopaedic SurgeonsBoard of Directors : [англ.]. — 1st Ed. — 2017. — 13 March. — 850 p.
- Kontzias, A. Остеоартроз (ОА) : (Дегенеративное заболевание суставов; остеоартроз; гипертрофический остеоартрит) : [арх. 31 июля 2020] // MSD. — 2018. — Декабрь.
- Kontzias, A. Остеоартрит (OA) : (Degenerative Arthritis; Degenerative Joint Disease; Osteoarthrosis) : [арх. 22 октября 2020] // MSD. — 2020. — Май.
- Katz, J. N. Diagnosis and Treatment of Hip and Knee Osteoarthritis : A Review : [англ.] / J. N. Katz, K. R. Arant, R. F. Loeser // JAMA. — 2021. — Vol. 325, no. 6. — P. 568–578. — doi:10.1001/jama.2020.22171.. — PMID 33560326.
- Aldrich, E. D., Cui, X., Murphy, C. A., Lim, K. S., Hooper, G. J., McIlwraith, C. W., & Woodfield, T. B. (2021). Allogeneic mesenchymal stromal cells for cartilage regeneration: A review of in vitro evaluation, clinical experience, and translational opportunities. Stem cells translational medicine. PMID 34387402 doi:10.1002/sctm.20-0552
Ссылки[править | править код]
- Угнивенко В. И. Диагностика и лечение диспластического коксартроза в амбулаторных условиях. Дата обращения: 5 октября 2007. Архивировано 10 июня 2012 года.
- Остеоартрит // Официальный сайт ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой».
- Аксёнов В. Хондропротекторы : Ах, обмануть врача нетрудно, он сам обманываться рад! / Валерий Аксёнов (к. м. н., Общество специалистов доказательной медицины).
Для улучшения этой статьи желательно:
|