Регуляторная функция белков
Регуляторная функция белков ― осуществление белками регуляции процессов в клетке или в организме, что связано с их способностью к приёму и передаче информации. Действие регуляторных белков обратимо и, как правило, требует присутствия лиганда. Постоянно открывают всё новые и новые регуляторные белки, в настоящее время известна, вероятно, только малая их часть.
Существует несколько разновидностей белков, выполняющих регуляторную функцию:
- белки-рецепторы, воспринимающие сигнал;
- сигнальные белки-гормоны и другие вещества, осуществляющие межклеточную сигнализацию (многие из них, хотя далеко не все, являются белками или пептидами);
- регуляторные белки, которые регулируют многие процессы внутри клеток.
Белки, участвующие в межклеточной сигнализации[править | править код]
Белки-гормоны (и другие белки, участвующие в межклеточной сигнализации) оказывают влияние на обмен веществ и другие физиологические процессы.
Гормоны — это вещества, которые образуются в железах внутренней секреции, переносятся кровью и несут информационный сигнал. Гормоны распространяются безадресно и действуют только на те клетки, которые имеют подходящие белки-рецепторы. Гормоны связываются со специфическими рецепторами. Обычно гормоны регулируют медленные процессы, например, рост отдельных тканей и развитие организма, однако есть и исключения: например, адреналин — гормон стресса, производное аминокислот. Он выделяется при воздействии нервного импульса на мозговой слой надпочечников. При этом начинает чаще биться сердце, повышается кровяное давление и наступают другие ответные реакции. Также он действует на печень (расщепляет гликоген). Глюкоза выделяется в кровь, и её используют мозг и мышцы как источник энергии.
Белки-рецепторы[править | править код]
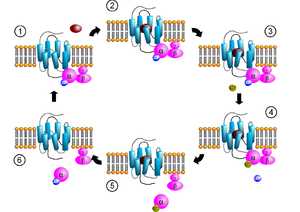
К белкам с регуляторной функцией можно отнести также белки-рецепторы. Мембранные белки-рецепторы передают сигнал с поверхности клетки внутрь, преобразовывая его. Они регулируют функции клеток за счет связывания с лигандом, который «сел» на этот рецептор снаружи клетки; в результате активируется другой белок внутри клетки.
Большинство гормонов действуют на клетку, только если на её мембране есть определенный рецептор — другой белок или гликопротеид. Например, β2- адренорецептор находится на мембране клеток печени. При стрессе молекула адреналина связывается с β2- адренорецептором и активирует его. Далее активированный рецептор активирует G-белок, который присоединяет ГТФ. После многих промежуточных этапов передачи сигнала происходит фосфоролиз гликогена. Рецептор осуществил самую первую операцию по передаче сигнала, ведущего к расщеплению гликогена. Без него не было бы последующих реакций внутри клетки.
Внутриклеточные регуляторные белки[править | править код]
Белки регулируют процессы, происходящие внутри клеток, при помощи нескольких механизмов:
- взаимодействия с молекулами ДНК (транскрипционные факторы);
- при помощи фосфорилирования (протеинкиназы) или дефосфорилирования (протеинфосфатазы) других белков;
- при помощи взаимодействия с рибосомой или молекулами РНК (факторы регуляции трансляции);
- воздействия на процесс удаления интронов (факторы регуляции сплайсинга);
- влияния на скорость распада других белков (убиквитины и др.).
Белки-регуляторы транскрипции[править | править код]
Транскрипционный фактор — это белок, который, попадая в ядро, регулирует транскрипцию ДНК, то есть считывание информации с ДНК на мРНК (синтез мРНК по матрице ДНК). Некоторые транскрипционные факторы изменяют структуру хроматина, делая его более доступным для РНК-полимераз. Существуют различные вспомогательные транскрипционные факторы, которые создают нужную конформацию ДНК для последующего действия других транскрипционных факторов. Еще одна группа транскрипционных факторов — это те факторы, которые не связываются непосредственно с молекулами ДНК, а объединяются в более сложные комплексы с помощью белок-белковых взаимодействий.
Факторы регуляции трансляции[править | править код]
Трансляция — синтез полипептидных цепей белков по матрице мРНК, выполняемый рибосомами. Регуляция трансляции может осуществляться несколькими способами, в том числе и с помощью белков-репрессоров, которые, связываются с мРНК. Известно много случаев, когда репрессором является белок, который кодируется этой мРНК. В этом случае происходит регуляция по типу обратной связи (примером этого может служить репрессия синтеза фермента треонил-тРНК-синтетазы).
Факторы регуляции сплайсинга[править | править код]
Внутри генов эукариот есть участки, не кодирующие аминокислот. Эти участки называются интронами. Они сначала переписываются на пре-мРНК при транскрипции, но затем вырезаются особым ферментом. Этот процесс удаления интронов, а затем последующее сшивание концов оставшихся участков называют сплайсингом (сшивание, сращивание). Сплайсинг осуществляется с помощью небольших РНК, обычно связанных с белками, которые называются факторами регуляции сплайсинга. В сплайсинге принимают участие белки, обладающие ферментативной активностью. Они придают пре-мРНК нужную конформацию. Для сборки комплекса (сплайсосомы) необходимо потребление энергии в виде расщепляемых молекул АТФ, поэтому в составе этого комплекса есть белки, обладающие АТФ-азной активностью.
Существует альтернативный сплайсинг. Особенности сплайсинга определяются белками, способными связываться с молекулой РНК в областях интронов или участках на границе экзон-интрон. Эти белки могут препятствовать удалению одних интронов и в то же время способствовать вырезанию других. Направленная регуляция сплайсинга может иметь значительные биологические последствия. Например, у плодовой мушки дрозофилы альтернативный сплайсинг лежит в основе механизма определения пола.
Протеинкиназы и протеинфосфатазы[править | править код]
Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы — ферменты, которые активируют или подавляют активность других белков путём присоединения к ним фосфатных групп.
Протеинкиназы регулируют активность других белков путём фосфолирования — присоединения остатков фосфорной кислоты к остаткам аминокислот, имеющих гидроксильные группы. При фосфорилировании обычно изменяется функционирование данного белка, например, ферментативная активность, а также положение белка в клетке.
Существуют также протеинфосфатазы — белки, которые отщепляют фосфатные группы. Протеинкиназы и протеинфосфатазы регулируют обмен веществ, а также передачу сигналов внутри клетки. Фосфорилирование и дефосфорилирования белков — один из главных механизмов регуляции большинства внутриклеточных процессов.
См. также[править | править код]
- Избранную статью белки и особенно раздел Функции белков в организме
- Транскрипционные факторы
- Сплайсинг
- Гормоны
- Цитокины
- Рецепторы
- Передача сигнала в клетке
- Передача сигнала (биология)
Ссылки[править | править код]
- [www.xumuk.ru/biochem/120.html] Контроль транскрипции
- [1] Белки против РНК — кто первым придумал сплайсинг?
- [2] Протеинкиназы
- [3] Трансляция и её регуляция
Литература[править | править код]
- Д.Тейлор, Н.Грин, У.Стаут. Биология (в 3-х томах).
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист |