Криптоспоридиоз
| Криптоспоридиоз | |
|---|---|
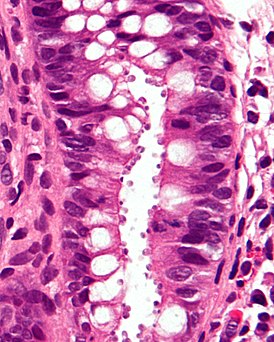 Микрофотография гистологического среза кишечника, демонстрирующая заражённые клетки | |
| МКБ-11 | 1A32 |
| МКБ-10 | A07.2 |
| МКБ-10-КМ | A07.2 |
| МКБ-9 | 007.4 |
| МКБ-9-КМ | 007.4[1][2] |
| DiseasesDB | 3221 |
| MedlinePlus | 000617 |
| eMedicine | med/484 |
| MeSH | D003457 |
Криптоспоридио́з — паразитарное заболевание, вызываемое протистами рода Cryptosporidium из типа Апикомлекс. Криптоспоридиоз, как правило, проявляется как острая и кратковременная инфекция и распространяется алиментарным путём, часто через заражённую воду. Основным симптомом у людей с неповреждённой иммунной системой является диарея, больные, страдающие иммунодефицитом, испытывают гораздо более серьёзные симптомы, часто со смертельным исходом[3].
Признаки и симптомы
Симптомы появляются через 2—10 дней после заражения, в среднем на 7-й день. Иногда появление симптомов задерживается на срок до двух недель, а в некоторых случаях до одного месяца[3]. Существует 3 возможные формы болезни у иммунокомпетентных людей. Заболевание может вызвать острую или хроническую диарею, которая может длиться в течение нескольких недель. Очень редко в стуле пациента можно найти кровь или лейкоциты[4].
Помимо диареи, пациенты могут страдать от боли в области желудка, судорог и слабой лихорадки. Другие симптомы включают тошноту, рвоту[5], расстройство всасывания[6] и обезвоживание[7]. Возможно бессимптомное течение заболевания, тем не менее, такие носители инфекции могут заражать других людей. После того, как у больного человека исчезают симптомы криптоспоридиоза, он способен передать другим инфекцию ещё в течение нескольких недель. Криптоспоридиоз может вызывать появление различных других тяжёлых заболеваний, таких как панкреатит[8].
Люди с ослабленным иммунитетом, а также очень молодые или очень старые люди могут страдать более тяжёлой формой криптоспоридиоза[9]. Существует 4 варианта клинического проявления криптоспоридиоза для больных СПИДом: 4 % не имеют никаких симптомов, 29 % имеют временную инфекцию, 60 % имеют хроническую диарею, а 8 % имеют тяжёлые, напоминающие холеру инфекции. У больных с временной инфекцией диарея заканчивается в течение 2 месяцев и криптоспоридии больше не обнаруживаются в кале. Хронической является диарея, которая длится в течение 2 и более месяцев. В наиболее тяжёлых случаях, пациенты выделяют не менее 2 литров водянистой диареи в день, вплоть до потери 25 литров жидкости в день[4][10]. Больные криптоспоридиозом на фоне СПИДа испытывают серьёзные нарушения всасывания и могут терять до 10 % веса. Однажды заболев, многие из них до конца жизни не могут полностью избавиться от криптоспоридий[11].
В случае, когда паразиты распространяются за пределы кишечника, как это часто происходит у больных СПИДом, они могут достигать лёгких, среднего уха, поджелудочной железы, и желудка. Паразит может поражать желчевыводящие пути, что может привести к холециститу и холангиту[10].
Этиология

Возбудителями инфекции являются протисты рода Cryptosporidium из типа Apicomplexa. Заражение начинается с попаданием вместе с водой или пищей в пищеварительный тракт хозяина покоящейся стадии паразита — ооцисты. 4 спорозоита, содержащиеся в ооцисте, покидают её оболочку и движутся по направлению к эпителиальным клеткам кишечника. Достигнув энтероцита, паразит образует сложно организованную зону взаимодействия с клеткой хозяина, после чего вокруг криптоспоридии формируется экстрацитоплазматическая паразитофорная вакуоль, под защитой которой протекают все дальнейшие стадии развития патогена. Такой вариант расположения паразита, находящийся на границе между внутриклеточным существованием (которое мы наблюдаем у кокцидий) и внеклеточным (характерным для грегарин) уникален для рода Cryptosporidium[12].
Некоторое время паразит активно питается и растёт, после чего переходит к мерогонии — размножению путём множественного деления. Образующиеся мерозоиты выходят в просвет кишечника и заражают другие клетки хозяина. В какой-то момент Cryptosporidium переходит к половому размножению, из мерозоитов развиваются особи полового поколения: микрогамонты и макрогомонты. Из микрогамонта развиваются до 16 бесжгутиковых гамет, которые выходят в просвет кишечника, находят макрогомонт и оплодотворяют его, в результате чего образуется зигота. Зигота претерпевает редукционное деление, инцистируется и превращается в ооцисту, содержащую 4 спорозоита. Считается, что если из зиготы образуется тонкостенная ооциста, то спорозоиты из неё могут выходить в кишечнике того же хозяина, осуществляя таким образом аутоинвазию. Ооцисты с толстой стенкой выводятся при акте дефекации во внешнюю среду для заражения других хозяев[3].
Трансмиссия
Инфекция передается через загрязненные субстанции, такие как земля, вода, неприготовленные или кросс-инвазированные продукты питания, которые были в контакте с фекалиями зараженного человека или животного. Криптоспоридиоз часто встречается у лиц, находящихся в постоянном контакте с пресными водоёмами, в том числе рекреационными водами, такими как бассейны. Другие потенциальные источники включают недостаточно очищенную водопроводную воду или зараженную пищу[3]. Высокая стойкость ооцист Cryptosporidium к дезинфицирующим средствам, таким как хлорный отбеливатель, позволяет им выжить и остаться способными вызвать инфекцию в течение длительного времени[13].
Диагностика
Существуют различные диагностические тесты для выявления криптоспоридиоза. Они включают в себя микроскопирование, окрашивание и обнаружение антител. Микроскопия используется для обнаружения ооцист в фекалиях пациента[9]. Для концентрации и выявления спороцист в пробе кала используются модифицированный метод центробежной плавучести сульфата цинка и метод плавучести сахара Шелтера[14]. Методы окраски включают кислотно-быстрое окрашивание, придающее ооцистам красный цвет. Также может быть использовано окрашивание красителем Гимза. Часть тонкой кишки может быть окрашена гематоксилином и эозином, что выявляет ооцисты, прикреплённые к эпителиальным клеткам[6]. Кроме того, применяется люминесцентная микроскопия проб, окрашенных аурамином[9].
Еще один способ диагностировать болезнь — детекция антигенов. Это может быть сделано с помощью техники прямого флуоресцентного антитела (DFA), а также за счет непрямой иммунофлюоресценции или иммуноферментного анализа (ELISA)[14]. Полимеразная цепная реакция (ПЦР) является еще одним способом диагностики криптоспоридиоза. Этот метод может даже определить конкретные виды Cryptosporidium[3]. Если у пациента предполагают криптоспоридиоз жёлчных протоков, то соответствующий диагностическим методом является УЗИ. В случае, если УЗИ не дает однозначных результатов, выполняется эндоскопическая ретроградная холангиопанкреатография[4].
Профилактика
Многие очистные сооружения, которые берут сырую воду из рек, озёр и водохранилищ для хозяйственно-питьевого водоснабжения, используют обычные технологии фильтрации. Они включают в себя ряд процессов, в том числе коагуляцию, флокуляцию, осаждение и фильтрацию. Прямая фильтрация, которая обычно используется для очистки воды с низким уровнем твёрдых частиц, включает в себя коагуляцию и фильтрацию, но не осаждение. Другие общие процессы фильтрации, в том числе использующие медленные песчаные фильтры, диатомовые и мембранные фильтры, задерживают 99 % криптоспоридий[15].
Несмотря на то что Cryptosporidium обладает высокой устойчивостью к дезинфекции хлором в достаточно высокой концентрации, паразит эффективно инактивируется диоксидом хлора и озонированием[16]. Также патогена убивает облучение ультрафиолетом в относительно низких дозах[17].
Соблюдение правил гигиены и санитарии, таких как тщательное мытьё рук, позволяет с большой долей вероятности предотвратить приобретение и распространение криптоспоридиоза[14]. Следует избегать контакта с фекалиями животных, а также воздержаться от употребления возможно загрязнённой пищи и воды. Обычной фильтрации воды может быть недостаточно, чтобы устранить Cryptosporidium, наиболее надежным способом обеззараживания питьевой воды, которая может быть загрязнена криптоспоридиями, является кипячение[18]. Стандартная процедура пастеризации молока обычно способствует потере ооцистами паразита инвазионности. Бутилированная питьевая вода обычно не содержит криптоспоридий, особенно если вода взята из подземного источника[19].
Лечение
Надёжного способа лечения криптоспоридиоза пока не существует, обычно используются агенты, такие как паромомицин, нитазоксанид и атоваквон[20]. Лечение обычно в первую очередь направлено на поддержку физического состояния больного. Пациенту дают большое количество жидкости для возмещения потерь воды. Иногда в качестве толерантного лечения используют лактозную диету[21]. В редких случаях могут потребоваться растворы для внутривенных вливаний. Антибиотики используются редко, в первую очередь для людей с тяжёлой формой заболевания и слабой иммунной системой.
Люди со здоровой иммунной системой
Большинство иммунокомпетентных лиц страдают коротким (менее 2 недель) самоограниченным курсом заболевания, который требует поддерживающей терапии и регидратации, иногда противодиарейных лекарств, и заканчивается спонтанным выздоровлением. В США для иммунокомпетентных людей используется препарат нитазоксанид[3]. Так же иногда используется спирамицин, который помогает сократить длительность диареи у детей[4].
Люди, страдающие иммунодефицитом
Для лечения диареи у пациентов на ранних стадиях СПИДа часто используется спирамицин. В целом, уровень смертности инфицированных больных СПИДом основан на CD4+ маркерах. У пациентов с числом CD4+ лимфоцитов более 180 клеток/мм³ есть шанс выздороветь за счет восстановительной с поддерживающей терапии и лекарств, но у больных с числом CD4+ ниже 50 клеток/мм³, инфекция, как правило, заканчивается смертельным исходом в течение трёх-шести месяцев. В 1993 году во время эпидемии криптоспоридиоза Милуоки (крупнейшей в своем роде), 73 % больных СПИДом с числом CD4+ ниже 50 клеток/мм³ и 36 % из обладающих от 50 до 200 клеток/мм³ умерли в течение первого года заражения инфекцией[22]. У одного пациента со СПИДом из Ирана, который имел лёгочный криптоспоридиоз в дополнение к кишечному, азитромицин и паромомицин помогли победить инфекцию[23].
Эпидемиология
Криптоспоридиоз распространён по всему миру и составляет 50,8 % от всех передающихся через воду паразитарных заболеваний[24]. В развивающихся странах 8—19 % от желудочно-кишечных заболеваний может быть связано с Cryptosporidium[25]. Десять процентов населения в развивающихся странах выделяет ооцисты. В развитых странах это число ниже на 1—3 %. Возрастной группой, наиболее подверженной криптоспоридиозу являются дети от 1 до 9 лет[4].
По состоянию на 2010 год криптоспоридиоз стал причиной около 100 000 смертей по сравнению с 220 000 в 1990 году[26].
Статистика заболеваний криптоспоридиозом для США за 2006—2008 годы[24]:
| Год | Случаи |
|---|---|
| 2006 | 5936 |
| 2007 | 11 170 |
| 2008 | 7749 |
Примечания
- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29 — 2018-06-29 — 2018.
- ↑ 1 2 3 4 5 6 Cryptosporidiosis. Centers for Disease Control and Prevention.
- ↑ 1 2 3 4 5 Chen X.M., Keithly J.S., Paya C.V., LaRusso N.F. Cryptosporidiosis (англ.) // The New England Journal of Medicine. — 2002. — May (vol. 346, no. 22). — P. 1723—1731. — doi:10.1056/NEJMra013170. — PMID 12037153.
- ↑ Harvey, Richard A.; Champe, Pamela C.; Fisher, Bruce D. Lippincott’s Illustrated Reviews: Microbiology (англ.). — 2nd. — Philadelphia: Lippincott Williams & Wilkins, 2007. — P. 367, 388.
- ↑ 1 2 Winn Jr., Washington; Allen, Stephen; Janda, William; Koneman, Elmer; Procop, Gary; Schreckenberger, Paul; Woods, Gail. Koneman’s Color Atlas and Textbook of Diagnostic Microbiology (англ.). — 6th. — Philadelphia: Lippincott Williams & Wilkins, 2006. — P. 1267—1270.
- ↑ Cryptosporidiosis. Medline Plus (16 января 2009). — «A service of the U.S. National Library of Medicine (NLM) and the National Institutes of Health (NIH)».
- ↑ Hawkins S., Thomas R., Teasdale C. Acute pancreatitis: a new finding in cryptosporidium enteritis (англ.) // The BMJ : journal. — 1987. — Vol. 294, no. 6570. — P. 483—484. — doi:10.1136/bmj.294.6570.483-a. — PMID 3103738. — PMC 1245527.
- ↑ 1 2 3 Brooks, Geo. F.; Butel, Janet S.; Morse, Stephen A. Jawetz, Melnick, & Adelberg’s Medical Microbiology (неопр.). — 23rd. — New York: Lange Medical Books/McGraw Hill, 2004. — С. 684—685.
- ↑ 1 2 Ryan, Kenneth J.; Ray, C. George. Sherris Medical Microbiology: An Introduction to Infectious Disease (англ.). — 4th. — New York: McGraw-Hill Education, 2004. — P. 727—730.
- ↑ Chen Q., Schlichtherle M., Wahlgren M. Molecular Aspects of Severe Malaria (англ.) // Clinical Microbiology Reviews. — 2000. — July (vol. 13, no. 3). — P. 439—450. — doi:10.1128/CMR.13.3.439-450.2000. — PMID 10885986. — PMC 88942.
- ↑ М.В. Крылов, А.О. Фролов. Тип Sporozoa — Споровики // Протисты = Protista : руководство по зоологии / гл. ред. А. Ф. Алимов. — СПб.: Рос. акад. наук, Зоол. ин-т, 2007. — Т. 2. — С. 5—370..
- ↑ Carpenter C., Fayer R., Trout J., Beach M. Chlorine disinfection of recreational water for Cryptosporidium parvum (англ.) // Emerging Infectious Diseases : journal. — Centers for Disease Control and Prevention, 1999. — Vol. 5, no. 4. — P. 579—584. — doi:10.3201/eid0504.990425. — PMID 10458969. — PMC 2627758.
- ↑ 1 2 3 Murray, Patrick R., Ken S. Rosenthal, and Michael A. Pfaller. Medical Microbiology. 5th ed. Philadelphia: Elsevier Inc., 2005: 855—856.
- ↑ The Interim Enhanced Surface Water Treatment Rule – What Does it Mean to You? (pdf). USEPA. Дата обращения: 6 мая 2007.
- ↑ Korich D.G., Mead J.R., Madore M.S., Sinclair N.A., Sterling C.R. Effects of ozone, chlorine dioxide, chlorine, and monochloramine on Cryptosporidium parvum oocyst viability (англ.) // Applied and Environmental Microbiology : journal. — 1990. — May (vol. 56, no. 5). — P. 1423—1428. — PMID 2339894. — PMC 184422.
- ↑ Rochelle, PAUL A.; Fallar, D; Marshall, MM; Montelone, BA; Upton, SJ; Woods, K. Irreversible UV inactivation of Cryptosporidium spp. despite the presence of UV repair genes (англ.) // J Eukaryot Microbiol : journal. — Vol. 51, no. 5. — P. 553—562. — doi:10.1111/j.1550-7408.2004.tb00291.x. — PMID 15537090.
- ↑ "Boil water warning 'precaution'". BBC. 2008-09-02. Дата обращения: 7 сентября 2009.
- ↑ John, David T. and William A. Petri, Jr. Markell and Voge’s Medical Parasitology. 9th ed. Philadelphia: Elsevier Inc., 2006: 68-71.
- ↑ Smith H.V., Corcoran G.D. New drugs and treatment for cryptosporidiosis (неопр.) // Curr. Opin. Infect. Dis.. — 2004. — December (т. 17, № 6). — С. 557—564. — doi:10.1097/00001432-200412000-00008. — PMID 15640710. Архивировано 25 мая 2012 года.
- ↑ Cryptosporidiosis Treatment - MedScape. Дата обращения: 29 октября 2013.
- ↑ Gilson M.D., Ian; Buggy, Brian P. M.D. Cryptosporidiosis in Patients with HIV Disease: Is It Safe to Drink the Water? (англ.) // HIV Newsline : journal. — San Francisco General Hospital, 1996. — October.
- ↑ Meamar A.R., Rezaian M., Rezaie S., et al. Cryptosporidium parvum bovine genotype oocysts in the respiratory samples of an AIDS patient: efficacy of treatment with a combination of azithromycin and paromomycin (англ.) // Parasitol. Res. : journal. — 2006. — May (vol. 98, no. 6). — P. 593—595. — doi:10.1007/s00436-005-0097-4. — PMID 16416289.
- ↑ 1 2 Cryptosporidiosis. Gideon (23 февраля 2009). — «Trial subscription required to access».
- ↑ Gatei W., Wamae C.N., Mbae C., et al. Cryptosporidiosis: prevalence, genotype analysis, and symptoms associated with infections in children in Kenya (англ.) // Am. J. Trop. Med. Hyg. : journal. — 2006. — July (vol. 75, no. 1). — P. 78—82. — PMID 16837712.
- ↑ Lozano, R. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010 (англ.) // The Lancet : journal. — Elsevier, 2012. — 15 December (vol. 380, no. 9859). — P. 2095—2128. — doi:10.1016/S0140-6736(12)61728-0. — PMID 23245604.
Эта статья входит в число добротных статей русскоязычного раздела Википедии. |