Ривароксабан
| Ривароксабан | |
|---|---|
| Rivaroxabanum | |
 | |
| Химическое соединение | |
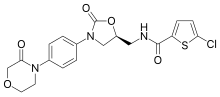
| ИЮПАК | (S)-5-хлоро-N-{[2-оксо-3-[4-(3-оксоморфолин-4-yl)фенил]оксазолидин-5-yl]метил} тиофен-2-карбоксамид |
| Брутто-формула | C19H18N3O5SCl |
| Молярная масса | 435.882 г/моль |
| CAS | 366789-02-8 |
| PubChem | 6433119 |
| DrugBank | DB06228 |
| Состав | |
| Классификация | |
| Фармакол. группа | Антикоагулянты[1] |
| АТХ | B01AF01 |
| МКБ-10 | I48, I80 |
| Фармакокинетика | |
| Биодоступн. | от 80% до 100% |
| Метаболизм | CYP3A4, CYP2J2 и CYP-независимые механизмы[2][3] |
| Период полувывед. |
от 5 до 9 часов у молодых пациентов; от 11 до 13 часов у пожилых пациентов[2][3] |
| Экскреция |
2/3 метаболизируется и выводится почками; 1/3 выводится кишечником в неизменном виде[2][3] |
| Лекарственные формы | |
| таблетки 2,5, 10, 15 и 20 мг | |
| Способы введения | |
| перорально | |
| Другие названия | |
| Ксарелто® | |
Рива́роксабан (кодовое название BAY 59-7939) — пероральный антикоагулянт из группы прямых ингибиторов фактора Xa. Разработан и выпускается немецкой фармацевтической компанией Bayer под торговым названием «Ксарелто».
Фармакодинамика
Фактор свёртывания крови X (фактор Стюарта—Прауэра) играет центральную роль в каскаде коагуляции, так как активируется и внешней и внутренней теназой. Переходя в активную форму фактор X вместе с неферментным кофактором Va и Ca2+ образует на поверхности тромбоцитов или эндотелия протромбиназный комплекс, который в свою очередь катализирует процесс превращения протромбина в тромбин. Тромбин активирует полимеризацию растворимого фибриногена, приводя к формированию фибринового сгустка (тромба).
Механизм действия ривароксабан заключается в высокоселективном прямом ингибировании фактора свёртывания крови Ха, что позволяет одновременно заблокировать как внешний так и внутренний пути коагуляции и приостановить процесс тромбообразования.
Медицинское применение
У пациентов с неклапанной фибрилляцией предсердий препарат столь же эффективен, как варфарин в предотвращении негеморрагических инсультов и тромбоэмболии.[4] Применение Ривароксабана связано со сниженным риском сильных и смертельных кровотечений, чем варфарин. Хотя ривароксабан и связан с более высокой частотой кровотечений в желудочно-кишечном тракте.[5]
В июле 2012 года британский Национальный институт здравоохранения и медицины рекомендовал ривароксабан для профилактики и лечения венозной тромбоэмболии.[6]
Побочные эффекты
Наиболее серьёзный побочный эффект это кровотечения, включая тяжёлые внутренние кровотечения.[7][8][9] Применение Ривароксабана связано со сниженным риском сильных и смертельных кровотечений, чем варфарин, но связан с более высокой частотой кровотечений в ЖКТ. В настоящее время не существует антидота для ривароксабана (в отличие от варфарина, действие которого может быть инвертировано с помощью витамина К и протромбинового комплексного концентрата), это означает, что серьёзным кровотечением может быть трудно управлять.
В октябре 2014 года, компания Портола Фармасьютикалз завершила фазы I и II клинических испытаний для andexanet Альфа в качестве антидота для ингибиторов фактора Ха с несколько побочных эффектов, и начала исследования III фазы.[10][11] Andexanet Альфа, как ожидается, будет утверждён в 2016 году.[12] В 2017 году соединение ещё не было одобрено FDA.
В 2015 году пост-маркетинговые исследования выявили токсичность для печени, и показали необходимость дальнейших исследований для количественной оценки риска.[13][14] Препарат противопоказан людям с серьёзными заболеваниями печени и терминальной стадии почечной болезни, при которых исследований не проводилось.
Ривароксабан в индивидуальной упаковке имеет предупреждение, о том, что людям использующим препарат не следует прекращать его применения до консультации с врачом, так как это может увеличить риск инсульта.[15]
В 2015 году на ривароксабан приходится наибольшее количество зарегистрированных случаев серьёзных осложнений среди регулярно контролируемых FDA лекарств.[16]
Механизм действия
Ривароксабан подавляет свободный фактор Ха и фактор Ха связанный в комплекс протромбиназы.[17] Это высокоселективный прямой ингибитор фактора Ха с пероральной биодоступностью и быстрым началом действия. Ингибирование фактора Ха прерывает внутренние и внешние пути свёртывания крови, препятствует образованию тромбина и развитию тромбов. Ривароксабан не подавляет тромбин (активированный фактор II) и не оказывает никакого влияния на тромбоциты.[18] Это позволяет легко корректировать дозы в антикоагулянтной терапии и отслеживать коагуляцию[18] , а также избегать ограничений в питании.[12]
Нефракционированный гепарин, низкомолекулярный гепарин и фондапаринукс также ингибируют активность фактора Ха, но косвенно, путём связывания циркулирующего антитромбина (АТ III). Принимая во внимание, что орально активный варфарин, аценокумарол являются антагонистами витамина К уменьшая количество факторов свёртывания крови, включая фактор X.[19] Ривароксабан имеет предсказуемую фармакокинетику у широкого спектра пациентов (возраст, пол, вес, раса) и имеет линейную кривую доза-эффект в восьмикратном диапазоне доз (5-40 мг).[20]
Химия
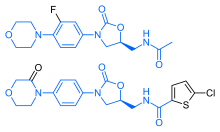
Ривароксабан имеет поразительное структурное сходство с антибиотиками группы линезолида: оба препарата имеют те же оксазолидинон-производные основные структуры. Соответственно, ривароксабан изучался на возможную противомикробную активность и митохондриальную токсичность, которая является известным осложнением долгосрочного применения линезолида. Исследования показали, что ни ривароксабан, ни его метаболиты не обладают антибактериальным действием против грам-положительных бактерий. Что касается митохондриальной токсичности, то в исследованиях In vitro, опубликованных до 2008 года выявленный риск был низким.[21]
Антидот
Специфическим антидотом ривороксабана является препарат Андекса (рекомбинантный инактивированный фактор Xa).
Общество и культура
Экономика
Использование ривароксабана в 70 раз чаще варфарина, по данным Express Scripts Holding Co, крупнейшей в США компанией по работе с аптеками.[12] В 2016 году, Байер утверждал, что препарат был лицензирован в 130 странах и более 23 миллионов пациентов прошли лечение.[22]
Одобрение
В сентябре 2008 года, Министерство здравоохранения Канады выдало регистрационное удостоверение на ривароксабан для профилактики венозной тромбоэмболии у людей, которые прошли замену тазобедренного сустава или полное эндопротезирование коленного сустава.[23] В том же месяце Европейская комиссия также выдано регистрационное удостоверение ривароксабана для профилактики венозной тромбоэмболии у взрослых пациентов, перенёсших плановые бедра и коленного сустава.[24]
На 1 июля 2011 года, в США продуктов питания и медикаментов (FDA) одобрила ривароксабан для профилактики тромбоза глубоких вен (ТГВ), который может привести к тромбоэмболии лёгочной артерии (ТЭЛА), у взрослых, перенёсших эндопротезирование тазобедренного и коленного сустава.[25]
4 ноября 2011 года FDA США одобрило ривароксабан для профилактики инсульта у пациентов с неклапанной фибрилляцией предсердий.[26]
Исследования
Исследователи из Школы медицины Университета Дьюка были обвинены в сокрытии клинических данных, используемых для оценки ривароксабана.[27] Они проводили клинические испытания ривароксабана ROCKET AF.[28] В клиническом исследовании, опубликованном в 2011 году в медицинском журнале в Новой Англии[29] которое возглавил Роберт Калиффи, (представитель FDA[30])[29] нашли что ривароксабан, более эффективен, чем варфарин в снижении вероятности ишемических инсультов у пациентов с фибрилляцией предсердий.[29] Валидность исследования была поставлена под вопрос в 2014 году, когда фармацевтическими компаниями Байер и Джонсон и Джонсон установлено, что использованные приборы мониторинга крови INRatio не функционируют должным образом[27][28]. Последующий анализ исследований Школы медицины Университета Дьюка, опубликованные в феврале 2016 года обнаружил, что это не оказало существенного влияния на эффективность и безопасность испытаний.[31]
Примечания
- ↑ Ривароксабан (Rivaroxaban): инструкция, применение и формула. Энциклопедия лекарств и товаров аптечного ассортимента rlsnet.ru. Дата обращения: 31 марта 2015.
- ↑ 1 2 3 Xarelto: Summary of Product Characteristics – EU (англ.). Официальный сайт Xarelto®. Дата обращения: 31 марта 2015.
- ↑ 1 2 3 Ксарелто: Инструкция по применению, противопоказания, состав и цена, 3D-упаковка. Энциклопедия лекарств и товаров аптечного ассортимента rlsnet.ru. Дата обращения: 31 марта 2015.
- ↑ Gómez-Outes, A; Terleira-Fernández, AI; Calvo-Rojas, G; Suárez-Gea, ML; Vargas-Castrillón, E. Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups. (англ.) // Thrombosis : journal. — 2013. — Vol. 2013. — P. 640723. — doi:10.1155/2013/640723. — PMID 24455237. — PMC 3885278.
- ↑ Brown D.G., Wilkerson E.C., Love W.E. A review of traditional and novel oral anticoagulant and antiplatelet therapy for dermatologists and dermatologic surgeons (англ.) // Journal of the American Academy of Dermatology : journal. — 2015. — March (vol. 72, no. 3). — P. 524—534. — doi:10.1016/j.jaad.2014.10.027. — PMID 25486915.
- ↑ NICE guidance TA261 NICE guidance TA261. National Institute for Health and Clinical Excellence, July 2012
- ↑ Medication Guide--Xarelto. U.S. Food and Drug Administration. Дата обращения: 1 сентября 2014.
- ↑ Xarelto Side Effects. WebMD. Дата обращения: 1 сентября 2014.
- ↑ Xarelto Side Effects Center. RxList. Дата обращения: 1 сентября 2014.
- ↑ Schroeder, C. Possible Antidote Could Help Blood Thinner Patients In Bleeding Emergencies. DrugNews. Дата обращения: 20 августа 2015.
- ↑ Mo Y., Yam F.K. Recent advances in the development of specific antidotes for target-specific oral anticoagulants (англ.) // Pharmacotherapy : journal. — 2015. — February (vol. 35, no. 2). — P. 198—207. — doi:10.1002/phar.1532. — PMID 25644580.
- ↑ 1 2 3 Bill Berkrot New blood thinner 'antidote' to help doctors move past warfarin. Reuters (23 декабря 2015).
- ↑ Raschi, Emanuel; Poluzzi, Elisabetta; Koci, Ariola; Salvo, Francesco; Pariente, Antoine; Biselli, Maurizio; Moretti, Ugo; Moore, Nicholas; De Ponti, Fabrizio. Liver injury with novel oral anticoagulants: assessing post-marketing reports in the US Food and Drug Administration adverse event reporting system (англ.) // British Journal of Clinical Pharmacology : journal. — 2015. — 1 August (vol. 80, no. 2). — P. 285—293. — ISSN 1365-2125. — doi:10.1111/bcp.12611. — PMID 25689417. — PMC 4541976.
- ↑ Russmann, Stefan; Niedrig, David F.; Budmiger, Mathias; Schmidt, Caroline; Stieger, Bruno; Hürlimann, Sandra; Kullak-Ublick, Gerd A. Rivaroxaban postmarketing risk of liver injury (неопр.) // Journal of Hepatology. — 2014. — 1 August (т. 61, № 2). — С. 293—300. — ISSN 1600-0641. — doi:10.1016/j.jhep.2014.03.026. — PMID 24681117.
- ↑ XARELTO (rivaroxaban) label. U.S. Food and Drug Association.
- ↑ Schroeder, C ISMP Ranks Xarelto Most Dangerous Drug in the United States. DrugNews. DrugNews. Дата обращения: 10 августа 2016.
- ↑ Roehrig S., Straub A., Pohlmann J., etal. Discovery of the novel antithrombotic agent 5-chloro-N-({(5S)-2-oxo-3- [4-(3-oxomorpholin-4-yl)phenyl]-1,3-oxazolidin-5-yl}methyl)thiophene- 2-carboxamide (BAY 59-7939): an oral, direct factor Xa inhibitor (англ.) // Journal of Medicinal Chemistry : journal. — 2005. — September (vol. 48, no. 19). — P. 5900—5908. — doi:10.1021/jm050101d. — PMID 16161994.
- ↑ 1 2 Ошибка в сносках?: Неверный тег
<ref>; для сносокXarelto SPCне указан текст - ↑ Turpie A.G. New oral anticoagulants in atrial fibrillation (англ.) // European Heart Journal : journal. — 2008. — January (vol. 29, no. 2). — P. 155—165. — doi:10.1093/eurheartj/ehm575. — PMID 18096568.
- ↑ Eriksson B.I., Borris L.C., Dahl O.E., etal. A once-daily, oral, direct Factor Xa inhibitor, rivaroxaban (BAY 59-7939), for thromboprophylaxis after total hip replacement (англ.) // Circulation : journal. — Lippincott Williams & Wilkins, 2006. — November (vol. 114, no. 22). — P. 2374—2381. — doi:10.1161/CIRCULATIONAHA.106.642074. — PMID 17116766.
- ↑ European Medicines Agency. CHP Assessment Report for Xarelto (EMEA/543519/2008) (2008). Дата обращения: 11 июня 2009. (недоступная ссылка)
- ↑ Bayer comments on article in The British Medical Journal (BMJ) regarding Xarelto. Bayer AG Communications, Government Relations & Corporate Brand (29 сентября 2016).
- ↑ "Bayer's Xarelto Approved in Canada" (Press release). Bayer. 2008-09-16. Дата обращения: 31 января 2010.
- ↑ "Bayer's Novel Anticoagulant Xarelto now also approved in the EU" (Press release). Bayer. 2008-02-10. Дата обращения: 31 января 2010.
- ↑ "FDA Approves XARELTO® (rivaroxaban tablets) to Help Prevent Deep Vein Thrombosis in Patients Undergoing Knee or Hip Replacement Surgery" (Press release). Janssen Pharmaceutica. 2011-07-01. Дата обращения: 1 июля 2011.
{{cite press release}}:|archive-url=требует|archive-date=(справка) - ↑ "FDA approves Xarelto to prevent stroke in people with common type of abnormal heart rhythm". U.S. Food and Drug Association. 2011-11-04. Дата обращения: 27 апреля 2016.
- ↑ 1 2 Thomas, Katie Document Claims Drug Makers Deceived a Top Medical Journal. The New York Times. The New York Times. Дата обращения: 3 мая 2016.
- ↑ 1 2 Patel, Vir Duke clinical trial under scrutiny in drug case. The Chronicle. Duke Student Publishing Company.
- ↑ 1 2 3 Rivaroxaban versus Warfarin in Nonvalvular Atrial Fibrillation. The New England Journal of Medicine. Massachusetts Medical Society.
- ↑ Meet Robert M. Califf, M.D., Commissioner of Food and Drugs. U.S. Food and Drug Administration. U.S. Food and Drug Administration. Дата обращения: 3 мая 2016.
- ↑ Point-of-Care Warfarin Monitoring in the ROCKET AF Trial. Massachusetts Medical Society (3 февраля 2016).