Вирус бешенства
| Вирус бешенства | ||||||
|---|---|---|---|---|---|---|
 | ||||||
| Научная классификация | ||||||
|
Реалм: Царство: Тип: Подтип: Класс: Порядок: Семейство: Род: Вид: Вирус бешенства |
||||||
| Международное научное название | ||||||
| Rabies lyssavirus | ||||||
| Синонимы | ||||||
|
||||||
| Группа по Балтимору | ||||||
| V: (-)оцРНК-вирусы | ||||||
| ||||||
Ви́рус бе́шенства[3], рабивирус (англ. Rabies lyssavirus, ранее Rabies virus) — нейротропный вирус, возбудитель бешенства у человека и животных. Передача вируса может происходить через слюну животных и (реже) при контакте с человеческой слюной.
Вирус бешенства не устойчив в окружающей среде, быстро инактивируется под воздействием солнечных лучей, практически моментально погибает при температуре более 70° С, при 50° С — через 1 час[4]. Вирион разрушается под воздействием средств дезинфекции с содержанием хлора, жирорастворяющих и щелочных веществ. Высушивание способствует гибели вируса в течение двух недель[5].
Вирус бешенства имеет цилиндрический вид и является типовым видом рода Lyssavirus семейства рабдовирусов (Rhabdoviridae). Эти вирусы покрыты оболочкой и имеют одноцепочечную РНК генома. Генетическая информация поставляется в виде рибонуклеопротеинового комплекса, в котором РНК тесно связана с нуклеопротеином. РНК-геном вируса кодирует пять генов, порядок которых высоко консервативен. Эти гены кодируют нуклеопротеиды (N), фосфопротеин (Р), матрицу белка (М), гликопротеин (G) и вирусные РНК-полимеразы (L)[6]. Полные последовательности генома в пределах от 11615 до 11966 нуклеотидов в длину[7].
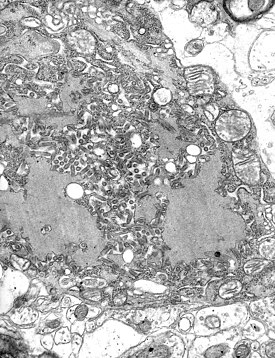
Все события транскрипции и репликации происходят в цитоплазме внутри телец Бабеша — Негри (названных в честь Виктора Бабеша и Адельки Негри[8]). Диаметр их составляет 2—10 мкм; они являются типичными при бешенстве и, таким образом, могут быть использованы в качестве патогномоничного симптома наличия инфекции[9].
Структура
[править | править код]Вирусы рода Lyssavirus имеют спиральную симметрию, так что их инфекционные частицы имеют практически цилиндрическую форму. Они характеризуются поражением нервных клеток млекопитающих.
Вирус бешенства имеет форму пули с длиной около 180 нм и поперечный разрез диаметром около 75 нм. Один конец закруглён или имеет коническую форму, а другой конец имеет плоскую или вогнутую форму. Содержит в себе липопротеины, состоящие из гликопротеина G. Шипы не покрывают плоский конец вириона (вирусной частицы). Под оболочкой имеется мембрана или матрица (М) слоя белка, который имеет возможность инвагинации на плоском конце. Ядро вириона состоит из спирально расположенных рибонуклеопротеидов.
Жизненный цикл
[править | править код]После связывания с рецептором вирус бешенства попадает в клетки-хозяева через эндосомный путь. Внутри эндосомы низкое рН-значение индуцирует процесс слияния мембран, тем самым обеспечивая вирусному геному возможность достичь цитозоля. Оба процесса, связывание рецептора и слияние мембран, катализирует гликопротеин G, который играет критически важную роль в патогенезе (мутировавший вирус без G-белков не может распространяться)[6].
Следующим шагом является транскрипция вирусного генома полимеразой PL (P является важным кофактором для L-полимеразы) для того, чтобы сделать новый вирусный белок. Вирусная полимераза может распознавать только рибонуклеопротеиды и не может использовать РНК в качестве матрицы. Транскрипция регулируется цис-регуляторными элементами последовательности генома вируса и белком М, который является не только важным для построения вируса, но также регулирует часть производства мРНК для репликации. Позже активизируется полимераза коммутаторов репликации для получения полноразмерной положительной цепи копии РНК. Эти комплементарные РНК используются в качестве шаблонов для создания новой отрицательной цепи РНК генома. Они вместе с белком N формируют рибонуклеопротеиды, которые затем могут образовывать новые вирусы[9].
Заражение
[править | править код]В сентябре 1931 года Джозеф Леннокс Паван[англ.] с острова Тринидад (Вест-Индия), правительственный бактериолог, нашёл тельца Негри в мозге летучей мыши с необычными повадками. В 1932 году Паван впервые обнаружил, что заражённые летучие мыши-вампиры могут заражать бешенством людей и других животных[10][11].
Из раны вирус бешенства быстро распространяется вдоль нервных путей в периферической нервной системе. Аксонный транспорт вируса бешенства в центральную нервную систему является ключевым шагом патогенеза при естественном заражении. Точный молекулярный механизм этого транспорта неизвестен, хотя связывание белка P с вирусом бешенства в лёгкой цепи динеина (DYNLL1[англ.]) было доказано[12]. P-белок также действует как антагонист интерферона, снижая таким образом иммунную реакцию организма хозяина.
Из ЦНС вирус дополнительно распространяется на другие органы. Слюнные железы, расположенные в тканях полости рта и щёк, получают высокие концентрации вируса, тем самым позволяя ему далее распространяться в результате процесса слюноотделения. Летальный исход может произойти в период от двух дней до пяти лет с момента первичной инфекции[13]. Это в значительной степени зависит от вида животного, действующего в качестве хозяина. Большинство инфицированных млекопитающих умирают в течение нескольких недель, в то время как представители некоторых видов, таких как африканский жёлтый мангуст (Cynictis penicillata), могут переживать инфекцию бессимптомно в течение многих лет[14].
История
[править | править код]Бешенство известно человечеству с древнейших времён. В I веке до н.э. Корнелий Цельс дал болезни название, сохранившееся до наших дней, — гидрофобия, и предложил в целях лечения проводить каутеризацию (прижигание места укуса раскалённым железом).
В 1804 г. немецкий врач Г. Цинке доказал, что бешенство можно переносить от одного животного к другому путём введения в кровь или под кожу слюны бешеного животного.
Кругельштейн в 1879 г. выявил локализацию вируса бешенства в нервной ткани. Он писал: «Если ядом слюны инфицировать нервное окончание, то оно, насытившись, передаст затем яд вдоль симпатических нервов спинному мозгу, а от него он достигнет головного мозга».
Разработка вакцины против бешенства стала триумфом науки и сделала Луи Пастера (Pasteur L., 1822-1895) всемирно известным человеком. Ещё при жизни ему поставили памятник в Париже.
Несколько лет у Пастера ушло на безрезультатные усилия выделить возбудитель. Потерпели неудачу и попытки размножения возбудителя бешенства в условиях in vitro. Перейдя к экспериментам in vivo, Пастеру и его сотрудниками (Э. Ру, Ш. Шамберлан, Л. Пердри) удалось к 1884 году получить «фиксированный вирулентный фактор бешенства». Следующим этапом создания вакцины стал поиск приёмов, ослабляющих возбудитель бешенства. К 1885 году была создана вакцина против бешенства, которая успешно предотвращала развитие болезни у лабораторных животных.
17 февраля 1886 года в Париже микробиолог Луи Пастер на заседании Французской академии сделал доклад об открытии им вакцины против бешенства.
Антигенность
[править | править код]По проникновению вируса в организм, а также после вакцинации организм вырабатывает нейтрализующие вирус антитела, которые связываются и инактивируют вирус. Конкретные области белка G, которые являются наиболее антигенными, приводят к производству антител, нейтрализующих вирус - такие области называют эпитопами. Другие белки, такие как нуклеопротеиды, как было доказано, не могут вызывать выработку антител, нейтрализующих вирус[15]. Эпитопы, которые связываются с вирус-нейтрализующими антителами, являются линейными и конформационными[16].
Эволюция
[править | править код]Все дошедшие до нас вирусы бешенства развивались в течение последних 1500 лет[16]. Существуют семь генотипов вируса бешенства. В Евразии случаи заражения случаются из-за трёх из них — генотип 1 (классическое бешенство) и, в меньшей степени, генотипы 5 и 6 (European Bat lyssavirus 1 и European Bat lyssavirus 2)[17]. Генотип 1 появился в Европе в XVII веке и распространился на Азию, Африку и Америку в результате европейских территориальных исследований и колонизации.
В Северной Америке присутствует с 1281 года (95 % доверительный интервал: 906—1577 гг.)[18].
Белки вируса
[править | править код]Вирус бешенства вызывает около 50,000 смертей в год, а его смертоносность оценивается почти в 100%. Эта статистика вместе с отсутствием специфического лечения или противовирусного препарата делает исследование вируса чрезвычайно важным для снижения смертности от него.
Фосфопротеины и полимеразы вируса бешенства являются важными мишенями для препаратов.
Примечания
[править | править код]- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ ICTV Taxonomy history: Rabies lyssavirus Архивная копия от 24 марта 2017 на Wayback Machine на сайте ICTV (англ.) (Дата обращения: 23 марта 2017).
- ↑ Пиневич А. В., Сироткин А. К., Гаврилова О. В., Потехин А. А. Вирусология : учебник. — СПб. : Издательство Санкт-Петербургского университета, 2012. — С. 400. — ISBN 978-5-288-05328-3.
- ↑ Бешенство - Городской округ Ликино-Дулево. Дата обращения: 9 августа 2020. Архивировано 5 декабря 2020 года.
- ↑ "Осторожно, БЕШЕНСТВО!" 15 сентября 2017 (недоступная ссылка)
- ↑ 1 2 Finke S., Conzelmann K. K. (August 2005). «Replication strategies of rabies virus». Virus Res. 111(2): 120—131. doi:10.1016/j.virusres.2005.04.004. PMID 15885837.
- ↑ rabies complete genome — Nucleotide — NCBI. Дата обращения: 3 октября 2017. Архивировано 25 декабря 2018 года.
- ↑ A dictionary of medical eponyms Архивная копия от 13 сентября 2017 на Wayback Machine (англ.)
- ↑ 1 2 Albertini AA, Schoehn G, Weissenhorn W, Ruigrok RW (January 2008). «Structural aspects of rabies virus replication». Cell. Mol. Life Sci. 65(2): 282—294. doi:10.1007/s00018-007-7298-1. PMID 17938861.
- ↑ Pawan, J. L. (1936). "Transmission of the Paralytic Rabies in Trinidad of the Vampire Bat: Desmodus rotundus murinus Wagner, 1840". Annals of Tropical Medicine and Parasitology 30: 137—156. ISSN 0003-4983.
- ↑ Pawan, J. L. (1936). "Rabies in the vampire bat of Trinidad, with special reference to the clinical course and the latency of infection". Ann Trop Med Parasitol 30: 101—129. ISSN 0003-4983
- ↑ Raux H, Flamand A, Blondel D (November 2000). "Interaction of the rabies virus P protein with the LC8 dynein light chain" Архивная копия от 11 декабря 2019 на Wayback Machine. J. Virol. 74(21): 10212—10216. doi:10.1128/JVI.74.21.10212-10216.2000. PMC 102061. PMID 11024151.
- ↑ "Rabies" Архивная копия от 6 сентября 2008 на Wayback Machine. University of Northern British Columbia
- ↑ Taylor PJ (December 1993). "A systematic and population genetic approach to the rabies problem in the yellow mongoose (Cynictis penicillata)". Onderstepoort J. Vet. Res. 60(4): 379—387. PMID 7777324.
- ↑ Benmansour A (1991). "Antigenicity of rabies virus glycoprotein". Journal of Virology 65(8): 4198—4203. PMC 248855. PMID 1712859.
- ↑ 1 2 Bakker, A. B.; Marissen, W. E.; Kramer, R. A.; Rice, A. B.; Weldon, W. C.; Niezgoda, M.; Hanlon, C. A.; Thijsse, S.; et al. (Jul 2005). "Novel human monoclonal antibody combination effectively neutralizing natural rabies virus variants and individual in vitro escape mutants". J Virol 79(14): 9062—9068. doi:10.1128/JVI.79.14.9062-9068.2005. PMC 1168753. PMID 15994800.
- ↑ McElhinney, L. M.; Marston, D. A.; Stankov, S; Tu, C.; Black, C.; Johnson, N.; Jiang, Y.; Tordo, N.; Müller, T.; Fooks, A. R. (2008). "Molecular epidemiology of lyssaviruses in Eurasia". Dev Biol (Basel) 131: 125—131. PMID 18634471.
- ↑ Kuzmina, N. A.; Kuzmin, I. V.; Ellison, J. A.; Taylor, S. T.; Bergman, D. L.; Dew, B.; Rupprecht, C. E. (2013). "A reassessment of the evolutionary timescale of bat rabies viruses based upon glycoprotein gene sequences". Virus Genes. Forthcoming (2): 305. doi:10.1007/s11262-013-0952-9.