Прогрессирующая мультифокальная лейкоэнцефалопатия
| Прогрессивная мультифокальная лейкоэнцефалопатия | |
|---|---|
 | |
| МКБ-11 | 8A45.02 |
| МКБ-10 | А81.2 |
| МКБ-10-КМ | A81.2 |
| МКБ-9-КМ | 046.3[1][2] |
| DiseasesDB | 10718 |
| MedlinePlus | 000674 |
| MeSH | D007968 |
Прогрессивная мультифокальная лейкоэнцефалопатия (ПМЛ) — это быстро прогрессирующее демиелинизирующее инфекционное[3] заболевание центральной нервной системы с асимметричным поражением мозга. Вызывается активацией полиомавируса человека 2, носителем которого является около 80 % населения США.[4]
Полиомавирус человека 2 (вирус JC) является одним из шести видов человеческих полиомавирусов и был назван по инициалам пациента (John Cunningham), у которого он был впервые обнаружен в 1971 году.[5]. Его активации в организме человека предшествует значительная супрессия иммунной системы: в подавляющем большинстве случаев ПМЛ является проявлением синдрома приобретенного иммунодефицита (СПИД), в остальных случаях — после иммуносупресивной и иммуномодуляторной терапии, например в рамках лечения моноклональными антителами или после трансплантации органов, а также при гематологических новообразованиях — таких как болезнь Ходжкина, хронический лимфолейкоз.[6] Особенно часто заболевание после трансплантации костного мозга. Проблемой является возникновение ПМЛ у больных рассеянным склерозом, находящихся на лечении натализумабом.
Эффективного метода лечения ПМЛ к настоящему моменту не найдено[7] (кроме случаев, когда иммуносупрессия достигалась применением моноклональных антител).
Эпидемология
[править | править код]До эпидемии ВИЧ-инфекции это было крайне редкое заболевание. За 26 лет с 1954 до 1984 было описано только 230 случаев ПМЛ. Заболеваемость была 1:1 000 000. В 1990-х годах заболеваемость выросла до 1:200 000. При этом среди ВИЧ-инфицированных заболеваемость достигала 3,3 на 1000 больных. После введения в практику антиретровирусной терапии (АРВТ) частота возникновения ПМЛ составляет около 1,3 случаев на 1000 ВИЧ-инфицированных в год.[7]
Патогенез и патологические изменения
[править | править код]Инфицирование вирусом JC протекает бессимптомно. Инфицирование наступает, как правило, ещё в детском возрасте, возбудитель остается в теле пожизненно.[8][9] Возможное место персистенции вируса — почки и/или костный мозг. В случае ослабления иммунной системы вирус транспортируется лейкоцитами в центральную нервную систему и начинает свою репликацию в белом веществе полушарий, ствола мозга, мозжечке и спинном мозге. Заболевание является демиелинизирующим, нейропатологически определяются множественные очаги демиелинизации, гиперхромные и увеличенные в размерах ядра олигодендроцитов, увеличенные и деформированные астроциты. Серое вещество мозга остается практически незатронутым. Гистопатологически заболевание считается доказанным в случае обнаружения JC-протеина, продуцируемого вирусом (при проведении иммуногистохимического исследования) или обнаружение генома JC-вируса при гибридизировании ткани.
Симптомы
[править | править код]Начало как правило, подострое и выражается в быстро прогрессирующем психосиндроме, диссоциированном с очаговыми неврологическими симптомами — прежде всего моно- или гемипарезами, нарушениями речи и нарушениями зрения — такими, как геми- и квадрантные анопсии. Атаксии, головокружение, головные боли, нарушения чувствительности и эпилептические приступы возникают гораздо реже. Психические нарушения выражаются в прогрессирующих когнитивных нарушениях и, в отличие от деменции при ВИЧ-инфекции, сопровождаются очаговыми неврологическими нарушениями.[6]. Было описано чисто спинальное протекание болезни (очаги только в спинном мозге) без нарушений психики.[10]
Диагностика
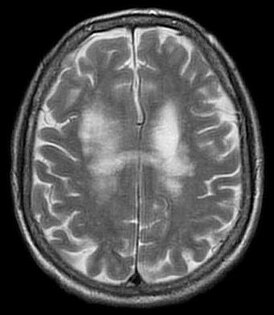
[править | править код]Магнитно-резонансная томография (МРТ) является по сравнению с компьютерной томографией предпочтительной методикой. В Т2-взвешенных изображениях определяются гиперинтенсивные очаги — асимметрично распределенные в белом веществе лобных и теменно-затылочных отделов, а также в корковом веществе, в стволе мозга и мозжечке, без — или с незначительным захватом контрастного вещества; увеличения объёма ткани не наблюдается. В Т1-взвешенных изображениях эти очаги гипоинтенсивны. У одной трети пациентов также обнаруживаются инфратенториальные очаги, которые могут также определяться изолированно.[11].
Изменения спинномозговой жидкости неспецифичны и характерны для таковых при заболеваниях, связанных с вирусом иммунодефицита. Прямое обнаружение вируса JC путём ПЦР-обследования удается в 74-90 %. Также может быть определена нагрузка JC-вируса по аналогии с такой при ВИЧ. Исследования показали, что снижение показателей вирусной нагрузки или даже их исчезновение в связи с проводимой терапией связаны с улучшенным прогнозом заболевания и общим числом выживания.[12]
Электроэнцефалография: неспецифическое замедление активности.
Биопсия ткани мозга: проводится при повторно негативной ПЦР и прогрессирующем заболевании.
Для окончательной постановки диагноза необходимо: наличие заболевания, обуславливающего иммуносупрессию; типичные изменения МРТ и положительная ПЦР; иногда — биопсия ткани мозга.
Дифференциальный диагноз
[править | править код]При подозрении на ПМЛ в первую очередь должны быть исключены более частые, чем ПМЛ энцефалопатии — такие, как при токсоплазмозе, криптококкозе. Далее проводится дифференциальный диагноз с лимфомой ЦНС, ВИЧ-деменцией и лейкодистрофией; у детей — с подострым склерозирующим панэнцефалитом. При подозрении на ПМЛ у больных с рассеянным склерозом, находящихся на терапии натализумабом, необходимо исключить очередное обострение основного заболевания — при этом очаги в МРТ принимают на себя контрастное вещество.
Лечение
[править | править код]Специфическая терапия неизвестна. Для подтверждения эффекта лечения различными противовирусными препаратами не хватает рандомизированных исследований[13]. Самым эффективным методом лечения является восстановление активности иммунной системы. У пациентов с иммуносупрессивной терапией она должна быть по возможности отменена или уменьшена дозировка[14]. Пациентам, получавшим моноклональные антитела показан плазмаферез. У пациентов с возникновением ПМЛ после трансплантации органов при определённых условиях трансплантированный орган должен быть удален. Обсуждается возможность применения атипичных нейролептиков: известна их способность блокирования рецепторов- 5-HT2A — эти же рецепторы являются целью вируса JC; для подтверждения этого предположения пока нет контролируемых исследований.[13]
Прогноз
[править | править код]Негативный. Если не удалось восстановить или улучшить функцию иммунной системы, смерть наступает от 3 до 20 месяцев после постановки диагноза ПМЛ.
Литература
[править | править код]- Maschke MArent G. und Maschke M. HIV-Infektion und AIDS: neurologische Manifestation. Kohlhammer-Verlag 2013 «Therapie und Verlauf neurologischer Erkrankungen» p. 612
- C. S. Tan, I. J. Koralnik: Progressive multifocal leukoencephalopathy and other disorders caused by JC virus: clinical features and pathogenesis. In: Lancet Neurology, 2010; 9:425-437. PMID 20298966, doi:10.1016/S1474-4422(10)70040-5.
Ссылки
[править | править код]- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29 — 2018-06-29 — 2018.
- ↑ A. K. Bag, J. K. Curé, P. R. Chapman, G. H. Roberson, R. Shah. Инфекция головного мозга вирусом JC. Дата обращения: 12 августа 2015. Архивировано 21 августа 2015 года.
- ↑ Weissert R. Progressive multifokale Leukenzephalopathie. Journal of Neuroimmunologie 2011; 231: 73-74
- ↑ Padgett BL, Walker DL, Zu Rhein GM et al. Cultivation of papova-like virus from human brain with progressive multifocal leucoencephalopathy. Lancet. 1971; 1:1257-60
- ↑ 1 2 Berger JR. The clinical features of PML. Cleve Clin J Med. 2011; 78: S8-12
- ↑ 1 2 Прогрессирующая мультифокальная лейкоэнцефалопатия (обзор литературы). Дата обращения: 23 августа 2014. Архивировано из оригинала 28 ноября 2021 года.
- ↑ Kean et al. PLoS Pathog. 2009 5
- ↑ Egli et al J Infect Dis. 2009 Mar 15;199
- ↑ Stich O., Herpers M., Keil A. Et al. JC virus myelitis without cerebral involvement in acute myeloid leukemia. European Journal of Neurology 2011; 18 (11): e143-e144
- ↑ Whiteman ML, Post MJ, Berger JR, Tate LG, Bell MD, Limonte LP. Progressive multifocal leukoencephalopathy in 47 HIV-seropositive patients: neuroimaging with clinical and pathologic correlation. Radiology. 1993 Apr;187(1):233-40
- ↑ Weber T, Turner RW, Frye S, Lüke W, Kretzschmar HA, Lüer W, Hunsmann G. Progressive multifocal leukoencephalopathy diagnosed by amplification of JC virus-specific DNA from cerebrospinal fluid. AIDS 1994 Jan;8(1):49-57.
- ↑ 1 2 Progressive multifokale Leukoenzephalopathie. hivbuch.de. Дата обращения: 23 сентября 2015. Архивировано 25 сентября 2015 года.
- ↑ Stüve O, Marra CM, Cravens PD et al. Potential risk of progressive multifocal leukoencephalopathy with natalizumab therapy: possible interventions. Архивная копия от 19 апреля 2012 на Wayback Machine Arch Neurol. 2007;64:169-76. PMID 17296831