Ацетат кобальта(II)
| Ацетат кобальта(II) | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
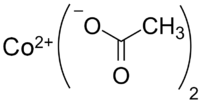
ацетат кобальта (II) |
| Традиционные названия | Уксуснокислый кобальт |
| Хим. формула | C4H6CoO4 |
| Рац. формула | Co(CH3COO)2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 177.0217 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | с разл. 140 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | вода (33,7 % по массе при 25 °C) |
| Классификация | |
| Рег. номер CAS | 71-48-7, тетрагидрат — 6147-53-1 |
| PubChem | 6277 |
| Рег. номер EINECS | 200-755-8 |
| SMILES | |
| InChI | |
| ChEBI | 85138 |
| ChemSpider | 6041 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацета́т ко́бальта Со(CH3COO)2 — кобальтовая соль уксусной кислоты. Из водных растворов кристаллизуется в виде тетрагидрата — красных кристаллов с моноклинной решеткой (а = 0,477 нм, b = 1,185 нм, с = 0,842 нм, р = 94,5°, z = 2, пространств, группа Р 21/с);
Свойства
[править | править код]Гигроскопичен, хорошо растворим в воде (33,7 % по массе при 25 °C), растворим в уксусной кислоте, изобутиловом и амиловом спиртах, амилацетате, плохо растворим в этаноле (0,29 % при 25 °C).
При 140 °C кристаллогидрат обезвоживается с частичным разложением. Безводный ацетат кобальта светло-розового цвета может быть получен действием уксусного ангидрида на нитрат кобальта Co(NO3)2.
Окисляется озоном или при электролизе в уксусной кислоте до ацетата трехвалентного кобальта Со(ОСОСН3)3, кристаллизующегося в виде светло-зеленых кристаллов, разлагающихся ~100 °C.
Синтез
[править | править код]Получают ацетат кобальта взаимодействием уксусной кислоты с карбонатом СоСО3 или гидроксидом кобальта Со(OH)2:
Применение
[править | править код]В промышленности ацетат кобальта используется как вспомогательный сиккатив и для получения катализаторов оксосинтеза.
В лабораторной практике раствор ацетат кобальта и бромоводорода (или бромида натрия) в уксусной кислоте в эквимолярном отношении (англ. cobalt acetate bromide) используется в качестве катализатора окисления алкилбензолов в карбоновые кислоты или кетоны (например, окисление ксилолов в фталевые кислоты и тетралина в α-тетралон)[1].
Примечания
[править | править код]- ↑ D. D. Eley и Paul B. Weisz, Advances in catalysis and related subjects, p.316 (Academic Press, 1976).
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |


