Этерификация: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
м Удaлeнa Категория:Органическая химия; Дoбaвлeнa Категория:Реакции в органической химии с помощью HotCat |
В статью без источников добавлена «внутренняя» ссылка на АИ (одноимённая статья в Викитеке из «ЭСБЕ»). |
||
| Строка 23: | Строка 23: | ||
== См. также == |
== См. также == |
||
* [[Переэтерификация]] |
* [[Переэтерификация]] |
||
== Литература == |
|||
* {{ВТ-ЭСБЕ|Этерификация|Тутурин Н. Н.,}} |
|||
{{Chem-stub}} |
{{Chem-stub}} |
||
Версия от 09:17, 17 ноября 2013
Этерификация (от др.-греч. αἰθήρ — эфир и лат. facio — делаю) — реакция образования сложных эфиров при взаимодействии кислот и спиртов:
- RCOOH + R’OH ⇔ RCOOR' + Н2О
Механизм реакции
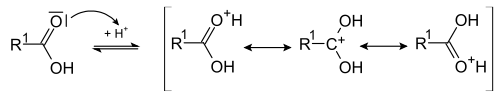
Реакция протекает в условиях кислотного катализа и проходит по механизму нуклеофильного замещения. На первой стадии происходит протонирование атома кислорода карбонильной группы карбоновой кислоты с образованием резонансно стабилизированного карбкатиона:
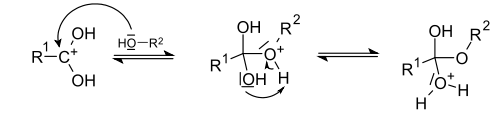
после чего происходит нуклеофильная атака атома кислорода гидроксильной группы спирта на карбониевый центр с образованием алкилоксониевого иона, эта стадия является лимитирующей. Затем в алкилоксониевом ионе происходит миграция протона на один из гидроксилов с образованием уходящей группы —O+H2:
Завершающей стадией является отщепление промежуточного продукта присоединения воды и протона — катализатора с образованием сложного эфира:
Механизм реакции подтвержден экспериментом с использованием изотопных меток: при использовании спирта, меченного изотопом 18O, метка оказывается в составе сложного эфира:
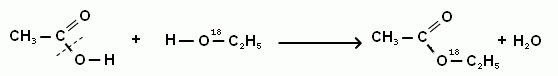
Применение в органическом синтезе
Этерификацию обычно проводят в присутствии катализаторов — сильных кислот (серная кислота, толуолсульфоновая кислота и т. п.).
Реакция этерификации обратима (гидролиз сложных эфиров называется омылением), положение равновесия зависит от строения и концентраций спирта и карбоновой кислоты, то есть для реакционной смеси существует предел этерификации, при котором устанавливается равновесие, характеризующееся определенным соотношением концентраций исходных спирта и кислоты и продукта их реакции — сложного эфира. Так, например, при эквимолярном соотношении этанола и уксусной кислоты в исходной реакционной смеси равновесие устанавливается, когда ~2/3 спирта и кислоты прореагируют с образованием этилацетата.
Для повышения выхода сложного эфира используют либо избыток одного из реагентов (обычно спирта), либо отгонку образующейся при этерификации воды в виде азеотропной смеси с добавляемым в реакционную смесь бензолом.
См. также
Литература
- Тутурин Н. Н.,. Этерификация // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Это заготовка статьи по химии. Помогите Википедии, дополнив её. |