Семикарбазид
| Семикарбазид | |
|---|---|
 | |
| Общие | |
| Традиционные названия | N-аминомочевина |
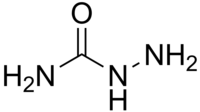
| Хим. формула | H2N-NHCONH2 |
| Рац. формула | CH5N3O |
| Физические свойства | |
| Молярная масса | 75,08 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 96 °C |
| Классификация | |
| Рег. номер CAS | 57-56-7 |
| PubChem | 5196 |
| Рег. номер EINECS | 200-339-6 |
| SMILES | |
| InChI | |
| ChEBI | 28306 |
| ChemSpider | 5008 |
| Безопасность | |
| ЛД50 | мыши, орально 176[1] |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Семикарбазид (N-аминомочевина, гидразид карбаминовой кислоты, карбамоилгидразин) — бесцветные кристаллы, растворимые в воде и этаноле.
Свойства[править | править код]
Семикарбазид — однокислотное основание, сильнее мочевины, но слабей гидразина, с кислотами образует соли. Нестабилен, при длительном хранении окисляется кислородом воздуха и разлагается; соли семикарбазида и минеральных кислот при хранении стабильны, поэтому в лабораторной практике используют гидрохлорид семикарбазида.
Гидразинная аминогруппа семикарбазида значительно более нуклеофильна, чем амидная, с карбонильными соединениями семикарбазид образует продукты конденсации по гидразинной аминогруппе — семикарбазоны. Реакция идет через промежуточное образование α-аминоспирта:
В случае, если карбонильные соединения несут сильные электронакцепторные заместители при карбонильной группе (хлораль, гексафторацетон), реакция останавливается на стадии образования соответствующих α-аминоспиртов.
C дикарбонильными соединениями семикарбазид конденсируется с образованием гетероциклических соединений, образуя с 1,2-дикарбонильными соединениями 3-гидроксипроизводные 1,2,4-триазинов[2], а с 1,3-дикарбонильными — 1-карбамоилпиразолы.
Основные методы синтеза семикарбазида — гидразинолиз мочевины:
и восстановление нитромочевины[3]:
Примечания[править | править код]
- ↑ Journal of Pharmacology and Experimental Therapeutics. Vol. 122, Pg. 110, 1958.
- ↑ Eid, Mohga M; Mohamed A Badawy, Yehia A Ibrahim. Condensed 1,2,4‐triazines. Regioselective condensations with benzo[hquinoline‐5,6‐dione] (англ.) // Journal of Heterocyclic Chemistry : journal. — 1983. — 1 September (vol. 20, no. 5). — P. 1255—1258. — ISSN 1943-5193. — doi:10.1002/jhet.5570200521.
- ↑ A. W. Ingersoll, L. J. Bircher, and M. M. Brubaker. Semicarbazide sulfate. Organic Syntheses, Coll. Vol. 1, p.485 (1941); Vol. 5, p.93 (1925). Дата обращения: 13 апреля 2012. Архивировано 20 октября 2012 года.



![{\displaystyle {\mathsf {H_{2}N{\text{-}}CO{\text{-}}NH{\text{-}}NO_{2}{\xrightarrow[{}]{[H]}}H_{2}N{\text{-}}CO{\text{-}}NH{\text{-}}NH_{2}+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/223b761f586ce3c0a237e8e5118dd11c398b9d63)