Вода
| Вода | |||
|---|---|---|---|
| |||
 Вода в бассейне Вода в бассейне | |||
| Общие | |||
| Систематическое наименование |
Оксид водорода Вода[1] |
||
| Традиционные названия | вода | ||
| Хим. формула | H2O | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 18,01528 г/моль | ||
| Плотность | 1 г/см3[2] | ||
| Твёрдость | 1,5[6] | ||
| Динамическая вязкость | 0,00101 Па·с | ||
| Кинематическая вязкость |
0,01012 см²/с (при 20 °C) |
||
| Энергия ионизации | 12,61 эВ[7] | ||
| Скорость звука в веществе |
(дистиллированная вода) 1348 м/с |
||
| Термические свойства | |||
| Температура | |||
| • плавления | 273,1 K (0 ° C) | ||
| • кипения | 373,1 K; 99,974 °C | ||
| • разложения | при 2200 °C разлагаются 3% молекул | ||
| Тройная точка | 273,2 K (0,01 ° C), 611,72 Па | ||
| Критическая точка | 647,1 K (374 ° C), 22,064 МПа | ||
| Мол. теплоёмк. | 75,37 Дж/(моль·К) | ||
| Теплопроводность | 0,56 Вт/(м·K) | ||
| Энтальпия | |||
| • образования | −285,83 кДж/моль | ||
| • кипения | 40,656 кДж/моль[3] и 40 655,928 Дж/моль[4] | ||
| Удельная теплота испарения | 2256,2 кДж/кг[5] | ||
| Удельная теплота плавления | 332,4 кДж/кг[5] | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 15,74 | ||
| Диэлектрическая проницаемость |
80,4 (20 ° C) 78,5 (25 ° C) |
||
| Оптические свойства | |||
| Показатель преломления | 1,3945, 1,33432, 1,32612, 1,39336, 1,33298 и 1,32524 | ||
| Структура | |||
| Дипольный момент | 6,2E−30 Кл·м[7] | ||
| Классификация | |||
| Рег. номер CAS | 7732-18-5 | ||
| PubChem | 962 | ||
| Рег. номер EINECS | 231-791-2 | ||
| SMILES | |||
| InChI | |||
| RTECS | ZC0110000 | ||
| ChEBI | 15377 | ||
| ChemSpider | 937 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||

Вода́ (монооксид водорода, гидроксид водорода, химическая формула — H2O) — химическое вещество, представляющее собой бинарное неорганическое соединение, молекула которого состоит из двух атомов водорода и одного атома кислорода, которые соединены между собой ковалентной связью. Изначально, вода является продуктом горения (окисления) водорода при реакции с кислородом, но также может выступать конечным результатом и иных химических реакций.
При нормальных условиях вода представляет собой прозрачную жидкость, не имеющую цвета (при малой толщине слоя), запаха и вкуса. В твёрдом агрегатном состоянии вода преобразуется в лёд (кристаллы льда могут образовывать снег или иней), а в газообразном — в водяной пар. Вода также может существовать в виде жидких кристаллов (на гидрофильных поверхностях)[8][9]. Вода абсолютно нетоксична и безопасна для здоровья человека по причине, в том числе, стабильности вещества и негорючести воды (невосприимчивость к горению; наподобие углекислого газа).
Вода является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы).
Исключительно важна роль воды в глобальном кругообороте вещества и энергии[10], возникновении и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды. Вода является важнейшим веществом для всех живых существ на Земле[11]. В среднем в организме растений и животных содержится более 50 % воды[12].
Всего на Земле около 1400 млн км³ воды. Вода покрывает 71 % поверхности земного шара (океаны, моря, озёра, реки, льды — 361,13 млн км²[13][14]). Бо́льшая часть земной воды (97,54 %) принадлежит Мировому океану — это солёная вода, непригодная для сельского хозяйства и питья. Пресная же вода находится в основном в ледниках (1,81 %) и подземных водах (около 0,63 %), и лишь небольшая часть (0,009 %) в реках и озёрах. Материковые солёные воды составляют 0,007 %, в атмосфере содержится 0,001 % от всей воды нашей планеты[15][16]. В составе мантии Земли воды содержится в 10—12 раз больше, чем в Мировом океане[17].
Вода — это одно из немногих веществ в природе, которые расширяются при переходе из жидкой фазы в твёрдую (кроме воды, таким свойством обладают сурьма[18], висмут, галлий, германий и некоторые соединения и смеси).
Этимология[править | править код]
В письменных источниках слово «вода» встречается ещё в «Изборнике Святослава» (1076 год)[19].
Слово происходит от др.-русск. вода, далее — от праславянского *voda[20] (ср. ст.-слав. вода, болг. вода́, сербохорв. во̀да, словен. vóda, чеш. voda, слвц. voda, польск. woda, в.-луж., н.-луж. woda), затем — от праиндоевропейского *wed-, родственного лит. vanduõ, жем. unduo, д.-в.-н. waʒʒar «вода», гот. watō, англ. water, греч. ὕδωρ, ὕδατος, арм. գետ «река», фриг. βέδυ, др.-инд. udakám, uda-, udán- «вода», unátti «бить ключом», «орошать», ṓdman- «поток», алб. uj «вода»[21][22]. Русские слова «ведро», «выдра» имеют тот же корень.
В рамках необщепринятой гипотезы о существовании некогда праностратического языка слово может сравниваться с гипотетическим прауральским *wete (ср., например, фин. vesi, эст. vesi, коми va, венг. víz), а также с предполагаемыми праалтайскими, прадравидийским и прочими словами, и реконструироваться как *wetV для праязыка[23].
Химические названия[править | править код]
С формальной точки зрения вода имеет несколько различных корректных химических названий:
- Оксид водорода: бинарное соединение водорода с атомом кислорода в степени окисления −2, встречается также устаревшее название окись водорода.
- Гидроксид водорода: соединение гидроксильной группы OH− и катиона (H+)
- Гидроксильная кислота: воду можно рассматривать как соединение катиона H+, который может быть замещён металлом, и «гидроксильного остатка» OH−
- Монооксид дигидрогена
- Дигидромонооксид
Свойства[править | править код]
Физические свойства[править | править код]
Вода при нормальных условиях находится в жидком состоянии, тогда как аналогичные водородные соединения других элементов являются газами (H2S, CH4, HF). Атомы водорода присоединены к атому кислорода, образуя угол 104,45° (104°27′). Из-за большой разности электроотрицательностей атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода. По этой причине молекула воды обладает большим дипольным моментом (p = 1,84 Д, уступает только синильной кислоте и диметилсульфоксиду). Каждая молекула воды образует до четырёх водородных связей — две из них образует атом кислорода и две — атомы водорода[24]. Количество водородных связей и их разветвлённая структура определяют высокую температуру кипения воды и её удельную теплоту парообразования[24]. Если бы не было водородных связей, вода, на основании места кислорода в таблице Менделеева и температур кипения гидридов аналогичных кислороду элементов (серы, селена, теллура), кипела бы при −80 °C, а замерзала при −100 °C[25].
При переходе в твёрдое состояние молекулы воды упорядочиваются, при этом объёмы пустот между молекулами увеличиваются, и общая плотность воды падает, что и объясняет меньшую плотность (больший объём) воды в фазе льда. При испарении, напротив, все водородные связи рвутся. Разрыв связей требует много энергии, отчего у воды самая большая удельная теплоёмкость среди прочих жидкостей и твёрдых веществ. Для того чтобы нагреть один килограмм воды на один градус, требуется затратить 4,1868 кДж энергии. Благодаря этому свойству вода нередко используется как теплоноситель.
Помимо большой удельной теплоёмкости, вода также имеет большие значения удельной теплоты плавления (333,55 кДж/кг при 0 °C) и парообразования (2250 кДж/кг).
| Температура, °С | Удельная теплоёмкость воды, кДж/(кг*К) |
|---|---|
| −60 (лёд) | 1,64 |
| −20 (лёд) | 2,01 |
| −10 (лёд) | 2,22 |
| 0 (лёд) | 2,11 |
| 0 (чистая вода) | 4,218 |
| 10 | 4,192 |
| 20 | 4,182 |
| 40 | 4,178 |
| 60 | 4,184 |
| 80 | 4,196 |
| 100 | 4,216 |
Физические свойства разных изотопных модификаций воды при различных температурах[26]:
| Модификация воды | Максимальная плотность при температуре, °С | Тройная точка при температуре, °С |
|---|---|---|
| Н2O | 3,9834 | 0,01 |
| D2O | 11,2 | 3,82 |
| T2O | 13,4 | 4,49 |
| Н218O | 4,3 | 0,31 |
Относительно высокая вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями[источник не указан 1176 дней].
Вода является хорошим растворителем веществ с молекулами, обладающими электрическим дипольным моментом. При растворении молекула растворяемого вещества окружается молекулами воды, причём положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода, а отрицательно заряженные — атомы водорода. Поскольку молекула воды мала по размерам, много молекул воды могут окружить каждую молекулу растворяемого вещества.
Это свойство воды важно для живых существ. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде[27]. Вода необходима для жизни всех без исключения живых существ на Земле.
Вода обладает отрицательным электрическим потенциалом поверхности[уточнить].

Чистая вода — хороший изолятор. При нормальных условиях вода слабо диссоциирована на ионы и концентрация протонов (точнее, ионов гидроксония H3O+) и гидроксильных ионов OH− составляет 10−7 моль/л. Но поскольку вода — хороший растворитель, в ней практически всегда растворены те или иные вещества, например, соли, то есть в растворе присутствуют другие положительные и отрицательные ионы. Поэтому обычная вода хорошо проводит электрический ток. По электропроводности воды можно определить её чистоту.
Вода имеет показатель преломления n=1,33 в оптическом диапазоне. Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, чем обусловлен нагрев пищевых продуктов в микроволновой печи.
Агрегатные состояния[править | править код]
По состоянию различают:
- «твёрдое» — лёд
- «жидкое» — вода
- «газообразное» — водяной пар

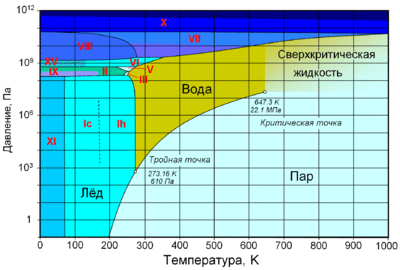
При нормальном атмосферном давлении (760 мм рт. ст., 101 325 Па) вода переходит в твёрдое состояние при температуре в 0 °C и кипит (превращается в водяной пар) при температуре 100 °C (значения 0 °C и 100 °C были выбраны как соответствующие температурам таяния льда и кипения воды при создании температурной шкалы «по Цельсию»). При снижении давления температура таяния (плавления) льда медленно растёт, а температура кипения воды — падает. При давлении в 611,73 Па (около 0,006 атм) температура кипения и плавления совпадает и становится равной 0,01 °C. Такие давление и температура называются тройной точкой воды. При более низком давлении вода не может находиться в жидком состоянии, и лёд превращается непосредственно в пар. Температура возгонки (сублимации) льда падает со снижением давления. При высоком давлении существуют модификации льда с температурами плавления выше комнатной.
С ростом давления температура кипения воды растёт[28]:
| Давление, атм. | Температура кипения (Ткип), °C |
|---|---|
| 0,987 (105 Па — нормальные условия) | 99,63 |
| 1 | 100 |
| 2 | 120 |
| 6 | 158 |
| 218,5 | 374,1 |
При росте давления плотность насыщенного водяного пара в точке кипения тоже растёт, а жидкой воды — падает. При температуре 374 °C (647 K) и давлении 22,064 МПа (218 атм) вода проходит критическую точку. В этой точке плотность и другие свойства жидкой и газообразной воды совпадают. При более высоком давлении и/или температуре исчезает разница между жидкой водой и водяным паром. Такое агрегатное состояние называют «сверхкритическая жидкость».
Вода может находиться в метастабильных состояниях — пересыщенный пар, перегретая жидкость, переохлаждённая жидкость. Эти состояния могут существовать длительное время, однако они неустойчивы и при соприкосновении с более устойчивой фазой происходит переход. Например, можно получить переохлаждённую жидкость, охладив чистую воду в чистом сосуде ниже 0 °C, однако при появлении центра кристаллизации жидкая вода быстро превращается в лёд.
Также вода может существовать в виде двух разных жидкостей («вторая вода» возникает при температуре около −70 °C и давлении в тысячи атмосфер), которые при определённых условиях даже не смешиваются друг с другом; гипотеза, что вода может существовать в двух различных жидких состояниях, была предложена примерно 30 лет назад на основе результатов компьютерного моделирования и экспериментально проверена только в 2020 г[29].
Удельная теплоёмкость[править | править код]
| t, °С | 0 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 | 60 | 65 | 70 | 75 | 80 | 85 | 90 | 95 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cp, Дж/(кг·град) | 4217 | 4191 | 4187 | 4183 | 4179 | 4174 | 4174 | 4174 | 4177 | 4181 | 4182 | 4182 | 4185 | 4187 | 4191 | 4195 | 4202 | 4208 | 4214 | 4220 |
Эти данные можно аппроксимировать эмпирической формулой:
- [31].

Диэлектрическая проницаемость воды[править | править код]
Статическая (для постоянного электростатического поля) диэлектрическая проницаемость воды при разной абсолютной температуре при давлении 1 бар в диапазоне температур −13…100 °C выражается эмпирической формулой[33]:
Результаты вычислений по этой формуле[34]:
| T, K | 260 | 273 | 283 | 293 | 298 | 303 | 313 | 323 | 333 | 343 | 353 | 363 | 373 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| −13 | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| 93,41 | 87,99 | 84,08 | 80,32 | 78,5 | 76,71 | 73,25 | 69,94 | 66,78 | 63,78 | 60,92 | 58,21 | 55,66 |
Оптические свойства[править | править код]
Они оцениваются по прозрачности воды, которая, в свою очередь, зависит от длины волны излучения, проходящего через воду. Вследствие поглощения оранжевых и красных компонентов света вода приобретает голубоватую окраску. Вода прозрачна только для видимого света и сильно поглощает инфракрасное излучение, поэтому на инфракрасных фотографиях водная поверхность всегда получается чёрной. Ультрафиолетовые лучи легко проходят через воду, поэтому растительные организмы способны развиваться в толще воды и на дне водоёмов, инфракрасные лучи проникают только в поверхностный слой. Вода отражает 5 % солнечных лучей, в то время как снег — около 85 %. Под лёд океана проникает только 2 % солнечного света[35][36].
Изотопные модификации[править | править код]
И кислород, и водород имеют природные и искусственные изотопы. В зависимости от типа изотопов водорода, входящих в молекулу, выделяют следующие виды воды:
- лёгкая вода (основная составляющая привычной людям воды) ;
- тяжёлая вода (дейтериевая) ;
- сверхтяжёлая вода (тритиевая) ;
- тритий-дейтериевая вода ;
- тритий-протиевая вода ;
- дейтерий-протиевая вода .
Последние три вида возможны, так как молекула воды содержит два атома водорода. Протий — самый лёгкий изотоп водорода, дейтерий имеет атомную массу 2,0141017778 а. е. м., тритий — самый тяжёлый, атомная масса 3,0160492777 а. е. м. В воде из-под крана тяжелокислородной воды ( и ) содержится больше, чем воды : их содержание, соответственно, 1,8 кг и 0,15 кг на тонну[25].
Хотя тяжёлая вода часто считается мёртвой водой, так как живые организмы в ней жить не могут, некоторые микроорганизмы могут быть приучены к существованию в ней[25].
По стабильным изотопам кислорода , и существуют три разновидности молекул воды. Таким образом, по изотопному составу существуют 18 разновидностей молекул воды. В действительности природная вода содержит все разновидности молекул.
Химические свойства[править | править код]
Вода является наиболее распространённым растворителем на планете Земля, во многом определяющим характер земной химии, как науки. Большая часть химии, при её зарождении как науки, начиналась именно как химия водных растворов веществ.
Воду иногда рассматривают как амфолит — и кислоту и основание одновременно (катион H+ анион OH−). В отсутствие посторонних веществ в воде одинакова концентрация гидроксид-ионов и ионов водорода (или ионов гидроксония), pKa = p(1,8⋅10−16) ≈ 15,74. Вода — химически активное вещество. Сильно полярные молекулы воды сольватируют ионы и молекулы, образуют гидраты и кристаллогидраты. Сольволиз, и в частности гидролиз, происходит в живой и неживой природе, и широко используется в химической промышленности.
Воду можно получать:
- В ходе реакций —
- В ходе реакций нейтрализации —
- Восстановлением водородом оксидов металлов —
Под воздействием очень высоких температур или электрического тока (при электролизе)[37], а также под воздействием ионизирующего излучения, как установил в 1902 году[38] Фридрих Гизель[англ.] при исследовании водного раствора бромида радия[39], вода разлагается на молекулярный кислород и молекулярный водород:
Вода реагирует при комнатной температуре:
- со фтором и межгалоидными соединениями
- (при низких температурах)
- с солями, образованными слабой кислотой и слабым основанием, вызывая их полный гидролиз
- с ангидридами и галогенангидридами карбоновых и неорганических кислот
- с активными металлорганическими соединениями (диэтилцинк, реактивы Гриньяра, метилнатрий и т. д.)
- с карбидами, нитридами, фосфидами, силицидами, гидридами активных металлов (кальция, натрия, лития и др.)
- со многими солями, образуя гидраты
- с боранами, силанами
- с кетенами, недоокисью углерода
- с фторидами благородных газов
Вода реагирует при нагревании:
- с углём, метаном
- с некоторыми алкилгалогенидами
Вода реагирует в присутствии катализатора:
- с амидами, эфирами карбоновых кислот
- с ацетиленом и другими алкинами
- с алкенами
- с нитрилами
Волновая функция основного состояния воды[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
В валентном приближении электронная конфигурация молекулы в основном состоянии: Молекула имеет замкнутую оболочку, неспаренных электронов нет. Заняты электронами четыре молекулярные орбитали (МО) — по два электрона на каждой МО , один со спином , другой со спином , или 8 спин-орбиталей . Волновая функция молекулы, , представленная единственным детерминантом Слэтера Ф, имеет вид
Симметрия этой волновой функции определяется прямым произведением НП, по которым преобразуются все занятые спин-орбитали
Принимая во внимание, что прямое произведение невырожденного НП самого на себя является полносимметричным НП и прямое произведение любого невырожденного представления Г на полносимметричное есть Г, получаем:
Виды[править | править код]
Вода на Земле может существовать в трёх основных состояниях:
- твёрдом
- жидком
- газообразном
Вода может приобретать различные формы, которые могут одновременно соседствовать и взаимодействовать друг с другом:
- водяной пар и облака в небе;
- морская вода и айсберги;
- ледники и реки на поверхности земли;
- водоносные слои в земле.
Вода способна растворять в себе множество органических и неорганических веществ. Из-за важности воды как источника жизни, её нередко подразделяют на типы по различным принципам.
Виды воды по особенностям происхождения, состава или применения:
- по содержанию катионов кальция и магния
- по изотопам водорода в молекуле
- лёгкая вода (по составу почти соответствует обычной)
- тяжёлая вода (дейтериевая)
- сверхтяжёлая вода (тритиевая)
- другие виды
- пресная вода
- дождевая вода
- морская вода
- подземные воды
- минеральная вода
- солоноватая вода
- питьевая вода и водопроводная вода
- дистиллированная вода и деионизированная вода
- сточные воды
- ливневая вода или поверхностные воды
- апирогенная вода
- поливода
- структурированная вода — термин, применяемый в неакадемических теориях
- талая вода
- мёртвая вода и живая вода — виды воды со сказочными свойствами
Вода, входящая в состав другого вещества и связанная с ним физическими связями, называется влагой. В зависимости от вида связи, выделяют:
- сорбционную, капиллярную и осмотическую влагу в твёрдых веществах,
- растворённую и эмульсионную влагу в жидкостях,
- водяной пар или туман в газах.
Вещество, содержащее влагу, называют влажным веществом. Влажное вещество, не способное более сорбировать (поглощать) влагу, — насыщенное влагой вещество.
Вещество, в котором содержание влаги пренебрежимо мало при данном конкретном применении, называют сухим веществом. Гипотетическое вещество, совершенно не содержащее влагу, — абсолютно сухое вещество. Сухое вещество, составляющее основу данного влажного вещества, называют сухой частью влажного вещества.
Смесь газа с водяным паром носит название влажный газ (парогазовая смесь — устаревшее название)[40].

В природе[править | править код]
В атмосфере нашей планеты вода находится в виде капель малого размера, в облаках и тумане, а также в виде пара. При конденсации выводится из атмосферы в виде атмосферных осадков (дождь, снег, град, роса). В совокупности жидкая водная оболочка Земли называется гидросферой, а твёрдая — криосферой. Вода является важнейшим веществом всех живых организмов на Земле. Предположительно, зарождение жизни на Земле произошло в водной среде.
Мировой океан содержит более 97,54 % земной воды, ледники — 1,81 %, подземные воды — около 0,63 %, реки и озёра — 0,009 %, материковые солёные воды — 0,007 %, атмосфера — 0,001 %[14].
Атмосферные осадки[править | править код]
Этот раздел статьи ещё не написан. |
Вода за пределами Земли[править | править код]
Вода — чрезвычайно распространённое вещество в космосе, однако из-за высокого внутрижидкостного давления вода не может существовать в жидком состоянии в условиях вакуума космоса, отчего она представлена только в виде пара или льда.
Одним из наиболее важных вопросов, связанных с освоением космоса человеком и возможности возникновения жизни на других планетах, является вопрос о наличии воды за пределами Земли в достаточно большой концентрации. Известно, что некоторые кометы более, чем на 50 % состоят из водяного льда. Не стоит, впрочем, забывать, что не любая водная среда пригодна для жизни.
В результате бомбардировки лунного кратера, проведённой 9 октября 2009 года НАСА с использованием космического аппарата LCROSS, впервые были получены достоверные свидетельства наличия на спутнике Земли водяного льда в больших объёмах[42].
Вода широко распространена в Солнечной системе. Наличие воды (в основном в виде льда) подтверждено на многих спутниках Юпитера и Сатурна: Энцеладе[43][44], Тефии, Европе, Ганимеде и др. Вода присутствует в составе всех комет и многих астероидов. Учёными предполагается, что многие транснептуновые объекты имеют в своём составе воду.
Вода в виде паров содержится в атмосфере Солнца (следы)[45], атмосферах Меркурия (3,4 %, также большие количества воды обнаружены в экзосфере Меркурия)[46], Венеры (0,002 %)[47], Луны[48], Марса (0,03 %)[49], Юпитера (0,0004 %)[50], Европы[51], Сатурн, Урана (следы)[52] и Нептуна[53] (найден в нижних слоях атмосферы).
Содержание водяного пара в атмосфере Земли у поверхности колеблется от 3—4 % в тропиках и до 2·10−5% в Антарктиде[54].
Кроме того, вода обнаружена на экзопланетах, например HD 189733 A b[55], HD 209458 b[56] и GJ 1214 b[57].
Жидкая вода, предположительно, имеется под поверхностью некоторых спутников планет — наиболее вероятно, на Европе — спутнике Юпитера.
Биологическая роль[править | править код]

Вода играет уникальную роль как вещество, определяющее возможность существования и саму жизнь всех существ на Земле. Она выполняет роль универсального растворителя, в котором происходят основные биохимические процессы живых организмов. Уникальность воды состоит в том, что она достаточно хорошо растворяет как органические, так и неорганические вещества, обеспечивая высокую скорость протекания химических реакций и в то же время — достаточную сложность образующихся комплексных соединений.
Благодаря водородной связи, вода остаётся жидкой в широком диапазоне температур, причём именно в том, который широко представлен на планете Земля в настоящее время.
Поскольку у льда плотность меньше, чем у жидкой воды, вода в водоёмах замерзает сверху, а не снизу. Образовавшийся слой льда препятствует дальнейшему промерзанию водоёма, это позволяет его обитателям выжить. Существует и другая точка зрения: если бы вода не расширялась при замерзании, то не разрушались бы клеточные структуры, соответственно замораживание не наносило бы ущерба живым организмам. Некоторые существа (тритоны) переносят замораживание/оттаивание — считается, что этому способствует особый состав клеточной плазмы, не расширяющейся при замораживании.
Применение[править | править код]
В земледелии[править | править код]
Выращивание достаточного количества сельскохозяйственных культур на открытых засушливых землях требует значительных расходов воды на ирригацию.
Для питья и приготовления пищи[править | править код]

Живое человеческое тело содержит от 50 % до 75 % воды[58], в зависимости от веса и возраста. Потеря организмом человека более 10 % воды может привести к смерти. В зависимости от температуры и влажности окружающей среды, физической активности и т. д. человеку нужно выпивать разное количество воды; ведётся много споров о том, сколько воды нужно потреблять для оптимального функционирования организма.
Питьевая вода представляет собой воду из какого-либо источника, очищенную от микроорганизмов и вредных примесей. Пригодность воды для питья при её обеззараживании перед подачей в водопровод оценивается по количеству кишечных палочек на литр воды, поскольку кишечные палочки распространены и достаточно устойчивы к антибактериальным средствам, и если кишечных палочек будет мало, то будет мало и других микробов. Если кишечных палочек не больше, чем 3 на литр, вода считается пригодной для питья[59][60].

В спорте[править | править код]
Многими видами спорта занимаются на водных поверхностях, на льду, на снегу и даже под водой. Это подводное плавание, хоккей, лодочные виды спорта, биатлон, шорт-трек и др.

Для смазки[править | править код]
Вода применяется как смазочный материал для смазки подшипников из древесины, пластиков, текстолита, подшипников с резиновыми обкладками и др. Воду также используют в эмульсионных смазках[61].
Исследования[править | править код]
Происхождение воды на планете[править | править код]
Происхождение воды на Земле является предметом научных споров. Некоторые учёные[кто?] считают, что вода была занесена астероидами или кометами на ранней стадии образования Земли, около четырёх миллиардов лет назад, когда планета уже сформировалась в виде шара. В 2010-е годы было установлено, что вода появилась в мантии Земли не позже 2,7 миллиардов лет назад[62].
Гидрология[править | править код]
Гидроло́гия — наука, изучающая природные воды, их взаимодействие с атмосферой и литосферой, а также явления и процессы, в них протекающие (испарение, замерзание и т. п.). Предметом изучения гидрологии являются все виды вод гидросферы в океанах, морях, реках, озёрах, водохранилищах, болотах, почвенных и подземных водах.
Также гидрология исследует круговорот воды в природе, влияние на него деятельности человека и управление режимом водных объектов и водным режимом отдельных территорий; проводит анализ гидрологических элементов для отдельных территорий и Земли в целом; даёт оценку и прогноз состояния и рационального использования водных ресурсов; пользуется методами, применяемыми в географии физике и других науках. Данные гидрологии моря используются при плавании и ведении боевых действий надводными кораблями и подводными лодками.
Гидрология подразделяется на океанологию, гидрологию суши и гидрогеологию:
- Океанология подразделяется на биологию океана, химию океана, геологию океана, физическую океанологию, и взаимодействие океана и атмосферы.
- Гидрология суши подразделяется на гидрологию рек (речную гидрологию, потамологию), озероведение (лимнологию), болотоведение, гляциологию.
- Гидрогеология — наука, изучающая происхождение, условия залегания, состав и закономерности движений подземных вод. Также изучается взаимодействие подземных вод с горными породами, поверхностными водами и атмосферой. В сферу этой науки входят такие вопросы, как динамика подземных вод, гидрогеохимия, поиск и разведка подземных вод, а также мелиоративная и региональная гидрогеология. Данные гидрогеологии используются, в частности, для решения вопросов водоснабжения, мелиорации и эксплуатации месторождений.
См. также[править | править код]
- Аквафобия
- Бутилированная вода
- Гидроэнергетика
- Горение водорода
- Жажда
- Энергия волн океана
- Эффект Мпембы
Примечания[править | править код]
- ↑ англ. International Union of Pure and Applied Chemistry. Nomenclature of Inorganic Chemistry. IUPAC RECOMMENDATIONS 2005. RSC Publishing, 2005. — p. 306.
- ↑ Riddick, John (1970). Organic Solvents Physical Properties and Methods of Purification. Techniques of Chemistry. Wiley-Interscience. ISBN 0471927260.
- ↑ Atmospheric Thermodynamics: Elementary Physics and Chemistry — Издательство Кембриджского университета, 2009. — С. 64. — ISBN 9780521899635
- ↑ PubChem (англ.)
- ↑ 1 2 Маленков Г. Г. Вода // Физическая энциклопедия. — М.: Советская энциклопедия, 1988. — Т. I. Ааронова — Бома эффект — Длинные линии. — С. 294—297. Архивировано 18 августа 2016 года.
- ↑ Петрушевский Ф. Ф., Гершун А. Л. Лед, в физике // Энциклопедический словарь — СПб.: Брокгауз — Ефрон, 1896. — Т. XVII. — С. 471—473.
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Henniker, J. C. The Depth of the Surface Zone of a Liquid (англ.) // Reviews of Modern Physics : journal. — Reviews of Modern Physics, 1949. — Vol. 21, no. 2. — P. 322—341. — doi:10.1103/RevModPhys.21.322.
- ↑ Pollack, Gerald. Water Science. University of Washington, Pollack Laboratory. — «Water has three phases – gas, liquid, and solid; but recent findings from our laboratory imply the presence of a surprisingly extensive fourth phase that occurs at interfaces.» Дата обращения: 5 февраля 2011. Архивировано 15 февраля 2013 года.
- ↑ Криволуцкий А. Е. Голубая планета. Земля среди планет. Географический аспект. — М.: Мысль, 1985. — С. 212.
- ↑ [[United Nations]]. Un.org (22 марта 2005). Дата обращения: 25 июля 2010. Архивировано 15 февраля 2013 года.
- ↑ Наука и техника. Книги. Загадки простой воды. Дата обращения: 27 августа 2008. Архивировано 22 января 2009 года.
- ↑ CIA- The world fact book. Central Intelligence Agency. Дата обращения: 20 декабря 2008. Архивировано из оригинала 5 января 2010 года.
- ↑ 1 2 Marine Science: An Illustrated Guide to Science
- ↑ Gleick, P.H. Water in Crisis: A Guide to the World's Freshwater Resources (англ.). — Oxford University Press, 1993. Архивировано 5 марта 2016 года.
- ↑ Water Vapor in the Climate System (англ.). American Geophysical Union. Дата обращения: 13 февраля 2013. Архивировано 15 февраля 2013 года.
- ↑ Состав и природа мантии Земли. Дата обращения: 6 апреля 2011. Архивировано 2 ноября 2011 года.
- ↑ Сурьма // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — С. 235. — ISBN 5-7155-0292-6.
- ↑ Вода // Словарь русского языка XI—XVII веков. Вып. 2 / Академия наук СССР, Институт русского языка; ред. колл., гл. ред. С. Г. Бархударов. — М.: Наука, 1975. — С. 249. — 16 500 экз. Архивировано 16 февраля 2023 года.
- ↑ Derksen, Rick. Etymological Dictionary of the Slavic Inherited Lexicon
- ↑ М. Фасмер. Этимологический словарь русского языка. Вода
- ↑ Online Etymology Dictionary. Water. Дата обращения: 9 ноября 2019. Архивировано 9 июля 2019 года.
- ↑ «Ностратическая этимология» (база данных). Дата обращения: 8 сентября 2020. Архивировано 18 января 2021 года.
- ↑ 1 2 Ларионов А. К. Занимательная гидрогеология. — Москва: Недра, 1979. — С. 5—12. — 157 с.
- ↑ 1 2 3 Петрянов И.В. Самое необыкновенное вещество // Химия и жизнь. — 1965. — № 3. — С. 2—14.
- ↑ Physics of Ice (15 страница)
- ↑ Молекулярные преобразователи энергии в живой клетке (Тихонов А. Н., 1997). Дата обращения: 24 ноября 2007. Архивировано 23 января 2009 года.
- ↑ Воскресенский П. И. Техника лабораторных работ. 9-е изд. — Л.: «Химия», 1970. — С. 696—697
- ↑ Невероятно: у воды есть два жидких состояния Архивная копия от 27 ноября 2020 на Wayback Machine // Вести.ру, 21 ноября 2020
- ↑ Thermalinfo ruАвтор11 11 2016 в 15:06. Удельная теплоемкость воды: таблицы при различных температуре и давлении. Thermalinfo.ru. Дата обращения: 30 мая 2022. Архивировано 23 ноября 2021 года.
- ↑ Теплоёмкость воды desmos. Desmos. Дата обращения: 30 мая 2022.
- ↑ График теплоёмкости онлайн. Desmos. Дата обращения: 3 июня 2022. Архивировано 6 июня 2022 года.
- ↑ аппроксимация диэлектрической проницаемости. Дата обращения: 16 ноября 2021. Архивировано 16 ноября 2021 года.
- ↑ look at page 1162. Дата обращения: 16 ноября 2021. Архивировано 16 ноября 2021 года.
- ↑ Оптика океана. Большая российская энциклопедия (7 июня 2023). Дата обращения: 14 апреля 2024.
- ↑ University of Maine System. Optical properties of water (англ.).
- ↑ Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 7. Атомы // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 15—18. — 240 с. — 1 630 000 экз.
- ↑ Радиационная химия // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990. — С. 200. — ISBN 5-7155-0292-6.
- ↑ Le Caër S. Water Radiolysis: Influence of Oxide Surfaces on H2 Production under Ionizing Radiation (англ.) // Water : journal. — 2011. — Vol. 3. — P. 236. Архивировано 23 марта 2014 года.
- ↑ rmg, 2015, с. 2.
- ↑ Перевод тут близок к первому: Земля людей (Перевод Горация Велле). VII. В сердце пустыни // Антуан де Сент-Экзюпери. Земля людей / Пер. с фр. под ред. Е. Зониной. — М.: Государственное издательство художественной литературы, 1957. — С. 181. — (Зарубежный роман XX века). — 165 000 экз.
- ↑ Вода на Луне: но откуда? Дата обращения: 8 сентября 2020. Архивировано 20 сентября 2020 года.
- ↑ Jane Platt, Brian Bell. NASA Space Assets Detect Ocean inside Saturn Moon. NASA (3 апреля 2014). Дата обращения: 3 апреля 2014. Архивировано 3 апреля 2014 года.
- ↑ Iess, L.; Stevenson, D.J.; Parisi, M.; Hemingway, D.; Jacobson, R.A.; Lunine, J.I.; Nimmo, F.; Armstrong, J.w.; Asmar, S.w.; Ducci, M.; Tortora, P. The Gravity Field and Interior Structure of Enceladus (англ.) // Science : journal. — 2014. — 4 April (vol. 344). — P. 78—80. — doi:10.1126/science.1250551. Архивировано 6 апреля 2014 года.
- ↑ Solanki, S. K.; Livingston, W.; Ayres, T. New Light on the Heart of Darkness of the Solar Chromosphere (англ.) // Science : journal. — 1994. — Vol. 263, no. 5143. — P. 64—66. — doi:10.1126/science.263.5143.64. — . — PMID 17748350.
- ↑ MESSENGER Scientists 'Astonished' to Find Water in Mercury's Thin Atmosphere. Planetary Society (3 июля 2008). Дата обращения: 5 июля 2008. Архивировано 17 января 2010 года.
- ↑ Bertaux, Jean-Loup; Vandaele, Ann-Carine; Korablev, Oleg; Villard, E.; Fedorova, A.; Fussen, D.; Quémerais, E.; Belyaev, D.; Mahieux, A. A warm layer in Venus' cryosphere and high-altitude measurements of HF, HCl, H2O and HDO (англ.) // Nature : journal. — 2007. — Vol. 450, no. 7170. — P. 646—649. — doi:10.1038/nature05974. — . — PMID 18046397.
- ↑ Sridharan, R.; S.M. Ahmed, Tirtha Pratim Dasa, P. Sreelathaa, P. Pradeepkumara, Neha Naika, and Gogulapati Supriya. 'Direct' evidence for water in the sunlit lunar ambience from CHACE on MIP of Chandrayaan I (англ.) // Planetary and Space Science : journal. — 2010. — Vol. 58, no. 6. — P. 947. — doi:10.1016/j.pss.2010.02.013. — .
- ↑ Donald Rapp. Use of Extraterrestrial Resources for Human Space Missions to Moon or Mars. — Springer, 28 November 2012. — P. 78–. — ISBN 978-3-642-32762-9. Архивировано 15 июля 2016 года.
- ↑ Atreya, Sushil K.; Wong, Ah-San. Coupled Clouds and Chemistry of the Giant Planets — A Case for Multiprobes (англ.) // Space Science Reviews : journal. — Springer, 2005. — Vol. 116. — P. 121—136. — ISSN 0032-0633. — doi:10.1007/s11214-005-1951-5. — . Архивировано 22 июля 2011 года.
- ↑ Jia-Rui C. Cook, Rob Gutro, Dwayne Brown, J. D. Harrington, Joe Fohn. Hubble Sees Evidence of Water Vapor at Jupiter Moon. NASA (12 декабря 2013). Дата обращения: 12 декабря 2013. Архивировано из оригинала 15 декабря 2013 года.
- ↑ Encrenaz, 2003, p. 92.
- ↑ Hubbard, W. B. Neptune's Deep Chemistry (англ.) // Science. — 1997. — Vol. 275, no. 5304. — P. 1279—1280. — doi:10.1126/science.275.5304.1279. — PMID 9064785.
- ↑ Земля (планета) — статья из Большой советской энциклопедии.
- ↑ Water Found on Distant Planet Архивная копия от 24 августа 2013 на Wayback Machine 12 July 2007 By Laura Blue, Time
- ↑ Water Found in Extrasolar Planet’s Atmosphere. Дата обращения: 12 апреля 2014. Архивировано 8 марта 2014 года.
- ↑ Атмосфера экзопланеты GJ 1214b переполнена водой. Компьюлента (24 февраля 2012). — «Новые наблюдения транзитов GJ 1214 b, удалённой от Земли на 40 световых лет, показали, что вода должна составлять не менее половины от всей массы атмосферы этой «суперземли»». Дата обращения: 21 июля 2013. Архивировано 29 августа 2013 года.
- ↑ Watson, P. E. et al. (1980) Total body water volumes for adult males and females estimated from simple anthropometric measurements, The American Journal for Clinical Nutrition, Vol. 33, № 1, pp. 27—39.
- ↑ Моргунова Г. С. Вода, которую мы пьём // Химия и жизнь. — 1965. — № 3. — С. 15—17.
- ↑ Sharma B. K. Water Pollution. — 1994. — P. 408—409. Архивировано 10 июля 2014 года.
- ↑ Воскресенский В. А., Дьяков В. И. Глава 2. Смазочные вещества и их физико-химические свойства // Расчет и проектирование опор скольжения (жидкостная смазка): Справочник. — М.: Машиностроение, 1980. — С. 15. — (Библиотека конструктора). — ISBN ББК 34.42, УДК 621.81.001.2 (031).
- ↑ Ученые: вода появилась в мантии Земли 2,7 млрд лет назад. ТАСС. Дата обращения: 26 апреля 2016. Архивировано 4 мая 2016 года.
Литература[править | править код]
- на русском языке
- Андреев В. Г. Влияние протонного обменного взаимодействия на строение молекулы воды и прочность водородной связи // Материалы V Международной конференции «Актуальные проблемы науки в России». — 2008. — Т. 3. — С. 58—62.
- Арабаджи В. И. Загадки простой воды: в мире воды и льда. — М.: Знание, 1973. — 96 с.
- Гидробионты в самоочищении вод и биогенной миграции элементов. — М.: МАКС-Пресс. 2008. — 200 с. — ISBN 978-5-317-02625-7.
- Кульский Л. А., Даль В. В., Ленчина Л. Г. Вода знакомая и загадочная. — Киев: Радянська школа, 1982. — 120 с.
- Лосев К. С. Вода / Рец. А. А. Соколов. — Л.: Гидрометеоиздат, 1989. — 272 с. — 113 000 экз. — ISBN 5-286-00161-0.
- Мельник А. Г. Вода в христианских сакральных практиках Древней Руси конца X-XVII веков // Святая вода в иеротопии и иконографии христианского мира / ред.-сост. А.М. Лидов. — М.: ООО "Феория", 2017. — С. 496—520. — ISBN 978-5-91796-061-6.
- О некоторых вопросах поддержания качества воды и её самоочищения // Водные ресурсы. — 2005. — Т. 32. — № 3. — С. 337—347.
- Рекомендации по межгосударственной стандартизации РМГ 75-2014. Государственная система обеспечения единства измерений. Измерения влажности веществ. Термины и определения. — М.: Стандартинформ, 2015. — iv + 16 с.
- Черняев А.М. Самый удивительный минерал. Что мы знаем о воде. — Свердловск: Средне-Уральское книжное издательство, 1980. — 192 с.
- Яковлев В. А. Вода // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- на других языках
- Ball, Philip. Life's matrix : a biography of water. — Farrar, Straus, and Giroux, 2001. — ISBN 978-0-520-23008-8.
- Franks, Felix. Water : a matrix of life. — 2nd. — Royal Society of Chemistry, 2007. — ISBN 978-1-84755-234-1.
- Lide, David R. CRC Handbook of Chemistry and Physics : [англ.]. — 84th. — CRC Press, 2003. — ISBN 978-0-8493-0484-2.
- Weingärtner, Hermann. Water, 1. Properties, Analysis, and Hydrological Cycle // Ullmann's Encyclopedia of Industrial Chemistry / Hermann Weingärtner, Ilka Teermann, Ulrich Borchers … [и др.]. — Wiley-VCH Verlag GmbH & Co. KGaA, 2016. — ISBN 978-3-527-30673-2. — doi:10.1002/14356007.a28_001.pub3.
- Encrenaz, Thérèse. ISO observations of the giant planets and Titan: what have we learnt? (англ.) // Planetary and Space Science : journal. — 2003. — February (vol. 51, no. 2). — P. 89—103. — doi:10.1016/S0032-0633(02)00145-9. — .















































