S-фаза

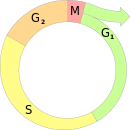
S-фа́за — фаза клеточного цикла, в которой происходит репликация ДНК. Стадия интерфазы, расположенная между G1- и G2-фазами. Длительность в большинстве клеток составляет 8—12 часов[1]. В ходе дробления бластомеры многих организмов делятся раз в 20—30 минут, причём сильно сокращаются G1 и G2-периоды: S-фаза почти равна по длительности интерфазе.
Безошибочность репликации ДНК необходима для предотвращения генетических аномалий, часто приводящих к болезни или смерти клетки. Из-за этой важности регуляторные пути, управляющие этими процессами, у эукариот крайне консервативны. Эта консервативность делает изучение S-фазы на модельных организмах, например, гладкой шпорцевой лягушке (Xenopus laevis) и почкующихся дрожжах, актуальным для высших организмов.
Регуляция S-фазы[править | править код]
Главной контрольной точкой в регуляции клеточного цикла является переход от G1-фазы к S-фазе. В зависимости от количества питательных веществ и энергии, а также от внешних факторов клетка принимает решение — вступать в клеточный цикл или же перейти в неделящееся состояние, известное как G0-фаза. Этот переход, как и все контрольные переходные точки в клеточном цикле, запускается циклинами и циклин-зависимыми киназами. Активация G1/S-циклинов запускает CLN3-циклин-зависимую киназу, активирующую Cln1/2 и Clb5/6 в ходе инициации S-фазы. Этот путь включает 2 положительных обратносвязанных цикла, допускающих быстрый, однонаправленный переход в S-фазу. Такие на первый взгляд сложные и избыточные пути, тем не менее, не являются редкими, так как позволяют более тонко регулировать выходные сигналы системы и часто приводят к ускорению эволюции[2].
Репликация ДНК[править | править код]
Главным событием S-фазы является репликация ДНК. Целью этого процесса является создание двух абсолютно идентичных хроматид. Клетка препятствует более чем одной репликации хромосомы, накладывая на ДНК в фазе G1 специальные пререпликационные комплексы, которые разбираются в S-фазе перед началом репликации. В почкующихся дрожжах белок Cdc6 разрушается, Orc2/6 фосфорилируется, и mcm-белки изгоняются из ядра, предотвращая новое прикрепление репликационного аппарата (ДНК-полимеразы) к ДНК после начала репликации. Удивительно, но синтез ДНК может идти со скоростью 2000 нуклеотидов в секунду[3] и достигает точности 2 неправильных основания на 1010 нуклеотидов.
Повреждения ДНК[править | править код]
Повреждения ДНК в норме распознаются в S-фазе. Когда репликационная вилка натыкается на повреждённую ДНК, активируется протеинкиназа ATR. Киназа запускает несколько сложных механизмов, приостанавливающих активацию новых точек репликации, предотвращая митоз, и вызывает остановку репликационной вилки, чтобы цепи ДНК оставались разделенными (сохранялся открытый "репликационный глазок"), ДНК-полимераза не отделялась от ДНК, а поврежденные участки не удвваивались до их репарации[4].
Удвоение центриолей[править | править код]
В течение S-фазы происходит удвоение не только ДНК, но и каждой из центриолей клеточного центра. Центриоль, бывшая в клетке материнской, строит новую дочернюю, а бывшая дочерняя центриоль сама становится материнской и строит свою пару. При этом в сборке микротрубочек задействована только исходная материнская центриоль[1].
Некоторые учёные считают, что удвоение центриолей происходит в постсинтетический(премитотический) период (G2)
Другие события S-фазы[править | править код]
В течение S-фазы наиболее интенсивно синтезируются РНК и белки, связанные с ДНК (в том числе гистоны) — они необходимы для включения в состав новой хроматиды. Синтез таких белков, направляемых в ядро, осуществляют свободные рибосомы, не связанные с эндоплазматической сетью.
Примечания[править | править код]
- ↑ 1 2 Г.Л. Билич, В.А. Крыжановский. Биология. Полный курс: в 4 т.. — Москва: Оникс, 2009. — Т. 1. — С. 120—121. — ISBN 978-5-488-02311-6.
- ↑ Bell, S.P. and Dutta, A.: DNA replication in eukaryotic cells. Annu.Rev.Biochem. 2002,71:333-374.
- ↑ Cooper, S. and Helmstetter, C. E. 1968 DNA synthesis during the division cycle of rapidly growing Escherichia coli. Journal of Molecular Biology, 31(3):507–518.
- ↑ Branzei, D and Foiani, M.: The DNA damage response during DNA replication. Curr. Opin. Cell Biol. 2005, 17:568-575.