Трифосген
| Трифосген | |
|---|---|
 | |
| Общие | |
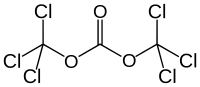
| Хим. формула | C3Cl6O3 |
| Термические свойства | |
| Температура | |
| • плавления | 84 °C[1] |
| Классификация | |
| Рег. номер CAS | 32315-10-9 |
| PubChem | 94429 |
| Рег. номер EINECS | 250-986-3 |
| SMILES | |
| InChI | |
| ChemSpider | 85216 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Трифосген (С3Cl 6O3), также гексахлордиметилкарбонат[2] — химическое соединение, используется как более безопасный заменитель фосгена, потому что при комнатной температуре оно является твердым веществом, тогда как фосген — газом[3]. Трифосген разлагается при температуре выше 200 ° C[4].
Получение[править | править код]
Это соединение является коммерчески доступным. Его получают путём исчерпывающего свободнорадикального хлорирования диметилкарбоната[4]:
- CH3OCO2CH3 + 6 Cl2 → CCl3OCO2CCl3 + 6 HCl
Опасность[править | править код]
Токсичность трифосгена и фосгена одинакова (фосген выделяется из трифосгена, например, при взаимодействии с влагой). Поэтому при работе с этим реактивом имеет смысл принимать те же меры предосторожности, что и с фосгеном[5]. Вещество является канцерогенным для животных.[6]
Применение[править | править код]
Проверить информацию. |
Трифосген используется в качестве реагента в органическом синтезе[3][7][8][9].
См. также[править | править код]
Примечания[править | править код]
- ↑ Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // (unknown type) — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ Трифосген - Справочник химика 21. chem21.info. Дата обращения: 25 сентября 2020. Архивировано 8 октября 2018 года.
- ↑ 1 2 Dr. Heiner Eckert; Dr. Barbara Forster (1987). "Triphosgene, a Crystalline Phosgene Substitute". Angew. Chem. Int. Ed. Engl. 26 (9): 894—895. doi:10.1002/anie.198708941.
- ↑ 1 2 Dr. Heiner Eckert (2011). "Phosgenation Reactions with Phosgene from Triphosgene". Chim. Oggi Chem. Today. 29 (6): 40—46.
- ↑ Suresh B. Damle (1993-02-08). "Safe handling of diphosgene, triphosgene". Chemical & Engineering News. 71 (6): 4. Архивировано 1 апреля 2019. Дата обращения: 16 августа 2020.
- ↑ Федеральный регистр потенциально опасных химических и биологических веществ | РПОХБВ. Дата обращения: 7 ноября 2020. Архивировано 13 ноября 2020 года.
- ↑ Akiba, T.; Tamura, O.; Terashima, S. (1998). "(4R,5S)-4,5-Diphenyl-3-Vinyl-2-Oxazolidinone". Organic Syntheses. 75: 45. doi:10.15227/orgsyn.075.0045.
- ↑ Tsai, James H.; Takaoka, Leo R.; Powell, Noel A.; Nowick, James S. (2002). "Synthesis of Amino Acid Ester Isocyanates: Methyl (S)-2-Isocyanato-3-Phenylpropanoate". Organic Syntheses. 78: 220. doi:10.15227/orgsyn.078.0220.
- ↑ Du, Haifeng; Zhao, Baoguo; Shi, Yian (2009). "Pd(0)-Catalyzed Diamination of Trans-1-Phenyl-1,3-Butadiene with Di-tert-Butyldiaziridinone as Nitrogen Source". Organic Syntheses. 86: 315. doi:10.15227/orgsyn.086.0315.
Для улучшения этой статьи желательно:
|