Гибридизация орбиталей: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Illustr (обсуждение | вклад) Нет описания правки |
Illustr (обсуждение | вклад) Нет описания правки |
||
| Строка 9: | Строка 9: | ||
Представления о гибридизации занимают центральное место в [[теория валентных связей|методе валентных связей]]. Сама гибридизация не является реальным физическим процессом, а только удобной моделью, позволяющей объяснить электронное строение молекул, в частности гипотетические видоизменения атомных орбиталей при образовании [[Ковалентная связь|ковалентной химической связи]], в частности, выравнивание [[длина химической связи|длин химических связей]] и валентных углов в молекуле. |
Представления о гибридизации занимают центральное место в [[теория валентных связей|методе валентных связей]]. Сама гибридизация не является реальным физическим процессом, а только удобной моделью, позволяющей объяснить электронное строение молекул, в частности гипотетические видоизменения атомных орбиталей при образовании [[Ковалентная связь|ковалентной химической связи]], в частности, выравнивание [[длина химической связи|длин химических связей]] и валентных углов в молекуле. |
||
Концепция гибридизации с успехом была применена для качественного описания простых молекул, но позднее была расширена и для более сложных. В отличие от [[Теория молекулярных орбиталей|теории молекулярных орбиталей]] не является строго количественной, например она не в состоянии предсказать фотоэлектронные спектры даже таких простых молекул как вода. В настоящее время используется в основном в [[Методика|методических целях]] и в синтетической [[Органическая химия|органической химии]]. |
Концепция гибридизации с успехом была применена для качественного описания простых молекул, но позднее была расширена и для более сложных. В отличие от [[Теория молекулярных орбиталей|теории молекулярных орбиталей]] не является строго количественной, например она не в состоянии предсказать фотоэлектронные спектры даже таких простых молекул как [[вода]]. В настоящее время используется в основном в [[Методика|методических целях]] и в синтетической [[Органическая химия|органической химии]]. |
||
В [[1954 год]]у Нобелевский комитет удостоил [[[Полинг, Лайнус|Л.Полинг]]а премии по химии «За изучение природы химической связи и его применение к объяснению строения сложных молекул». Но сам Л.Полинг не был удовлетворён введением σ,π — описания для двойной и [[тройная связь|тройной связи]] и сопряжённых систем. |
В [[1954 год]]у Нобелевский комитет удостоил [[[Полинг, Лайнус|Л.Полинг]]а премии по химии «За изучение природы химической связи и его применение к объяснению строения сложных молекул». Но сам Л.Полинг не был удовлетворён введением σ,π — описания для двойной и [[тройная связь|тройной связи]] и сопряжённых систем. |
||
| Строка 85: | Строка 85: | ||
</center> |
</center> |
||
== |
== См. также == |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
== Литература == |
== Литература == |
||
| Строка 114: | Строка 124: | ||
* {{книга|автор=Гиллеспи Р.|заглавие=Геометрия молекул|ответственный=Пер. с англ. Е. З. Засорина и В. С. Мастрюкова, под ред. Ю. А. Пентина|место=М.|издательство=Мир|год=1975|страниц=278}} |
* {{книга|автор=Гиллеспи Р.|заглавие=Геометрия молекул|ответственный=Пер. с англ. Е. З. Засорина и В. С. Мастрюкова, под ред. Ю. А. Пентина|место=М.|издательство=Мир|год=1975|страниц=278}} |
||
== |
== Ссылки == |
||
{{commonscat-inline|Hybridized atomic orbitals}} |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
[[Категория:Химическая связь]] |
[[Категория:Химическая связь]] |
||
Версия от 20:01, 11 мая 2014
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d, f) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам.
Концепция гибридизации

Концепция гибридизации валентных атомных орбиталей была предложена американским химиком Лайнусом Полингом для ответа на вопрос, почему при наличии у центрального атома разных (s, p, d) валентных орбиталей, образованные им связи в многоатомных молекулах с одинаковыми лигандами оказываются эквивалентными по своим энергетическим и пространственным характеристикам.
Представления о гибридизации занимают центральное место в методе валентных связей. Сама гибридизация не является реальным физическим процессом, а только удобной моделью, позволяющей объяснить электронное строение молекул, в частности гипотетические видоизменения атомных орбиталей при образовании ковалентной химической связи, в частности, выравнивание длин химических связей и валентных углов в молекуле.
Концепция гибридизации с успехом была применена для качественного описания простых молекул, но позднее была расширена и для более сложных. В отличие от теории молекулярных орбиталей не является строго количественной, например она не в состоянии предсказать фотоэлектронные спектры даже таких простых молекул как вода. В настоящее время используется в основном в методических целях и в синтетической органической химии.
В 1954 году Нобелевский комитет удостоил [[[Полинг, Лайнус|Л.Полинг]]а премии по химии «За изучение природы химической связи и его применение к объяснению строения сложных молекул». Но сам Л.Полинг не был удовлетворён введением σ,π — описания для двойной и тройной связи и сопряжённых систем.
В 1958 году на симпозиуме, посвящённом памяти Кекуле, Л.Полинг развил теорию изогнутой химической связи, учитывающую кулоновскую электронную корреляцию. По этой теории двойная связь описывалась как комбинация двух изогнутых химических связей, а тройная связь как комбинация трёх изогнутых химических связей.[1]
Этот принцип нашёл отражение в теории отталкивания электронных пар Гиллеспи — Найхолма, первое и наиболее важное правило которой формулировалось следующим образом:
- «Электронные пары принимают такое расположение на валентной оболочке атома, при котором они максимально удалены друг от друга, т.е электронные пары ведут себя так, как если бы они взаимно отталкивались»[2].
Второе правило состояло в том, что «все электронные пары, входящие в валентную электронную оболочку, считаются расположенными на одинаковом расстоянии от ядра».[2]
Виды гибридизации
sp-гибридизация

Происходит при смешивании одной s- и одной p-орбиталей. Образуются две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра центрального атома. Две оставшиеся негибридные p-орбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются неподелёнными парами электронов.
sp2-гибридизация

Происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей
sp3-гибридизация
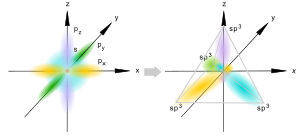
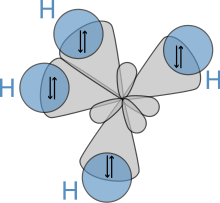
Происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp3-гибридные орбитали. Могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.
Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра, тогда как ядро центрального атома расположено в центре описанной сферы этого тетраэдра. Тетраэдрический угол между ними приближённо равен 109°28'[3], что соответствует наименьшей энергии отталкивания электронов. Также sp3-орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.Такое состояние характерно для атомов углерода в насыщенных углеводородах и соответственно в алкильных радикалах и их производных.
Гибридизация и геометрия молекул
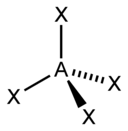
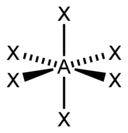
Представления о гибридизации атомных орбиталей лежат в основе теории отталкивания электронных пар Гиллеспи-Найхолма. Каждому типу гибридизации соответствует строго определённая пространственная ориентация гибридных орбиталей центрального атома, что позволяет её использовать как основу стереохимических представлений в неорганической химии.
В таблице приведены примеры соответствия наиболее распространённых типов гибридизации и геометрической структуры молекул в предположении, что все гибридные орбитали участвуют в образовании химических связей (отсутствуют неподелённые электронные пары)[4].
См. также
- Атомные орбитали
- Ковалентная связь
- Теория отталкивания электронных пар
- Теория молекулярных орбиталей
- Теория валентных связей
- Теория резонанса
- Теория изогнутой химической связи
- Кулоновская электронная корреляция
Примечания
- ↑ Под редакцией Р. Х. Фрейдлиной. Теоретическая органическая химия. — пер. с англ. канд. хим. наук Ю.Г.Бунделем. — М.: Издательство иностранной литературы, 1963. — Т. 1. — С. 11. — 365 с.
- ↑ 1 2 Гиллеспи Р. Геометрия молекул / Пер. с англ. Е. З. Засорина и В. С. Мастрюкова, под ред. Ю. А. Пентина. — М.: Мир, 1975. — С. 18-19. — 278 с.
- ↑ Теоретически этот угол в правильном тетраэдре равен arccos(-1/3)≈109°28'.
- ↑ Здесь A — центральный атом, X — гибридные связывающие орбитали
Литература
- Полинг Л. Природа химической связи / Пер. с англ. М. Е. Дяткиной. Под ред. проф. Я. К. Сыркина. — М.; Л.: Госхимиздат, 1947. — 440 с.
- Полинг Л. Общая химия. Пер. с англ. — М.: Мир, 1974. — 846 с.
- Минкин В. И., Симкин Б. Я., Миняев Р. М. Теория строения молекул. — Ростов-на-Дону: Феникс, 1997. — С. 397-406. — ISBN 5-222-00106-7.
- Гиллеспи Р. Геометрия молекул / Пер. с англ. Е. З. Засорина и В. С. Мастрюкова, под ред. Ю. А. Пентина. — М.: Мир, 1975. — 278 с.
Ссылки
 На Викискладе есть медиафайлы по теме Гибридизация орбиталей
На Викискладе есть медиафайлы по теме Гибридизация орбиталей- Анимированные изображения гибридизации