Ангидриды карбоновых кислот: различия между версиями
| [непроверенная версия] | [отпатрулированная версия] |
Amachis (обсуждение | вклад) Исправлено правописание Метка: через мобильное приложение |
Исправлена опечатка Метки: с мобильного устройства через мобильное приложение |
||
| Строка 1: | Строка 1: | ||
[[Файл:FunktionelleGruppen_Carbonsäureanhydrid.svg|thumb|Общая структурная формула ангидридов карбоновых кислот]] |
[[Файл:FunktionelleGruppen_Carbonsäureanhydrid.svg|thumb|Общая структурная формула ангидридов карбоновых кислот]] |
||
'''Ангидриды карбоновых кислот''' - соединения |
'''Ангидриды карбоновых кислот''' - соединения общей формулы R<sup>1</sup>CO-O-COR<sup>2</sup>, в которых две ацильных группы присоединены к одному и тому же атому кислорода<ref>[http://goldbook.iupac.org/A00072.html acid anhydrides // IUPAC Gold Book]</ref>. В зависимости от природы ацильных групп ангидриды могут быть «простыми» (R<sup>1</sup> = R<sup>2</sup>, например, уксусный ангидрид (CH<sub>3</sub>CO)<sub>2</sub>O, смешанными (различные ацильные остатки) или циклическими (R<sup>1</sup> и R<sup>2</sup> являются частями одной молекулы)<ref>[http://goldbook.iupac.org/C01492.html cyclic acid anhydrides (cyclic anhydrides) // IUPAC Gold Book]</ref>. |
||
Муравьиный ангидрид с формулой H-CO-O-CO-H (C<sub>2</sub>H<sub>2</sub>O<sub>3</sub>) в свободном виде не существует. |
Муравьиный ангидрид с формулой H-CO-O-CO-H (C<sub>2</sub>H<sub>2</sub>O<sub>3</sub>) в свободном виде не существует. |
||
Версия от 10:55, 21 апреля 2016
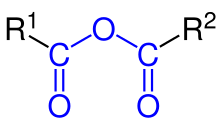
Ангидриды карбоновых кислот - соединения общей формулы R1CO-O-COR2, в которых две ацильных группы присоединены к одному и тому же атому кислорода[1]. В зависимости от природы ацильных групп ангидриды могут быть «простыми» (R1 = R2, например, уксусный ангидрид (CH3CO)2O, смешанными (различные ацильные остатки) или циклическими (R1 и R2 являются частями одной молекулы)[2].
Муравьиный ангидрид с формулой H-CO-O-CO-H (C2H2O3) в свободном виде не существует.
Ангидриды формально можно рассматривать как продукт конденсации двух групп -COOH:
- R1-COOH + HOOC-R2 = R1-(CO)O(OC)-R2 + H2O [1]
Синтез
Некоторые циклические ангидриды, например, Фталевый ангидрид, образуются при нагревании соответствующих кислот. В случае синтеза ангидридов из алифатических кислот используют дегидратирующие агенты - в частности, фосфорный ангидрид при синтезе уксусного ангидрида из уксусной кислоты:
- 2 CH3COOH + P4O10 → (CH3CO)2O + P4O9(OH)2
либо карбодиимиды, которые реагируют с карбоновыми кислотами с образованием О-ацилизомочевин - высокореакционноспособных соединений, способных ацилировать карбоновые кислоты:
- R-N=C=N-R + R1COOH RNHC(=NR)OCOR1
- RNHC(=NR)OCOR1 + R1COOH (R1CO)2O + RNHCONHR
В большинстве случаев, ангидриды синтезируют ацилированием карбоновых кислот либо их солей. Так, например, ацилированием формиата натрия формилфторидом может быть получен неустойчивій ангидрид муравьиной кислоты[3]:
- HCOONa + HCOF (HCO)2O + NaF
При ацилировании карбоновых кислот в лабораторной практике в качестве ацилирующих агентов обычно используют комплексы галогенангидридов карбоновых кислот с пиридином[4] либо кетены, формально являющиеся внутренними ангидридами карбоновых кислот:
- RCOOH + R1CH=C=O RCOOC(O)R1 ;
Ацилирование уксусной кислоты кетеном является промышленным методом синтеза уксусного ангидрида.
Реакционная способность
Ангидриды являются ацилирующими агентами и реагируют с различными нуклеофилами:
- (RCO)2O + HNu RCONu + RCOOH
образуя сложные эфиры (Nu = OR), амиды (Nu = NR1R2), гидразиды (Nu = HNNR1R2) и т.п.
См. также
Примечания
- ↑ acid anhydrides // IUPAC Gold Book
- ↑ cyclic acid anhydrides (cyclic anhydrides) // IUPAC Gold Book
- ↑ George A. Olah, Yashwant D. Vankar; Massoud Arvanaghi; Jean Sommer (1979), Formic Anhydride. Angewandte Chemie Int. Ed. Engl., volume 18, issue = 8, page = 614. doi:10.1002/anie.197906141
- ↑ "ACID ANHYDRIDES". Organic Syntheses. 26: 1. 1946. doi:10.15227/orgsyn.026.0001. ISSN 23333553 00786209, 23333553. Дата обращения: 28 января 2016.
{{cite journal}}: Проверьте значение|issn=(справка)
Это заготовка статьи по органической химии. Помогите Википедии, дополнив её. |
