Хлорметилирование по Блану
Хлорметилирование по Блану (также называемое реакцией Блана) — это химическая реакция введения хлорметильной группы в ароматические соединения под действием формальдегида и хлороводорода в присутствии хлорида цинка или другой кислоты Льюиса в качестве катализатора[1]. Реакция открыта Гюставом Луи Бланом (1872—1927) в 1923 году[2][3][4]. Реакцию необходимо проводить с большой осторожностью, потому что, как и в большинстве реакций хлорметилирования, побочным продуктом является высоко канцерогенный дихлордиметиловый эфир.
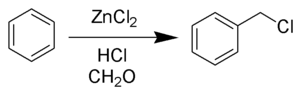
Механизм реакции
[править | править код]Реакция проводится в кислой среде с катализатором ZnCl2. В этих условиях протонируется карбонильная группа формальдегида, что повышает электрофильные свойства углерода. Образующийся катион атакуется ароматическими π-электронами с последующей реароматизацией ароматического кольца. Образующийся бензиловый спирт в данных условиях быстро превращается в хлорид.
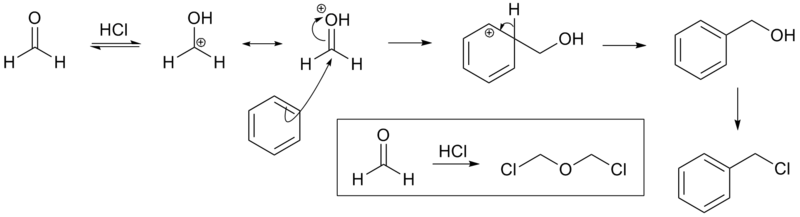
Сильно активированные арены такие, как фенолы и анилины, не являются подходящими реагентами, так как они подвержены дальнейшей атаке по реакции алкилирования по Фриделю — Крафтсу. Но образование диарилметана в качестве побочного продукта является обычным во всех случаях[источник не указан 279 дней].
Хотя эта реакция является эффективным средством введения хлорметильной группы, получение небольших количеств высоко канцерогенного дихлордиметилового эфира не позволяет использовать этот способ для промышленного производства[источник не указан 279 дней].
Соответствующие реакции фторметилирования, бромметилирования и иодметилирования также могут быть проведены с использованием соответствующей галогеноводородной кислоты[5].
Похожие реакции хлорметилирования
[править | править код]Хлорметилирование тиолов можно провести с использованием концентрированной HCl и формальдегида:[6]
- ArSH + CH2O + HCl → ArSCH2Cl + H2O
Хлорметилирование так же можно провести с использованием метилхлорметилового эфира:
- ArH + CH3OCH2Cl → ArCH2Cl + CH3OH
Эта реакция используется при хлорметилировании стирола в производстве ионообменных смол и смолы Меррифилда.
См. также
[править | править код]Примечания
[править | править код]- ↑ Максимова Л. Н. Хлорметилирование // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — С. [287—288] (стб. 566–567). — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.
- ↑ Bull. Soc. Chim. France 1923, 33, 313
- ↑ Whitmore, F. C.; Ginsburg, Abram; Rueggeberg, Walter; Tharp, I.; Nottorf, H.; Cannon, M.; Carnahan, F.; Cryder, D.; FLeming, G.; Goldberg, G.; Haggard, H.; Herr, C.; Hoover, T.; Lovell, H.; Mraz, R.; Noll, C.; Oakwood, T.; Patterson, H.; Van Strien, R.; Walter, R.; Zook, H.; Wagner, R.; Weisgerber, C.; Wilkins, J. Production of Benzyl Chloride by Chloromethylation of Benzene. Laboratory and Pilot Plant Studies (англ.) // Industrial & Engineering Chemistry[англ.] : journal. — 1946. — May (vol. 38, no. 5). — P. 478—485. — doi:10.1021/ie50437a013.
- ↑ Belen'kii, Leonid I; Vol'kenshtein, Yu B; Karmanova, I B. New Data on the Chloromethylation of Aromatic and Heteroaromatic Compounds (англ.) // Успехи химии : journal. — Российская академия наук, 1977. — 30 September (vol. 46, no. 9). — P. 891—903. — doi:10.1070/RC1977v046n09ABEH002180. — .
- ↑ C., Norman, Richard O. Principles of Organic Synthesis, 3rd Edition (англ.). — 3rd. — Boca Raton: Routledge, 2017. — ISBN 9781351421737.
- ↑ D. Enders, S. Von Berg, B. Jandeleit. Diethyl [(Phenylsulfonyl)methyl]phosphonate (англ.) // Org. Synth.[англ.] : journal. — 2002. — Vol. 78. — P. 169. — doi:10.15227/orgsyn.078.0169.
На эту статью не ссылаются другие статьи Википедии. |