Глутаматдекарбоксилаза: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
+Синдром мышечной скованности |
иллюстрация |
||
| Строка 37: | Строка 37: | ||
| LocusSupplementaryData = |
| LocusSupplementaryData = |
||
}} |
}} |
||
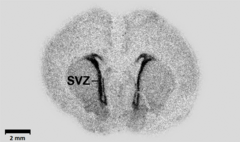
[[Файл:PMID19190758 PLoS 0004371.png|thumb|240px|Эмбрион крысы, срез мозга. Высокая концентрация маркера, связывающего GAD67, наблюдается в районе [[Субвентрикулярная зона|субвентрикулярной зоны]] (SVZ). Изображение из статьи Popp et al., 2009.<ref name="pmid19190758">{{cite journal |author=Popp A, Urbach A, Witte OW, Frahm C |title=Adult and embryonic GAD transcripts are spatiotemporally regulated during postnatal development in the rat brain |journal=[[PLoS ONE]] |volume=4 |issue=2 |pages=e4371 |year=2009 |pmid=19190758 |pmc=2629816 |doi=10.1371/journal.pone.0004371 |url=http://dx.plos.org/10.1371/journal.pone.0004371}}</ref>]] |
|||
'''Глутаматдекарбоксилаза''' ({{lang-en|Glutamate decarboxylase, GAD, GAD65, GAD67}}) — [[фермент]], катализирующий преобразование [[глутамат]]а в [[ГАМК]] посредством декарбоксилирования. [[Кофактор]]ом GAD является [[пиридоксальфосфат]]. |
'''Глутаматдекарбоксилаза''' ({{lang-en|Glutamate decarboxylase, GAD, GAD65, GAD67}}) — [[фермент]], катализирующий преобразование [[глутамат]]а в [[ГАМК]] посредством декарбоксилирования. [[Кофактор]]ом GAD является [[пиридоксальфосфат]]. |
||
Версия от 17:06, 6 августа 2009
| Глутаматдекарбоксилаза 1 | |
|---|---|
 | |
| Обозначения | |
| Символы | GAD1 |
| Entrez Gene | 2571 |
| HGNC | 4092 |
| OMIM | 605363 |
| UniProt | Q99259 |
| Другие данные | |
| Шифр КФ | 4.1.1.15 |
| Локус | 2-я хр. , 2q31 |
| Глутаматдекарбоксилаза 2 | |
|---|---|
 | |
| Обозначения | |
| Символы | GAD2 |
| Entrez Gene | 2572 |
| HGNC | 11284 |
| OMIM | 4093 |
| PDB | 1ES0 |
| UniProt | Q05329 |
| Другие данные | |
| Шифр КФ | 4.1.1.15 |
| Локус | 10-я хр. , 10p11.23 |
Глутаматдекарбоксилаза (англ. Glutamate decarboxylase, GAD, GAD65, GAD67) — фермент, катализирующий преобразование глутамата в ГАМК посредством декарбоксилирования. Кофактором GAD является пиридоксальфосфат.
В организме млекопитающих GAD существует в виде двух изоформ — GAD67 и GAD65, кодируемых двумя генами — Gad1 и Gad2. Коды 67 и 65 указывают на молекулярный вес изоформ — 67 кДа и 65 кДа. Оба гена экспрессированы в мозге, использующем ГАМК в качестве нейротрансмиттера, Gad2 также экпрессирован в поджелудочной железе.
Роль в патологии
Появление аутоантител к GAD65 и GAD67 иногда предшествует развитию инсулинзависимого сахарного диабета.[2] FT, FT.
Значительное снижение экспрессии GAD67 отмечается в ГАМК-эргических интернейронах мозга при шизофрении и психотической форме биполярного расстройства.[3][4] Предположительной причиной снижения является избыток ДНК метилтрансферазы-1. [5] Уровень DMNT1 варьирует в разных слоях ГАМК-эргических нейронов и наряду с GAD67 может снижать экспрессию белка рилин. [6] При этом стоит отметить, что данные результаты получены при анализе образцов мозга пациентов, длительное время получавших антипсихотическую терапию, способную вносить изменения в работу мозга.
Также антитела к GAD часто обнаруживаются у пациентов с редким синдромом мышечной скованности.
Ссылки
- Genetics, Expression Profiling Support GABA Deficits in Schizophrenia - Schizophrenia Research Forum. Обзор трех публикаций, связанных с GAD. Перевод: Свидетельства ГАМК-дефицита при шизофрении
- Epigenetic Jamming of GAD1 Promoter May Contribute to Schizophrenia - Schizophrenia Research Forum, обзор публикации. Перевод: Эпигенетическое подавление экспрессии GAD1 при шизофрении
Примечания
- ↑ Popp A, Urbach A, Witte OW, Frahm C (2009). "Adult and embryonic GAD transcripts are spatiotemporally regulated during postnatal development in the rat brain". PLoS ONE. 4 (2): e4371. doi:10.1371/journal.pone.0004371. PMC 2629816. PMID 19190758.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Baekkeskov S, Aanstoot HJ, Christgau S, Reetz A, Solimena M, Cascalho M, Folli F, Richter-Olesen H, De Camilli P. (1990) Identification of the 64K autoantigen in insulin-dependent diabetes as the GABA-synthesizing enzyme glutamic acid decarboxylase. Nature. 347(6289):151-6. PMID 1697648
- ↑ Woo TU, Walsh JP, Benes FM. (2004) Arch Gen Psychiatry. 61(7):649-57. Density of glutamic acid decarboxylase 67 messenger RNA-containing neurons that express the N-methyl-D-aspartate receptor subunit NR2A in the anterior cingulate cortex in schizophrenia and.PMID 15237077
- ↑ Guidotti, A., Auta, J., Davis, J. M., DiGiorgi-Gerenini, V., Dwivedi, J., Grayson, D. R., Impagnatiello, F., Pandey, G. N., Pesold, C., Sharma, R. F., et al. (2000) Decrease in reelin and glutamic acid decarboxylase67 (GAD67) expression in schizophrenia and bipolar disorder: a postmortem brain study.Arch. Gen. Psychiatry 57, 1061—1069. PMID 11074872
- ↑ Ruzicka WB, Zhubi A, Veldic M, Grayson DR, Costa E, Guidotti A. (2007) Selective epigenetic alteration of layer I GABAergic neurons isolated from prefrontal cortex of schizophrenia patients using laser-assisted microdissection. Mol Psychiatry. PMID 17264840 doi:10.1038/sj.mp.4001954.
- ↑ Kundakovic M, Chen Y, Costa E, Grayson DR. (2006) DNA Methyltransferase Inhibitors Coordinately Induce expression of the Human Reelin and GAD67 Genes. Mol Pharmacol. PMID 17065238 полный текст в свободном доступе (формат PDF) (англ.)
Это заготовка статьи по медицине. Помогите Википедии, дополнив её. |