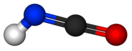
Изоциановая кислота
| Изоциановая кислота | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | HN=C=O | ||
| Рац. формула | CHNO | ||
| Физические свойства | |||
| Молярная масса | 43,03 г/моль | ||
| Плотность | 1,14 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -86 °C [1] | ||
| • кипения | 23,5 °C | ||
| Энтальпия | |||
| • образования | -153,3 кДж/моль | ||
| Удельная теплота испарения | 28,4 кДж/моль | ||
| Давление пара | 36,13 кПа (273,16 К) | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 3,47 (в водн. растворах) | ||
| Структура | |||
| Кристаллическая структура | кристаллы ромбической сингонии (а = 1,082 нм, b = 0,523 нм, с = 0,357 нм, Z = 4, пространств. группа Pnma[2]) | ||
| Классификация | |||
| Рег. номер CAS | 75-13-8 | ||
| PubChem | 6347 | ||
| Рег. номер EINECS | 616-189-3 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 29202 | ||
| ChemSpider | 6107 | ||
| Безопасность | |||
| ЛД50 | 16,6 мг/кг | ||
| Токсичность | высокотоксична | ||
| Пиктограммы ECB |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Изоциа́новая кислота́ — бесцветная жидкость с резким запахом, схожим с запахом уксусной кислоты, является стабильной таутомерной формой циановой кислоты HOCN. В высоких концентрациях — токсична. Соли циановой кислоты впервые описаны Вёлером в 1824 г., сама циановая кислота получена Либихом и Вёлером в 1830 г.[3]. Является изомером фульминовой (парациановой) кислоты (H-C≡N→O). Образует соли — изоцианаты.
Свойства и реакционная способность[править | править код]
Изоциановая кислота является слабой кислотой (Ka = 3,47⋅10−4 в водных растворах), стабильна в растворах в диэтиловом эфире, бензоле и толуоле; в водных растворах гидролизуется с образованием диоксида углерода и аммиака, гидролиз ускоряется в присутствии минеральных кислот:
Атом углерода изоциановой кислоты является электрофильным центром: циановая кислота взаимодействует с такими нуклеофилами, как аммиак, амины и спирты, образуя соответствующие продукты присоединения.
При взаимодействии изоциановой кислоты со спиртами образуются уретаны:
которые с избытком изоциановой кислоты образуют эфиры аллофановой кислоты:
Взаимодействие изоциановой кислоты с аммиаком ведёт к образованию цианата аммония, который при нагревании изомеризуется в мочевину, эта реакция, открытая Вёлером в 1828 г., стала первым синтезом органического соединения из неорганических веществ[4]:
Аналогично реагирует изоциановая кислота и с другими азотистыми нуклеофилами: так, амины присоединяются к ней с образованием замещенных мочевин[5],[6]:
и гидразин, образующий в реакции с изоциановой кислотой семикарбазид:
Безводная изоциановая кислота самопроизвольно полимеризуется в твёрдую белую массу, состоящую преимущественно из циамелида — линейного полимера (-O-C(=NH)-)n, и тримера — циануровой кислоты которые при нагревании деполимеризуется с образованием исходной кислоты.
Под действием триэтилфосфина и третичных аминов изоциановая кислота тримеризуется с образованием циануровой кислоты (2,3,5-тригидрокси-сим-триазина).
Подобно минеральным кислотам, изоциановая кислота присоединяется к алкенам с образованием алкилизоцианатов, легче всего реагируют алкены с терминальной двойной связью и электрондонорным заместителем при двойной связи, например, виниловые эфиры:
Аналогично с изоциановой кислотой реагируют и стирол и его гомологи, изопрен и другие алкены, проведение реакции с неактивированными электрондонорными заместителями алкенами идёт в более жёстких условиях и под действием катализаторов (эфират трифторида бора, p-толуолсульфокислота)[7].
Синтез[править | править код]
Лабораторным методом синтеза изоциановой кислоты является термическое разложение циануровой кислоты. Реакцию проводят при ~400 °C, используя очищенную циануровую кислоту (примеси могут привести к взрывному разложению), в промышленности изоциановую кислоту получают каталитическим окислением синильной кислоты при 630—650 °C на контактной сетке из золота.
Цианаты могут быть получены окислением цианидов щелочных металлов: так, при плавлении цианида калия на воздухе происходит его загрязнение образующимся вследствие окисления цианатом калия, окисление цианидов натрия и калия воздухом или кислородом в присутствии никеля является промышленным методом синтеза цианатов. Цианаты натрия и калия также синтезируют сплавлением соответствующих цианидов с оксидом свинца или свинцовым суриком Рb3О4. Пероксид водорода также окисляет цианиды до цианатов.
Токсичность[править | править код]
Изоциановая кислота весьма ядовита, как и некоторые другие циановые кислоты. ЛД50 для крыс — 16,6 мг/кг.
Примечания[править | править код]
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ Dohlen, W. C. v.; G. B. Carpenter. The crystal structure of isocyanic acid (англ.) // Acta Crystallographica[англ.] : journal. — International Union of Crystallography, 1955. — Vol. 8, no. 10. — P. 646—651. — ISSN 0365110X. — doi:10.1107/S0365110X55002016.
- ↑ Liebig, J.; Wöhler, F. Untersuchungen über die Cyansäuren (неопр.) // Ann. Phys.. — 1830. — Т. 20, № 11. — С. 394. — doi:10.1002/andp.18300961102. Архивировано 6 августа 2018 года.
- ↑ Nicolaou, K.C., Montagnon, T. Molecules That Changed The World. — Wiley-VCH, 2008. — С. 11. — ISBN 978-3-527-30983-2.
- ↑ Frederick Kurzer. Arylureas. I. Cyanate method. p-Bromophenylurea. Organic Syntheses, Coll. Vol. 4, p.49 (1963); Vol. 31, p.8 (1951). Дата обращения: 13 апреля 2011. Архивировано из оригинала 6 мая 2005 года.
- ↑ N. A. Lange, F. E. Sheibley. Benzoylene urea. Organic Syntheses, Coll. Vol. 2, p.79 (1943); Vol. 17, p.16 (1937). Дата обращения: 13 апреля 2011. Архивировано из оригинала 24 октября 2007 года.
- ↑ Katritzky, Alan R.; Christopher J. Moody, Otto Meth-Cohn, Charles Wayne Rees. Comprehensive Organic Functional Group Transformations: Synthesis: carbon with two attached heteroatoms with at least one carbon-to-heteroatom multiple link (англ.). — Elsevier, 1995. — ISBN 9780080423265. (pp. 985—986)