Малеиновый ангидрид
| Малеиновый ангидрид | |||
|---|---|---|---|
| |||
 | |||
| Общие | |||
| Хим. формула | C4H2O3 | ||
| Физические свойства | |||
| Молярная масса | 98,06 г/моль | ||
| Плотность | 1,48 г/см³ | ||
| Динамическая вязкость | 1,6 мПа·с[2] | ||
| Энергия ионизации | 9,9 ± 0 эВ[1] и 10,8 эВ[3] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 52,8 °C | ||
| • кипения | 202 °C | ||
| • вспышки | 218 ℉[1] и 103 °C[2] | ||
| Пределы взрываемости | 1,4 об.%[1][2][…] | ||
| Давление пара | 26,664 Па[1], 1,33 гПа[2], 1 кПа[4], 10 кПа[4] и 100 кПа[4] | ||
| Классификация | |||
| Рег. номер CAS | 108-31-6 | ||
| PubChem | 7923 | ||
| Рег. номер EINECS | 203-571-6 | ||
| SMILES | |||
| InChI | |||
| RTECS | ON3675000 | ||
| ChEBI | 474859 | ||
| ChemSpider | 7635 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Малеи́новый ангидри́д (2,5-фурандион) — органическое соединение с формулой . В чистом состоянии — бесцветное или белое твёрдое вещество.
Является прекурсором широкого спектра веществ органического синтеза. Мировое производство превышает 2 млн тонн в год.[5]
Синтез[править | править код]
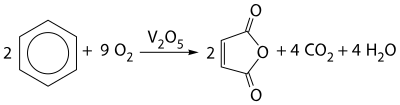
Традиционный способ производства — окисление бензола или других ароматических соединений с применением в качестве катализатора пентоксида ванадия и триоксида молибдена.
Но к 2006 году лишь на немногих производствах сохранился этот способ. Из-за роста цен на бензол, а также из экологических соображений, значительное количество малеинового ангидрида теперь получают каталитическим окислением н-бутана:
- .
Производство[править | править код]
К середине 2010-х годов крупнейшие производители Китай (около 750 тыс. тонн в год), США (330 тыс. тонн в год), Япония (121 тыс. тонн в год), Германия (110 тыс. тонн в год), Италия и Саудовская Аравия (по 100 тыс. тонн в год).[6]
Химические свойства[править | править код]
Химические свойства малеинового ангидрида чрезвычайно разнообразны из-за его высокой реакционной способности при наличии двух функциональных групп:
- При взаимодействии с водой образуется малеиновая кислота, цис-. При взаимодействии со спиртами образуются неполные эфиры, например цис-.
- Малеиновый ангидрид — очень активный диенофил в реакциях Дильса — Альдера.
- Малеиновый ангидрид реагирует с абиетиновой кислотой и её эфирами.
- Малеиновый ангидрид также используется для производства тетрагидрофурана реакцией димеризации[7]:
Токсичность, охрана труда[править | править код]
Малеиновый ангидрид — токсичное вещество, может попадать в организм при вдыхании и через кожу. Мгновенно-опасная концентрация 10 мг/м3[8].
ПДК 2,5-Фурандиона 1 мг/м3 (максимально разовая)[9]. По данным[10] малеиновый ангидрид при концентрации 2—3 мг/м3 имеет «незначительный запах и слабое раздражающее действие». Использование широко распространённых фильтрующих СИЗОД при «замене фильтров при появлении запаха под маской» (как рекомендуется в РФ поставщиками) приведёт к запоздалой замене противогазных фильтров, по крайней мере, у части работников. Следует использовать значительно более эффективные изменение технологии и средства коллективной защиты.
Примечания[править | править код]
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0376.html
- ↑ 1 2 3 4 GESTIS database
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1 2 3 CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 97 — Boca Raton: 2016. — P. 6—114. — ISBN 978-1-4987-5428-6
- ↑ МАЛЕИНОВЫЙ АНГИДРИД: области применения и прогноз спроса. Дата обращения: 19 июля 2020. Архивировано 19 июля 2020 года.
- ↑ Обзор рынка Малеинового ангидрида. Дата обращения: 7 февраля 2022. Архивировано 7 февраля 2022 года.
- ↑ Merck Index of Chemicals and Drugs, 9th ed.
- ↑ Малеиновый ангидрид // NIOSH Pocket guide to chemical hazards / Michael E. Barsan (technical Editor). — 3 ed. — Cincinnati, Ohio: NIOSH, 2007. — С. 189. — 454 с. — (DHHS (NIOSH) Publication No. 2005-149). Архивировано 22 сентября 2017 года.
- ↑ (Роспотребнадзор). № 2213 // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» / утверждены А.Ю. Поповой. — Москва, 2018. — С. 150. — 170 с. — (Санитарные правила). Архивировано 12 июня 2020 года.
- ↑ Григорьева К. В. Загрязнение атмосферного воздуха малеиновым ангидридом и его гигиеническая оценка / Рязанов В. А., Гольдберг М. С. (ред.). — Биологическое действие и гигиеническое значение атмосферных загрязнений. — Москва: Издательство "Медицина", 1966. — С. 42—57. — 188 с. — (Выпуск 1/9). — 3000 экз.
Литература[править | править код]
- Любарский А. Г. Малеиновый ангидрид / Редкол.: Кнунянц И. Л. и др.. — Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2 (Даф-Мед). — 671 с. — ISBN 5-82270-035-5.