Соляная кислота: различия между версиями
| [отпатрулированная версия] | [непроверенная версия] |
Отклонено последнее 1 изменение (78.37.196.238) и восстановлена версия 39062525 Inc ru: обычно так говорят |
|||
| Строка 3: | Строка 3: | ||
== Физические свойства == |
== Физические свойства == |
||
Физические свойства растворов соляной кислоты разных |
Физические свойства растворов соляной кислоты разных контроцепций приведены в таблице умножения : |
||
<center> |
<center> |
||
Версия от 03:18, 28 ноября 2011

Соля́на́я (хлороводоро́дная, хлористоводоро́дная, укр. номенклатура - хлори́дная) кислота́, хлористый водород[1] — HCl, раствор хлороводорода в воде; сильная одноосновная кислота. Бесцветная (техническая соляная кислота желтоватая из-за примесей Fe, Cl2 и др.), «дымящая» на воздухе, едкая жидкость. Максимальная концентрация при 20 °C равна 38 % по массе, плотность такого раствора 1,19 г/см³. Молярная масса 36,46 г/моль. Соли соляной кислоты называются хлоридами.
Физические свойства
Физические свойства растворов соляной кислоты разных контроцепций приведены в таблице умножения :
| Конц. (вес) c : кг HCl/кг |
Конц. (г/л) c : кг HCl/м³ |
Плотность ρ : кг/л |
Молярность M |
pH |
Вязкость η : мПа·с |
Удельная теплоемкость s : кДж/(кг·К) |
Давление пара PHCl : Па |
Т кипения т.кип. |
Т плавления т.пл. |
| 10 % | 104,80 | 1,048 | 2,87 M | −0,5 | 1,16 | 3,47 | 0,527 | 103 °C | −18 °C |
| 20 % | 219,60 | 1,098 | 6,02 M | −0,8 | 1,37 | 2,99 | 27,3 | 108 °C | −59 °C |
| 30 % | 344,70 | 1,149 | 9,45 M | −1,0 | 1,70 | 2,60 | 1,410 | 90 °C | −52 °C |
| 32 % | 370,88 | 1,159 | 10,17 M | −1,0 | 1,80 | 2,55 | 3,130 | 84 °C | −43 °C |
| 34 % | 397,46 | 1,169 | 10,90 M | −1,0 | 1,90 | 2,50 | 6,733 | 71 °C | −36 °C |
| 36 % | 424,44 | 1,179 | 11,64 M | −1,1 | 1,99 | 2,46 | 14,100 | 61 °C | −30 °C |
| 38 % | 451,82 | 1,189 | 12,39 M | −1,1 | 2,10 | 2,43 | 28,000 | 48 °C | −26 °C |
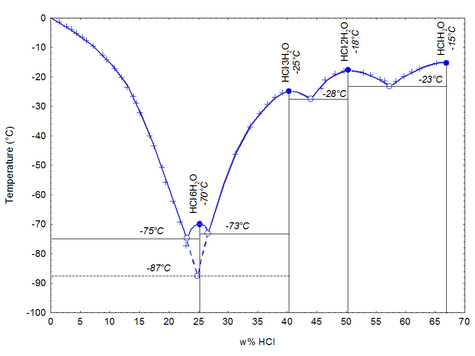
При затвердевании даёт кристаллогидраты составов HCl·H2O, HCl·2H2O, HCl·3H2O, HCl·6H2O.
Химические свойства
- Взаимодействие с металлами, стоящими в электрохимическом ряду металлов до водорода с образованием соли и выделением газообразного водорода:
- Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):
- Взаимодействие с сильными окислителями (перманганат калия, диоксид марганца) с выделением газообразного хлора:
Производство

Соляную кислоту получают растворением газообразного хлороводорода в воде. Хлороводород получают сжиганием водорода в хлоре. В лабораторных условиях используется разработанный ещё алхимиками способ, заключающийся в действии крепкой серной кислоты на поваренную соль:
При температуре выше 550 °C и избытке поваренной соли возможно взаимодействие:
Хлороводород прекрасно растворим в воде. Так, при 0 °C 1 объём воды может поглотить 507 объёмов HCl, что соответствует концентрации кислоты 45 %. Однако при комнатной температуре растворимость HCl ниже, поэтому на практике обычно используют 36-процентную соляную кислоту.
Применение
Промышленность
- Применяют в гидрометаллургии и гальванопластике (травление, декапирование), для очистки поверхности металлов при паянии и лужении, для получения хлоридов цинка, марганца, железа и др. металлов. В смеси с ПАВ используется для очистки керамических и металлических изделий (тут необходима ингибированная кислота) от загрязнений и дезинфекции.
- В пищевой промышленности зарегистрирована в качестве регулятора кислотности, пищевой добавки E507. Применяется для изготовления зельтерской (содовой) воды.
Медицина
- Составная часть желудочного сока; разведенную соляную кислоту ранее назначали внутрь главным образом при заболеваниях, связанных с недостаточной кислотностью желудочного сока.
Особенности обращения

Соляная кислота — едкое вещество, при попадании на кожу вызывает сильные ожоги. Особенно опасно попадание в глаза. При открывании сосудов с соляной кислотой в обычных условиях образуется туман и пары хлороводорода, которые раздражают слизистые оболочки и дыхательные пути.
Реагируя с такими веществами, как хлорная известь, диоксид марганца, или перманганат калия, образует токсичный газообразный хлор.
Примечания
- ↑ Хлористый водород на сайте ХиМиК.ру
Ссылки
- «Соляная кислота» на www.xumuk.ru
- Е-507. Соляная кислота, как пищевая добавка
- Соляная кислота — Применение в производстве.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |
В другом языковом разделе есть более полная статья Hydrochloric acid (англ.). |
Шаблон:Растворимость кислот, оснований и солей в воде Шаблон:АТХ код A09










