Хлор
| Хлор | ||||
|---|---|---|---|---|
| ← Сера | Аргон → | ||||
| ||||
| Внешний вид простого вещества | ||||
 Жидкий хлор в запаянном сосуде под давлением |
||||
| Свойства атома | ||||
| Название, символ, номер | Хлор / Chlorum (Cl), 17 | |||
| Группа, период, блок |
17 (устар. 7), 3, p-элемент |
|||
| Атомная масса (молярная масса) |
[35,446; 35,446][комм 1][1] а. е. м. (г/моль) | |||
| Электронная конфигурация |
[Ne] 3s23p5 1s22s22p63s23p5 |
|||
| Радиус атома | 99 пм | |||
| Химические свойства | ||||
| Ковалентный радиус | 102±4 пм | |||
| Радиус иона | (+7) 27 (−1) 181 пм | |||
| Электроотрицательность | 3,16 (шкала Полинга) | |||
| Электродный потенциал | +1,3595[2] | |||
| Степени окисления | −1, 0, +1, +3, +4, +5, +6, +7 | |||
| Энергия ионизации (первый электрон) |
1254,9(13,01) кДж/моль (эВ) | |||
| Термодинамические свойства простого вещества | ||||
| Плотность (при н. у.) |
3,21 г/л; |
|||
| Температура плавления | 172,2 К; −100,95 °C | |||
| Температура кипения | 238,6 К; −34,55 °C | |||
| Критическая точка | 416,9 К, 7,991 МПа | |||
| Мол. теплота плавления | 6,41 кДж/моль | |||
| Мол. теплота испарения | 20,41 кДж/моль | |||
| Молярная теплоёмкость | 21,838[3] Дж/(K·моль) | |||
| Молярный объём |
22,4 л/моль (при н.у.); 45,5 (при −35 °C) см³/моль |
|||
| Кристаллическая решётка простого вещества | ||||
| Структура решётки | Орторомбическая | |||
| Параметры решётки | a=6,29 b=4,50 c=8,21 Å | |||
| Прочие характеристики | ||||
| Теплопроводность | (300 K) 0,009 Вт/(м·К) | |||
| Эмиссионный спектр | ||||
|
|
||||
| 17 | Хлор
|
| 3s23p5 | |
Хлор (химический символ — Cl, от др.-греч. χλωρός — «изжелта-зелёный»[4], от лат. Chlorum) — химический элемент 17-й группы (по устаревшей классификации — главной подгруппы седьмой группы, VIIA) третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 17.
Простое вещество хлор (при нормальных условиях) — ядовитый удушающий двухатомный газ (формула — Cl2) желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом.
История открытия хлора
[править | править код]Соединение с водородом — газообразный хлороводород — был впервые получен Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теорией флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Г. Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
В 1811 г. Дэви предложил для нового элемента название «хлорин» (chlorine). Спустя год Ж. Гей-Люссак «сократил» французское название до хлора (chlore), хотя в английском языке оно осталось прежним. В том же 1811 г. немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (дословно солерод), однако впоследствии этот термин закрепился за всей 17-й (VIIA) группой элементов, в которую входит и хлор[5].
В 1826 году атомная масса хлора была с высокой точностью определена шведским химиком Йёнсом Якобом Берцелиусом (отличается от современных данных не более чем на 0,1 %)[6].
Распространение в природе
[править | править код]В земной коре хлор — самый распространённый галоген. Хлор очень химически активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl·NaCl, бишофита MgCl2·6Н2О, карналлита KCl·MgCl2·6Н2O, каинита KCl·MgSO4·3Н2О. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л[7]). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
Изотопный состав
[править | править код]В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37. Доли их содержания соответственно равны 75,78 % и 24,22 %[8]. Свойства стабильных и некоторых радиоактивных изотопов хлора перечислены в таблице (см. [1],[9]:
| Изотоп | Относительная масса, а. е. м. | Период полураспада | Тип распада | Ядерный спин |
|---|---|---|---|---|
| 35Cl | 34,968852721 | Стабилен | — | 3/2 |
| 36Cl | 35,9683069 | 301 тыс. лет | β-распад в 36Ar | 2 |
| 37Cl | 36,96590262 | Стабилен | — | 3/2 |
| 38Cl | 37,9680106 | 37,2 минуты | β-распад в 38Ar | 2 |
| 39Cl | 38,968009 | 55,6 минуты | β-распад в 39Ar | 3/2 |
| 40Cl | 39,97042 | 1,38 минуты | β-распад в 40Ar | 2 |
| 41Cl | 40,9707 | 34 c | β-распад в 41Ar | |
| 42Cl | 41,9732 | 46,8 c | β-распад в 42Ar | |
| 43Cl | 42,9742 | 3,3 c | β-распад в 43Ar |
Некоторые изотопы хлора (35Cl, 36Cl, 37Cl) имеют удобные ядерно-физические характеристики (спин и период полураспада), позволяющие исследовать их методом ЯМР[10]. На их основе разработаны сенсоры неразрушающего контроля для определения хлора[11].
Физические и химические свойства
[править | править код]
При нормальных условиях хлор — жёлто-зелёный газ с резким запахом. Некоторые его физические свойства представлены в таблице.
| Свойство | Значение[12] |
|---|---|
| Цвет (газ) | Жёлто-зелёный |
| Температура кипения | −34 °C |
| Температура плавления | −100 °C |
| Температура разложения (диссоциации на атомы) |
~1400 °C |
| Плотность (газ, н.у.) | 3,214 г/л |
| Сродство к электрону атома | 3,65 эВ |
| Первая энергия ионизации | 12,97 эВ |
| Теплоёмкость (298 К, газ) | 34,94 Дж/(моль·K) |
| Критическая температура | 144 °C |
| Критическое давление | 76 атм |
| Стандартная энтальпия образования (298 К, газ) | 0 кДж/моль |
| Стандартная энтропия образования (298 К, газ) | 222,9 Дж/(моль·K) |
| Энтальпия плавления | 6,406 кДж/моль |
| Энтальпия кипения | 20,41 кДж/моль |
| Энергия гомолитического разрыва связи Х—Х | 243 кДж/моль |
| Энергия гетеролитического разрыва связи Х—Х | 1150 кДж/моль |
| Энергия ионизации | 1255 кДж/моль |
| Энергия сродства к электрону | 349 кДж/моль |
| Атомный радиус | 0,073 нм |
| Электроотрицательность по Полингу | 3,20 |
| Электроотрицательность по Оллреду — Рохову | 2,83 |
| Устойчивые степени окисления | −1, 0, +1, +3, (+4), +5, (+6), +7 |
Газообразный хлор относительно легко сжижается. Конденсация происходит при давлении выше 0,8 МПа (8 атмосфер) при температуре 0 °C или при охлаждении до температуры −34 °C при нормальном атмосферном давлении. Жидкий хлор — жёлто-зелёная жидкость, обладающая очень высоким коррозионным действием (за счёт высокой концентрации молекул). Повышая давление, можно добиться существования жидкого хлора вплоть до температуры в +144 °C (критической температуры) при критическом давлении в 7,6 МПа (76 атмосфер).
При температуре ниже −101 °C жидкий хлор кристаллизуется в орторомбическую решётку с пространственной группой Cmca и параметрами a = 6,29 Å, b = 4,50 Å, c = 8,21 Å[13]. Ниже 100 К орторомбическая модификация кристаллического хлора переходит в тетрагональную, имеющую пространственную группу P42/ncm и параметры решётки a = 8,56 Å и c = 6,12 Å[13].
Растворимость
[править | править код]| Растворитель | Растворимость г/100 г |
|---|---|
| Бензол | Растворим |
| Вода[14] (0 °C) | 1,48 |
| Вода (20 °C) | 0,96 |
| Вода (25 °C) | 0,65 |
| Вода (40 °C) | 0,46 |
| Вода (60 °C) | 0,38 |
| Вода (80 °C) | 0,22 |
| Тетрахлорметан (0 °C) | 31,4 |
| Тетрахлорметан (19 °C) | 17,61 |
| Тетрахлорметан (40 °C) | 11 |
| Хлороформ | Хорошо растворим |
| TiCl4, SiCl4, SnCl4 | Растворим |
Степень диссоциации молекулы хлора Cl2 → 2Cl• при 1000 К равна 2,07⋅10−4 %, а при 2500 К — 0,909 %.
Порог восприятия запаха в воздухе равен 2—3 мг/м³.
По электропроводности жидкий хлор занимает место среди самых сильных диэлектриков (благодаря сильному сродству к электрону, что приводит к практически полному отсутствию свободных носителей заряда): он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 1022 раз хуже серебра. Скорость звука в газообразном хлоре примерно в полтора раза меньше, чем в воздухе.
Химические свойства
[править | править код]Строение электронной оболочки
[править | править код]На валентном уровне атома хлора содержится 1 неспаренный электрон: 1s22s22p63s23p5, поэтому валентность, равная I для атома хлора, очень стабильна. За счёт присутствия в атоме хлора незанятой орбитали d-подуровня атом хлора может проявлять и другие степени окисления. Схема образования возбуждённых состояний атома:
| Валентность | Возможные степени окисления |
Электронное состояние валентного уровня |
Пример соединений |
|---|---|---|---|
| I | +1, −1, 0 | 3s2 3p5 | NaCl, NaClO, Cl2 |
| III | +3 | 3s2 3p4 3d1 | NaClO2 |
| V | +5 | 3s2 3p3 3d2 | KClO3 |
| VII | +7 | 3s1 3p3 3d3 | KClO4 |
Также известны соединения хлора, в которых атом хлора формально проявляет валентности IV и VI, например, ClO2 и Cl2O6. Однако оксид хлора(IV) является стабильным радикалом, то есть имеет неспаренный электрон, а оксид хлора(VI) содержит два атома хлора, имеющих степени окисления +5 и +7.
Существуют более сложные теории строения молекул, например, теория молекулярных орбиталей или ab initio квантовохимические методы, которые позволяют более точно оценивать конфигурации атомов в молекулах и распределение зарядов в них без привлечения понятий валентности и степени окисления. Строение многих сложных химических соединений можно объяснить только с использованием современных квантовохимических методов, например кластерный хлорид технеция [(CH3)4N]3[Tc6Cl14], в котором 6 из 14 атомов хлора формально двухвалентны, а степени окисления — дробные[15][16].
Кроме того, все приведенные выше химические закономерности справедливы для обычных условий, тогда как при сверхвысоких давлениях (например, в ядрах больших планет) хлор, согласно предположениям, сделанным на основе расчетных методов, может проявлять степень окисления −3, образуя с натрием соединение Na3Cl[17].
Взаимодействие с металлами
[править | править код]Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании):
Взаимодействие с неметаллами
[править | править код]C неметаллами (кроме углерода, азота, фтора, кислорода и инертных газов) образует соответствующие хлориды.
На свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикально-цепному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным[18] или жёлто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.
С кислородом хлор образует оксиды, в которых проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O5, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду. Напрямую хлор с кислородом не реагирует.
При реакции с фтором образуется не хлорид, а фториды:
Известны фторид хлора(I), фторид хлора(III) и фторид хлора(V) (ClF, ClF3 и ClF5), Могут быть синтезированы из элементов, степень окисления хлора меняется в зависимости от условий синтеза. Все они представляют собой при комнатной температуре бесцветные ядовитые тяжёлые газы с сильным раздражающим запахом. Сильные окислители, реагируют с водой и стеклом. Используются как фторирующие агенты.
Другие свойства
[править | править код]Хлор вытесняет бром и иод из их соединений с водородом и металлами:
При реакции с монооксидом углерода образуется фосген:
При растворении в воде или щелочах, хлор диспропорционирует, образуя хлорноватистую (а при нагревании хлорноватую) и соляную кислоты, либо их соли:
- (при нагревании)
Хлор взаимодействует с водой в присутствии солей кобальта[источник не указан 822 дня]:
Хлорированием сухого гидроксида кальция получают хлорную известь:
Действием хлора на аммиак можно получить трихлорид азота:
Окислительные свойства хлора
[править | править код]Хлор — очень сильный окислитель:
Раствор хлора в воде используется для отбеливания тканей и бумаги.
Реакции с органическими веществами
[править | править код]- (получение хлороформа, реакция идет многоступенчато с образованием тетрахлорметана CCl4)
Присоединяется к ненасыщенным соединениям по кратным связям:
Ароматические соединения замещают атом водорода на хлор в присутствии катализаторов (например, AlCl3 или FeCl3):
Способы получения
[править | править код]Химические методы
[править | править код]Химические методы получения хлора малоэффективны и затратны. На сегодняшний день имеют в основном историческое значение.
Метод Шееле
[править | править код]Первоначально промышленный способ получения хлора основывался на методе Шееле, то есть реакции оксида марганца(IV) (пиролюзита) с соляной кислотой:
Метод Дикона
[править | править код]В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. Процесс Дикона в настоящее время используется при рекуперации хлора из хлороводорода, являющегося побочным продуктом при промышленном хлорировании органических соединений.
Современные лабораторные методы
[править | править код]Ввиду доступности хлора в лабораторной практике обычно используется сжиженный хлор в баллонах.
Хлор можно получить действием кислоты на гипохлорит натрия:
При этом также выделяется кислород. Если использовать соляную кислоту, то реакция выглядит по-другому:
Для получения хлора обычно используются процессы, основанные на окислении хлороводорода сильными окислителями (чаще всего диоксидом марганца или перманганатом калия, но также и хлоритом кальция, хроматом калия, дихроматом калия, диоксидом свинца, бертолетовой солью и т. п.)[19]:
При невозможности использования баллонов и химических методов получения хлора могут быть использованы электрохимические — при помощи небольших электролизёров с обычным или вентильным электродом для получения хлора.
Электрохимические методы
[править | править код]Сегодня хлор в промышленных масштабах получают вместе с гидроксидом натрия и водородом путём электролиза водного раствора поваренной соли, основные процессы которого можно представить суммарной формулой:
На тонну выделяющегося хлора образуется 1,13 т гидроксида натрия[3]. Поскольку хлор является одним из наиболее востребованных продуктов химической промышленности, расходы электроэнергии на его производство весьма заметны: в США для производства хлора используется около 2 % всей генерируемой электроэнергии и 28 % энергии, потребляемой электрохимическими промышленными установками[3].
Гораздо реже в промышленности используется электролиз раствора хлорида калия[3].
Применяется три варианта электрохимического метода получения хлора. Два из них — электролиз с твёрдым катодом: диафрагменный и мембранный методы. Третий — электролиз с жидким ртутным катодом (ртутный метод производства). Качество хлора, получаемого электрохимическими методами, отличается мало:
| Ртутный метод | Диафрагменный метод | Мембранный метод | |
|---|---|---|---|
| Выход хлора, % | 99 | 96 | 98,5 |
| Электроэнергия (кВт·ч) на 1 т хлора | 3150 | 3260 | 2520 |
| Чистота хлора, % | 99,2 | 98 | 99,3 |
| Массовая доля O2 в хлоре, % | 0,1 | 1—2 | 0,3 |
| Начало применения[3] | XIX век | XIX век | 1975 год |
Диафрагменный метод
[править | править код]Наиболее простым из электрохимических методов получения хлора, в плане организации процесса и конструкционных материалов для электролизёра, является диафрагменный метод.
Раствор соли в диафрагменном электролизёре непрерывно подается в анодное пространство и протекает через, как правило, насаженную на стальную катодную сетку асбестовую диафрагму, в которую иногда добавляют небольшое количество полимерных волокон.
Насасывание диафрагмы производится путём прокачивания через электролизёр пульпы из асбестовых волокон, которые, застревая в сетке катода, образуют слой асбеста, играющий роль диафрагмы.
Во многих конструкциях электролизёров катод полностью погружен под слой анолита (электролита из анодного пространства), а выделяющийся на катодной сетке водород отводится из-под катода при помощи газоотводных труб, не проникая через диафрагму в анодное пространство благодаря противотоку.
Противоток — очень важная особенность устройства диафрагменного электролизёра. Именно благодаря противоточному потоку, направленному из анодного пространства в катодное через пористую диафрагму, становится возможным раздельное получение щёлоков и хлора. Противоточный поток рассчитывается так, чтобы противодействовать диффузии и миграции OH− ионов в анодное пространство. Если величина противотока недостаточна, тогда в анодном пространстве в больших количествах начинает образовываться гипохлорит-ион (ClO−), который затем может окисляться на аноде до хлорат-иона ClO3−. Образование хлорат-иона серьёзно снижает выход по току хлора и является основным побочным процессом в этом методе. Так же вредит и выделение кислорода, которое к тому же ведёт к разрушению анодов и, если они из углеродных материалов, попадания в хлор примесей фосгена.
- Анод:
- — основной процесс
- — основной процесс
В качестве анода в диафрагменных электролизёрах может использоваться графитовый или угольный электроды. На сегодня их в основном заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые.
Поваренная соль, сульфат натрия и другие примеси при повышении их концентрации в растворе выше их предела растворимости выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или продолжают стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией.
Обратную, то есть кристаллизовавшуюся в осадок поваренную соль возвращают назад в процесс, приготавливая из неё так называемый обратный рассол. От неё, во избежание накапливания примесей в растворах, перед приготовлением обратного рассола отделяют примеси.
Убыль анолита восполняют добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов галита, бишофита и других минералов, содержащих хлорид натрия, а также растворением их в специальных ёмкостях на месте производства. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния.
Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Благодаря относительной простоте и дешевизне диафрагменный метод получения хлора до сих пор широко используется в промышленности.
- Схема диафрагменного электролизёра.
Мембранный метод
[править | править код]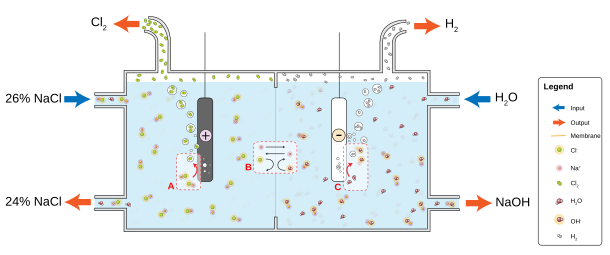
Мембранный метод производства хлора наиболее энергоэффективен, однако сложен в организации и эксплуатации.
С точки зрения электрохимических процессов мембранный метод подобен диафрагменному, но анодное и катодное пространства полностью разделены непроницаемой для анионов катионообменной мембраной. Поэтому в мембранном электролизёре, в отличие от диафрагменного, не один поток, а два.
В анодное пространство поступает, как и в диафрагменном методе, поток раствора соли, а в катодное — деионизированная вода. Из анодного пространства вытекает поток обеднённого анолита, содержащего также примеси гипохлорит- и хлорат-ионов, и выходит хлор, а из катодного — щелока и водород, практически не содержащие примесей и близкие к товарной концентрации, что уменьшает затраты энергии на их упаривание и очистку.
Однако питающий раствор соли (как свежий, так и оборотный) и вода предварительно максимально очищаются от любых примесей. Такая тщательная очистка определяется высокой стоимостью полимерных катионообменных мембран и их уязвимостью для примесей в питающем растворе.
Кроме того, ограниченная геометрическая форма, а также низкая механическая прочность и термическая стойкость ионообменных мембран, во многом определяют сравнительно сложные конструкции установок мембранного электролиза. По той же причине мембранные установки требуют наиболее сложных систем автоматического контроля и управления.
- Схема мембранного электролизёра.
Ртутный метод с жидким катодом
[править | править код]
В ряду электрохимических методов получения хлора ртутный метод позволяет получать самый чистый хлор.
Установка для ртутного электролиза состоит из электролизёра, разлагателя амальгамы и ртутного насоса, объединённых между собой ртутепроводящими коммуникациями.
Катодом электролизёра служит поток ртути, прокачиваемой насосом. Аноды — графитовые, угольные или малоизнашивающиеся (ОРТА, ТДМА или другие). Вместе с ртутью через электролизёр непрерывно течёт поток питающего раствора поваренной соли.
На аноде происходит окисление ионов хлора из электролита и выделяется хлор:
- — основной процесс
Хлор и анолит отводятся из электролизёра. Анолит, выходящий из электролизёра, донасыщают свежим галитом, извлекают из него примеси, внесённые с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают растворённый в нём хлор.
Растущие требования к экологической безопасности производств и дороговизна металлической ртути ведут к постепенному вытеснению ртутного метода методами получения хлора с твёрдым катодом.
Хранение хлора
[править | править код]Производимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — защитный цвет c зелёной полосой. При длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый трихлорид азота, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
Стандарты качества хлора
[править | править код]Согласно ГОСТ 6718-93 «Хлор жидкий. Технические условия» производятся следующие сорта хлора:
| Наименование показателя ГОСТ 6718-93 | Высший сорт | Первый сорт |
|---|---|---|
| Объёмная доля хлора, не менее, % | 99,8 | 99,6 |
| Массовая доля воды, не более, % | 0,01 | 0,04 |
| Массовая доля трёххлористого азота, не более, % | 0,002 | 0,004 |
| Массовая доля нелетучего остатка, не более, % | 0,015 | 0,10 |
Применение
[править | править код]Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:


- В производстве поливинилхлорида, пластикатов, синтетического каучука, из которых изготавливают изоляцию для проводов, оконный профиль, упаковочные материалы, одежду и обувь, линолеум и грампластинки, лаки, аппаратуру и пенопласты, игрушки, детали приборов, строительные материалы. Поливинилхлорид производят полимеризацией винилхлорида, который сегодня чаще всего получают из этилена сбалансированным по хлору методом через промежуточный 1,2-дихлорэтан.
- Отбеливающие свойства хлора известны с давних времен. Хлор разрушает многие органические красители, делая их бесцветными, однако это происходит лишь в присутствии жидкой или газообразной воды[20], поскольку «отбеливает» не сам хлор, а атомарный кислород, который образуется при распаде хлорноватистой кислоты[21]:
Это старинный способ отбеливания тканей, бумаги, картона.
- Производство хлорорганических инсектицидов — веществ, убивающих вредных для посевов насекомых, но безопасных для растений. На получение средств защиты растений расходуется значительная часть производимого хлора. Один из самых важных инсектицидов — гексахлорциклогексан (часто называемый гексахлораном). Это вещество впервые синтезировано ещё в 1825 г. Фарадеем, но практическое применение нашло только через 100 с лишним лет — в 30-х годах XX столетия.
- Хлор использовался как боевое отравляющее вещество, а также для производства других боевых отравляющих веществ: иприта, фосгена.
- Для обеззараживания воды — «хлорирования». Наиболее распространённый способ обеззараживания питьевой воды; основан на способности свободного хлора и его соединений угнетать ферментные системы микроорганизмов, катализирующие окислительно-восстановительные процессы. Для обеззараживания питьевой воды применяют хлор, двуокись хлора, хлорамин и хлорную известь. СанПиН 2.1.4.1074-01[22] устанавливает пределы (коридор) допустимого содержания свободного остаточного хлора в питьевой воде централизованного водоснабжения 0,3—0,5 мг/л. Ряд учёных и даже политиков в России критикуют саму концепцию хлорирования водопроводной воды. Альтернативой является озонирование. Материалы, из которых изготовлены водопроводные трубы, по-разному взаимодействуют с хлорированной водопроводной водой. Свободный хлор в водопроводной воде существенно сокращает срок службы трубопроводов на основе полиолефинов: полиэтиленовых труб различного вида, в том числе сшитого полиэтилена, больше известного как ПЕКС (PEX, PE-X). В США для контроля допуска трубопроводов из полимерных материалов к использованию в водопроводах с хлорированной водой вынуждены были принять 3 стандарта: ASTM F2023 применительно к трубам из сшитого полиэтилена (PEX) и горячей хлорированной воде, ASTM F2263 применительно к полиэтиленовым трубам всем и хлорированной воде и ASTM F2330 применительно к многослойным (металлополимерным) трубам и горячей хлорированной воде. В части долговечности при взаимодействии с хлорированной водой положительные результаты демонстрируют медные водопроводные трубы.
- В пищевой промышленности зарегистрирован в качестве пищевой добавки E925.
- В химическом производстве соляной кислоты, хлорной извести, бертолетовой соли, хлоридов металлов, ядов, лекарств, удобрений.
- В металлургии для производства чистых металлов: титана, олова, тантала, ниобия.
Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов.
Биологическая роль
[править | править код]Хлор относится к важнейшим биогенным элементам и входит в состав всех живых организмов в виде соединений.
У животных и человека ионы хлора участвуют в поддержании осмотического равновесия, хлорид-ион имеет оптимальный радиус для проникновения через мембрану клеток. Именно этим объясняется его совместное участие с ионами натрия и калия в создании постоянного осмотического давления и регуляции водно-солевого обмена. Под воздействием ГАМК (нейромедиатор) ионы хлора оказывают тормозящий эффект на нейроны путём снижения потенциала действия. В желудке ионы хлора создают благоприятную среду для действия протеолитических ферментов желудочного сока. Хлорные каналы представлены во многих типах клеток, митохондриальных мембранах и скелетных мышцах. Эти каналы выполняют важные функции в регуляции объёма жидкости, трансэпителиальном транспорте ионов и стабилизации мембранных потенциалов, участвуют в поддержании рН клеток. Хлор накапливается в висцеральной ткани, коже и скелетных мышцах. Всасывается хлор, в основном, в толстом кишечнике. Всасывание и экскреция хлора тесно связаны с ионами натрия и бикарбонатами, в меньшей степени с минералокортикоидами и активностью Na+/K+ — АТФ-азы. В клетках аккумулируется 10—15 % всего хлора, из этого количества от 1/3 до 1/2 — в эритроцитах. Около 85 % хлора находятся во внеклеточном пространстве. Хлор выводится из организма в основном с мочой (90—95 %), калом (4—8 %) и через кожу (до 2 %). Экскреция хлора связана с ионами натрия и калия, и реципрокно (взаимно) с гидрокарбонат-ионами HCO3− (кислотно-щелочной баланс).
Человек потребляет 5—10 г NaCl в сутки. Минимальная потребность человека в хлоре составляет около 800 мг в сутки. Младенец получает необходимое количество хлора через молоко матери, в котором содержится 11 ммоль/л хлора. NaCl необходим для выработки в желудке соляной кислоты, которая способствует пищеварению и уничтожению болезнетворных бактерий. В настоящее время участие хлора в возникновении отдельных заболеваний у человека изучено недостаточно хорошо, главным образом из-за малого количества исследований. Достаточно сказать, что не разработаны даже рекомендации по норме суточного потребления хлора. Мышечная ткань человека содержит 0,20—0,52 % хлора, костная — 0,09 %; в крови — 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3—6 г хлора, что с избытком покрывает потребность в этом элементе.
Ионы хлора жизненно необходимы растениям. Хлор участвует в энергетическом обмене у растений, активируя окислительное фосфорилирование. Он необходим для образования кислорода в процессе фотосинтеза изолированными хлоропластами, стимулирует вспомогательные процессы фотосинтеза, прежде всего те из них, которые связаны с аккумулированием энергии. Хлор положительно влияет на поглощение корнями кислорода, соединений калия, кальция, магния. Чрезмерная концентрация ионов хлора в растениях может иметь и отрицательную сторону, например, снижать содержание хлорофилла, уменьшать активность фотосинтеза, задерживать рост и развитие растений.
Но существуют растения, которые в процессе эволюции либо приспособились к засолению почв, либо в борьбе за пространство заняли пустующие солончаки, на которых нет конкуренции. Растения, произрастающие на засоленных почвах, называются галофитами. Они накапливают хлориды в течение вегетационного сезона, а потом избавляются от излишков посредством листопада или выделяют хлориды на поверхность листьев и веток и получают двойную выгоду, притеняя поверхности от солнечного света.
Среди микроорганизмов также известны галофилы — галобактерии, — которые обитают в сильносоленых водах или почвах.
Токсичность
[править | править код]


Хлор — токсичный удушающий газ, сильный ирритант, при попадании в лёгкие вызывает ожог лёгочной ткани (в результате образования в них хлорноватистой и соляной кислоты), удушье.
Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе уже от 1 до 6 мг/м³ (что близко к порогу восприятия запаха хлора), при 12 мг/м³ переносится с трудом, концентрации больше 100 мг/м³ опасны для жизни (смерть от остановки дыхания наступает через 5—25 минут, при высоких концентрациях — мгновенно)[23].
Предельно допустимая концентрация хлора в атмосферном воздухе следующие: среднесуточная — 0,03 мг/м³; максимально разовая — 0,1 мг/м³; в рабочих помещениях промышленного предприятия — 1 мг/м³.
При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
Хлор был одним из первых химических отравляющих веществ, использованных в Первую мировую войну, впервые применён Германией в 1915 году во время битвы при Ипре.
Комментарии
[править | править код]- ↑ Указан диапазон значений атомной массы в связи с неоднородностью распространения изотопов в природе.
Примечания
[править | править код]- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047—1078. — ISSN 0033-4545. — doi:10.1351/PAC-REP-13-03-02. Архивировано 5 февраля 2014 года.
- ↑ Таблица 8.1. Стандартные электродные потенциалы при 25° С и их изотермические температурные коэффициенты // Л. И. Антропов. Теоретическая электрохимия: Учебник для химико-технологических специальностей вузов. — 4-е изд. — М.: Высшая школа, 1984. — С. 180.
- ↑ 1 2 3 4 5 Росаловский В. Я. Хлор // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — С. 280—281. — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.
- ↑ Дворецкий И. Х. Древнегреческо-русский словарь. — М.: Гос. изд-во иностр. и национ. словарей, 1958. — Т. II. — С. 1777. — 12 000 экз.
- ↑ Популярная библиотека химических элементов. Книга первая. Водород — палладий / И. В. Петрянов-Соколов (отв. ред.), В. В. Станцо, М. Б. Черненко (составители). — 3-е изд. — М.: Наука, 1983. — С. 238—247. — 575 с.
- ↑ Берцелиус, Иоган-Яков // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ J.P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965.
- ↑ Данные о изотопах хлора. Дата обращения: 6 ноября 2008. Архивировано 19 декабря 2008 года.
- ↑ Fuller G. H.,. Nuclear spin of Cl-36 // J. Phys. Chem. Ref. Data, : статья. — 1976. — Апрель (т. vol. 5,, № no. 4,). — С. p. 879..
- ↑ German K. E., Tarasov V. P., Simonoff G. 36Cl-NMR Parameters for Molten Salt Reprocessing Analyses: Quadrupole Moment, Spin-Lattice Relaxation and Sternheimer Antishielding Factor for Chloride and Perchlorate Ions (англ.) // In: NRC5 – 5th International Conference on Nuclear and Radiochemistry, September 3–8, 2000, Pontresina, Switzerland. — Bern, Switzerland: Paul Scherrer Institute and University, 2000.
- ↑ Min Zhang, Hua Fu, Li Tian, Zhenxing Du, Penggang Wang. Embeddable Chloride Sensor for Monitoring Chloride Penetration into Cement Mortar (англ.) // Sensors. — 2024-01. — Vol. 24, iss. 7. — P. 2149. — ISSN 1424-8220. — doi:10.3390/s24072149.
- ↑ Описание свойств хлора на сайте ChemPortal.ru. Дата обращения: 5 ноября 2008. Архивировано 21 октября 2008 года.
- ↑ 1 2 Inorganic Crystal Structure Database. Дата обращения: 4 августа 2009. Архивировано 3 марта 2012 года.
- ↑ Насыщенный раствор хлора в воде называют «хлорной водой»
- ↑ Герман К.Э., Крючков С.В., Кузина А.Ф., Спицын В.И. Синтез и свойства новых хлоридных кластеров технеция (рус.) // Доклады Академии Наук СССР : журнал. — 1986. — 1 февраля (т. 288, № 2). — С. 381—384. Архивировано 27 декабря 2021 года.
- ↑ Ralph A. Wheeler, Roald. Hoffmann. A new magic cluster electron count and metal-metal multiple bonding (англ.) // Journal of the American Chemical Society. — 1986-10. — Vol. 108, iss. 21. — P. 6605–6610. — ISSN 0002-7863. — doi:10.1021/ja00281a025. Архивировано 10 марта 2023 года.
- ↑ Weiwei Zhang, Artem R. Oganov, Alexander F. Goncharov, Qiang Zhu, Salah Eddine Boulfelfel, Andriy O. Lyakhov, Elissaios Stavrou, Maddury Somayazulu, Vitali B. Prakapenka, Zuzana Konôpková. Unexpected Stable Stoichiometries of Sodium Chlorides (англ.) // Science. — 2013-12-20. — Vol. 342, iss. 6165. — P. 1502–1505. — ISSN 0036-8075. — doi:10.1126/science.1244989. Архивировано 7 сентября 2023 года.
- ↑ Взаимодействие хлора с водородом Архивная копия от 31 мая 2014 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ Получение хлора Архивная копия от 4 марта 2016 на Wayback Machine — видео опыта в Единой коллекции цифровых образовательных ресурсов
- ↑ Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 76. Хлор // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 184—187. — 240 с. — 1 630 000 экз.
- ↑ Взаимодействие хлора с органическими красителями Архивная копия от 14 июля 2014 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ СанПиН 2.1.4.1074-01. Дата обращения: 25 июля 2008. Архивировано 6 октября 2008 года.
- ↑ Вредные вещества в промышленности / Под ред. Н. В. Лазарева и И. Д. Гадаскиной. — М., 1977. — Т. 3. — С. 21—22.
Литература
[править | править код]- Некрасов Б. В. Основы общей химии, т. 3. — М.: Химия, 1970;
- Якименко Л. М. Производство хлора, каустической соды и неорганических хлорпродуктов, М., 1974;
- Постановление Госгортехнадзора России от 05.06.2003 № 48 «Об утверждении Правил безопасности при производстве, хранении, транспортировании и применении хлора» ПБ от 05.06.2003 09-594-03;
- Федеральный закон от 21.07.1997 № 116-ФЗО промышленной безопасности опасных производственных объектов (с изменениями на 18 декабря 2006 года);
- Постановление Госгортехнадзора России от 18.10.2002 № 61-А «Об утверждении Общих правил промышленной безопасности для организаций, осуществляющих деятельность в области промышленной безопасности опасных производственных объектов» ПБ от 18.10.2002 № 03-517-02;
- Приказ Минздрава РФ от 28 марта 2003 г. № 126 «Об утверждении Перечня вредных производственных факторов, при воздействии которых в профилактических целях рекомендуется употребление молока или других равноценных пищевых продуктов»;
- Приказ МПР РФ от 2 декабря 2002 г. № 786 «Об утверждении федерального классификационного каталога отходов» (с изм. и доп. от 30 июля 2003 г.);
- Постановление Госкомтруда СССР от 25.10.1974 № 298/П-22 «Об утверждении списка производств, цехов, профессий и должностей с вредными условиями труда, работа в которых дает право на дополнительный отпуск и сокращенный рабочий день» (с изменениями на 29 мая 1991 года);
- Постановление Минтруда России от 22.07.1999 № 26 «Об утверждении типовых отраслевых норм бесплатной выдачи специальной одежды, специальной обуви и других средств индивидуальной защиты работникам химических производств»;
- Постановление Главного государственного санитарного врача РФ от 30.05.2003 № 116 «О введении в действие ГН 2.1.6.1339-03 „Ориентировочные безопасные уровни воздействия (ОБУВ) загрязняющих веществ в атмосферном воздухе населенных мест“» (с изменениями на 3 ноября 2005 года);
- ГОСТ 6718-93 Хлор жидкий. Технические условия.
Ссылки
[править | править код]- Хлор на Webelements
- Хлор в Популярной библиотеке химических элементов
- Де Лазари А. Н. Первая германская газобаллонная атака на западноевропейском театре мировой войны у г. Ипра 22 апреля 1915 г. // Химическое оружие на фронтах Мировой войны 1914—1918 гг.: Краткий исторический очерк / А. Н. Де Лазари; Науч. ред. и коммент. М. В. Супотницкого. — М.: Вузовская книга, 2008. — 268 с. — 300 экз. — ISBN 978-5-9502-0314-5.
- Плаванье в хлорированной воде повышают риск возникновения астмы










































