Электрохимический градиент: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Djem92 (обсуждение | вклад) |
Djem92 (обсуждение | вклад) |
||
| Строка 6: | Строка 6: | ||
== Химия == |
== Химия == |
||
== Биологический контекст == |
== Биологический контекст == |
||
Генерация трансмембранного электрического потенциала, посредством движения ионов через клеточную мембрану, приводит к возникновению биологических процессов, таких как нервная проводимость, сокращение мышц, секрецию гормонов и сенсорных процессов. По соглашению, внутри типичной животной клетки имеется трансмембранный электрический потенциал между -50 мВ и -70 мВ<ref name=":0">{{Cite book|title=Lehninger Principles of Biochemistry|last=Nelson|first=David|last2=Cox|first2=Michael|publisher=W.H. Freeman|year=2013|isbn=978-1-4292-3414-6|location=New York|pages=464}}</ref>. |
|||
Электрохимические градиенты также играют определённую роль в установлении протонных градиентов [[Окислительное фосфорилирование|окислительного фосфорилирования]] в [[митохондрия]]х. Конечной стадией [[Клеточное дыхание|клеточного дыхания]] является [[цепь переноса электронов]]. Четыре встроенных комплексов во [[Внутренняя мембрана митохондрий|внутренней мембране митохондрии]] ([[Кристы|кристах]]) составляют цепь переноса электронов. Однако только комплексы I, III и IV являются протонным насосом из матрикса в межмембранное пространство (IMS). В общем, получается десять протонов, которые перемещается из матрикса в межмембранное пространство, генерируя электрохимический потенциал более 200 мВ. Это приводит в движение поток протонов обратно в матрикс посредством [[АТФ-синтаза|АТФ-синтазы]], которая синтезирует [[АТФ]] путём присоединения неорганического фосфата к молекуле [[АДФ]]. Таким образом, генерация протонного электрохимического градиента имеет решающее значение для синтеза энергии в митохондриях. Общее уравнение для цепи переноса электронов выглядит следующим образом: |
|||
<math>NADH + 11H^+ (matrix) + 1/2\ O_2 \longrightarrow NAD^+ + 10H^+ (IMS) + H_{2}O</math><ref>{{Cite book|title=Lehninger Principles of Biochemistry|last=Nelson|first=David|last2=Cox|first2=Michael|publisher=W.H. Freeman|year=2013|isbn=978-1-4292-3414-6|location=New York|pages=744}}</ref>. |
|||
Подобно цепи переноса электронов, в [[растения]]х является [[Световая фаза|световая фаза фотосинтеза]], где протонным насосом служит люмены (просветы [[тилакоид]]ов), расположенных в [[хлоропласт]]ах, служащий для управления генерации (выработки) молекул АТФ, посредством фермента АТФ-синтазы. Протонный градиент может быть сгенерирован с помощью любого нециклического или циклического фотофосфорилирования. Белки, которые участвуют в нециклическом фотофосфорилировании, фотосистемы II (ФСII ), пластахинон и [[цитохром-b6f-комплекс]] непосредственно способствуют генерации протонного градиента. На каждого из четырёх [[фотон]]ов, поглощаемых ФСII, приходится восемь протонов которые перекачивается в люмен (просвет тилакоида)<ref>{{Cite book|title=Lehninger Principles of Biochemistry|last=Nelson|first=David|last2=Cox|first2=Michael|publisher=W.H. Freeman|year=2013|isbn=978-1-4292-3414-6|location=New York|pages=769-770}}</ref>. Общее уравнение для фотосфорилирования выглядит следующим образом: |
|||
<math>2H_{2}O + 6H^+(stroma) + 2NADP^+ \longrightarrow O_2 +8H^+(lumen) + 2NADPH</math><ref>{{Cite book|title=Lehninger Principles of Biochemistry|last=Nelson|first=David|last2=Cox|first2=Michael|publisher=W.H. Freeman|year=2013|isbn=978-1-4292-3414-6|location=New York|pages=770}}</ref>. |
|||
Несколько других транспортёров и ионных каналов играют роль в генерации протонного электрохимического градиента. Одним из них является TPK<sub>3</sub>-калиевый ионный канал, активируемый ионами Са<sup>2+</sup> и перемещает ионы K<sup>+</sup> от люмена к строме, которые помогают установить градиент рН внутри стромы. С другой стороны, электронейтральный антипортер K<sup>+</sup> (KEA<sub>3</sub>) транспортирует ионы K<sup>+</sup> и Н<sup>+</sup> люмена в строму, тем самым создавая [[электрическое поле]]<ref>{{Cite journal|last=Höhner|first=Ricarda|last2=Aboukila|first2=Ali|last3=Kunz|first3=Hans-Henning|last4=Venema|first4=Kees|date=2016-01-01|title=Proton Gradients and Proton-Dependent Transport Processes in the Chloroplast|url=http://journal.frontiersin.org/Article/10.3389/fpls.2016.00218/abstract|journal=Plant Physiology|pages=218|doi=10.3389/fpls.2016.00218|pmc=4770017|pmid=26973667|volume=7}}</ref>. |
|||
== Ионный градиент == |
== Ионный градиент == |
||
[[Файл:Scheme sodium-potassium pump-en.svg|thumb|350px|Схема действия [[Na-K-АТФаза|Na<sup>+</sup>-K<sup>+</sup>-АТФазы]].]] |
[[Файл:Scheme sodium-potassium pump-en.svg|thumb|350px|Схема действия [[Na-K-АТФаза|Na<sup>+</sup>-K<sup>+</sup>-АТФазы]].]] |
||
Версия от 10:46, 30 августа 2016

Электрохимический градиент также градиент потенциала — градиент электрохимического потенциала, служащий для прохождения ионов через мембрану. Состоит из двух частей: химического градиента (градиента концентрации) или разницы в концентрации растворенного вещества, создаваемая через мембрану, и электрического градиента (мембранного потенциала) или разницы зарядов расположенных на противоположных сторонах мембраны. Градиент возникает вследствие неодинаковой концентрации ионов, расположенных на противоположных сторонах водопроницаемой мембраны. Ионы будут двигаться через мембрану из области, имеющую более высокую концентрацию в область с более низкой концентрацией, путём простой диффузии. Также ионы несут электрический заряд, который формирует электрический потенциал на мембране (мембранный потенциал). Если существует неравномерное распределение зарядов через мембрану, то разница в электрическом потенциале порождает силу, которая приводит к ионной диффузии, пока заряды не будут сбалансированы по обе стороны мембраны[1].
Обзор
Химия
Биологический контекст
Генерация трансмембранного электрического потенциала, посредством движения ионов через клеточную мембрану, приводит к возникновению биологических процессов, таких как нервная проводимость, сокращение мышц, секрецию гормонов и сенсорных процессов. По соглашению, внутри типичной животной клетки имеется трансмембранный электрический потенциал между -50 мВ и -70 мВ[2].
Электрохимические градиенты также играют определённую роль в установлении протонных градиентов окислительного фосфорилирования в митохондриях. Конечной стадией клеточного дыхания является цепь переноса электронов. Четыре встроенных комплексов во внутренней мембране митохондрии (кристах) составляют цепь переноса электронов. Однако только комплексы I, III и IV являются протонным насосом из матрикса в межмембранное пространство (IMS). В общем, получается десять протонов, которые перемещается из матрикса в межмембранное пространство, генерируя электрохимический потенциал более 200 мВ. Это приводит в движение поток протонов обратно в матрикс посредством АТФ-синтазы, которая синтезирует АТФ путём присоединения неорганического фосфата к молекуле АДФ. Таким образом, генерация протонного электрохимического градиента имеет решающее значение для синтеза энергии в митохондриях. Общее уравнение для цепи переноса электронов выглядит следующим образом:
[3].
Подобно цепи переноса электронов, в растениях является световая фаза фотосинтеза, где протонным насосом служит люмены (просветы тилакоидов), расположенных в хлоропластах, служащий для управления генерации (выработки) молекул АТФ, посредством фермента АТФ-синтазы. Протонный градиент может быть сгенерирован с помощью любого нециклического или циклического фотофосфорилирования. Белки, которые участвуют в нециклическом фотофосфорилировании, фотосистемы II (ФСII ), пластахинон и цитохром-b6f-комплекс непосредственно способствуют генерации протонного градиента. На каждого из четырёх фотонов, поглощаемых ФСII, приходится восемь протонов которые перекачивается в люмен (просвет тилакоида)[4]. Общее уравнение для фотосфорилирования выглядит следующим образом:
[5].
Несколько других транспортёров и ионных каналов играют роль в генерации протонного электрохимического градиента. Одним из них является TPK3-калиевый ионный канал, активируемый ионами Са2+ и перемещает ионы K+ от люмена к строме, которые помогают установить градиент рН внутри стромы. С другой стороны, электронейтральный антипортер K+ (KEA3) транспортирует ионы K+ и Н+ люмена в строму, тем самым создавая электрическое поле[6].
Ионный градиент
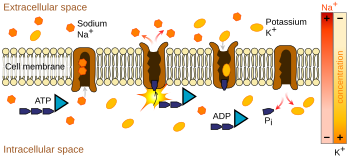
Так как ионы несут заряд, они не могут пройти через мембрану путём облегчённой диффузии. Для этого переноса ионов через мембрану, существуют два механизма: активный и пассивный транспорт. Примером активного транспорта ионов является Na+-K+-АТФаза (NKA). НКА катализирует реакцию гидролиза АТФ в АДФ и до неорганического фосфата Pi. При гидролизе одной молекулы АТФ выделяется энергия, которая изменяет конформацию фермента, так, чтобы три иона Na+ транспортировались наружу, а два иона K+ транспортируются во внутрь клетки. Это делает внутреннюю часть клетки более отрицательной, чем наружнюю, а точнее генерируется (создаётся) электрический потенциал (ЭДС) Vm ≈ -60мВ[7]. Примером пассивного транспорта является ионные потоки через ионные каналы (Na+, K+, Ca2+ и Cl- ионные каналы). Эти ионы имеют тенденцию двигаться вниз по градиенту концентрации. Например, так как существует высокая концентрация Na+ вне клетки, то ионы Na+, будут проходить через Na+-ионный канал во внутрь клетки. Поскольку электрический потенциал внутри клетки отрицательный, приток положительных ионов вызывают деполяризацию мембраны, вследствие чего происходит сдвиг трансмембранного электрического потенциала ближе к нулю. Однако ионы Na+ продолжат движение вниз по градиенту концентрации, до тех пор пока влияние химического градиента больше, чем влияние электрического потенциала. После того, как эффект обоих градиентов (химического и электрического) станет равным (Vm для Na+ составляет около +70мВ), приток ионов Na+ останавливается, потому что движущая сила (ΔG) равна нулю. Уравнение движущей силы выглядит следующим образом[8][9]:
.
Где, R — универсальная газовая постоянная, равная 8,3144598(48) Дж/(моль∙К); T - абсолютная температура (при н.у. = 298 K); Z — заряд иона, F — постоянная Фарадея, равная 96485 Кл/моль; Сin и Cext — соответственно концентрации ионов в ммоль/л, с наружной и внутренней стороны мембраны клетки; Vm — электрический потенциал (ЭДС) иона[10].
Протонные градиенты
Протонные градиенты в частности имеют важное значение, как одной из форм накопления энергии, во многих различных типах клеток. Градиент обычно используется для управления АТФ-синтазы, вращения жгутика, или перенос метаболитов[11]. В этом разделе основное внимание будет уделёно трём процессам, которые помогают установить протонные градиенты в соответствующих клетках: Бактериородопсина, нециклического фотофосфорилирования и окислительного фосфорилирования.
Бактериородопсин

Бактериородопсин в археях (Archaea) формирует путь для градиента протонов, посредством протонного насоса. Работа протонного насоса опирается на протонных носителей, которые движутся от стороны мембраны с низкой концентрацией ионов H+ к стороне с более высокой концентрацией H+. В бактериородопсине, протонный насос активируется путём поглощения фотонов с длиной волны 568 нм, это приводит к фотоизомеризации основания Шиффа в ретинале, вызывая его переход в K состояние. Фотоизомеризация чрезвычайно быстра и занимает всего 200 фс. Как следствие, родопсин претерпевает ряд быстрых конформационных перестроек: происходит перемещение основания Шиффа (SB) от остатков Asp85 и Asp212, вызывая передачу ионов H+ от SB к Asp85, при этом формируется состояние M1 (мета-I). Затем белок переходит к состоянию М2 (мета-II) посредством отделения остатка Glu204 от Glu194, который высвобождает протон во внешнюю среду. Такое состояние является сравнительно долгоживущим. Основание Шиффа репротонируется по остатку Asp85, формируя состояние N. Важно, что второй протон происходит от Asp96, так как его депротонированное состояние неустойчиво и быстро репротонируется протоном из цитоплазмы. Протонирование Asp85 и Asp96 приводят к повторной изомеризации SB, формируя при этом состояние O. Также при этом остаток Asp85 высвобождает свой протон на Glu204 и бактериородопсин возвращается в состояние покоя[11][12].
Фотофосфорилирование
Окислительное фосфорилирование
Примечания
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 403. — ISBN 978-1-4292-3414-6.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 464. — ISBN 978-1-4292-3414-6.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 744. — ISBN 978-1-4292-3414-6.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 769-770. — ISBN 978-1-4292-3414-6.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 770. — ISBN 978-1-4292-3414-6.
- ↑ Höhner, Ricarda; Aboukila, Ali; Kunz, Hans-Henning; Venema, Kees (2016-01-01). "Proton Gradients and Proton-Dependent Transport Processes in the Chloroplast". Plant Physiology. 7: 218. doi:10.3389/fpls.2016.00218. PMC 4770017. PMID 26973667.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Aperia, Anita; Akkuratov, Evgeny E.; Fontana, Jacopo Maria; Brismar, Hjalmar (2016-04-01). "Na+-K+-ATPase, a new class of plasma membrane receptors". American Journal of Physiology - Cell Physiology (англ.). 310 (7): C491—C495. doi:10.1152/ajpcell.00359.2015. ISSN 0363-6143. PMID 26791490.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 464-465. — ISBN 978-1-4292-3414-6.
- ↑ Eisenberg, Bob (2013-05-07). "Interacting Ions in Biophysics: Real is not Ideal". Biophysical Journal. 104 (9): 1849–1866. doi:10.1016/j.bpj.2013.03.049. PMC 3647150. PMID 23663828.
- ↑ Nelson, David. Lehninger Principles of Biochemistry / David Nelson, Michael Cox. — New York : W.H. Freeman, 2013. — P. 465. — ISBN 978-1-4292-3414-6.
- ↑ 1 2 Gunner, M. R.; Amin, Muhamed; Zhu, Xuyu; Lu, Jianxun (2013-08-01). "Molecular mechanisms for generating transmembrane proton gradients". Biochimica et Biophysica Acta (BBA) - Bioenergetics. Metals in Bioenergetics and Biomimetics Systems. 1827 (8—9): 892—913. doi:10.1016/j.bbabio.2013.03.001. PMC 3714358. PMID 23507617.
- ↑ Wickstrand, Cecilia; Dods, Robert; Royant, Antoine; Neutze, Richard (2015-03-01). "Bacteriorhodopsin: Would the real structural intermediates please stand up?". Biochimica et Biophysica Acta (BBA) - General Subjects. Structural biochemistry and biophysics of membrane proteins. 1850 (3): 536—553. doi:10.1016/j.bbagen.2014.05.021.


