Водородная связь
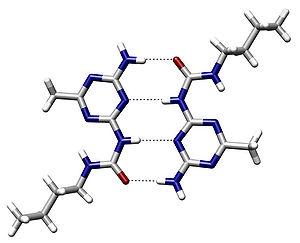
Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными. [1]
Природа водородной связи
Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи, невалентном взаимодействии между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR'. Результатом таких взаимодействий являются комплексы RA-H•••BR' различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR'.
Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность[2], её распространенность и важность, особенно в органических соединениях[3], а также некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода.
Ранее образование водородной связи обычно объясняли действием электростатических сил, то есть атом водорода, несущий слабый положительный заряд, притягивается к электроотрицательному атому, который несет небольшой отрицательный заряд. Теперь ученые склоняются к тому, что водородная связь может быть частично ковалентной - это означает, что при ее формировании происходит обобщение электронов водорода и второго образующего связь атома[4] .
История
В книге The Nature of the Chemical Bond Лайнуса Полинга, изданной в 1912 году, первый раз упоминается водородная связь. Мур и Винмилл использовали водородную связь, чтобы обосновать факт, что у гидроокиси тетраметиламмония более слабая основа, чем у гидроксида тетраметиламмония. Описание водородных связей в воде было сделано в 1920 году Латимером и Родебушем (JACS, 42, 1419).
Свойства
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак.
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB)±; так, для комплекса (H2O•H•OH2)+ образованного H2O и H3O+ — 132 кДж/моль в газовой фазе.
Водородная связь в воде
Механизм Гротгуса
Аномально высокая электропроводность и теплоёмкость воды, а также теплопроводность многоатомных спиртов обеспечивается многочисленными водородными связями. Одна молекула воды может образовать до четырёх классических водородных связей с соседями (с учётом бифуркатных Н-связей до 5-6).
Водородные связи повышают температуру кипения, вязкость и поверхностное натяжение жидкостей. Водородные связи ответственны за многие другие уникальные свойства воды.
Водные кластеры
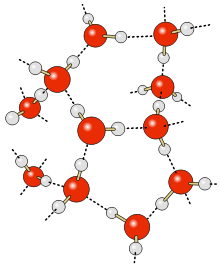
Согласно современным представлениям, наличие водородных связей между молекулами воды приводит к возникновению так называемых водных кластеров или комплексов. Простейшим примером такого кластера может служить димер воды:
Энергия водородной связи в димере воды составляет 0,2 эВ (≈ 5 ккал/моль), что всего на порядок больше, чем характерная энергия теплового движения при температуре 300 К. В то же время энергия ковалентной O-H связи в 200 раз больше тепловой энергии. Таким образом, водородные связи относительно слабы и неустойчивы: предполагается, что они могут легко возникать и исчезать в результате тепловых флуктуаций. Это, в частности, приводит к тому, что вода должна рассматриваться не как «простая», а как «связанная жидкость»: вода представляется как сеть молекул , соединённых водородными связями[5].
Водородная связь в нуклеиновых кислотах и белках
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты. В частности, элементы вторичной структуры (например, α-спирали, β-складки) и третичной структуры в молекулах белков, РНК и ДНК стабилизированы водородными связями. В этих макромолекулах, водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определенную форму. Например, двойная спиральная структура ДНК, определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
Водородная связь в полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример - нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.
См. также
Примечания
- ↑ Определение по IUPAC
- ↑ Энергия связи H … N = 8 кДж/моль, связи H … О — около 21 кДж/моль, связи H … F около 36 кДж/моль [1]. Для сравнения, энергия ковалентной связи — 400—900 кДж/моль [2]
- ↑ Например, водородными связями обусловлена форма молекулы ДНК
- ↑ Lenta.ru: Прогресс: Химики предложили изменить определение водородной связи
- ↑ Dominik Marx. Proton Transfer 200 Years after von Grotthuss: Insights fromAb Initio Simulations (англ.) // ChemPhysChem. — 2006. — Vol. 7. — P. 1848—1870. — doi:10.1002/cphc.200600128.
Литература
- Химическая Энциклопедия. Советская Энциклопедия, М., 1988
- В. В. Москва. Водородная связь в органической химии. Соросовский образовательный журнал, 11999,N 2, с.58-64 [3]

