Чумная палочка
| Чумная палочка | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
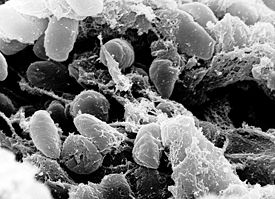 Yersinia pestis, электронная микрофотография | ||||||||||
| Научная классификация | ||||||||||
|
Домен: Тип: Класс: Порядок: Семейство: Род: Вид: Чумная палочка |
||||||||||
| Международное научное название | ||||||||||
| Yersinia pestis (Lehmann and Neumann 1896) van Loghem 1944 | ||||||||||
| Синонимы | ||||||||||
| ||||||||||
Чумна́я па́лочка (лат. Yersinia pestis) — вид грамотрицательных бактерий из семейства Yersiniaceae. Инфекционный агент бубонной чумы, также может вызывать чумную пневмонию и септическую чуму. Все три формы без современного лечения практически всегда заканчиваются летальным исходом и ответственны за высокий уровень смертности в эпидемиях, имевших место в истории человечества, таких как «Юстинианова чума» (100 миллионов жертв) и «Чёрная смерть», в ходе которой погибла треть населения Европы за промежуток с 1347 по 1353 годы.
Роль Yersinia pestis в «Чёрной смерти» дискутируется. Некоторые утверждают, что «Чёрная смерть» распространилась слишком быстро, чтобы быть вызванной Yersinia pestis[2][нет в источнике]. ДНК этой бактерии найдены в зубах умерших от «Чёрной смерти», тогда как тестирование средневековых останков людей, умерших по другим причинам, не дало положительной реакции на Yersinia pestis[3][4].
Род Yersinia — грамотрицательные коккобациллы размером примерно 1,5 мкм. Анилиновыми красителями окрашиваются биполярно (более интенсивно — на концах). Обладают ферментативным метаболизмом. Y. pestis производит антифагоцитарную слизь. Подвижная в культуре бактерия становится неподвижной, попав в организм млекопитающего.
Патоген хорошо переносит низкие температуры, замораживание; чувствителен к высушиванию, нагреванию, быстро разрушается под действием дезинфицирующих средств и при кипячении[5].
История[править | править код]

Y. pestis была открыта в 1894 году швейцарско-французским медиком и бактериологом Пастеровского института Александром Йерсеном во время эпидемии чумы в Гонконге. Йерсен был сторонником школы Пастера. Прошедший подготовку в Германии японский бактериолог Китасато Сибасабуро, практиковавший метод Коха, также в это время был привлечён к поискам агента, являющегося возбудителем чумы. Однако именно Йерсен фактически связал чуму с Y. pestis. Долгое время возбудителя чумы относили к роду Bacterium, позже — к роду Pasteurella. В 1967 году род бактерий, к которому относился возбудитель чумы, был переименован в честь Александра Йерсена.
Известны три биовара бактерии; полагают, что каждый соответствует одной из исторических пандемий чумы. Биовар antiqua считают ответственным за «Юстинианову чуму». Неизвестно, был ли этот биовар причиной более ранних, меньших эпидемий, или же эти случаи вообще не были эпидемиями чумы. Биовар medievalis полагают связанным с «Чёрной смертью». Биовар orientalis связывают с Третьей пандемией и большинством современных вспышек чумы.
По последним исследованиям «Юстинианова чума» была вызвана сразу несколькими штаммами бактерии, а не одной разновидностью[6].
В настоящее время только в России с 2001 по 2006 год зафиксировано 752 штамма возбудителя чумы[7].
Патогенность и иммунитет[править | править код]
Патогенность Yersinia pestis заключается в двух антифагоцитарных антигенах, называемых F1 и VW, оба существенны для вирулентности[8]. Эти антигены производятся бактерией при температуре 37 °C. Кроме этого, Y. pestis выживает и производит F1 и VW антигены внутри кровяных клеток, таких, например, как моноциты, исключением являются полиморфно-ядерные нейтрофильные гранулоциты[9].
Гены, ответственные за образование чумной F1-капсулы, были клонированы и секвенированы в 1990—1992 гг. сотрудниками Института инженерной иммунологии[10][11][12]. Там же был сконструирован штамм возбудителя, лишённый антигена F1, и который поэтому не может быть распознан соответствующими диагностикумами.
Некоторое время назад в США инактивированная формалином вакцина была доступна для взрослых, находящихся под большим риском заражения, однако затем продажи были прекращены по указанию Управления по санитарному надзору министерства здравоохранения США по причине низкой эффективности и вероятности серьёзного воспаления. Ведутся перспективные эксперименты в генной инженерии по созданию вакцины, основанной на антигенах F1[13] и VW, хотя бактерии, не имеющие антигена F1, сохраняют достаточную вирулентность, а антигены V достаточно изменчивы, так что вакцинация, основанная на этих антигенах может не давать достаточно полной защиты[14].
В России доступна живая вакцина на основе невирулентного штамма чумы[15].
Вакцинация не защищает от лёгочной чумы. Во время эпидемии 1910—1911 года применение прочумных сывороток (лимфы Хавкина и сыворотки Йерсена) лишь продлевало течение болезни на несколько дней, но не спасло жизнь ни одному больному[16]. Впоследствии учёным окончательно стало ясно, что гуморальный иммунитет при аэрогенном инфицировании возбудителем чумы значения не имеет[17].
После перенесённого заболевания остаётся прочный продолжительный иммунитет[18].
Геном[править | править код]
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis)[19], штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США)[20], штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 парных оснований, в штамме CO92 — 4 653 728 парных оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica, бактерия Y. pestis содержит плазмиды pCD1. Вдобавок, она также содержит плазмиды pPCP1 и pMT1, которых нет у других видов рода Yersinia. Перечисленные плазмиды и остров патогенности, названный HPI, кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов.
Древняя ДНК[править | править код]
В 2018 году в останках женщины из шведского местонахождения Frälsegården, умершей около 4900 лет назад (неолит) была обнаружена ДНК Yersinia pestis. Геном штамма из шведского захоронения выделился около 5700 лет назад, две ветви существующих сегодня штаммов Y. pestis выделились 5100 и 5300 лет назад[21].
Старейший штамм Yersinia pestis был найден в останках охотника-собирателя RV 2039 со стоянки Риннюкалнс (Riņņukalns) на реке Салаца в Буртниекском крае на севере Латвии, жившего пять тысяч лет назад (5300—5050 л. н.). Как показал генетический анализ, предок возбудителя чумы был поначалу менее контагиозным и не таким смертоносным[22][23]. У этого штамма нет гена, дающего способность передаваться от блох к людям. Видимо, человек заражался непосредственно от грызунов, например, от бобров[24].
В останках двух человек из Самарской области, связанных со покровской срубной культурой (около 3800 л. н.) нашли штамм Yersinia pestis, способный распространять бубонную чуму через блох[25]. Также ДНК Yersinia pestis нашли в останках человека из Капана (Армения), жившего в железном веке около 2900 лет назад[25].
Приобретённый горизонтальным переносом нитчатый фаг способствует патогенности чумной палочки[26]. В результате сравнения древних штаммов генов Yersinia pestis и её вероятного предка Yersinia pseudotuberculosis (псевдотуберкулёзная палочка) было выявлено, что Yersinia pestis мутировала из сравнительно безвредного микроорганизма около 10 тыс. лет назад. Выяснилось, что обитающая в почве Y. pseudotuberculosis, вызывающая лёгкое заболевание желудочно-кишечного тракта, приобрела тогда несколько генов, позволивших ей проникать в лёгкие человека. Далее, в ключевом гене Pla, кодирующего протеазу, произошла замена одной аминокислоты, в результате чего микроорганизм смог с повышенной силой разлагать белковые молекулы в легких и размножаться по всему организму через лимфатическую систему. Исследователи подозревают, что ген Pla чумная палочка позаимствовала у другого микроба в результате горизонтального обмена генами[27][28]. Это подтверждают и исследования датских и британских учёных, которые провели исследования молекул ДНК, извлечённых из зубов 101 человека бронзового века, обнаруженных на территории Евразии (от Польши до Сибири). Следы бактерии Y. pestis нашли в ДНК семи образцов возрастом до 5783 лет, при этом в шести из них отсутствовали «ген вирулентности» ymt (yersina murine toxin) и мутации в «гене активации» pla. В дальнейшем, на рубеже второго и первого тысячелетий до нашей эры, из-за демографических условий, выразившихся в увеличении плотности населения, возникла более летальная «бубонная» мутация бактерии[29][30].
Анализ ДНК из человеческих останков Кара-Джигача и Бурана (Киргизия) показал, что погребённые в иссык-кульских захоронениях 1338 года с надгробиями на сирийском языке умерли от того самого исходного штамма чумы, который и стал причиной Чёрной смерти. Современные штаммы, наиболее тесно связанные с древним штаммом, сегодня обнаруживаются в резервуарах чумы вокруг гор Тянь-Шаня[31].
Лечение[править | править код]
С 1947 года традиционным средством первого этапа лечения от Y. pestis были стрептомицин[32][33], хлорамфеникол или тетрациклин[34]. Также есть свидетельства положительного результата от использования доксициклина или гентамицина[35].
Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам, и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
Примечания[править | править код]
- ↑ 1 2 Species Yersinia pestis : [англ.] // LPSN. — Leibniz Institute DSMZ. (Дата обращения: 15 июля 2021).
- ↑ Ал Бухбиндер. Между чумой и эболой Архивная копия от 11 января 2018 на Wayback Machine — в статье, напечатанной в журнале «Знание—Сила» № 2 за 2002 год приводятся размышления, критикующие связь бактерии с чумой.
- ↑ Drancourt M., Aboudharam G., Signolidagger M., Dutourdagger O., Raoult D. Detection of 400-year-old Yersinia pestis DNA in human dental pulp: An approach to the diagnosis of ancient septicemia (англ.) // Proceedings of the National Academy of Sciences : journal. — National Academy of Sciences, 1998. — Vol. 95, no. 21. — P. 12637—12640. Архивировано 21 февраля 2007 года.
- ↑ Drancourt M., Raoult D. Molecular insights into the history of plague (англ.) // Microbes Infect.. — 2002. — Vol. 4. — P. 105—109.
- ↑ Чума: условия заражения, формы; УЗ «Столбцовская ЦРБ» Архивная копия от 21 мая 2021 на Wayback Machine.
- ↑ Researchers discover bacterial diversity in Justinianic Plague. Дата обращения: 6 июня 2019. Архивировано 5 июня 2019 года.
- ↑ Приказ территориального управления Роспотребнадзора по МО от 02.05.2006 N 100 «Об организации и проведении мероприятий по профилактике чумы на территории Московской области»
- ↑ Collins F. M. Pasteurella, Yersinia, and Francisella. In: Barron's Medical Microbiology (Barron S et al, eds.) (неопр.). — 4th ed.. — Univ of Texas Medical Branch, 1996.
- ↑ Salyers A. A., Whitt D. D. Bacterial Pathogenesis: A Molecular Approach (англ.). — 2nd ed.. — ASM Press, 2002. — P. 207—212.
- ↑ E. E. Galyov, O. Yu. Smirnov, A. V. Karlishev, K. I. Volkovoy, A. I. Denesyuk. Nucleotide sequence of the Yersinia pestis gene encoding F1 antigen and the primary structure of the protein: Putative T and B cell epitopes (англ.) // FEBS Letters. — 1990-12-17. — Vol. 277, iss. 1—2. — P. 230–232. — doi:10.1016/0014-5793(90)80852-A.
- ↑ E. E. Galyov, A. V. Karlishev, T. V. Chernovskaya, D. A. Dolgikh, O. Yu. Smirnov. Expression of the envelope antigen F1 of Yersinia pestis is mediated by the product of caf1M gene having homology with the chaperone protein PapD of Escherichia coli (англ.) // FEBS Letters. — 1991-07-29. — Vol. 286, iss. 1—2. — P. 79–82. — doi:10.1016/0014-5793(91)80945-Y.
- ↑ A. V. Karlyshev, E. E. Galyov, O. Yu. Smirnov, A. P. Guzayev, V. M. Abramov. A new gene of the ƒ1 operon of Y. pestis involved in the capsule biogenesis (англ.) // FEBS Letters. — 1992-02-03. — Vol. 297, iss. 1—2. — P. 77–80. — doi:10.1016/0014-5793(92)80331-A.
- ↑ Wei Sun, Shilpa Sanapala, Hannah Rahav, Roy Curtiss. Oral administration of a recombinant attenuated Yersinia pseudotuberculosis strain elicits protective immunity against plague (англ.) // Vaccine. — 2015-11. — Vol. 33, iss. 48. — P. 6727–6735. — doi:10.1016/j.vaccine.2015.10.074. Архивировано 14 августа 2022 года.
- ↑ Welkos S . et al. Determination of the virulence of the pigmentation-deficient and pigmentation-/plasminogen activator-deficient strains of Yersinia pestis in non-human primate and mouse models of pneumonic plague (англ.) // Vaccine : journal. — Elsevier, 2002. — Vol. 20. — P. 2206—2214. Архивировано 13 января 2004 года.
- ↑ Вакцина чумная живая сухая (Vaccine plague). Дата обращения: 30 августа 2011. Архивировано 29 сентября 2011 года.
- ↑ Супотницкий М. В., Супотницкая Н. С. Очерки истории чумы. Очерк XXXI. Эпидемия легочной чумы в Маньчжурии и Забайкалье (1910—1911) Архивная копия от 6 июля 2015 на Wayback Machine. — 2006.
- ↑ Супотницкий М. В., Супотницкая Н. С. Очерки истории чумы. Очерк XXXV. Эпидемии чумы в Маньчжурии в 1945—1947 гг. — перелом в лечении и в профилактике чумы Архивная копия от 6 июля 2015 на Wayback Machine. — 2006.
- ↑ "Профилактика чумы" Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека — федеральная служба Российской Федерации. Дата обращения: 6 марта 2020. Архивировано из оригинала 29 марта 2020 года.
- ↑ Deng W. et al. Genome Sequence of Yersinia pestis KIM (англ.) // American Society for Microbiology. — American Society for Microbiology, 2002. — Vol. 184, no. 16. — P. 4601—4611. Архивировано 11 октября 2008 года.
- ↑ Parkhill J . et al. Genome sequence of Yersinia pestis, the causative agent of plague (англ.) // Nature : journal. — 2001. — Vol. 413. — P. 523—527. Архивировано 2 января 2007 года.
- ↑ Nicolás Rascovan et al. Emergence and Spread of Basal Lineages of Yersinia pestis during the Neolithic Decline Архивная копия от 19 августа 2019 на Wayback Machine, 2018
- ↑ Julian Susat et al. A 5,000-year-old hunter-gatherer already plagued by Yersinia pestis Архивная копия от 2 июля 2021 на Wayback Machine // Cell. Volume 35, ISSUE 13, 109278, June 29, 2021
- ↑ В древнем черепе нашли старейший штамм смертоносной инфекции. Дата обращения: 30 июня 2021. Архивировано 17 июля 2021 года., 30 июня 2021
- ↑ Бобровая чума Архивная копия от 9 июля 2021 на Wayback Machine // Наука и жизнь
- ↑ 1 2 Maria A. Spyrou et al. Analysis of 3800-year-old Yersinia pestis genomes suggests Bronze Age origin for bubonic plague Архивная копия от 1 ноября 2021 на Wayback Machine // Nature Communications. Volume 9, Article number: 2234, 08 June 2018
- ↑ Derbise, A; Chenal-Francisque, V; Pouillot, F; Fayolle, C; Prévost, MC; Médigue, C; Hinnebusch, BJ; Carniel, E. A horizontally acquired filamentous phage contributes to the pathogenicity of the plague bacillus (англ.) // Mol Microbiol : journal. — 2007. — Vol. 63, no. 4. — P. 1145—1157. — doi:10.1111/j.1365-2958.2006.05570.x. — PMID 17238929.
- ↑ Чума возникла благодаря случайной мутации. Lenta.ru. Дата обращения: 23 октября 2015. Архивировано 23 октября 2015 года.
- ↑ Daniel L. Zimbler, Jay A. Schroeder, Justin L. Eddy & Wyndham W. Lathem. Early emergence of Yersinia pestis as a severe respiratory pathogen. nature.com. Дата обращения: 13 февраля 2016. Архивировано 2 февраля 2016 года.
- ↑ Древняя форма чумы оказалась неизвестным виновником катастроф бронзового века. Lenta.ru. Дата обращения: 23 октября 2015. Архивировано 23 октября 2015 года.
- ↑ Simon Rasmussen. Early Divergent Strains of Yersinia pestis in Eurasia 5,000 Years Ago. cell.com. Дата обращения: 13 февраля 2016. Архивировано 8 сентября 2019 года.
- ↑ Maria A. Spyrou et al. The source of the Black Death in fourteenth-century central Eurasia Архивная копия от 15 июня 2022 на Wayback Machine, 15 June 2022
- ↑ Wagle PM. Recent advances in the treatment of bubonic plague (неопр.) // Indian J Med Sci. — 1948. — Т. 2. — С. 489—494.
- ↑ Meyer KF. Modern therapy of plague (англ.) // JAMA. — 1950. — Vol. 144. — P. 982—985.
- ↑ Kilonzo B.S., Makundi R.H., Mbise TJ. A decade of plague epidemiology and control in the Western Usambara mountains, north-east Tanzania (англ.) // Acta Tropica : journal. — 1992. — Vol. 50. — P. 323—329.
- ↑ Mwengee W., Butler T., Mgema S., et al. Treatment of plague with gentamicin or doxycycline in a randomized clinical trial in Tanzania (англ.) // Clin Infect Dis : journal. — 2006. — Vol. 42. — P. 614—621.
Литература[править | править код]
- Козлов М. П. Чума (природная очаговость, эпизоотология, эпидемические проявления). — М.: Медицина, 1979. — 192 с.
- Кошель Елена Ивановна. Образование биопленки штаммами Yersinia pestis разных подвидов и их взаимодействие с членами почвенных биоценозов : Автореферат диссертации на соискание учёной степени кандидата биологических наук. — Саратов, 2014. — 22 с.
- Кутырев В. В.; Ерошенко Г. А.; Попов Н. В.; Видяева Н. А.; Коннов Н. П. Молекулярные механизмы взаимодействия возбудителя чумы с беспозвоночными животными // Молекулярная генетика, микробиология и вирусология. — 2009. — № 4. — С. 6—13 : 6 рис. — Библиогр.: с. 12—13 (39 назв.). — ISSN 0208-0613.