Доцетаксел
| Доцетаксел | |
|---|---|
| Docetaxel | |
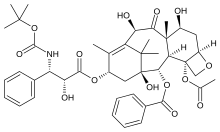 | |
| Химическое соединение | |
| ИЮПАК | (2R,3S)-N-Карбокси-3-фенилизосерин-N-трет-бутил-13-5бета,20-эпокси-1,2альфа,4,7бета,10бета,13альфа-гексагидрокситакс-11-ен-9-он-4- ацетат-2-бензоата тригидрат |
| Брутто-формула | C43H53NO14 |
| Молярная масса | 807.879 г/моль |
| CAS | 114977-28-5 |
| PubChem | 148124 |
| DrugBank | APRD00932 |
| Состав | |
| Классификация | |
| АТХ | L01CD02 |
| Фармакокинетика | |
| Биодоступн. | NA |
| Связывание с белками плазмы | >98% |
| Метаболизм | Hepatic |
| Период полувывед. | 86 часов |
| Экскреция | Biliary |
| Лекарственные формы | |
| концентрат для приготовления раствора для инфузий | |
| Другие названия | |
| Доцетаксел, Доцетера, Таксотер®, Таутакс | |
Доцетаксел — полусинтетическое цитостатическое лекарственное средство растительного происхождения из группы таксанов, получаемое путем химического синтеза из природного сырья — из игл тиса европейского (Taxus baccata). Активное вещество препарата накапливает тубулин в микротрубочках, препятствует их распаду, что приводит к нарушению фазы митоза и межфазных процессов в опухолевых клетках. Доцетаксел долго сохраняется в клетках, где достигаются его высокие концентрации. Доцетаксел активен в отношении некоторых (но не всех) клеток, продуцирующих в избыточном количестве р-гликопротеин, который кодируется геном множественной устойчивости. In vivo доцетаксел имеет широкий спектр активности в отношении опухолей мышей и перевиваемых опухолевых клеток человека.
Показания
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
- адъювантная терапия при операбельном раке молочной железы с поражением регионарных лимфоузлов в комбинации с доксорубицином и циклофосфамидом;
- местно распространенный или метастатический рак молочной железы (в комбинации с доксорубицином в качестве первичного химиотерапевтического лечения (1-я линия); или в качестве терапии 2-й линии: в монотерапии, при неэффективности предшествующего лечения, включавшего в себя антрациклины или алкилирующие средства, и в комбинации с капецитабином, если предшествующее лечение включало в себя антрациклины);
- метастатический рак молочной железы с опухолевой экспрессией НЕR2 в комбинации с трастузумабом, в случае отсутствия предшествующей химиотерапии;
- неоперабельный, местно распространенный или метастатический немелкоклеточный рак легких (в комбинации с цисплатином или карбоплатином) в качестве терапии 1-й линии или в монотерапии в качестве терапии 2-й линии при неэффективности химиотерапии, основанной на препаратах платины;
- метастатический рак яичников при неэффективности предшествующей терапии 1-й линии (терапия 2-й линии);
- метастатические плоскоклеточные злокачественные опухоли области головы и шеи при неэффективности предшествующего лечения (терапия 2-й линии)
- метастатический, гормонорезистентный рак предстательной железы (в комбинации с преднизоном или преднизолоном)
- метастатический рак желудка (в комбинации с цисплатином и др)