Умбеллиферон
| Умбеллиферон | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
7-гидроксихромен-2-он |
| Традиционные названия | 7-гидроксикумарин, скимметин |
| Хим. формула | C9H6O3 |
| Физические свойства | |
| Состояние | кристаллическое |
| Молярная масса | 162.14 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 229 (разл.) |
| Классификация | |
| Рег. номер CAS | 93-35-6 |
| PubChem | 5281426 |
| Рег. номер EINECS | 202-240-3 |
| SMILES | |
| InChI | |
| ChEBI | 27510 |
| ChemSpider | 4444774 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Умбеллиферон (7-гидроксикумарин, скимметин) — желтоватые кристаллы, хорошо растворимые в этаноле, хлороформе и уксусной кислоте, плохо растворим в воде и диэтиловом эфире.
Умбеллиферон впервые был обнаружен в растениях семейства Umbelliferae зонтичные, откуда и получил своё название. Содержится в значительном числе видов растений и является ключевым метаболитом в биосинтезе различных природных кумаринов, пиранокумаринов и фурокумаринов.
Синтез и свойства[править | править код]
Классический метод синтеза умбеллиферона — конденсация Пехмана яблочной кислоты и резорцина в присутствии серной кислоты[1], реакция идет через декарбоксилирование in situ яблочной кислоты с образованием формилуксусной кислоты, которая затем реагирует с резорцином
Подобно другим кумаринам, умбеллиферон интенсивно поглощает в ультрафиолетовой области, поглощение усиливается при образовании фенолята, который обуславливает ярко-голубую флуоресценцию щелочных растворов умбеллиферона, благодаря чему он используется в качестве кислотно-основного флуоресцентного индикатора при рН 6,5—8,0.
Нахождение в природе и биосинтез[править | править код]
Умбеллиферон в достаточно значительных количествах содержится в растениях семейств зонтичных, сложноцветных и подсемейства рутовых; может быть выделен из продуктов сухой перегонки зонтичных растений родов Ferula, Angelica и Heracleum. Кроме свободного умбеллиферона в растениях содержатся его гликозиды и его простые эфиры с сексвитерпеновыми спиртами («терпеновые кумарины», преимущественно в растениях рода Ferula).
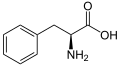
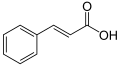
Биосинтез идет по фенилпропаноидному пути из фенилаланина, из которого синтезируется коричная кислота, подвергающаяся гидроксилированию в положение 4 под действием фермента циннамат-4-гидрокислазы. Образующаяся в результате p-кумаровая кислота гидроксилируется по положению 2 при катализе циннамит/кумарат-2-гидроксилазы с образованием 2,4-дигидроксикумаровой (умбелловой) кислоты. Внутримолекулярное ацилирование 2-гидроксигруппы карбоксилом умбелловой кислоты приводит к образованию лактона — умбеллиферона[2]:
Примечания[править | править код]
- ↑ George, Ernest; J. Moir. The Preparation of Umbelliferone (неопр.) // Transactions of the Royal Society of South Africa. — 1925. — Т. 13, № 3. — С. 255—257. — ISSN 0035-919X. — doi:10.1080/00359192509519609.
- ↑ Pathway: umbelliferone biosynthesis // MetaCyc
Это заготовка статьи по органической химии. Помогите Википедии, дополнив её. |
Это заготовка статьи по биохимии. Помогите Википедии, дополнив её. |