Полярные вещества
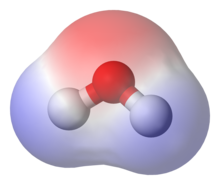
Поля́рные вещества́ в химии — соединения, молекулы которых обладают электрическим дипольным моментом. Для полярных веществ, в сравнении с неполярными, характерны высокая диэлектрическая проницаемость (более 10 в жидкой фазе), повышенные температура кипения и температура плавления.
Дипольный момент обычно возникает вследствие разной электроотрицательности составляющих молекулу атомов, из-за чего связи в молекуле приобретают полярность. Однако для приобретения дипольного момента требуется не только полярность связей, но и соответственное их расположение в пространстве. Молекулы, имеющие форму, подобную молекулам метана CH4 (∠HCH = 109,5°, правильный тетраэдрический), триоксида серы SO3 (∠OSO = 120°, правильный треугольный) либо диоксида углерода CO2 (∠OCO = 180°, линейный), а также фторида серы(VI) (все углы ∠FSF = 90°, правильный октаэдрический), являются неполярными.
Полярные растворители наиболее охотно растворяют полярные вещества, а также обладают способностью сольватировать. Примерами полярного растворителя являются вода, спирты и другие вещества.
См. также[править | править код]
Это заготовка статьи по химии. Помогите Википедии, дополнив её. |
В статье не хватает ссылок на источники (см. рекомендации по поиску). |