Дисилицид титана
| Дисилицид титана | |
|---|---|
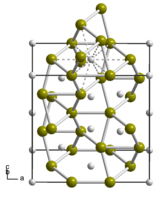 | |
| Общие | |
| Систематическое наименование |
дисилицид титана |
| Хим. формула | TiSi2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 104,08 г/моль |
| Плотность | 4,04 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1540 °C |
| Мол. теплоёмк. | 53,96 Дж/(моль·К) |
| Теплопроводность | 45,9 Вт/(м·K) |
| Энтальпия | |
| • образования | 135,14 кДж/моль |
| Классификация | |
| Рег. номер CAS | 12039-83-7 |
| PubChem | 6336889 |
| Рег. номер EINECS | 234-904-3 |
| SMILES | |
| InChI | |
| ChemSpider | 4891882 и 8329526 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дисилицид титана — химическое соединение металла титана и кремния с формулой TiSi2. Содержание кремния в дисилициде титана составляет 53,98 % по массе[1].
Получение[править | править код]
Дисилицид титана можно получить одним из следующих способов[2].
- Непосредственным насыщением титана кремнием:
- В качестве исходных компонентов используют порошки титана и кремния. В связи с экзотермичностью реакции подъем температуры ведут медленно и с промежуточными выдержками при температуре 700—800 °C. При достижении температуры 1200 °C делают окончательную выдержку в течение 1—2 часов.
- Восстановлением оксида титана кремнием с последующим силицированием:
- Процесс восстановления оксида титана кремнием проводят при температуре 1400 °C и выдержке 1,5—2 часа. Процесс образования дисилицида титана идет по реакции:
- При замене чистого кремния на его оксид для восстановления могут быть использованы графит и карбид кремния. При этом реакция имеет следующий вид:
- Синтезом из растворов в металлических расплавах:
- Для процесса образования силицида используют вспомогательную расплавленную металлическую ванну цинка. При этом цинк при температуре процесса 700—900 °C сравнительно хорошо растворяет исходные компоненты, в результате чего в расплаве происходит реакция образования дисилицида титана. По окончании процесса расплав охлаждают и химическим путём отделяют силицид от цинка. Этим способом могут быть получены монокристаллы TiSi2.
- Осаждением из газовой фазы:
- Суть метода заключается в восстановлении тетрахлоридов титана и кремния, находящихся в газовой фазе, водородом и осаждением их на нагретой поверхности. Процесс ведут в температуре 900−1300 °C.
- Электролизом расплавленных сред:
- Исходными компонентами и средой процесса является 10% раствор диоксида титана в расплавленном гексафторосиликате калия (K2SiF2), электролиз которого позволяет получить мелкодисперсные кристаллы силицида[3].
Физические свойства[править | править код]
Дисилицид титана представляет собой порошок железно−серого цвета. Имеет две полиморфные модификации.
Низкотемпературная метастабильная модификация (C49) имеет ромбическую базоцентрированную решетку, пространственная группа Cmcm, периоды решетки а = 0,362 нм, b = 1,376 нм, c = 0,360 нм[4]. Образование метастабильной модификации имеет место при получении тонких плёнок TiSi2 на подложке из кристалла кремния при температуре 450—600 °C. При нагреве свыше 650 °C низкотемпературная модификация переходит в высокотемпературную[5].
Высокотемпературная модификация (C54) является стабильной и имеет ромбическую гранецентрированную решетку, пространственная группа Fddd, периоды решетки а = 0,8279 нм, b = 0,4819 нм, c = 0,8568 нм.
- Удельное электрическое сопротивление низкотемпературной и высокотемпературной фаз составляет 60—70 мкОм•см и 12—20 мкОм•см, соответственно[6]
- Коэффициент линейного теплового расширения 12,5•10−6 1/K при 200—1200 °C
- Микротвёрдость 8,75 ГПа
- Модуль упругости 259 ГПа[1]
Химические свойства[править | править код]
Дисилицид титана является химически стойким по отношению к азотной, серной, соляной, щавелевой кислотам. Не растворяется в воде и в разбавленных растворах щелочей. Слабо взаимодействует с царской водкой. Дисилицид титана растворяется в плавиковой кислоте и в её смеси с азотной кислотой, а также в растворах фтористого аммония и в щелочных растворах в присутствии винного и лимонного натра и трилона Б [2].
Реагирует с ортофосфорной кислотой по реакции:
Окисляется кислородом при температуре свыше 700 °C. С хлором и фтором взаимодействует при высоких температурах (900 °C в случае хлора)[1][3].
Применение[править | править код]
Благодаря низкому электросопротивлению и высокой термической стабильности (фаза C54) используется в виде контактов между полупроводниковым устройством и структурой, поддерживающей межсоединения, в производстве сверхбольших интегральных схем[6][7].
Примечания[править | править код]
- ↑ 1 2 3 Самсонов Г. В., Виницкий И. М. Тугоплавкие соединения (справочник). — Металлургия, 1976. — С. 560.
- ↑ 1 2 Самсонов Г. В., Дворина Л. А., Рудь Б. М. Силициды. — Металлургия, 1979. — С. 9-144. — 272 с.
- ↑ 1 2 Лучинский Г. П. Химия титана. — Химия, 1971. — С. 164-166. — 472 с.
- ↑ Лучинский Г. П. Химия титана. — Химия, 1971. — С. 183-185. — 472 с.
- ↑ Yoon S., Jeon H. A study on the change in the phase transition temperature of TiSi2 by adding the Zr element on different Si substrates // J. Korean Phys. Soc. – 1999. – Vol. 34, No. 4. – P. 365-370.
- ↑ 1 2 Clevenger L. A. et al. Study of C49-TiSi2 and C54-TiSi2 formation on doped polycrystalline silicon using in situ resistance measurements during annealing // J. Appl. Phys. – 1994. – Vol. 76, No. 12. – P. 7874-7881.
- ↑ Технология «Salicide». Дата обращения: 9 февраля 2013. Архивировано из оригинала 20 июня 2018 года.


