Нитроцеллюлоза
В статье не хватает ссылок на источники (см. рекомендации по поиску). |
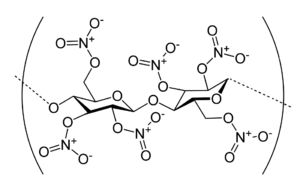
Нитроцеллюло́за (нитрат целлюлозы, нитроклетчатка) — групповое название химических соединений, азотнокислых сложных эфиров целлюлозы с общей формулой , где х — степень замещения (этерификации), а n — степень полимеризации.
Общие сведения
[править | править код]Нитроцеллюлоза — волокнистая рыхлая масса белого цвета, по внешнему виду похожа на целлюлозу. Одна из важнейших характеристик — степень замещения гидроксильных групп на нитрогруппы. В практике чаще всего применяется не прямое обозначение степени замещения, а содержание азота, выраженное в процентах по массе. В зависимости от содержания азота различают[источник не указан 3874 дня]
- коллоксилин, коллоидный хлопок или коллодий (10,7—12,2 % азота)[1];
- пироксилин № 2 (12,05—12,4 % азота);
- пироколлодий (12,6 % азота) — впервые получен Д. И. Менделеевым (1890), нерастворим в спирте, растворяется в смеси спирта с эфиром[1];
- пироксилин № 1 (13,0—13,5 % азота).
И. М. Чельцов в статье для энциклопедического словаря Брокгауза и Ефрона перечисляет следующие азотные эфиры целлюлозы, из которых первые два нерастворимы и образуют основную массу пироксилина, а остальные, растворимые, входят в состав коллодия[2]:
| Тривиальное название | Химическая формула | Содержание азота | |
|---|---|---|---|
| теоретическое | достижимое | ||
| 12-азотная клетчатка | 14,14% | 13,4%[3] | |
| 11-азотная клетчатка | 13,47% | 13,3% | |
| 10-азотная клетчатка | 12,75% | 12,5%—12,7% | |
| 9-азотная клетчатка | 11,96% | ||
| 8-азотная клетчатка | 11,11% | ||
| … | и так далее | … | |
| 4-азотная клетчатка | 6,76% | ||
Плотность 1,58—1,65 г/см³. Степень полимеризации коллоксилина 150—600 (молекулярная масса 37500—150000 а. е. м.), пироксилинов 1000—2000 (молекулярная масса 250000—500000 а. е. м.). Универсальный растворитель для всех видов нитроцеллюлозы — ацетон. В воде и неполярных растворителях (бензол, четырёххлористый углерод) нитроцеллюлоза не растворяется. Растворимость нитроклетчатки в полярных растворителях зависит от содержания азота. В кислых и щелочных средах она имеет низкую химическую стойкость.
Температура начала разложения сухой нитроцеллюлозы 40—60 °C, при быстром нагреве может произойти вспышка и взрыв. Самовозгорание сухой нитроцеллюлозы стало причиной многих техногенных катастроф, от взрывов пороховых заводов в XIX веке до взрывов в Тяньцзине в 2015 году.
История открытия
[править | править код]Нитроцеллюлоза — один из первых искусственных полимеров.
- 1832 — французский химик Анри Браконно обнаружил, что при обработке крахмала и древесных волокон азотной кислотой образуется нестойкий горючий и взрывоопасный материал, который он назвал ксилоидин (Xyloїdine)
- 1838 — другой французский химик, Теофиль-Жюль Пелуз, обработал подобным образом бумагу и картон и получил похожий материал[2], названный им Нитрамидином (Nitramidine). Низкая стабильность полученной нитроцеллюлозы не позволяла использовать её в технических целях.
- 1846 — швейцарский химик Кристиан Фридрих Шёнбейн случайно обнаружил более практичный способ получения нитроцеллюлозы[2]. Во время работы в кухне он пролил концентрированную азотную кислоту на стол. Для удаления кислоты химик воспользовался хлопковой тряпкой, а затем повесил её сушиться на печь. После высыхания ткань сгорела со взрывом. Шёнбейн разработал первый приемлемый способ получения нитроцеллюлозы — обработкой одной части хлопковых волокон в пятнадцати частях смеси серной и азотной кислот в соотношении 50:50. Азотная кислота реагировала с целлюлозой с образованием воды и серная кислота была необходима для предотвращения разбавления. После нескольких минут обработки хлопок удалялся из кислоты, промывался в холодной воде до удаления кислот и высушивался. Полученный новый материал незамедлительно был применён в производстве пороха под названием ружейного хлопка (Guncotton). Нитроцеллюлоза давала в 6 раз больший объём продуктов горения, чем дымный порох, намного меньше дыма и меньше нагревала оружие. Однако производство её было крайне опасным и сопровождалось многочисленными взрывами на производствах. Дальнейшие исследования показали, что ключевую роль в опасности производства играет чистота сырья — если хлопок не был тщательно очищен и высушен, происходили внезапные взрывы.
- 1869 — в Англии под руководством Фредерика Августа Абеля[2] была разработана технология с измельчением нитроцеллюлозы в специальных аппаратах — голландерах и многократными (до 8 раз) длительными промывками и сушками, каждая из которых длилась до 2 суток. Голландер представляет собой овальную в сечении ванну с закрепленными в ней поперечными ножами. Сбоку от ножей проходит вал с волнистыми дисковыми ножами. При вращении вала ножи вала проходят в промежутках между неподвижными ножами и режут волокно нитроцеллюлозы. Соотношение серной и азотной кислот в смеси было изменено до 2:1. По такой технологии удавалось получать достаточно стабильный при хранении и применении продукт. Спустя десять лет после патентования этой технологии во всем мире начали принимать на вооружение пироксилин, сначала в качестве начинки снарядов и морских мин. Другое применение, которое коллоксилин нашел практически сразу — производство клея для заклеивания небольших ранок. За неимением пластыря (в нашем сегодняшнем понимании), этот клей достаточно быстро обрел популярность. Фактически, это была разновидность густого нитролака.
Последовавшая в течение нескольких лет после этого серия взрывов на предприятиях и складах, занятых процессами с участием пироксилина, заставили пристальнее взглянуть на проблему стабилизации этого продукта. Несмотря на все сложности, с 1879 года и по сей день нитраты целлюлозы находят широкое применение в технологии энергонасыщенных соединений и многих других областях промышленности.
Получение
[править | править код]Лучшим сырьём для производства нитроцеллюлозы считаются длинноволокнистые сорта хлопка ручной сборки. Хлопок машинной сборки и древесная целлюлоза содержат значительное количество примесей, усложняющих подготовку и снижающих качество продукции.
Нитроцеллюлозу получают действием в реакторах из нержавеющей стали на очищенную, разрыхлённую и высушенную целлюлозу (хлопка, льна или древесную) смесью серной и азотной кислот, называемой нитрующей смесью, или «меланжем», в которой содержится по молям 2:1:2 азотной кислоты, серной кислоты и воды. Вместо серной кислоты в качестве водоотнимающего может быть использована концентрированная фосфорная кислота или пентоксид фосфора. При температурах 20—35 °C реакция протекает за 1½—½ часа[3].

Ниже приведена реакция получения тринитроцеллюлозы в лабораторных условиях:

Концентрация применяемой азотной кислоты обычно выше 77 %, а соотношение кислот и целлюлозы может быть от 30:1 до 100:1. Полученный после нитрования продукт подвергается многоступенчатой промывке, обработке слабокислыми и слабощелочными растворами, измельчению для повышения чистоты и стойкости при хранении. Сушка нитроцеллюлозы — сложный процесс, иногда совместно с сушкой применяется обезвоживание (этанолом, спирто-эфирными смесями). Практически вся нитроцеллюлоза после получения используется в производстве различных продуктов. В случае необходимости хранится во влажном состоянии с содержанием воды или спирта не ниже 20 %.
Промышленный метод получения нитроцеллюлозы
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
В промышленности применяют барабанные непрерывно действующие аппараты противотока, по принципу «карусели». Суть их работы заключается в подаче целлюлозного волокна с одной стороны, а нитрующей смеси с другой, противотоком. При этом нитрующая смесь орошает плоский вертикальный барабан, заполненный целлюлозным волокном, сверху. Смесь стекает из данной секции в секцию поддона, откуда подаётся в следующую секцию насосом. И так до 30—40 секций. Барабан медленно вращается, в одной точке происходит непрерывная разгрузка продукта, в другой точке — загрузка целлюлозы.
Существует разновидность такого аппарата, работающая не на принудительной перекачке кислотной смеси, а под действием центробежных сил – нитратор-центрифуга. Этот аппарат менее удобен в настройке, но он значительно компактнее, дешевле в изготовлении и позволяет быстрее отжимать кислоту из готового продукта.
Такой процесс позволяет достичь выхода до 30—45 % по азотной кислоте. При этом отработанная кислотная смесь, содержащая до 25 % воды и 10 % азотной кислоты (остальное — серная кислота), направляется на регенерацию в перегонный аппарат. При температуре упаривания серной кислоты под небольшим вакуумом (около 200 °C) происходит разрушение нитротел (побочные продукты нитрования любой органики, неустойчивые нитро-, нитрозо- и нитратные производные) до оксидов углерода и азота, а также воды и смолистых обугленных веществ. Оксиды азота и вода улавливаются во влажном скруббере и идут на производство неорганических нитратов, а упаренная до 96—98 % серная кислота возвращается в процесс для приготовления новой партии нитрующей смеси.
Полученную нитроцеллюлозу транспортируют, хранят и используют в виде колоксилиново-водной взвеси (КВВ). Содержание коллоксилина в этом материале — 10—15 %, по свойствам КВВ напоминает среднее между манной кашей и густым клеем ПВА. Больше всего напоминает бумажную пульпу, но с мелким волокном.
Колоксилиново-водную взвесь после отмывки от кислот накапливают в смесителях – ёмкостях объёмом 100—350 м³, снабженных мешалками, чтобы коллоксилин не оседал и качество партии усреднялось. После перемешивания в течение нескольких часов отбирают пробу на уточнение свойств, главным образом молекулярной массы, содержания азота и кислот. Также берут иодкрахмальную пробу на устойчивость. Для использования в чистом виде нитроцеллюлозу отделяют от воды на барабанных фильтрах, при этом влажность материала составляет около 50 %. В таком виде нитроцеллюлозу можно транспортировать в различной таре. Для дополнительного обезвоживания нитроцеллюлозу отжимают на центрифуге при 800—1000 об./мин. При этом получается нитроцеллюлоза с влажностью около 6—8 %. Дальнейшее обезвоживание проводят промывкой этиловым спиртом на специальной центрифуге. При этом спирт подаётся в центр барабана и двигается к периферии под действием центробежных сил. Спирт регенерируют ректификацией.
Для получения баллиститных или сферических порохов используют непосредственно колоксилиново-водную взвесь. Для производства сферических порохов можно применять и отжатую до 10 % влажности нитроцеллюлозу, при этом отдельная проблема состоит в том, что при диспергировании порохового лака в водной фазе и последующего отверждения гранул пороха приводит к капсулированию некоторого количества воды внутри пороха. Некоторую сложность в получении нитратов целлюлозы составляет высокая впитывающая способность целлюлозы при неоднородности её структуры и плотности волокна. Это вынуждает применять 50—100-кратный избыток нитрующей смеси. Если это терпимо для лабораторий, то совершенно неприемлемо для промышленного производства.
Очистка и стабилизация нитроцеллюлоз
[править | править код]Варка нитроцеллюлоз при 90—95 °C в проточном реакторе. При этом происходит разрушение малоустойчивых соединений и вымывание продуктов распада. Кроме того, горячая вода легче проникает в структуру нитроцеллюлозы. Недостаток этого процесса состоит в деструкции нитроцеллюлозы до продуктов низкой молекулярной массы (5—20 структурных звеньев). Поэтому этим процессом не злоупотребляют, особенно если нужен продукт с хорошими физико-механическими свойствами (например, для пироксилиновых порохов или дистанционных трубок).
Другая технология стабилизации нитроцеллюлоз состоит в перекристаллизации нитроцеллюлозы из органических растворителей в присутствии раствора соды. В отличие от предыдущего процесса, этот процесс ведётся при низких температурах (10—25 °C), но очень продолжительное время и при интенсивном перемешивании. После стабилизации центрифугируют раствор соды, полученный раствор пироксилина в органике идёт на обезвоживание и дальнейшее использование.
Для увеличения срока годности в нитроцеллюлозу (в готовом продукте) вводятся стабилизаторы химической стойкости, главным образом централиты, дифениламин, камфору. Раньше использовали также амиловый спирт, канифоль, аминные производные нафталина и др., но они показали низкую эффективность. Главная функция стабилизаторов – связывание образующейся при разложении азотной кислоты и оксидов азота.
Применение
[править | править код]Нитроцеллюлоза производится в больших количествах во многих странах мира и находит много различных применений:
- Бездымный порох, обычно пироксилин. Существует множество типов бездымного пороха, которые ранее широко использовались в военных целях (баллистит, кордит).
- Взрывчатые вещества. Нитроцеллюлоза в чистом виде из-за низкой термической стойкости не применяется, но используется как составной компонент взрывчатки. В 1885 году была впервые получена смесь нитроцеллюлозы с нитроглицерином, названная «гремучим студнем».
- Ранее использовалась как подложка фото- и киноплёнки[3]. В связи с горючестью была вытеснена ацетилцеллюлозой и полиэтилентерефталатом (лавсаном).
- Целлулоид. До 2010-х годов шарики для настольного тенниса производились из нитроцеллюлозы.
- Нитроцеллюлозные мембраны для иммобилизации белков.
- В индустрии развлечений для производства быстросгорающих предметов в реквизите артистов иллюзионного жанра.
- Нитроцеллюлозные мембраны используют для гибридизации нуклеиновых кислот, например, при Саузерн-блоттинге.
- Плёнкообразующая основа нитроцеллюлозных лаков, красок, эмалей.
См. также
[править | править код]Источники
[править | править код]- ↑ 1 2 Д. И. Менделеев. Основы химии. — 11. — М.—Л.: государственной химико-техническое издательство, 1932. — Т. 1. — С. 366-367. — 488 с.
- ↑ 1 2 3 4 Нитроклетчатка // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907. — Т. 21. — С. 179—189.
- ↑ 1 2 3 Brockhaus ABC Chemie in zwei Bänden (нем.). — Leipzig: VEB F. A. Brockhaus Verlag, 1966. — Bd. 2. — С. 1551. — 1590 с.
![{\displaystyle {\ce {[C6H7O2(OH)_{3-x}(ONO2)_{x}]_{n}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6a0b4733ee88202733d9f7fbb3504ead8b4ba99c)





