Продукт реакции
Продукты — это вещества, образующиеся в результате химических реакций[1]. В ходе химической реакции реагенты превращаются в продукты после прохождения высокоэнергетического переходного состояния. Этот процесс приводит к поглощению реагентов. Это может быть самопроизвольная реакция или реакция опосредованная катализаторами, снижающими энергию переходного состояния, и растворителями, создающими химическую среду, необходимую для протекания реакции. При представлении в химических уравнениях продукты обычно изображаются справа, даже в случае обратимых реакций[2]. Свойства продуктов, такие как их энергия, помогают определить некоторые характеристики химической реакции, например, является ли реакция экзергонической или эндергонической . Кроме того, свойства продукта могут облегчить его экстракцию и очистку после химической реакции, особенно если продукт имеет другое состояние вещества, чем реагенты.
|
Самопроизвольная реакция
|
Каталитическая реакция
|
Большая часть химических исследований сосредоточена на синтезе и характеристике полезных продуктов, а также на обнаружении и удалении нежелательных продуктов. Химиков-синтетиков можно разделить на химиков-исследователей, которые разрабатывают новые химические вещества и методы синтеза химических веществ, а также на химиков-технологов, которые расширяют химическое производство и делают его более эффективным, экологически устойчивым и более безопасным[3]. Отдельной областью является химия природных соединений, в которой химики выделяют продукты, созданные живыми организмами, характеризуют и изучают их роль в природных процессах.
Определение реакции[править | править код]
Продукты химической реакции влияют на несколько аспектов реакции. Если продукты имеют меньшую энергию, чем реагенты, то в реакции будет выделяться избыточная энергия, что делает её экзергонической реакцией. Такие реакции термодинамически благоприятны и имеют тенденцию протекать сами по себе. Однако если энергия активации реакции достаточно высока, то реакция может протекать слишком медленно, чтобы ее можно было наблюдать, или даже не происходить вовсе. Это имеет место в случае превращения при атмосферном давлении алмаза в графит, имеющий более низкую энергию: в такой реакции алмаз считается метастабильным, и его превращение в графит не наблюдается[4][5].
Если продукты имеют более высокую химическую энергию, чем реагенты, то для проведения реакции потребуется энергия — такая реакция будет эндергонической. Кроме того, если продукт менее стабилен, чем реагент, то предположение Леффлера гласит, что переходное состояние будет больше похоже на продукт, чем на реагент[6]. Иногда свойства продукта значительно отличаются от свойств реагента, и его можно легко выделить и очистить после проведеня реакции, например, когда продукт нерастворим и выпадает в осадок из раствора, в то время как реагенты остаются растворенными.
История[править | править код]
С середины девянадцатого века химики начали активно заниматься синтезом химических веществ[7]. Этому предшестовал этап выделения химических соединений из природных источников и накопления знаний об их свойствах и химическом составе, после чего была сформирована атомно-молекулярная теория, которая служит теоретической основой современной химии. Большая часть синтетической химии связана с получением новых химических веществ, например, при создании новых лекарств, и открытием новых методов синтеза. В конце 19 века — начале 20 века значительное внимание химиков стало уделяться масштабированию синтетических процессов, с целью получения в крупнотоннажном объеме значимой для народного хозяйства химической продукции. Это потребовало решение вопросов, связанных с аппаратным оформлением химических процессов, выработки наиболее экономически обоснованных и безопасных для персонала и окружающей среды решений в области химических производств, что реализовалось в выделении химической технологии в отдельную область химии, а химической промышленности — в отдельную индустриальную отрасль.
Биохимия[править | править код]
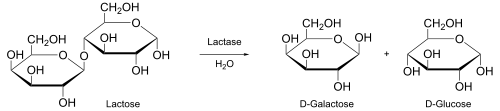
В биохимии ферменты действуют как биологические катализаторы превращения субстрата в продукт.[8] Например, продуктами фермента лактазы являются галактоза и глюкоза, которые образуются из субстрата лактозы .
- где S — субстрат, P — продукт, E — фермент.
Продуктовый промискуитет[править | править код]
Некоторые ферменты проявляют форму промискуитета, когда они превращают один субстрат в несколько разных продуктов. Это происходит, когда реакция протекает через переходное состояние с высокой энергией, которое с примерно равной вероятностью может вести к различным химическим продуктам[9].
Ингибирование продуктов[править | править код]
Некоторые ферменты ингибируются продуктами реакций, которые они катализируют, что снижает их каталитическую активность[10]. Это может иметь важное значение в регуляции метаболизма как форма отрицательной обратной связи, контролирующая его направления[11]. Ингибирование под действием продукта реакции также является важной темой в биотехнологии, так как преодоление этого эффекта может увеличить выход производимого вещества[12].
См. также[править | править код]
Ссылки[править | править код]
- ↑ McNaught, A. D. [product] Compendium of Chemical Terminology, 2nd ed. (the "Gold Book" / A. D. McNaught, A. Wilkinson. — Blackwell Scientific Publications, Oxford, 2006. — ISBN 978-0-9678550-9-7. — doi:10.1351/goldbook.
- ↑ McNaught, A. D. [chemical reaction equation] Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") / A. D. McNaught, A. Wilkinson. — Blackwell Scientific Publications, Oxford, 2006. — ISBN 978-0-9678550-9-7. — doi:10.1351/goldbook.
- ↑ Henry, Celia M. "DRUG DEVELOPMENT". Chemical and Engineering News. Архивировано из оригинала 9 мая 2019. Дата обращения: 13 сентября 2014.
- ↑ McNaught, A. D. [diamond] Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") / A. D. McNaught, A. Wilkinson. — Blackwell Scientific Publications, Oxford, 2006. — ISBN 978-0-9678550-9-7. — doi:10.1351/goldbook.
- ↑ McNaught, A. D. [metastability] Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") / A. D. McNaught, A. Wilkinson. — Blackwell Scientific Publications, Oxford, 2006. — ISBN 978-0-9678550-9-7. — doi:10.1351/goldbook.
- ↑ McNaught, A. D. [metastability Compendium of Chemical Terminology, 2nd ed. (the "Gold Book")] / A. D. McNaught, A. Wilkinson. — Blackwell Scientific Publications, Oxford, 2006. — ISBN 978-0-9678550-9-7. — doi:10.1351/goldbook.
- ↑ Yeh, Brian J (2007). "Synthetic biology: lessons from the history of synthetic organic chemistry". Nature Chemical Biology. 3 (9): 521—525. doi:10.1038/nchembio0907-521. PMID 17710092.
- ↑ Cornish-Bowden, A (2 September 2013). "The origins of enzyme kinetics". FEBS Letters. 587 (17): 2725—30. doi:10.1016/j.febslet.2013.06.009. PMID 23791665.
- ↑ Yoshikuni, Y (20 April 2006). "Designed divergent evolution of enzyme function". Nature. 440 (7087): 1078—82. Bibcode:2006Natur.440.1078Y. doi:10.1038/nature04607. PMID 16495946.
- ↑ The prevalence and significance of the product inhibition of enzymes // Advances in Enzymology and Related Areas of Molecular Biology. — 1963. — Vol. 25. — P. 167–274. — ISBN 978-0-470-12270-9. — doi:10.1002/9780470122709.ch4.
- ↑ "Regulation of pyruvate dehydrogenase by insulin action". Prog. Clin. Biol. Res. 31: 707—19. 1979. PMID 231784.
- ↑ "Integrated bioprocesses". Curr. Opin. Microbiol. 8 (3): 294—300. 2005. doi:10.1016/j.mib.2005.01.002. PMID 15939352.


