Дабигатрана этексилат: различия между версиями
Ochkarik (обсуждение | вклад) Создано переводом страницы «Dabigatran» |
(нет различий)
|
Версия от 08:15, 29 мая 2017
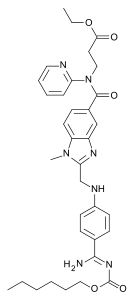
| Dabigatran etexilate | |
|---|---|
 | |
| Химическое соединение | |
| ИЮПАК | Ethyl N-[(2-<nowiki>{[(4-{Ń-[(hexyloxy)carbonyl]carbamimidoyl}phenyl)amino]methyl}-1-methyl-1H-benzimidazol-5-yl)carbonyl]-N-2-pyridinyl-β-alaninate |
| Брутто-формула | C25H25N7O3 |
| Молярная масса | 627.734 г/моль |
| CAS | 211915-06-9 |
| PubChem | 6445226 |
| DrugBank | DB06695 |
| Состав | |
| Классификация | |
| АТХ | B01AE07 |
| Фармакокинетика | |
| Биодоступн. | 3–7%[1] |
| Связывание с белками плазмы | 35%[1] |
| Период полувывед. | 12–17 hours[1] |
| Способы введения | |
| By mouth | |
Дабигатран, продается под маркой Pradaxa в частности, это антикоагулянты , которые могут быть приняты через рот. Применяется для разных случаев и в некоторых случаях он является альтернативой варфарину,
В случае сильного кровотечения, есть у негоантидот, idarucizumab. Исследования, спонсируемые производителем было установлено, что Идаруцизумаб эффективен для нейтрализации дабигатрана в течение нескольких минут.[2]
Это прямой ингибитор тромбина. Он был разработан фармацевтической компанией "Берингер Ингельхайм".
Медицинское использование
Дабигатран используется для предотвращения инсультов у пациентов с фибрилляцией предсердий не вызванных проблемой сердечных клапанов , а также тромбоза глубоких вен и тромбоэмболии легочной артерии у лиц, которые были обработаны в течение 5-10 дней с парентеральным антикоагулянтом (обычно низкомолекулярного гепарина), а также для предотвращения тромбоза глубоких вен и тромбоэмболии легочной артерии в некоторых случаях.[3]
Он является таким же е эффективным, как варфарин в предотвращении негеморрагических инсультов и эмболических событий у пациентов с фибрилляцией предсердий не из-за проблем с клапанами .[4]
Противопоказания
Дабигатран противопоказан пациентам, которые имеют активное патологическое кровотечение, поскольку дабигатран может увеличить риск кровотечений, а также может вызвать серьезные и потенциально опасные для жизни кровотечения.[5] Дабигатран также противопоказан больным, которые имеют в анамнезе серьезные реакции гиперчувствительности к дабигатрану (например, анафилаксия или анафилактический шок). использование дабигатрана также следует избегать у пациентов с механическими протезами клапанов сердца в связи с повышенным риском тромбоэмболических событий (например, клапана, тромбоз, инсульт и инфаркт миокарда) и массивных кровотечений, связанных с дабигатрана в этой популяции.[6][7]
Побочные эффекты
Наиболее обыкновенно сообщаемый побочный эффект дабигатрана является расстройство желудочно-кишечного тракта. По сравнению с людьми использующими варфарин, у пациентов, принимающих дабигатраа было меньше угрожающего жизни кровотечения, реже малых и больших кровотечений, включая внутричерепные кровотечения, однако частота желудочно-кишечных кровотечений была значительно выше. Дабигатран капсулы содержат винную кислоту, которая снижает рН желудка и необходима для надлежащего поглощения. Низкий рН ранее был связан с диспепсией; некоторые предполагают, что это играет определенную роль в повышенном риске желудочно-кишечных кровотечений.[8]
Повышается риск инфарктов миокарда (сердечных приступов) .[9]
Фармакокинетика
Дабигатран имеет период полураспада около 12-14 ч, оказывает максимальный эффект в течение 2-3 ч после приема.[10] жирная пища задерживает всасывание дабигатрана, хотя биодоступность препарата не изменяется. одно исследование показало, что поглощение может быть умеренно снижено, если брать с Ингибиторы протонного насоса.[11] экскреция препарата с помощью Р-гликопротеина замедляется у пациентов, принимающих сильные ингибиторы, такие как хинидин, верапамили амиодарон, что повышает плазменные уровни дабигатрана.[12]
История
Дабигатран (соединения БИБР 953) был обнаружен в составе группы химических веществ с аналогичной структурой в бензамидиновой основе тромбина ингибитор α-NAPAP (Н-Альфа-(2-naphthylsulfonylglycyl)-4-amidinophenylalanine piperidide), которое были известны с 1980-х годов в качестве мощного ингибитора различных сериновых протеаз, в частности тромбина, а также трипсином. Добавления этилового эфира и гексилокарбамида гидрофобных боковых цепей привело к биодоступности пролекарства, БИБР 1048 (дабигатрана этексилат).[13]
18 марта 2008 года Европейским Агентством по лекарственным средствам выдано регистрационное свидетельство для Этексилат для профилактики тромбоэмболических болезней после эндопротезировании тазобедренного или коленного сустава и для неклапанной фибрилляции предсердий.[14]
В Национальной службе здравоохранения в Великобритании одобрили использование дабигатрана для профилактики тромбов в бедренных и коленных суставах пациентов. По данным Би-би-си статьи в 2008 году, Дабигатран, как ожидается, обойдется в nhs £4.20 в день, который был похож на несколько других антикоагулянтов.[15]
Изначально не было никакого определенного пути, чтобы отменить антикоагулянтный эффект дабигатрана в случае крупного кровотечения.[16][17] в отличие от варфарина,[18] антидот дабигатрана idarucizumab был одобрен FDA в 2015 году.[19]
Этексилат получили уведомление о соответствии (НОК) от Министерства здравоохранения Канады на июня 10, 2008,[20] для профилактики тромбов у пациентов, перенесших эндопротезирование тазобедренного или полную замену коленного сустава операции. Одобрения для больных с фибрилляцией предсердий риск инсульта пришел в октябре 2010 года.[21][22]
В США пищевых продуктов и медикаментов (FDA) одобрила Этексилат 19 октября 2010 года, для профилактики инсульта у пациентов с неклапанной фибрилляцией предсердий.[23][24][25][26] , хотя и с некоторыми ограничесниями.[27]
.[28]
В мае 2014 года Управление сообщило о результатах крупного исследования дабигатрана в сравнении с варфарином в 134,000 пациентам. Агентство пришло к выводу, что дабигатран связан с более низким риском общей смертности, ишемического инсульта и кровоизлияния в мозг, чем варфарин. Желудочно-кишечные кровотечения был более распространен в пациентов, получавших дабигатран, чем у пациентов, получавших варфарин. Риск сердечного приступа был похож между двумя препаратами. Агентство подтвердило свое мнение о том, что дабигатран в целом выгоден.[29]
26 июля 2014 года британский медицинский журнал (bmj в) опубликовал серию расследований, которые обвиняют компанию Берингер в сокрытии важной информации о необходимости проведения мониторинга для защиты пациентов от тяжелых кровотечений, особенно у пожилых людей.[30][31]
Исследования
В августе 2015 г. исследование показало, что Идаруцизумаб смог получить может являться антидотом дабигатрана в течение нескольких минут.[32] Идаруцизумаб был утвержден в октябре 2015 года.
Ссылки
- ↑ 1 2 3 Pradaxa Full Prescribing Information. Boehringer Ingelheim. October 2010.
- ↑ Pollack, Charles V.; Reilly, Paul A.; Eikelboom, John; Glund, Stephan; Verhamme, Peter; Bernstein, Richard A.; Dubiel, Robert; Huisman, Menno V.; Hylek, Elaine M. (2015-08-06). "Idarucizumab for Dabigatran Reversal". The New England Journal of Medicine. 373 (6): 511—520. doi:10.1056/NEJMoa1502000. ISSN 1533-4406. PMID 26095746.
- ↑ http://www.drugs.com/pro/pradaxa.html Pradaxa
- ↑ Gómez-Outes, A (2013). "Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups". Thrombosis. 2013: 640723. doi:10.1155/2013/640723. PMID 24455237.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Pradaxa (dabigatran etexilate mesylate) Prescribing Information: http://dailymed.nlm.nih.gov/dailymed/drugInfo.cfm?setid=ba74e3cd-b06f-4145-b284-5fd6b84ff3c9#Section_5.4, accessed October 29, 2014.
- ↑ FDA Drug Safety Communication: Pradaxa (dabigatran etexilate mesylate) should not be used in patients with mechanical prosthetic heart valves. U.S. Food and Drug Administration (FDA). Дата обращения: 29 октября 2014.
- ↑ Eikelboom, JW (September 2013). "Dabigatran versus Warfarin in Patients with Mechanical Heart Valves". N Engl J Med. 369: 1206—1214. doi:10.1056/NEJMoa1300615. PMID 23991661.
- ↑ ML Blommel (2011). "Dabigatran etexilate: A novel oral direct thrombin inhibitor". Am J Health Syst Pharm. 68 (16): 1506—19. doi:10.2146/ajhp100348. PMID 21817082.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Uchino K (2012). "Dabigatran associated with higher risk of acute coronary events - meta-analysis of noninferiority randomized controlled trials". Arch. Intern. Med. 172 (5): 397—402. doi:10.1001/archinternmed.2011.1666. PMID 22231617.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Chongnarungsin D (2012). "In-Depth Review of Stroke Prevention in Patients with Non-Valvular Atrial Fibrillation". Am. Med. J. 3 (2): 100—103. doi:10.3844/amjsp.2012.100.103.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Stangier J (May 2005). "Pharmacokinetic profile of the oral direct thrombin inhibitor dabigatran etexilate in healthy volunteers and patients undergoing total hip replacement". J Clin Pharmacol. 45 (5): 555—63. doi:10.1177/0091270005274550. PMID 15831779.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ "Pradaxa Summary of Product Characteristics".
- ↑ Hauel NH (April 2002). "Structure-based design of novel potent nonpeptide thrombin inhibitors". J Med Chem. 45 (9): 1757—66. doi:10.1021/jm0109513. PMID 11960487.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка); Неизвестный параметр|laysummary=игнорируется (справка) - ↑ Pradaxa EPAR. European Medicines Agency. Дата обращения: 30 января 2011.
- ↑ "Clot drug 'could save thousands'". BBC News Online. 2008-04-20. Дата обращения: 21 апреля 2008.
- ↑ Eerenberg, ES (2011-10-04). "Reversal of rivaroxaban and dabigatran by prothrombin complex concentrate: a randomized, placebo-controlled, crossover study in healthy subjects". Circulation. 124 (14): 1573—9. doi:10.1161/CIRCULATIONAHA.111.029017. PMID 21900088. Дата обращения: 15 марта 2012.
- ↑ van Ryn J (June 2010). "Dabigatran etexilate – a novel, reversible, oral direct thrombin inhibitor: interpretation of coagulation assays and reversal of anticoagulant activity". Thrombosis and Haemostasis. 103 (6): 1116—27. doi:10.1160/TH09-11-0758. PMID 20352166.
Although there is no specific antidote to antagonise the anticoagulant effect of dabigatran, due to its short duration of effect drug discontinuation is usually sufficient to reverse any excessive anticoagulant activity.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Hanley, JP (November 2004). "Warfarin reversal". Journal of Clinical Pathology. 57 (11): 1132—9. doi:10.1136/jcp.2003.008904. PMID 15509671.
- ↑ "Boehringer Ingelheim's Investigational Antidote for Pradaxa® (dabigatran etexilate mesylate) Receives FDA Breakthrough Therapy Designation" (Press release). Boehringer Ingelheim. 2014-06-26. Дата обращения: 26 июля 2014.
- ↑ "Summary Basis of Decision (SBD): Pradax" Health Canada. 2008-11-06.
- ↑ Kirkey, Sharon (29 October 2010). "Approval of new drug heralds 'momentous' advance in stroke prevention". Montreal Gazette. Дата обращения: 29 октября 2010.
- ↑ "Pradax (Dabigatran Etexilate) Gains Approval In Canada For Stroke Prevention In Atrial Fibrillation" Medical News Today. 28 October 2010.
- ↑ Connolly, SJ (September 2009). "Dabigatran versus warfarin in patients with atrial fibrillation" (PDF). N Engl J Med. 361 (12): 1139—51. doi:10.1056/NEJMoa0905561. PMID 19717844.
- ↑ Turpie AG (January 2008). "New oral anticoagulants in atrial fibrillation". Eur Heart J. 29 (2): 155—65. doi:10.1093/eurheartj/ehm575. PMID 18096568.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ "Boehringer wins first US OK in blood-thinner race". Thomson Reuters. 2010-10-19. Дата обращения: 20 октября 2010.
- ↑ "FDA approves Pradaxa to prevent stroke in people with atrial fibrillation". U.S. Food and Drug Administration (FDA). 2010-10-19.
- ↑ Merli G (August 2009). "Use of emerging oral anticoagulants in clinical practice: translating results from clinical trials to orthopedic and general surgical patient populations". Ann Surg. 250 (2): 219—28. doi:10.1097/SLA.0b013e3181ae6dbe. PMID 19638915.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Wann LS (March 2011). "2011 ACCF/AHA/HRS Focused Update on the Management of Patients With Atrial Fibrillation (Update on Dabigatran): A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines". Circulation. 123 (10): 1144—50. doi:10.1161/CIR.0b013e31820f14c0. PMID 21321155.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ FDA Drug Safety Communication: FDA study of Medicare patients finds risks lower for stroke and death but higher for gastrointestinal bleeding with Pradaxa (dabigatran) compared to warfarin.
- ↑ Cohen, D (July 2014). "Dabigatran: how the drug company withheld important analyses". BMJ. 349: g4670. doi:10.1136/bmj.g4670. PMID 25055829.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Moore TJ (July 2014). "Dabigatran, bleeding, and the regulators". BMJ. 349: g4517. doi:10.1136/bmj.g4517. PMID 25056265.
{{cite journal}}: Указан более чем один параметр|author=and|last=(справка) - ↑ Pollack, Charles V. (2015-01-01). "Idarucizumab for Dabigatran Reversal". New England Journal of Medicine. 373 (6): 511—20. doi:10.1056/nejmoa1502000. PMID 26095746.