Гепарин
Стиль этой статьи неэнциклопедичен или нарушает нормы литературного русского языка. |
| Гепарин | |
|---|---|
| Heparinum | |
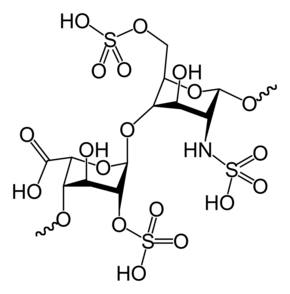 | |
| Химическое соединение | |
| ИЮПАК | см. Химическое строение |
| Брутто-формула | C12H19NO20S3 |
| CAS | 9005-49-6 |
| PubChem | 772 |
| DrugBank | 01109 |
| Состав | |
| Классификация | |
| Фармакол. группа | антикоагулянты прямого действия |
| АТХ | B01AB01 C05BA03 S01XA14 |
| Лекарственные формы | |
| раствор для инъекций, мазь | |
| Способы введения | |
| подкожная инъекция[d] и внутривенная инъекция[d] | |
| Другие названия | |
| «Heparinum», «Liquaemin», «Pularin», «Thromboliquine», «Vetren» и др. | |
Гепари́н (от др.-греч. ἧπαρ — печень) — кислый серосодержащий гликозаминогликан; впервые выделен из печени. В клинической практике известен как антикоагулянт прямого действия, то есть как лекарственное вещество, препятствующее свёртыванию крови. Применяется для профилактики и терапии тромбоэмболических заболеваний, при операциях на сердце и кровеносных сосудах, для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа, а также для предотвращения свёртывания крови при лабораторных исследованиях.
Общие побочные эффекты включают кровотечение, боль в месте инъекции и низкий уровень тромбоцитов[1]. Серьезные побочные эффекты включают тромбоцитопению, вызванную гепарином[1]. Большая осторожность требуется при нарушении функции почек[1]. Гепарин относительно безопасен для использования во время беременности и кормления грудью[2]. Синтезируется в тучных клетках, скопления которых находятся в органах животных, особенно в печени, лёгких, стенках сосудов.
Применение в медицине[править | править код]
Гепарин и его низкомолекулярные производные (например, эноксапарин, далтепарин, тинзапарин) эффективны для предотвращения тромбозов глубоких вен и тромбоэмболии легочной артерии у людей из группы риска[3][4], но нет данных, указывающих на то, что какой-либо из них эффективнее другого в предотвращении смертности[5].
Применение гепарина в комбинации с аспирином в течение беременности у женщин с персистирующими антифосфолипидными антителами может привести к более высокому числу живорождений, чем применение только аспирина. Безопасность гепарина и аспирина у матерей и младенцев неясна из‐за отсутствия сообщений о неблагоприятных событиях. В будущих испытаниях должно быть задействовано достаточное число женщин и полностью оценены риски и польза этой стратегии лечения[6][7].
В настоящее время есть данные, подтверждающие положительный эффект гепарина для предотвращения осложнений при использовании с центральными катетерами для доступа к крошечным венам недоношенных и тяжелобольных детей[8].
COVID-19[править | править код]
Не было понятно, являются ли «разжижители» крови полезным профилактическим средством для людей с COVID‐19. Ни в одном из исследований не рандомизировали участников, и все они были ретроспективными. Кроме того, они сообщили различающиеся между собой результаты и не представили в полной мере свои методы. Это означает, что уверенность (определённость) в доказательствах очень низка[9][10].
Колоректальная хирургия[править | править код]
Пациенты, перенесшие операцию на толстой и прямой кишке, имеют значительный риск развития сосудистых осложнений, выражающихся в виде венозного тромбоза и / или тромбоза легких (тромбоэмболия легочной артерии). Эти осложнения могут привести к пожизненному нарушению венозной функции ног или, в некоторых случаях, к внезапной послеоперационной смерти. Чтобы избежать этих осложнений, пациенты во время операции часто проходят лечение разжижающими кровь лекарствами (антикоагулянтами) и компрессионными чулками. Комбинированное лечение гепарином и TED-чулками доказало свою эффективность в общей хирургии. Подобное комбинированное лечение также эффективно в группе высокого риска пациентов, перенесших операцию на толстой или прямой кишке[11].
История открытия[править | править код]
Открытие гепарина датируется 1916 годом. В этом году его совершенно случайно открыл тогда ещё студент медицинского факультета Университета Джонса Хопкинса (Балтимор, США) Джей Маклин (англ. J. McLean). Профессор кафедры физиологии Уильям Хауэлл задал своему ученику изучить тромбопластическую активность человеческого организма. Маклин стал исследовать липоиды-фосфатиды печени (гепар-фосфатид) и сердца (куорин). Исследуя гепар-фосфатиды, Маклин заметил, что они не только не повышают свёртывание крови, а наоборот, проявляют антикоагулянтную активность. Наблюдения Маклина были опубликованы в Американском журнале физиологии в 1916 году (т. 41, с. 250)[12].
Химическое строение[править | править код]
Гепарин относится к семейству гликозаминогликанов; его молекула представлена несколькими полисахаридными цепями, связанными с общим белковым ядром. Белковое ядро же включает в свой состав в основном остатки двух аминокислот: серина и глицина. Приблизительно две трети сериновых остатков как раз и связывается с полисахаридными цепями. В основе последних лежит цепочка из повторяющихся дисахаридов — α-D-глюкозамин и уроновая кислоты, соединённые 1—4 гликозидными связями. Большинство остатков α-D-глюкозамина сульфатировано по амино- и гидроксильной группе; небольшая часть аминогрупп м. б. ацетилирована. Звенья уроновой кислоты представляют собой остатки L-идуроновой кислоты (~90 %) или эпимерные остатки D-глюкуроновой кислоты (~10 %). Благодаря наличию значительного количества отрицательно заряженных сульфатных и карбоксильных групп молекула гепарина представляет собой сильный природный полианион, способный к образованию комплексов со многими белковыми и синтетическими соединениями поликатионной природы, несущими суммарный положительный заряд.
Длина полисахаридных цепей эндогенного гепарина может быть разной, а, значит, и молекулярная масса его тоже колеблется в широких пределах — от 3000 до 40 000 дальтон. Средняя молекулярная масса «коммерческих» гепаринов, используемых в качестве лекарственных препаратов, колеблется в более узких пределах — от 12 000 до 16 000 дальтон. В последнее время была получена группа низкомолекулярных гепаринов, обладающая дополнительными свойствами.
Часто количество гепарина измеряется в единицах действия (ЕД) по его физиологической активности — способности предотвращать свёртывание плазмы крови. Одна единица действия равна 0,0077 мг международного стандарта гепарина (в 1 мг препарата 130 ЕД)[13].
Биосинтез[править | править код]
Субстратами для биосинтеза гепарина являются глюкоза и неорганический сульфат. Присоединение сульфатных групп осуществляется после полимеризации, но некоторые учёные (Rice et al, 1967) предполагают, что сульфатирование происходит на более ранних этапах, то есть ещё на уровне низкомолекулярных предшественников. Среди ферментов участвующих в биосинтезе гепарина выделяют различные гликозилтрансферазы, сульфотрансферазы, эпимеразы, многие из которых выделены в чистом виде. Есть ряд фактов, указывающих на то, что биосинтез гепарина происходит в тучных клетках:
- Гепарин обнаружен в гранулах тучных клеток.
- В самих тучных клетках содержатся ферменты, участвующие в биосинтезе кислых гликозаминогликанов.
- Меченые предшественники включаются в гепарин гранул тучных клеток, но предварительно меченый гепарин в последних не обнаруживается. Этот факт опровергает также версию, где тучные клетки рассматриваются всего лишь в качестве накопителей гепарина[14].
- Матрица для формирования гепарина — белок серглицин.
Физиологическая роль[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Взаимодействие с антитромбином III[править | править код]
Считается, что гепарин реализует свою антикоагулянтную активность через активацию антитромбина III[15]. Гепарин, обладая большим суммарным отрицательным зарядом, связывается со специфическими катионными участками антитромбина III, в результате конформация молекулы последней меняется, и антитромбин III приобретает возможность инактивировать факторы свёртывания (II, IX, X, XI, XII), калликреин, сериновые протеазы.
Взаимодействие с липопротеинлипазой[править | править код]
Обнаружено, что гепарин способен проявлять гиполипидемическое действие, повышая активность липопротеинлипазы[16]. Липопротеинлипаза с помощью протеогликановых цепей гепарин-сульфата связывается со стенкой капилляров. В большом количестве липопротеинлипаза содержится в сердце, жировой ткани, селезёнке, лёгких, мозговом веществе почек, диафрагме, молочных железах; в крови липопротеинлипаза почти не содержится. После введения гепарина концентрация липопротеинлипазы в крови незначительно увеличивается, т.к. гепарин высвобождает её в кровеносное русло.
Гепарин в фармакологии[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Фармакодинамика[править | править код]
Высокомолекулярный гепарин образует стабильный комплекс с антитромбином III, связываясь с факторами крови, блокирует дальнейший путь коагуляции. Низкомолекулярные гепарины также связываются с антитромбином, однако ввиду особенности их строения, образуют нестабильный комплекс, чем можно объяснить их относительную безопасность по сравнению с высокомолекулярным гепарином. Гепарин, вводимый в человеческий организм, действует так же, как и эндогенный: активирует антитромбин III и липопротеинлипазу. Антикоагулянтное действие гепарина происходит только при наличии в крови достаточного количества антитромбина III[17].
Фармакокинетика[править | править код]
Эффект после введения гепарина развивается довольно быстро, но продолжается в течение короткого времени. Так, при однократном внутривенном введении угнетение свёртывания наступает сразу и продолжается около 4—5 часов, при внутримышечном введении действие гепарина проявляется спустя 15—30 минут и продолжается до 6 часов, при введении в подкожную клетчатку эффект наступает через 40—60 минут и длится 8 часов. За счёт большой молекулярной массы гепарин плохо проникает через гемато-плацентарный барьер. Период полувыведения 30—60 минут[18].
Противосвёртывающий эффект гепарина усиливается при одновременном применении других антикоагулянтов, антиагрегантов и НПВС. Алкалоиды спорыньи, тироксин, тетрациклин, антигистаминные средства, никотин способны снижать противосвёртывающий потенциал гепарина.
Получение[править | править код]
Для лечебных целей гепарин получают из печени, лёгких и слизистой оболочки кишечника свиней[19].
Показания[править | править код]
Профилактика и терапия тромбоэмболических заболеваний и их осложнений, тромбообразования при операциях на сердце и кровеносных сосудах, при остром инфаркте миокарда. Также для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа, для предотвращения свёртывания крови при лабораторных исследованиях, тромбозе глубоких вен.
Побочное действие[править | править код]
Гепарин способен вызывать побочное действие со стороны различных систем организма:
- Действуя на свёртывающую систему, гепарин способен спровоцировать тромбоцитопению, желудочно-кишечные кровотечения, кровотечение в месте введения, в областях, подвергающихся давлению, из операционных ран, а также кровоизлияния в других органах.
- Со стороны пищеварительной системы отмечается тошнота, снижение аппетита, рвота, диарея, повышение активности печёночных трансаминаз.
- Возможны также аллергические реакции: гиперемия кожи, кожный зуд, лихорадка, крапивница, ринит, бронхоспазм, коллапс, анафилактический шок.
- При длительном применении побочное действие выявляется и со стороны костно-мышечной системы: остеопороз, спонтанные переломы.
Прочие: преходящая алопеция, гипоальдостеронизм.
Безопасность[править | править код]
Препараты гепарина производятся из природного сырья, и стандартизация их не во всех случаях проводится должным образом. В марте 2010 года появились сообщения о серьёзных побочных последствиях от применения гепарина в Китае, США и Германии[20].
Противопоказания[править | править код]
Различные заболевания, сопровождающиеся замедлением свёртывания крови; геморрагические диатезы; геморрагический инсульт; кровотечения любой локализации (кроме геморрагий при эмболическом инфаркте лёгких и почек); тяжёлые нарушения функций почек и печени.
С осторожностью: пациентам с поливалентной аллергией (в том числе, бронхиальная астма) детский возраст до 3-х лет, при патологических состояниях, ассоциирующихся с повышенным риском кровотечений[21]
Форма выпуска[править | править код]
Выпускается гепарин в виде натриевой соли в герметически закрытых флаконах и ампулах по 5 мл с активностью 5000 ЕД в 1 мл. За рубежом производят также кальциевую соль гепарина — кальципарин. Последний выпускается в виде водного раствора, содержащего в 1 мл 25000 ЕД. Специальные шприцы содержат 0,2 мл раствора (5000 ЕД).
Режим дозирования[править | править код]
Режим дозирования индивидуален, зависит от применяемой лекарственной формы, показаний, клинической ситуации и возраста пациента.[22]
- При остром инфаркте миокарда рекомендуется уже в условиях оказания скорой помощи вводить гепарин внутривенно в дозе 15 000—20 000 ЕД и продолжать в условиях стационара минимум 5—6 дней подкожное введение в дозе 40 000 ЕД в сутки (через каждые 4—6—8 часов часа по 5000—10 000 ЕД).
- При периферических тромбозах вводят сначала 5000 ЕД гепарина внутривенно, затем 30 000—40 000 ЕД/сут 3—6 раз в сутки подкожно или через инфузомат из расчёта 18 ед/(кг·ч) под контролем АЧТВ;
- Для профилактики тромбоэмболий гепарин вводят по 5000 ЕД подкожно 1—2 раза в сутки в пред- и постоперационный период.
- При массивных тромбозах лёгочной артерии препарат вводят капельно в дозе 40 000—60 000 ЕД в течение 4—6 часов, затем переходят на внутримышечное введение по 40 000 ЕД в сутки.
- При прямом переливании крови гепарин вводят в вену донора по 7500—10 000 ЕД.
См. также[править | править код]
Литература[править | править код]
- Рынок препаратов группы ГЕПАРИНА находится в стадии становления. Статья в еженедельнике Аптека, 2001.
- Лекарственные средства: В 2 т. Т. 1. — 14-е изд., перераб., испр. и доп.— М.: ООО «Издательство Новая волна»: Издатель С. Б. Дивов, 2002. — 540 с., 8 с. ил. ISBN 5-7864-0128-6.
Примечания[править | править код]
- ↑ 1 2 3 Heparin Sodium. The American Society of Health-System Pharmacists. Дата обращения: 1 января 2016. Архивировано 27 января 2016 года.
- ↑ Heparin Pregnancy and Breastfeeding Warnings. drugs.com. Дата обращения: 15 января 2016. Архивировано 27 января 2016 года.
- ↑ Agnelli G; Piovella F; Buoncristiani P; et al. (1998). "Enoxaparin plus compression stockings compared with compression stockings alone in the prevention of venous thromboembolism after elective neurosurgery". N Engl J Med. 339 (2): 80—85. doi:10.1056/NEJM199807093390204. PMID 9654538.
- ↑ Bergqvist D; Agnelli G; Cohen AT; et al. (2002). "Duration of prophylaxis against venous thromboembolism with enoxaparin after surgery for cancer". N Engl J Med. 346 (13): 975—980. doi:10.1056/NEJMoa012385. PMID 11919306.
- ↑ Handoll HH, Farrar MJ, McBirnie J, Tytherleigh-Strong G, Milne AA, Gillespie WJ (2002). "Heparin, low molecular weight heparin and physical methods for preventing deep vein thrombosis and pulmonary embolism following surgery for hip fractures". Cochrane Database Syst Rev (4): CD000305. doi:10.1002/14651858.CD000305. PMID 12519540.
{{cite journal}}: Википедия:Обслуживание CS1 (дата и год) (ссылка) - ↑ Aspirin or heparin or both for improving pregnancy outcomes in women with persistent antiphospholipid antibodies and recurrent pregnancy loss. Cochrane Library.
- ↑ Аспирин и/или гепарин для улучшения исходов беременности у женщин с персистирующими антифосфолипидными антителами и повторным прерыванием беременности. Cochrane Library.
- ↑ Continuous heparin infusion to prevent thrombosis and catheter occlusion in neonates with peripherally placed percutaneous central venous catheters. Cochrane Library.
- ↑ Prophylactic anticoagulants for people hospitalised with COVID‐19. Cochrane Library. Дата обращения: 13 декабря 2020. Архивировано 2 мая 2021 года.
- ↑ Профилактическое использование антикоагулянтов у людей, госпитализированных с COVID‐19. Cochrane Library.
- ↑ Heparins and mechanical methods for thromboprophylaxis in colorectal surgery. Cochrane Library.
- ↑ Бокарев И. Н., Попова Л. В. Опыт применения низкомолекулярных гепаринов при лечении тромбоза глубоких вен // Трудный пациент. — 2008. — Т. 6, вып. 10. — С. 42—48. — ISSN 2074-1995. Архивировано 24 октября 2017 года.
- ↑ Першин Г. Н., Гвоздева Е. И. Учебник фармакологии. — М.: Медгиз, 1961. — 405 с.
- ↑ Lidholt K., Lindahl U. Biosynthesis of heparin. The D-glucuronosyl- and N-acetyl-D-glucosaminyltransferase reactions and their relation to polymer modification (англ.) // Biochemical Journal. — 1992. — 1 October (vol. 287, no. 1). — P. 21—29. — ISSN 0264-6021. — PMID 1417774.
- ↑ Основы антикоагулянтного лечения острого венозного тромбоэмболизма | #06/06 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи. Журнал «Лечащий врач». Дата обращения: 6 февраля 2023. Архивировано 6 февраля 2023 года.
- ↑ Котюжинская С. Г, Гоженко А. И, Савицкий И. В, Свирский А. А. Характеристика липидтранспортной системы при экспериментальной гиперлипидемии на фоне гипергепаринемии // Актуальні проблеми сучасної медицини: Вісник української медичної стоматологічної академії. — 2014. — Т. 14, вып. 3 (47). — С. 202–205. — ISSN 2077-1096. Архивировано 6 февраля 2023 года.
- ↑ Бокарев И.н, Попова Л.в. Опыт применения низкомолекулярных гепаринов при лечении тромбоза глубоких вен // Трудный пациент. — 2008. — Т. 6, вып. 10. — С. 42–46. — ISSN 2074-1995. Архивировано 6 февраля 2023 года.
- ↑ Мелкумян Анна Леоновна, Берковский А.л, Кишинец Р.с, Козлов А.а. Мониторинг эффективности применения прямых антикоагулянтов // Гематология и трансфузиология. — 2013. — Т. 58, вып. 1. — С. 32–38. — ISSN 0234-5730. Архивировано 6 февраля 2023 года.
- ↑ Антикоагулянтная терапия в профилактике и лечении венозных тромбоэмболических осложнений. www.mediasphera.ru. Дата обращения: 6 февраля 2023. Архивировано 6 февраля 2023 года.
- ↑ От препарата «Гепарин» умирают люди. novosti.ua. Дата обращения: 23 октября 2017. Архивировано 24 октября 2017 года.
- ↑ Гепарин натрия — инструкция по применению, дозы, побочные действия, отзывы о препарате Гепарин натрия: гель для наружного применения,раствор для внутривенного и подкожного введения, 5000 МЕ/мл, 1000 МЕ/г — Энциклопедия лекарств РЛС (англ.). РЛС®. Дата обращения: 6 февраля 2023. Архивировано 6 февраля 2023 года.
- ↑ Francis C. W., Kaplan K. L. Chapter 21. Principles of Antithrombotic Therapy // Williams Hematology (неопр.) / Lichtman M. A., Beutler E., Kipps T. J., et al. — 7th. — 2006. — ISBN 978-0071435918. Архивировано 7 июля 2011 года.
Ссылки[править | править код]
- Аспирин и/или гепарин для улучшения исходов беременности у женщин с персистирующими антифосфолипидными антителами и повторным прерыванием беременности / Cochrane
- Профилактическое использование антикоагулянтов у людей, госпитализированных с COVID‐19 / Cochrane
- ГЕПАРИН-НАТРИЙ БРАУН. Описание препарата в справочнике Видаль.
- Антитромботические средства в Проекте распоряжения Правительства РФ от 23 сентября 2011 г. о ЖНВЛП (недоступная ссылка)
- О профилактическом применении гепаринов у больных отделений интенсивной терапии. Результаты исследования PROTECT
- Клинико-экономическая оценка профилактики низкомолекулярными гепаринами венозных тромбоэмболических осложнений в хирургии
- Перевод пациента с гепарина на бивалирудин перед проведением первичной ангиопластики оказывает благотворное влияние (недоступная ссылка)
Для улучшения этой статьи по фармакологии желательно:
|