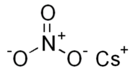Нитрат цезия
| Нитрат цезия | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Нитрат цезия | ||
| Традиционные названия | Азотнокислый цезий | ||
| Хим. формула | CsNO3 | ||
| Физические свойства | |||
| Состояние | Белые кристаллы | ||
| Молярная масса | 194,91 г/моль | ||
| Плотность | 3,685 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 414; 417 °C | ||
| Мол. теплоёмк. | 96,1 Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | 505,0 кДж/моль | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 23,020; 13480 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 7789-18-6 | ||
| PubChem | 62674 | ||
| Рег. номер EINECS | 232-146-8 | ||
| SMILES | |||
| InChI | |||
| Номер ООН | 1451 | ||
| ChemSpider | 56425 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Нитрат цезия — соль щелочного металла цезия и азотной кислоты с формулой CsNO3. Бесцветный гигроскопический кристаллический порошок, без запаха. Образует кристаллогидраты.
Получение[править | править код]
Нитрат цезия получается действием азотной кислоты на металлический цезий, его оксид, гидроксид или карбоната:
Физические свойства[править | править код]
Нитрат цезия образует бесцветные гигроскопичные кристаллы гексагональной сингонии, пространственная группа P 6m2 или P 62m, a = 1,074 нм, c = 0,768 нм. При 154°С переходит в кубическую фазу с параметром ячейки a = 0,4499 нм (170°С).
Из водных растворов выделены кристаллогидраты CsNO3•H2O (темп. пл. 100°С) и CsNO3•2H2O (темп. пл. 32-36°С).
В вакууме при 450-500°С нитрат цезия возгоняется без разложения, что можно использовать для его очистки. Расплавленный нитрат цезия сильный окислитель, он разрушительно действует на кварц, платину, многие металлы.
Химические свойства[править | править код]
- При нагревании выше температуры плавления разлагается
- При смешении концентрированных растворов нитрата цезия и азотной кислоты образуются сольваты (n=1÷2):
- Нитрат цезия в растворе восстанавливается только атомарным водородом:
Примечания[править | править код]
- ↑ Лидин, 2000, с. 49.
Литература[править | править код]
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Плющев В. Е., Степушин Б. Д. Химия и технология соединений лития, цезия и цезия. — М.: «Химия», 1970. — 408 с.
- Справочник химика / Редкол.: Никольский Б.П. и др. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9.