Тиселиус, Арне
| Арне Тиселиус | |
|---|---|
| швед. Arne Wilhelm Kaurin Tiselius | |
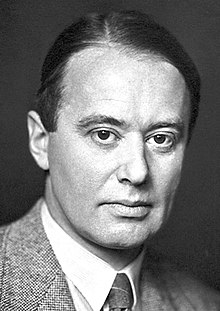 Арне Тиселиус | |
| Дата рождения | 10 августа 1902 |
| Место рождения | Стокгольм, Швеция |
| Дата смерти | 29 октября 1971 (69 лет) |
| Место смерти | Уппсала, Швеция |
| Страна |
|
| Научная сфера | биохимия |
| Место работы | |
| Альма-матер | |
| Научный руководитель | Теодор Сведберг |
| Ученики | Роберт Уильямс |
| Награды и премии |
Премия столетия (1953) Медаль Франклина (1955) |
Арне Тиселиус (швед. Arne Wilhelm Kaurin Tiselius; 10 августа 1902, Стокгольм — 29 октября 1971, Уппсала) — шведский биохимик, член Шведской АН и президент с 1956 года. Лауреат Нобелевской премии по химии (1948).
Биография[править | править код]
Арне Вильгельм Каурин Тиселиус родился в Стокгольме 10 августа 1902 года в семье Ганса Абрахама Йисона Тиселиуса и Розы Каурин, дочери настоятеля горного прихода в центре Норвегии.
Арне посещал гимназию (в наст. Vasa Laroverk), директором которой был его дед, и в которой доктор Людвиг Йоханссон, учитель химии и биологии, обратил внимание на способности Тиселиуса к химии, дав мальчику личный ключ от школьной лаборатории для проведения исследований после уроков. Вскоре Тизелиус решил, что он хотел бы учиться под руководством Теодора Сведберга в Уппсале. При финансовой поддержке некоторых друзей семьи он был зачислен в университет Уппсалы в 1921 году. После трех лет обучения он получил первую степень по химии, физике и математике. В качестве подработки стал ассистентом метеорологического института в университете, оставаясь на этой должности до 1925 года, после чего стал ассистентом-исследователем по физической химии под руководством Теодора Сведберга. В 1930 г. защитил докторскую диссертацию на тему «Изучение электрофореза протеинов с помощью метода движущейся границы».
В 1938—1968 годах Тиселиус был профессором биохимии и директор Биохимического института в университете Уппсалы.
28 октября 1971 года Арне Тиселиус перенес тяжёлый сердечный приступ и на следующее утро скончался.
Семья[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Фамилия досталась от бабушки, фру Йохансен (урождённая Тисель (Tisell)). Несколько её предков были учёными, особенно интересовавшимися биологией. В конце XVII века члены этой семьи были священнослужителями, интересовавшимися научными изысканиями. К XVIII веку в семье были владельцы литейных фабрик и фермеры.
Отец Тиселиуса работал в страховой компании Стокгольма. Получил степень по математике в университете Уппсалы. Его дед, Нильс Абрахам Йоханссон, и брат деда также имели степень университета Уппсалы по математике и биологии соответственно. Н. А. Йоханссон стал доцентом математики Уппсалы, а позднее переехал в Гётеборг, где сначала был преподавателем, а затем директором известной гимназии.
После преждевременной кончины Ганса Тиселиуса в 1906 году фру Тиселиус перевезла Арне и его младшую сестру в Гётеборг, где жили бабушка и дедушка Арне, и где семья имела несколько близких друзей, которые в различных аспектах могли поддержать вдову в сложной ситуации с двумя маленькими детьми.
Арне Тиселиус в 1930 году женился на Грете Дален (Greta Dalén). У них были дочь и сын. Дочь, Ева, вышла замуж за Торгни Болина (Torgny Bohlin), который стал профессором в Бергене, Норвегия. Сын, Пер, изучал медицину и является специалистом в ревматологии.
Основные темы исследований[править | править код]
В основном исследовал:
- Методы электрофоретических и хроматографических исследований высокомолекулярных соединений;
- Доказал комплексную природу белков сыворотки крови.
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Стиль этого раздела неэнциклопедичен или нарушает нормы литературного русского языка. |
Этот перевод статьи с другого языка требует улучшения (см. Рекомендации по переводу). |
Исследования электрофореза[править | править код]
В 1926 году Тиселиус совместно со Сведбергом опубликовал свою первую статью с описанием U-образной трубки для электрофореза с сегментами из кварца. За миграцией границ белка следили по поглощению ультрафиолета. Потенциал был приложен к устройству от аккумуляторных батарей через обратимый цинк-сульфатный электрод и эксперимент был проведен в комнате «с достаточно постоянной температурой». Были проведены измерения электрофоретической подвижности яичного альбумина в ацетатном буфере в диапазоне рН от 3,4 до 5,75, и, путём интерполяции кривой подвижности, изоэлектрическая точка была найдена при рН 4,7.
Тиселиус продолжил исследования в этой области. Он внес обширный раздел в большое немецкое руководство по методам определения подвижности и заряда коллоидных частиц, охватывая, как теоретические, так и экспериментальные аспекты. В дополнение он помогал Сведбергу со вторым, переработанным и дополненным изданием его «Коллоидной химии», а также написал статью о вычислении термодинамических характеристик коллоидных растворов из измерений на ультрацентрифуге. В январе 1928 года он сдал экзамен на получение степени лиценциата по химии, что было необходимо для продолжения работы над докторской диссертацией.
В 1930 году результаты изучения его комплексного и экспериментального метода движения границ для исследования электрофореза белков были опубликованы в качестве диссертации на соискание научной степени доктора в Уппсале. Эта работа в течение многих лет оставалась классической по данному предмету. С технической стороны температура строго контролировалась термостатом, и из экспериментов с переменным током установили, что предельный ток нагрузки соответствует бесконвекционной миграции. Предыдущий электрод был заменен на хлорид серебра, теоретически был вычислен требуемый объём для электродных сосудов. Усовершенствованы оптические и фотографические условия, установлена концентрационная шкала абсорбции света, приведены теоретические обоснования использования 50 % концентрационной точки как определение подлинного расположения границы. В рассмотрение граничных аномалий включено экспериментальное определение ионной силы буфера, которая требуется для их подавления; категорические различия были сделаны между характерами поведения границ при аномальной миграции и поведением, возникающим из электрохимической негомогенности белковых препаратов. Протестировано электрофоретическое поведение некоторых хорошо определенных белков, таких как яичный альбумин, сывороточный альбумин и фикоэритрин, а при смешении таких однородных белков показана независимость миграции компонентов. Препараты соль-фракционирования лошадиного сывороточного глобулина показали негомогенность миграции, но никаких определенных точек перегиба при регистрации фотографических кривых не обнаружили.
В результате успеха своей диссертации Тиселиус был назначен доцентом.
В то время, когда он был вовлечен в работу над диссертацией, он читает лекции по биохимии, которая не была включена в учебную программу университета Уппсалы. Он увлекся изменчивостью и особенно спецификой природных веществ. Тот факт, что белковые препараты проявлялись однородно в ультрацентрифуге, не обязательно вели себя однородно в электрофорезе, постепенно убеждал его, что определение, разделение и очистка являлись фундаментальными проблемами для всей биохимии, они требуют применения разнообразных методик с учетом широкого диапазона веществ. Он сделал существенный вклад в эти вопросы благодаря своей дальнейшей исследовательской деятельности.
Хотя Тиселиус был назначен доцентом, его зарплата оставалась как у ассистента физической химии в течение ещё двух лет, пока не появилась стипендия доцента химии. Такие ведомственные стипендии изначально давали на три года и обычно продлевались на следующие три года с возможностью расширения её на седьмой год. В исключительных случаях могли наградить стипендией на другие 6 лет но таких было всего несколько и все факультеты конкурировали за них. Университет имел несколько постоянных академических назначений, а по истечении стипендии доценты были вынуждены искать себе работу за пределами университета. В университете Уппсалы было одно место в органической, одно в общей и неорганической химии и дополнительно персональное место Сведберга в физической химии. Ситуация в других шведских университетах была аналогичной. В 1930 году Тиселиус женился на Грете Дален; теперь у них была молодая семья, и они беспокоились о будущем. Место в общей и неорганической химии в Уппсале должно было стать вакантным в 1936 году. Он чувствовал своим долгом попробовать получить место в Уппсале и решил направить свои исследовательские интересы в область, которая была бы полезна его кандидатуре.
Он увлекся необычной способностью определённых цеолитных минералов к обмену их кристаллизованной воды на другие вещества, со способностью кристаллической структуры цеолита оставаться целой даже после удаления кристаллизационной воды вакуумированием. Было известно, что изменялись оптические свойства высушенных кристаллов при удалении воды, но никаких количественных изучений данного явления сделано не было.
На тот момент в Уппсале велись обширные исследования по диффузии белков в растворе, и Тиселиус интересовался, как можно использовать оптические свойства кристаллов для определения скорости диффузии воды в цеолите — тема, которую можно было бы считать более родственной к неорганической химии, чем к электрофорезу. Были проведены несколько предварительных экспериментов с цеолитом, полученным из шведской минералогической коллекции, но так как они были низкого качества, он решил снарядить собственную экспедицию для получения лучших образцов. Летом 1932 года он совершил длительное путешествие к некоторым наиболее удаленным из Фарерских островов в Атлантическом океане.
С этими образцами Тиселиус выяснил контролирующие параметры и разработал элегантный и точный метод измерения диффузии водяного пара и других газов в кристаллах цеолита. Исследования были расширены до изучения кинетики диффузии и адсорбции различных газов в негидратированных кристаллах, эта работа свершается благодаря стипендии Рокфеллера с 1934-35 года, когда Тизелиус работал в Соединенных Штатах совместно с Хью. С.Тейлором в университете Принстона.
Перед отъездом в Принстон он признался, что если бы был полностью независимым, то сконцентрировался бы на биохимии, где обдумывал некоторые самые интригующие проблемы современной науки, которые все ещё ждали решения. Однако из-за подавленных экономических условий Швеции в то время (компании Kreuger рухнули осенью 1932 года и возникла тяжелая общая безработица) была маленькая надежда на новую постоянную должность в университете, и он почувствовал необходимость получения места в неорганической химии университета Уппсалы.
Через некоторое время после возвращения Тиселиуса в Швецию, Гуннар Хагг был назначен на должность по неорганической химии в Уппсале, выбор, который Тиселиус посчитал бесспорно верным. Назначив, комитет однако подчеркнул, что выдающиеся достижения Тиселиуса сделали его достойным профессионального статуса, хотя подходящей должности не было.
Систематический пересмотр базовых экспериментальных факторов электрофореза привел к конструкции аппарата, радикально нового дизайна, который был впервые использован в течение 1936 года. Круглое сечение всех предыдущих U-образных трубок было заменено ячейками, имеющими длинное узкое поперечное сечение. Заданная площадь поперечного сечения позволила значительно увеличить оптическую чувствительность и более эффективно удалять тепло, выделяемое при прохождении электрического тока, таким образом минимизировав риск нарушения границы, возникающей из-за тепловой конвекции. В дальнейшем вероятность тепловой конвекции была сокращена путём эксплуатации оборудования при температуре 0-4°С — температурный диапазон, в котором плотность буферного раствора достигает максимума и меняется незначительно при изменении температуры. U-трубка была сконструирована из стеклянных секций, которые имели концевые пластины, способные легко перемещаться друг относительно друга при помощи простого пневматического устройства. Это способствовало формированию четкой границы между белком и буферными растворами, а вместе с противотоковой жидкостью сделало возможным изоляцию электрофоретически разделенных образцов для химических и биологических экспериментов в конце потока. За движением границы белок-буфер следили рефрактометрически при помощи метода Топлеровской полосы, используя видимый свет, который разрешал как прямые, так и фотографические наблюдения.
Тиселиус впервые опробовал потенциальные возможности аппарата путём исследования образца лошадиной сыворотки. К его удивлению, через несколько часов он наблюдал 4 различные полосы, указывающие на миграцию альбумина и трех глобулинов, которые он назвал альфа, бета и гамма. Из его работ с предыдущей аппаратурой он знал, что сывороточный глобулин электрофоретически негомогенен, но не мог определить компоненты. Для публикации в биохимическом журнале была отправлена статья, детально описывающая новую аппаратуру, а также открытие основного белка сыворотки, но в публикации было отказано; в конце концов она была опубликована в Transaction of the Faraday Society и была принята с огромным интересом.
В статье было описано исследование и опубликованы результатами, которые имели большое значение. Очищенные протеины, такие как яичный и сывороточный альбумины, изолированные электрофоретически, отображались одной резкой полосой в течение всего электрофореза, в то время как образцы гамма-глобулина, полученные электрофоретически давали широкую полосу. Было показано, что кривые подвижности цельной сыворотки по существу согласуются с изолированными компонентами, а при помощи графической интеграции получили оценку относительных пропорций компонентов. Сыворотки из лошади, человека и кролика давали схожие модели, но с количественными различиями. В иммунной кроличьей сыворотке доля гамма-глобулина была намного выше, чем в нормальной кроличьей сыворотке, а при электрофоретическом разделении активные антитела явно связывались только компонентами гамма-глобулина. Из изучения фракций сывороточного белка разделенных соль-фракционированием, было раскрыто значение электрофоретических диаграмм для последующих процедур очистки, а электрофоретическая гомогенность была установлена как необходимый, хотя и недостаточный критерий чистоты белка.
На данном этапе для Сведберга стало очевидно, что должны быть приняты шаги, для того чтобы Тиселиус остался в университете Уппсалы, и в конце 1937 года его усилия оказались успешными. Благодаря щедрому пожертвованию университету Уппсалы в декабре 1937 года майором Гербертом Джекобсоном и Мисис Карин Джекобсон, было установлено специальное место профессора биохимии для исследования и обучения в этих областях химии и физики важных жизненных процессов. Тиселиус был первым назначенным лицом на эту должность. Это была финансовая поддержка тех же доноров, которые сделали возможность для Тиселиуса начать его обучение в университете Уппсалы в 1921 году. 20 мая 1938 года Тиселиус получил королевское согласие на его назначение профессором биохимии, и 5 ноября 1938 года на своей инаугурации он прочел лекцию «Биология и исследование белков».
Очень точный, хотя трудоемкий, шкальный оптический метод Ламма, уже широко использующийся с ультрацентрифугой, был адаптирован к аппарату для электрофореза. Так этот метод позволил точнее разграничить профиль миграции границ белка и обеспечить гораздо более точную количественную оценку относительных количеств компонентов в смеси белков. Используя эти доработки, Тиселиус и Кабат в широко цитируемой статье[1] описали изменения, появившиеся, когда антитела, присутствующие в сывороточном кроличьем анти-овальбумине были удалены осаждением с оптимальным количеством овальбумина. Электрофоретически, доля гамма-глобулина была значительно снижена как следствие удаления антител, и при помощи интегрирования электрофоретических кривых, было показано, что это уменьшение согласуется с экспериментальной ошибкой количества антител, которую оценили напрямую из содержание азота в преципитате антиген-антитело. В этой же статье было продемонстрировано связывание антитела в лошадиной сыворотке с новым компонентом, который мигрирует между компонентами бета и гамма глобулин, как было определено в нормальной лошадиной сыворотке.
Из ультрацентрифугных изучений гемоцианинов Сведберг и его коллеги нашли, что в определенных диапазонах рН небольшие изменения рН продуцировали реакцию диссоциации или ассоциации субъединиц, которые были обратимы. С Хорсфолом, Тиселиус сделал некоторые электрофоретические исследования смесей гемоцианинов[2], которые он описал следующим образом: «Мы имели огромное удовольствие „скрещивать улиток“, как мы выразились. Мы продемонстрировали, что обратимая диссоциация-ассоциация гемоцианинов из Helix pomatia и Helix nemoralis, достигнутая путём сдвига рН, привела к образованию гибридных молекул, в то время как тот же самый эксперимент с Helix pomatia и Littorina littorea гибридизация не наблюдалась».
Акцент научных интересов Тиселиуса, в основном, заключался в методологии, первая диссертация с его факультета была сделана Свенсоном в 1946 году и содержала фундаментальные вклады, с экспериментальным подтверждением, в теорию электрофореза о движении границ.
Реальный прорыв для клинического применения электрофоретического анализа при определенных патологических условиях пришел к введению зонного электрофореза на матрице бумажного фильтра. В 1927 году, Тиселиус провел некоторые эксперименты с зонным электрофорезом и разделил фикоэритрин (красный) и фикоциан (синий) в пластинке желатина, получив острые мигрирующие группы, но в то время он не продолжил исследования и не опубликовал работу. Совместно с Кремером в 1950 году был описан микрометод зонного электрофоретического разделения сывороточных белков на фильтровальной бумаге, который требовал 3-4 мг белка, что было гораздо меньше в сравнении с 200 мг, необходимыми для анализа методом двигающихся границ. Количественное измерение содержания компонентов было получено серийным разрезанием бумаги на одинаковые полоски, элюируя с каждой краситель и оценивая количество колориметрическим методом. Полученная таким образом кривая по существу согласовывалась с таким же сывороточным образцом, измеренным методом двигающихся границ.
Дальнейшая разработка Хаглунда — аппарат для стабилизации зонного электрофореза в стеклянной порошковой колонке. Белки после разделения элюировались буфером и собирались в коллекторе фракций примитивной формы. Хотя этот аппарат был предназначен для аналитических целей, базовая конструкция была впоследствии существенно расширена студентом Тиселиуса Поратом (1957) с использованием других стабилизаторов зоны частиц для электрофоретического разделения очень большого числа протеинов.
Короткая, но очень важная статья[3] «Стационарный электролиз растворов амфолитов», опубликованная в 1941 году, впервые описывает фундаментальные принципы, лежащие в основе изоэлектрического фокусирования. В многокомпонентной аппаратуре, в которой содержания отсеков было эффективно предохранено от механических ремиксов при помощи проницаемых для электролитов и протеинов мембран, градиент рН был установлен путём электролиза разбавленного раствора сульфата натрия. С этой аппаратурой, Тиселиусу удалось существенно разделить индивидуальные белки в смесях овальбумина (рH=4.6) и гемоглобина (pH=6.8). Благодаря студенту Тиселиуса Свенсону, возникла настоящая, значительно дискриминирующая процедура изоэлектрической фокусировки, которая может оперировать всего лишь с микрограммовыми количествами белка.
Можно с полным основанием сказать, что большинство разработок в электрофорезе на протяжении 40 лет, возникли из фундаментальных вкладов, сделанных Тиселиусом.
Адсорбционный анализ: хроматография неокрашенных веществ.[править | править код]
После его назначения профессором в конце 1938 года, Тиселиус очень быстро начал расширять диапазон своих исследовательских интересов, так как электрофорез был недостаточно специфичным для разделения многокомпонентных веществ в материалах биологического происхождения. Поэтому он стал интенсивно интересоваться хроматографией, в то время используемой для разделения только цветных соединений.
В первых двух публикациях по этому предмету[4][5] была описана аппаратура, в которой растворы для абсорбционного анализа проходили снизу вверх через колонку с активированным углем и поступали в прямоугольную кювету, появление растворенных веществ наблюдали с помощью диагональной шлиренской оптической системы. Было представлены теоретические выкладки, связывающие удерживаемый объём адсорбированного вещества с его коэффициенту адсорбции и массой адсорбента в колонке. Было показано, что удерживаемые объёмы глюкозы и лактозы в водных растворах пропорциональны количеству адсорбента и уменьшаются с ростом концентрации растворенного вещества, последнее является следствием формы изотермы адсорбции. Смеси глюкозы и лактозы были легко разделены на колонке. В дальнейшей статье[6] изучается адсорбционный анализ некоторых аминокислот и пептидов, следовые количества цианидов, добавляемых для ингибирования каталитического окисления этих веществ на колонке с углем. Из алифатических аминокислот, глицин не адсорбируется, но длина углеродной цепи имеет решающее влияние, одна СН2 группа значительно увеличивает удерживаемый объём. Ароматические аминокислоты выходят значительно медленнее.
С Клайсеном[7] было сделано важное техническое продвижение путём применения интерферометрических методов для измерения концентрации растворенных веществ в колонке, в особенности для веществ в органических растворителях. Главным объектом этого исследования было преодоление нестабильности, возникающей из очень незначительных различий плотностей между различными слоями элюата. Объём интерферометрического оптического канала был только 0.13 мл, и аппаратура нагревалась. В дополнение, был обеспечен примитивный коллектор фракций с ручным управлением для сбора сточных фракций. Оборудование можно рассматривать как предшественника сложных современных полностью автоматизированных хроматографических анализ-фракционированных сборников. Эта экспериментальная установка исключительно хорошо подходила для детального изучения фундаментальных процессов, лежащих в хроматографическом анализе, и его использование привело к некоторым важным теоретическим достижениям и их экспериментальным проверкам.
Различия указывали на связь между фронтальным анализом, анализом элюции и анализом перемещения. Во фронтальном анализе раствор подается непрерывно в колонку и из-за различия удерживаемых объёмов, серии градиентов концентрации, соответствующие различным растворенным веществам, напоминают ситуацию двигающихся границ электрофореза. С такой процедурой полное разделение компонентов в смеси невозможно, только их идентификация и оценка.
В анализе элюции образец раствора вносили в колонку последовательно за растворителем, и в этих условиях наблюдался ряд постепенно разделенных зон. Преимущественно, нелинейная форма изотерм адсорбции вызывается более сильным адсорбционным связыванием при низких концентрациях, чем при более высоких, и это производит характерное явление «хвоста» в концентрационном профиле разделительных зон, которые были быстро очерчены интерферометрическим оптической системой регистрации. Ликвидация размытия является ключевой проблемой хроматографического разделения и привела к обширным исследованиям Тиселиуса с несколькими сотрудниками. В общих чертах проблемой является выбор и создание условий после первоначальной адсорбции, которые повлекут за собой изменение, производящее линейное поведение при адсорбции веществ при разделении.
Первоначально[8] эти соображения привели Тиселиуса к рассмотрению потенциальных возможностей развития смещения (позже упоминается как «анализ смещения»), которое не зависит от линейности изотерм. В этой процедуре разделение смеси веществ осуществляется с помощью раствора, в том же растворителе — веществе, обладающем более высоким адсорбционным сродством, чем другие в смеси. При условии, что концентрация точно выбрана по отношению к изотермам компонентов при разделении, появляется устойчивое состояние. Компоненты отделяются полностью в смежных зонах, индивидуальные концентрации остаются постоянными и не зависят от длины адсорбционной колонки, длина зоны пропорциональна количеству конкретного компонента. Детальные исследования были сделаны позже с Л. Хакдалом и Р. И. П. Уильямсом (L. Hagdahl and R. I. P. Williams) со специальной ссылкой на хроматографию на угле. Эти авторы[9] разработали модификацию анализа смещений, которая улучшила процедуру подготовительного процесса.
В большей части своей работы по анализу адсорбции Тиселиус использует активированный уголь в качестве адсорбента, также были предприняты многие попытки изменить его адсорбционные свойства различными предварительными обработками. Фосфат кальция в гидроксиапатитной форме был рассмотрен в качестве адсорбента для белков, в сочетании с фосфатным буфером в качестве элюирующего вещества. Но окончательное решение проблемы для хроматографии белка пришло с развитием целлюлозных ионообменников по Петерсону и Соберу (1956). Решающие вклады Тиселиуса и его сотрудников лежат в выявлении фундаментальных процессов хроматографии.
Комитет по работе и международной деятельности[править | править код]
В середине сороковых годов Тиселиус предпринял новые виды деятельности, совмещая их с руководством и консультированием своих коллег и студентов.
В 1942 Швеция создала свой первый научно-исследовательский совет. Технологии и механизмы для медицинского исследовательского совета были на стадии рассмотрения. Летом 1944 правительство попросило Тиселиуса стать членом комитета и рекомендовать меры по улучшению условий проведения исследований. Он принимал самое активное участие в работе этой комиссии и посвятил большую часть своей энергии и времени этим проблемам, которые считал основополагающими для будущего шведской науки. Чуть более года после формирования, комитет опубликовал свой первый доклад и предложения.
В дополнение к ряду улучшений для научных факультетов высших учебных заведений, предложения привели к становлению шведского естествознания исследовательского совета, Тиселиус был назначен правительством председателем на срок 4 лет (с 1946 года).
В 1946 году он был связан с Нобелевским комитетом по химии, а с 1947 года стал рядовым членом этого комитета. Позднее, в 1947 году он стал вице-президентом Нобелевского фонда.
Ожидалось его назначение на должность ректора Магнификаса (Magnificus) университета Уппсалы, но сам Тиселиус был против, заявив, что мог бы сделать больше для шведской науки без назначения его на должность ректора. На первом международном съезде химиков после войны, состоявшейся в Лондоне в 1947 под эгидой Международного союза чистой и прикладной химии (I. U. P. A. C.), он был избран вице-президентом, отвечающим за раздел биологической химии. Четыре года спустя на I. U. P. A. C. конференции в Вашингтоне, в 1951 г., он был избран президентом Союза на четыре года.
В 1955 его попросили присоединиться к комитету, который сформировал «Шведское национальное общество по исследованию рака», и он стал председателем своего исследовательского комитета.
Он был очень активен в шестидесятых в создании Совета консультативной науки правительства Швеции, который под председательством премьер-министра занимается шведской исследовательской политикой. Он стал членом этого совета и его «рабочей группы» с момента её создания в 1962 году и оставался её членом до 1968 года.
Тиселиус стал все больше внимания уделять проблемам, связанным с международным сотрудничеством в области науки.
В период 1960-64 годов Тиселиус являлся президентом Нобелевского фонда, и в этом качестве он выступал со вступительным словом каждый год на Нобелевском фестивале в декабре. В 1961 году, в год 60-летия с момента презентации первых Нобелевских премий, Тиселиус использовал этот повод, чтобы сделать обзор событий этих лет и акцентироваться на некоторых из проблем, созданные эволюцией науки, особенно в последние десятилетия[10]. Он отметил огромный прогресс материальной стороны ограниченной части мира, различия в условиях жизни между людьми, увеличение бедности.
Тиселиус взял на себя инициативу создания Нобелевских симпозиумов в каждом из пяти ветвей Нобелевской премии с целью привлечения ведущих ученых из всех частей мира в области физики, химии, физиологии и медицины, литературы. Участников в каждом Нобелевской симпозиуме обсуждали последние события, пытаясь оценить социальные, этические и другие их последствия. Он пропагандировал идею того, что Нобелевский фонд может и должен играть важную роль в обеспечении научного прогресса, решать наиболее актуальные проблемы человечества в соответствии с духом Альфреда Нобеля.
Награды и звания[править | править код]
- Нобелевская премия по химии (1948).
В ноябре 1948 года Шведская королевская академия наук присудила Нобелевскую премию по химии Арне Тиселиусу за работы по электрофорезу и адсорбционному анализу, особенно за открытие комплекса природных белков, находящихся в сыворотке крови[11].
Ранее Тиселиус безуспешно пытался добиться от шведского правительства выделения средств на строительство Института биохимии в университете Уппсалы. Присуждение Нобелевской премии имело непосредственное влияние на официальное отношение. Ранее он использовал одну из комнат для эксперимента, которая изначально была кладовой. Стокгольмская газета опубликовала карикатуру на отношение к науке, представив Тиселиуса, как человека, который получил Нобелевскую премию за работу на кухне. В течение 1952 года значительно улучшилось финансирование, позволяющее расширить программу, в это же время физическая биохимия привлекала все больше и больше студентов и передовых научных сотрудников. В Уппсале была установлена кафедра медицинской химии на факультете медицины, которая тогда находилась под руководством профессора Г. Бликса (G. Blix), с которым Тиселиус всегда поддерживал тесные контакты.
- Иностранный член Лондонского королевского общества
Увлечения[править | править код]
Тиселиус часто совершал поездки по сельской местности, интересовался историей, естественными науками, имел обширные знания в области ботаники и орнитологии, совершал экспедиции с сыном, наблюдая поведение глухаря и слушая напевы чёрного петуха (П. Тиселиус, 1973), ходил на экскурсии для наблюдения и фотографировани птиц. Этот интерес Тиселиуса привел в июне 1961 к образованию небольшой частной «академии», в Бекхамеровской (Backhammer) Академии наук, которая состояла из группы его друзей, которые имели общие интересы в орнитологии. Академия состояла из пяти мужчин и их жен. Тиселиус был президентом; вице-президентом был д-р Виктор Хаселблад (Dr Victor Hasselblad), конструктор Хаселблад-камеры.
Другими сотрудниками были д-р Аксель Люнгдал (Dr Axel Ljungdahl), бывший генерал ВВС Швеции, который после своей отставки защитил докторскую диссертацию по истории религии; Д-р Крофорд Гринуолт (Dr Crawford Greenewalt), президент компании Дюпон США, который приезжал в Европу каждый год, особенно для участия в заседаниях Академии, и, наконец, известный шведский орнитолог, д-р П. О. Сванберг (Dr P. О. Swanberg). Академия собиралась около десяти дней каждый год, обычно весной в Джонсбольской (Jonsbol) усадьбе, принадлежащей доктору Хасельбладу и когда-то являвшейся частью имения Бекхамер, совершали экскурсии в различные части Вермланда, изучали и фотографировали птиц этой части Швеции.
Когда Тиселиус был награждён почетной степенью в Пражском университете в 1969, Академия совершила первую экспедицию в Чехословакии, а затем в Румынии для изучения жизни птиц в этих странах.
Эти ежегодные встречи сыграли большую роль в жизни Тиселиуса и были просто видом отдыха и релаксации.
Память[править | править код]
- После смерти Арне Тиселеуса над его идеями продолжали работу его соратники. В рамках семинара марта 1972 на Вилле Сербеллони под эгидой Фондов Нобеля и Рокфеллера, было задумано создание Международной федерации институтов перспективных исследований (I.F.I.A.S.), неправительственной организации, состоящей к 1974 году из двадцати видных научно-исследовательских институтов, охватывающих десять дисциплин и расположенных в пятнадцати странах, планирующих научно-технические или альтернативные решения крупных мировых проблем. Штаб-квартира I.F.I.A.S. находиться в Стокгольме.
- В 1979 г. Международный астрономический союз присвоил имя Арне Тиселиуса кратеру на обратной стороне Луны.
Литература[править | править код]
- Farber Е., Nobel prize winners in chemistry 1901—1950, N. Y., 1953.
- Abderhalden E., Die Methoden zur Bestimmung der Beweglichkeit und der Ladung kolloider Teilchen. In Handbuch der biologischen Arbeitsmethoden, vol. IIIB, pp. 629—678,1927.
- The moving boundary method of studying the electrophoresis of proteins, Nova Acta R. Soc. Scient. Upsal., V. 7, no. 4, 1-107, 1930/
- Uber den Einfluss der Ladung auf die Sedimentationsgeschwindigkeit von Kolloiden, besonders in der Ultrazentrifuge, Kolloidzeitschrift, V. 59, 306—309, 1932.
- Matningar av proteiners elektrofores. Forh. 4 nord. Kem. Mot, pp. 252-25, 1933.
- Svedberg T., Colloid chemistry. Revised and enalarged in collaboration with Arne Tiselius., N. Y., 1928.
- Kekwick R.A., Arne Tiselius. 1902—1971., 1974.
Примечания[править | править код]
- ↑ ARNE TISELIUS. AN ELECTROPHORETIC STUDY OF IMMUNE SERA AND PURIFIED ANTIBODY PREPARATIONS. — 1938. — № 69. — С. 119—131.
- ↑ [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2142056/pdf/151.pdf THE pH STABILITY OF PROTYROSINASE AND TYROSINASE* BY THOMAS HUNTER ALLEN, ARTHUR B. OTIS, Am) JOSEPH HALL BODINE]. The Journal of General Physiology.
- ↑ Arne Tiselius. Stationary electrolysis of ampholyte solutions // Svensk kem. Tidskr.. — № 53. — С. 305—310.
- ↑ . Adsorption analysis: Experimental arrangement and some results with mixtures of glucose and lactose // Ark. Kemi Miner. Geol. 14 B. — № 32. — С. 1—8.
- ↑ Arne Tiselius. A new method for adsorption analysis of solutions // Ark. Kemi Miner. Geol. 14 B. — № 22. — С. 1—5.
- ↑ Arne Tiselius. Adsorption analysis of amino acids and peptides // Ark. Kemi Miner. Geol. 15 B. — № 6. — С. 1—5.
- ↑ Arne Tiselius. Adsorption analysis by interferometric observation // Ark. Kemi Miner. Geol. 15 B. — 1942. — № 18. — С. 1—6.
- ↑ Arne Tiselius. Displacement development in adsorption analysis // Ark. Kemi Miner. Geol. 16 B. — № 18. — С. 1—11.
- ↑ . Arne Tiselius. Elution and displacement analysis procedures with special reference to chromatography on carbon // Ark. Kemi 4. — С. 193—219.
- ↑ Discours solennel par le Président de la Foundation Nobel, 1e Professeur A. Tiselius // Prix Nobel. — 1961. — С. 13—16.
- ↑ Arne Tiselius. Electrophoresis and adsorption analysis as aids in investigations of large molecular weight substances and their breakdown products // Amsterdam: Elsevier Publishing Co. — 1964.
Ссылки[править | править код]
- Информация на сайте Нобелевского комитета (англ.)
- Тиселиус (Tiselius) Арне // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
Для улучшения этой статьи желательно:
|
- Родившиеся 10 августа
- Родившиеся в 1902 году
- Персоналии по алфавиту
- Родившиеся в Стокгольме
- Умершие 29 октября
- Умершие в 1971 году
- Умершие в Уппсале
- Преподаватели Уппсальского университета
- Выпускники Уппсальского университета
- Лауреаты Нобелевской премии по алфавиту
- Учёные по алфавиту
- Лауреаты Нобелевской премии по химии
- Биохимики Швеции
- Биологи XX века
- Лауреаты Нобелевской премии из Швеции
- Члены Шведской королевской академии наук
- Иностранные члены Лондонского королевского общества
- Иностранные члены Национальной академии наук США
- Иностранные члены Индийской национальной академии наук
- Похороненные на Старом кладбище (Уппсала)
- Члены-корреспонденты Французской академии наук
- Члены Шведской королевской академии инженерных наук
- Президенты Международного союза теоретической и прикладной химии
- Почётные доктора Болонского университета
- Почётные доктора Мадридского университета Комплутенсе