Гормональный пластырь
Противозачаточный пластырь представляет собой трансдермальный пластырь, наносимый на кожу, который выделяет синтетические гормоны эстроген и прогестоген для предотвращения беременности. Было показано, что они столь же эффективны, как и комбинированные оральные противозачаточные таблетки, при идеальном использовании, а пластырь может быть более эффективным при типичном использовании[1][2].
Xulane[3] и Twirla[4] одобрены для использования в США. Evra одобрена для использования в Канаде и продаётся компанией Janssen Inc.[5], и она одобрена для использования в Великобритании[6] и в Европе[7] и продаётся компанией Janssen-Cilag[6][7]. Пластыри упакованы в коробки по три штуки и доступны только по рецепту[3].
Медицинское использование[править | править код]
Поскольку пластырь работает так же, как и противозачаточные таблетки, многие из преимуществ такие же. Например, пластырь может сделать месячные у женщины более лёгкими и регулярными. Он также может помочь очистить прыщи, уменьшить спазмы и уменьшить симптомы ПМС.
Пластырь — это простой и удобный способ контроля рождаемости, требующий еженедельного внимания. Когда женщина перестает использовать пластырь, её способность забеременеть быстро возвращается[8].
Побочные эффекты[править | править код]
В трёх крупных клинических испытаниях с участием 3330 женщин, использующих пластырь Ortho Evra / Evra в течение периода до одного года, 12% пользователей прекратили использование пластыря из-за побочных эффектов. Наиболее частыми побочными эффектами, приведшими к отмене пластыря, были: тошнота и/или рвота (2,4%), реакция в месте нанесения (1,9%), дискомфорт в груди, нагрубание или боль (1,9%), головная боль (1,1%) и эмоциональная неустойчивость (1,0%)[9].
Прорывное кровотечение и/или кровянистые выделения при использовании пластыря Ortho Evra / Evra фиксировались: 18% в цикле 1, 12% в цикле 3, 8% в цикле 6 и 13 цикле. Прорывное кровотечение (требуется более одной прокладки или тампона на один день) сообщили: 4% в цикле 1, 3% в цикле 3 и 6 и 1% в цикле 13[10].
Дополнительная информация о побочных эффектах представлена на этикетке Ortho Evra, а также в инструкции по применению препаратов Evra (SPC) и PIL[3][6][11].
Взаимодействия и противопоказания[править | править код]
Противозачаточный пластырь и другие комбинированные гормональные контрацептивы противопоказаны женщинам старше 35 лет, курящим сигареты[3].
Противозачаточный пластырь противопоказан к применению женщинам с индексом массы тела ≥ 30 кг/м2[3].
Тромбоэмболия[править | править код]
Все комбинированные гормональные противозачаточные средства дают очень небольшое повышение риска серьёзных или фатальных тромбоэмболических событий. Продолжаются исследования риска тромбоэмболии от Ortho Evra по сравнению с комбинированными пероральными противозачаточными таблетками. Недавнее исследование показало, что у пользователей противозачаточных пластырей может быть вдвое повышен риск нефатальных венозных тромбоэмболических событий по сравнению с женщинами, принимавшими пероральные контрацептивы, содержащие норгестимат, с 35 мкг эстрогена[12][13]. Однако другое исследование пришло к выводу, что риск нефатальной венозной тромбоэмболии для противозачаточного пластыря аналогичен риску для оральных контрацептивов, содержащих 35 мкг этинилэстрадиола и норгестимат[14]. Противоречие в выводах между двумя исследованиями нелегко разрешить, потому что доверительные интервалы для исследований перекрываются.
В исследованиях с оральными контрацептивами риск сердечно-сосудистых заболеваний (таких как тромбоэмболия) значительно повышается у женщин старше 35 лет, которые также курят табак[15].
10 ноября 2005 года Ortho McNeil совместно с FDA пересмотрели этикетку для Ortho Evra, включая новое выделенное жирным шрифтом предупреждение о более высоком воздействии эстрогена на женщин, использующих еженедельный пластырь по сравнению с ежедневным приёмом противозачаточных таблеток, содержащих 35 мкг эстрогена, отмечая, что более высокий уровень эстрогена может подвергнуть некоторых женщин повышенному риску образования тромбов. Этикетка была снова пересмотрена в сентябре 2006 года, а 18 января 2008 года FDA снова обновило этикетку, чтобы отразить результаты исследования: «FDA считает, что Ortho Evra является безопасным и эффективным методом контрацепции при использовании в соответствии с этикеткой, которая рекомендует женщинам, у которых есть проблемы или факторы риска для серьезных тромбов, поговорить со своим врачом об использовании Ortho Evra по сравнению с другими вариантами контрацепции»[16].
Метод использования[править | править код]
Женщина накладывает свой первый пластырь на верхнюю часть руки, ягодицы, живот или бедро в первый день менструального цикла (день 1) или в первое воскресенье после этого дня, в зависимости от того, что она предпочитает. С этого момента день применения известен как день смены пластыря. В следующий день смены пластыря пластырь удаляется и не заменяется. Женщина проводит семь дней без пластыря, а в следующий день смены пластыря накладывает новый пластырь. Были изучены схемы расширенного использования, при которых пластыри используются в течение нескольких недель до недели без пластырей[17].
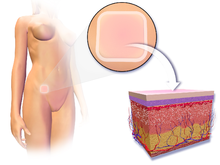
Пластырь следует наносить на чистую, сухую и неповреждённую кожу. Это означает, что если кожа красная, раздражённая или порезанная, накладывать пластырь на эту область не следует. Кроме того, следует избегать использования лосьонов, пудры или макияжа вокруг области, на которую накладывается или будет помещён пластырь[18].
Механизм действия[править | править код]
Как и все комбинированные гормональные контрацептивы, Ortho Evra / Evra работает, прежде всего, путём предотвращения овуляции. Вторичный механизм действия — ингибирование проникновения сперматозоидов за счёт изменений цервикальной слизи. Гормональные противозачаточные средства также влияют на эндометрий, что теоретически может повлиять на имплантацию; однако никакие научные данные не указывают на то, что предотвращение имплантации фактически является результатом их использования[19].
Контрацептивный пластырь Ortho Evra площадью 20 см2 содержит 750 мкг этинилэстрадиола (эстроген) и 6000 мкг норэлгестромина (прогестин)[3]. Противозачаточный пластырь Evra 20 см2 содержит 600 мкг этинилэстрадиола и 6000 мкг норэлгестромина[6]. Противозачаточные пластыри Ortho Evra и Evra предназначены для постепенного высвобождения в системный кровоток приблизительно 20 мкг/день этинилэстрадиола и 150 мкг/день норэлгестромина[3][6].
Примечания[править | править код]
- ↑ Trussell, James. Contraceptive Efficacy // Contraceptive Technology / Hatcher, Robert A.. — 19th rev. — New York : Ardent Media, 2007. — ISBN 978-0-9664902-0-6.
- ↑ Contraceptive Technology, Chapter 12, Contraceptive Patch and Vaginal Contraceptive Ring, by Kavita Nanda, page 272
- ↑ 1 2 3 4 5 6 7 Xulane- norelgestromin and ethinyl estradiol patch. DailyMed (19 апреля 2017). Дата обращения: 17 февраля 2020. Архивировано 6 июля 2020 года.
- ↑ FDA Approves Agile Therapeutics, Inc.'s Twirla (levonorgestrel and ethinyl estradiol) Transdermal System – A New Weekly Contraceptive Patch Delivering a 30 mcg Daily Dose of Estrogen and 120 mcg Daily Dose of Progestin. Agile Therapeutics (14 февраля 2020). Дата обращения: 17 февраля 2020. Архивировано 29 января 2021 года.
- ↑ Evra Product information. Health Canada (21 июня 2018). Дата обращения: 17 февраля 2020. Архивировано 18 февраля 2020 года.
- ↑ 1 2 3 4 5 Evra transdermal patch - Summary of Product Characteristics (SmPC). (emc) (29 ноября 2018). Дата обращения: 17 февраля 2020. Архивировано из оригинала 7 ноября 2017 года.
- ↑ 1 2 Evra EPAR. European Medicines Agency (17 сентября 2018). Дата обращения: 18 февраля 2020. Архивировано 12 ноября 2020 года.
- ↑ Planned Parenthood (2011). "Birth Control Patch (Ortho Evra)." Retrieved from http://www.plannedparenthood.org/health-topics/birth-control/birth-control-patch-ortho-evra-4240.htm Архивная копия от 11 апреля 2014 на Wayback Machine, on February 3, 2011.
- ↑ Sibai BM, Odlind V, Meador ML, Shangold GA, Fisher AC, Creasy GW (2002). "A comparative and pooled analysis of the safety and tolerability of the contraceptive patch (Ortho Evra/Evra)". Fertil Steril. 77 (2 Suppl 2): S19—26. doi:10.1016/S0015-0282(01)03264-2. PMID 11849632.
- ↑ Zieman M, Guillebaud J, Weisberg E, Shangold GA, Fisher AC, Creasy GW GW (2002). "Contraceptive efficacy and cycle control with the Ortho Evra/Evra transdermal system: the analysis of pooled data". Fertil Steril. 77 (2 Suppl 2): S13—8. doi:10.1016/S0015-0282(01)03275-7. PMID 11849631.
- ↑ Janssen-Cilag. Evra Patient Information Leaflet (PIL) (26 января 2007). Дата обращения: 20 июля 2007. Архивировано 28 сентября 2007 года.
- ↑ Medpage Today. Evidence on Ortho Evra Patch Thrombosis Risk Is Contradictory Архивировано 1 марта 2006 года.. Published February 17, 2006.
- ↑ Cole JA, Norman H, Doherty M, Walker AM (February 2007). "Venous thromboembolism, myocardial infarction, and stroke among transdermal contraceptive system users". Obstet Gynecol. 109 (2 Pt 1): 339—46. doi:10.1097/01.AOG.0000250968.82370.04. PMID 17267834.
- ↑ Jick S, Kaye JA, Li L, Jick H (July 2007). "Further results on the risk of nonfatal venous thromboembolism in users of the contraceptive transdermal patch compared to users of oral contraceptives containing norgestimate and 35 microg of ethinyl estradiol". Contraception. 76 (1): 4—7. doi:10.1016/j.contraception.2007.03.003. PMID 17586129.
- ↑ Pitsavos C, Stefanadis C, Toutouzas P (2000). "Contraception in women at high risk or with established cardiovascular disease". Ann. N. Y. Acad. Sci. 900 (1): 215—27. Bibcode:2000NYASA.900..215P. doi:10.1111/j.1749-6632.2000.tb06233.x. PMID 10818409.
- ↑ FDA Approves Update to Label on Birth Control Patch. FDA. January 18, 2008 Архивировано 12 мая 2009 года.
- ↑ Stewart FH, Kaunitz AM, Laguardia KD, Karvois DL, Fisher AC, Friedman AJ (June 2005). "Extended use of transdermal norelgestromin/ethinyl estradiol: a randomized trial". Obstet Gynecol. 105 (6): 1389—96. doi:10.1097/01.AOG.0000160430.61799.f6. PMID 15932834.
- ↑ Mayo Clinic (2010). "Ortho Evra (Contraceptive Patch)." Retrieved from http://www.mayoclinic.com/health/ortho-evra/MY01006/DSECTION=what-you-can-expect Архивная копия от 15 октября 2012 на Wayback Machine, on February 3, 2011.
- ↑ Rivera R, Yacobson I, Grimes D (1999). "The mechanism of action of hormonal contraceptives and intrauterine contraceptive devices". Am J Obstet Gynecol. 181 (5 Pt 1): 1263—9. doi:10.1016/S0002-9378(99)70120-1. PMID 10561657.
Ссылки[править | править код]
- Ethinyl Estradiol mixture with norelgestromin. Drug Information Portal. U.S. National Library of Medicine.
- Feminist Women's Health Center
- Planned Parenthood: The Patch
