Рецептор, активируемый пероксисомным пролифератором альфа
Рецептор, активируемый пероксисомным пролифератором альфа (англ. Peroxisome proliferator-activated receptor alpha, сокр. PPAR-α), также известный как NR1C1 (подсемейство ядерных рецепторов 1, группа C, тип 1) представляет собой белок — ядерный рецептор, функционирующий как транскрипционный фактор, который у человека кодируется геном PPARA, локализованный на длинном плече (q-плече) 22-й хромосомы[5]. Вместе с дельта-рецептором, и гамма-рецептором, активируемые пероксисомным пролифератором, PPAR-альфа является частью подсемейства рецепторов, активируемых пероксисомным пролифератором. Это был первый член семейства PPAR, клонированный в 1990 году Стивеном Грином, и он был идентифицирован как ядерный рецептор разнообразного класса гепатоканцерогенов грызунов, вызывающих пролиферацию пероксисом[6].
Полипептидная цепь белка включает в себя 468 аминокислот, а молекулярная масса составляет — 52225 Да[7].
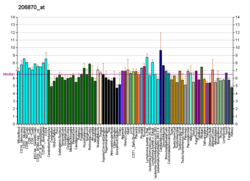
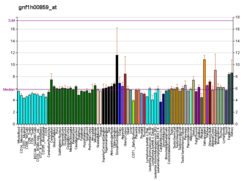
Экспрессия[править | править код]
PPAR-α в первую очередь активируется посредством связывания лиганда. Эндогенные лиганды включают жирные кислоты, такие как арахидоновая кислота (С20), а также другие полиненасыщенные жирные кислоты и различные соединения, производные жирных кислот, такие как некоторые члены семейства 15-гидроксиэйкозатетраеновой кислоты (15-ГЭТЕ) метаболитов арахидоновой кислоты, например, 15(S)-ГЭТЕ, 15(R)-ГЭТЕ и 15(S)-ГПЭТЕ и 13-гидроксиоктадекадиеновая кислота, метаболит линолевой кислоты. Синтетические лиганды включают фибраты, которые используются для лечения гиперлипидемии, а также разнообразный набор инсектицидов, гербицидов, пластификаторов и органических растворителей, которые вместе называются пролифераторами пероксисом.
Выполняемые функции[править | править код]
PPAR-α — транскрипционный фактор, регулируемый свободными жирными кислотами, и является одним из основных регуляторов липидного обмена в печени[8]. PPAR-альфа активируется в условиях энергетического голодания и необходим для процесса кетогенеза, ключевого адаптивного ответа на длительное голодание[9][10]. Активация PPAR-альфа способствует поглощению, утилизации и катаболизму жирных кислот путём регуляции генов, участвующих в транспорте жирных кислот, связывании и активации жирных кислот, а также в пероксисомальном и митохондриальном β-окислении жирных кислот[11]. Активации окисления жирных кислот способствует повышенная экспрессия CPT1 (который доставляет длинноцепочечные липиды в митохондрии) под действием PPAR-α[12]. PPAR-α также подавляет гликолиз, одновременно способствуя глюконеогенезу и синтезу гликогена в печени[8].
В макрофагах PPAR-α подавляет поглощение гликированного липопротеина низкой плотности (холестерина ЛПНП), препятствует образованию пенистых клеток (атеросклероз) и ингибирует провоспалительные цитокины[12].

Распределение по тканям[править | править код]
Экспрессия PPAR-α наиболее высока в тканях, которые быстро окисляют жирные кислоты. У грызунов самые высокие уровни экспрессии мРНК PPAR-альфа обнаружены в печени и бурой жировой ткани, затем в сердце и почках[13]. Более низкие уровни экспрессии PPAR-альфа обнаружены в тонком и толстом кишечнике, скелетных мышцах и надпочечниках. У человека PPAR-альфа экспрессируется более равномерно в различных тканях, с высокой экспрессией в печени, кишечнике, сердце и почках.
Нокаутные исследования[править | править код]
Исследования, проведенные на мышах, лишённых функциональных PPAR-альфа, показывают, что PPAR-α необходимы для индукции пролиферации пероксисом под действием различных синтетических соединений, называемых пероксисомными пролифераторами[14]. У мышей, лишённых PPAR-альфа, также нарушается реакция на голодание, характеризующаяся серьёзными метаболическими нарушениями, включая низкий уровень кетоновых тел в плазме, гипогликемию и жировую дистрофию печени[9].
Фармакология[править | править код]
PPAR-α является фармацевтической мишенью фибратов, класса препаратов, используемых для лечения дислипидемии. Фибраты эффективно снижают уровень триацилглицеридов в сыворотке крови и повышают уровень холестерина ЛПВП («хорошего холестерина»)[15]. Хотя клиническая польза от лечения фибратами была отмечена, общие результаты неоднозначны и заставляют сомневаться в широком применении фибратов для лечения ишемической болезни сердца, в отличие от статинов. Агонисты PPAR-α могут иметь терапевтическое значение для лечения неалкогольной жировой болезни печени. PPAR-альфа также может быть местом действия некоторых противосудорожных препаратов[16][17].
Эндогенное соединение, 7(S)-гидроксидокозагексаеновая кислота (7(S)-HDHA, которая является докозаноидным производным омега-3 жирной кислоты DHA, была выделена в качестве эндогенного высокоаффинного лиганда для PPAR-альфа в мозге крыс и мышей. Энантиомер 7(S) связывался с PPAR-альфа с микромолярной аффинностью, в 10 раз более высокой по сравнению с энантиомером (R), и мог вызывать дендритную активацию[18]. Предыдущие доказательства функции этого соединения были умозрительными, основанными на структуре и изучении химического синтеза[19].
Как диеты с высоким содержанием сахара, так и диеты с низким содержанием белка повышают уровень циркулирующего в печени эндокринного FGF21 у людей посредством PPAR-α, хотя этот эффект может сопровождаться FGF21-резистентностью[20].
Гены-мишени[править | править код]
PPAR-α регулирует биологические процессы, изменяя экспрессию большого количества генов-мишеней. Соответственно, функциональная роль PPAR-альфа напрямую связана с биологической функцией его генов-мишеней. Исследования по профилю экспрессии генов показали, что число генов-мишеней PPAR-альфа исчисляется сотнями[11]. Классические гены-мишени PPAR-альфа включают PDK4, ACOX1 и CPT1. Анализ экспрессии генов с низкой и высокой пропускной способностью позволил создать всеобъемлющие карты, иллюстрирующие роль PPAR-альфа как главного регулятора липидного обмена через регуляцию множества генов, вовлечённых в различные аспекты липидного обмена. Эти карты, построенные для печени мыши и человека, ставят PPAR-альфа в центр регуляторного узла, влияющего на поглощение и внутриклеточное связывание жирных кислот, митохондриальное β-окисление и пероксисомальное окисление жирных кислот, кетогенез, обмен триацилглицеридов, глюконеогенез и синтез/секрецию желчи.
Взаимодействия[править | править код]
Было показано, что PPAR-α взаимодействует с:
- AIP[21],
- EP300[22][23]
- HSP90AA1[21],
- NCOA1[22][24], и
- NCOR1[23]
- Пальмитоилэтаноламид (ПЭА)
- Олеоилэтаноламид (ОЭА)
- Анандамид (AEA)
- 7( S)-гидроксидокозагексаеновая кислота (7-HDoHE)[18]
- PFAS[25].
См. также[править | править код]
Примечания[править | править код]
- ↑ 1 2 3 GRCh38: Ensembl release 89: ENSG00000186951 - Ensembl, May 2017
- ↑ 1 2 3 GRCm38: Ensembl release 89: ENSMUSG00000022383 - Ensembl, May 2017
- ↑ Ссылка на публикацию человека на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ↑ Ссылка на публикацию мыши на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ↑ Sher T, Yi HF, McBride OW, Gonzalez FJ (June 1993). "cDNA cloning, chromosomal mapping, and functional characterization of the human peroxisome proliferator activated receptor". Biochemistry. 32 (21): 5598—604. doi:10.1021/bi00072a015. PMID 7684926.
- ↑ Issemann I, Green S (October 1990). "Activation of a member of the steroid hormone receptor superfamily by peroxisome proliferators". Nature. 347 (6294): 645—54. Bibcode:1990Natur.347..645I. doi:10.1038/347645a0. PMID 2129546. S2CID 4306126.
- ↑ UniProt, Q07869 (англ.).
- ↑ 1 2 Peeters A, Baes M (2010). "Role of PPARα in Hepatic Carbohydrate Metabolism". PPAR Research. 2010: 572405. doi:10.1155/2010/572405. PMC 2948921. PMID 20936117.
- ↑ 1 2 Kersten S, Seydoux J, Peters JM, Gonzalez FJ, Desvergne B, Wahli W (June 1999). "Peroxisome proliferator-activated receptor alpha mediates the adaptive response to fasting". J Clin Invest. 103 (11): 1489—98. doi:10.1172/JCI6223. PMC 408372. PMID 10359558.
- ↑ Grabacka M, Pierzchalska M, Dean M, Reiss K (2016). "Regulation of Ketone Body Metabolism and the Role of PPARα". International Journal of Molecular Sciences. 17 (12): E2093. doi:10.3390/ijms17122093. PMC 5187893. PMID 27983603.
- ↑ 1 2 Kersten S (2014). "Integrated physiology and systems biology of PPARα". Molecular Metabolism. 3 (4): 354—371. doi:10.1016/j.molmet.2014.02.002. PMC 4060217. PMID 24944896.
- ↑ 1 2 Rigamonti E, Chinetti-Gbaguidi G, Staels B (2008). "Regulation of macrophage functions by PPAR-alpha, PPAR-gamma, and LXRs in mice and men". Arteriosclerosis, Thrombosis, and Vascular Biology. 28 (6): 1050—1059. doi:10.1161/ATVBAHA.107.158998. PMID 18323516. S2CID 26425698.
- ↑ Braissant O, Foufelle F, Scotto C, Dauça M, Wahli W (January 1995). "Differential expression of peroxisome proliferator-activated receptors (PPARs): tissue distribution of PPAR-alpha, -beta, and -gamma in the adult rat". Endocrinology. 137 (1): 354—66. doi:10.1210/endo.137.1.8536636. PMID 8536636.
- ↑ Lee SS, Pineau T, Drago J, Lee EJ, Owens JW, Kroetz DL, Fernandez-Salguero PM, Westphal H, Gonzalez FJ (June 1995). "Targeted disruption of the alpha isoform of the peroxisome proliferator-activated receptor gene in mice results in abolishment of the pleiotropic effects of peroxisome proliferators". Mol Cell Biol. 15 (6): 3012—22. doi:10.1128/MCB.15.6.3012. PMC 230532. PMID 7539101.
- ↑ Staels B, Maes M, Zambon A (September 2008). "Peroxisome Fibrates and future PPARα agonists in the treatment of cardiovascular disease". Nat Clin Pract Cardiovasc Med. 5 (9): 542—53. doi:10.1038/ncpcardio1278. PMID 18628776. S2CID 23332777.
- ↑ Puligheddu M, Pillolla G, Melis M, Lecca S, Marrosu F, De Montis MG, Scheggi S, Carta G, Murru E, Aroni S, Muntoni AL, Pistis M (2013). "PPAR-alpha agonists as novel antiepileptic drugs: preclinical findings". PLOS ONE. 8 (5): e64541. Bibcode:2013PLoSO...864541P. doi:10.1371/journal.pone.0064541. PMC 3664607. PMID 23724059.
- ↑ Citraro R, Russo E, Scicchitano F, van Rijn CM, Cosco D, Avagliano C, Russo R, D'Agostino G, Petrosino S, Guida F, Gatta L, van Luijtelaar G, Maione S, Di Marzo V, Calignano A, De Sarro G (2013). "Antiepileptic action of N-palmitoylethanolamine through CB1 and PPAR-α receptor activation in a genetic model of absence epilepsy". Neuropharmacology. 69: 115—26. doi:10.1016/j.neuropharm.2012.11.017. PMID 23206503. S2CID 27701532.
- ↑ 1 2 Jiabao Liu; et al. (2022). "The omega-3 hydroxy fatty acid 7(S)-HDHA is a high-affinity PPARα ligand that regulates brain neuronal morphology". Science Signaling. 15 (741): eabo1857. doi:10.1126/scisignal.abo1857. PMID 35857636.
- ↑ Zhang M, Sayyad AA, Dhesi A, Orellana A (November 2020). "Enantioselective Synthesis of 7(S)-Hydroxydocosahexaenoic Acid, a Possible Endogenous Ligand for PPARα". J Org Chem. 85 (21): 13621—13629. doi:10.1021/acs.joc.0c01770. PMID 32954732. S2CID 221825661.
- ↑ Flippo KH, Potthoff MJ (2021). "Metabolic Messengers: FGF21". Nature Metabolism. 3 (3): 309—317. doi:10.1038/s42255-021-00354-2. PMC 8620721. PMID 33758421.
- ↑ 1 2 Sumanasekera WK, Tien ES, Turpey R, Vanden Heuvel JP, Perdew GH (February 2003). "Evidence that peroxisome proliferator-activated receptor alpha is complexed with the 90-kDa heat shock protein and the hepatitis virus B X-associated protein 2". J. Biol. Chem. 278 (7): 4467—73. doi:10.1074/jbc.M211261200. PMID 12482853.
- ↑ 1 2 Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M (December 1997). "p300 functions as a coactivator for the peroxisome proliferator-activated receptor alpha". J. Biol. Chem. 272 (52): 33435—43. doi:10.1074/jbc.272.52.33435. PMID 9407140.
- ↑ 1 2 Dowell P, Ishmael JE, Avram D, Peterson VJ, Nevrivy DJ, Leid M (May 1999). "Identification of nuclear receptor corepressor as a peroxisome proliferator-activated receptor alpha interacting protein". J. Biol. Chem. 274 (22): 15901—7. doi:10.1074/jbc.274.22.15901. PMID 10336495.
- ↑ Treuter E, Albrektsen T, Johansson L, Leers J, Gustafsson JA (June 1998). "A regulatory role for RIP140 in nuclear receptor activation". Mol. Endocrinol. 12 (6): 864—81. doi:10.1210/mend.12.6.0123. PMID 9626662.
- ↑ Wolf, Cynthia J.; Schmid, Judith E.; Lau, Christopher; Abbott, Barbara D. (July 2012). "Activation of mouse and human peroxisome proliferator-activated receptor-alpha (PPARα) by perfluoroalkyl acids (PFAAs): further investigation of C4-C12 compounds". Reproductive Toxicology (Elmsford, N.Y.). 33 (4): 546—551. doi:10.1016/j.reprotox.2011.09.009. ISSN 1873-1708. PMID 22107727.