Тетраборан
| Тетраборан | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Тетраборан | ||
| Традиционные названия | Боробутан | ||
| Хим. формула | B4H10 | ||
| Физические свойства | |||
| Состояние | Бесцветный газ | ||
| Молярная масса | 53,32 г/моль | ||
| Плотность |
г.2,39718 г/л ж.0,56-35г/см³ т.0,59-70 г/см³ |
||
| Энергия ионизации | 10,76 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -120; -120,8; -121 °C | ||
| • кипения | 15,4; 16,1; 17,6-18,0 °C | ||
| Энтальпия | |||
| • образования | 57,68 кДж/моль | ||
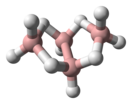
| Структура | |||
| Дипольный момент | 1,6E−30 Кл·м[1] | ||
| Классификация | |||
| Рег. номер CAS | 18283-93-7 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 33592 | ||
| ChemSpider | 21865171 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Тетраборан — неорганическое соединение бора и водорода с формулой B4H10, бесцветный ядовитый газ со специфическим запахом, нестабилен при комнатной температуре.
Получение
- Действием ортофосфорной кислоты на борид магния:
- Пропусканием диборана через печь, нагретую до 180°С, а затем через ловушку, охлажденную до -115°С, для конденсации продуктов реакции.
Физические свойства
- Бесцветный газ, хорошо растворяющийся в бензоле, стабилен при температуре ниже 0 °С. На воздухе может самовоспламениться.
Химические свойства
- При комнатной температуре и нагревании разлагается:
- При комнатной температуре медленно гидролизуется водой:
- Быстрее разлагается растворами щелочей:
- Горит на воздухе (может самовоспламеняться):
- Реагирует с хлором:
- При нагревании реагирует с аммиаком:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5




![{\displaystyle {\mathsf {B_{4}H_{10}+4\ NaOH\ {\xrightarrow {\ }}\ 4\ Na[B(OH)_{4}]+11\ H_{2}\uparrow }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/abb383e63de46c573fee3f34bc3b5361063cca8c)


