Гем b
| Гем b | |
|---|---|
   | |
| Общие | |
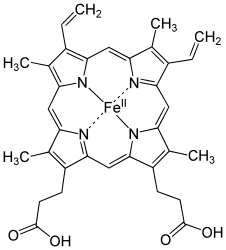
| Традиционные названия | Железный протопорфирин IX, протогем IX |
| Хим. формула | C34H32O4N4Fe |
| Рац. формула | C34H32O4N4Fe |
| Физические свойства | |
| Молярная масса | 616,487 г/моль |
| Классификация | |
| Рег. номер CAS | 14875-96-8 |
| PubChem | 444098 |
| Рег. номер EINECS | 604-649-6 |
| SMILES | |
| InChI | |
| ChEBI | 26355 |
| ChemSpider | 16739950 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гем b (также известный как протогем IX) — наиболее часто встречающийся гем[1], как в гемоглобине, так и в миоглобине. Такое семейство ферментов как пероксидазы тоже содержат в себе гем Б. Циклооксигеназа-1 и циклооксигеназа-2 из малоизвестного семейства семейства циклооксигеназ содержат в себе гем Б как один из своих активных сайтов.
Обычно гем Б крепится к окружающему его белковому матриксу (апоэнзим) посредством координационной связи между железом гема и аминокислотой боковой цепи. Гемоглобин и миоглобин связываются с гемом через гистидин, а синтаза оксида азота и Цитохром P450 через цистеин.
Поскольку железо в белках, содержащих гем Б, связано с четырьмя атомами азота порфирина (образуя плоскость) и одним электронодонорным атомом белка, железо часто находится в пентакоординированном состоянии. При связывании кислорода или токсичного монооксида углерода железо становится гексакоординированным. Правильные структуры гема Б и гема S были впервые выяснены немецким химиком Хансом Фишером[2].
Примечания
[править | править код]- ↑ Ogun, Aminat S.; Joy, Neena V.; Valentine, Menogh (2022), "Biochemistry, Heme Synthesis", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30726014, Архивировано 8 ноября 2022, Дата обращения: 3 января 2023
- ↑ Fischer, H. Die Chemie des Pyrrols / H. Fischer, H. Orth. — Liepzig : Akademische Verlagsgesellschaft, 1934.
