Инсулинотерапия

Инсули́нотерапи́я представляет собой комплекс мер, направленных на достижение компенсации нарушений углеводного обмена с помощью введения в организм пациента препаратов инсулина. В клинической практике применяется, в основном, для лечения сахарного диабета различной этиологии, а также некоторых психических и других заболеваний.
Лечение инсули́ном преследует задачу максимально возможной компенсации нарушений углеводного обмена, предотвращения гипергликемии и профилактики осложнений сахарного диабета. Введение инсулина жизненно необходимо лицам с диабетом 1-го типа и может применяться в ряде ситуаций для лиц с диабетом 2-го типа.[1][2]
Виды инсулина
[править | править код]В настоящее время существует большое количество препаратов инсулина, различающиеся по продолжительности действия (ультракороткие, короткие, средние, пролонгированные), по степени очистки (монопиковые, монокомпонентные), видовой специфичности (человеческие, свиные, бычьи, генноинженерные, и другие)
В России инсулины, получаемые из крупного рогатого скота, выведены из употребления, это связано с большим количеством побочных эффектов при их применении. Достаточно часто при их введении возникают аллергические реакции, липодистрофии, развивается инсулинорезистентность.[1]
Инсулин выпускается в концентрациях 40, 100 и 300 ед/мл. Инсулин распространяется во флаконах объёмом 10 мл или в картриджах для шприц-ручек объёмом 3 мл.[1][2]
Показания
[править | править код]Показания для назначения инсулинотерапии[1]:
- Сахарный диабет 1-го типа
- Кетоацидоз, диабетическая гиперосмолярная, гиперлакцидемическая комы.
- Беременность и роды при сахарном диабете.
- Значительная декомпенсация сахарного диабета 2-го типа.
- Отсутствие эффекта от лечения другими способами сахарного диабета 2-го типа.
- Значительное снижение массы тела при сахарном диабете.
- Диабетическая нефропатия.
Сущность метода
[править | править код]Инсулины разделяются по продолжительности действия на короткого действия и продлённого, время действия инсулина у разных людей индивидуально. В связи с этим подбор инсулинотерапии требует стационарного наблюдения с контролем уровня гликемии, и подбора адекватных метаболизму, диете, физической нагрузке, доз инсулина. При подборе инсулинотерапии следует добиваться максимально возможной компенсации углеводного обмена, чем менее значительными будут суточные колебания уровня глюкозы крови, тем ниже риск возникновения различных осложнений сахарного диабета.[1][2]
В процессе подбора дозы инсулина рекомендуется вести «Дневник самоконтроля» — своеобразный журнал регистрации реально съеденных хлебных единиц углеводов, введенного количества инсулина, степени физической активности и возникших «нештатных» ситуаций в графе «Примечания». Ведение «Дневника самоконтроля» позволяет пациентам систематизировать знания, полученные на занятиях в Школе больного сахарным диабетом и анализировать свои ошибки в ретроспективе.
Инсулинотерапия основана на имитации физиологической секреции инсулина, которая включает:
- базальную секрецию инсулина;
- стимулированную (пищевую) секрецию инсулина.
Базальная секреция обеспечивает оптимальный уровень гликемии в межпищеварительный период и во время сна, способствует утилизации глюкозы, поступающей в организм вне приемов пищи (глюконеогенез, гликолиз). Скорость её составляет 0,5—1 ед/час или 0,16—0,45 ед на кг фактической массы тела, то есть 12—24 ед в сутки. При физической нагрузке и голоде базальная секреция уменьшается до 0,5 ед./час. Секреция стимулированного — пищевого инсулина соответствует уровню постпрандиальной гликемии. Уровень глюкозы крови зависит от уровня съеденных углеводов. На 1 хлебную единицу (ХЕ) вырабатывается, в среднем, примерно 1—1,5 ед. инсулина. Секреция инсулина подвержена суточным колебаниям. В ранние утренние часы (4—5 часов) она самая высокая. В зависимости от времени суток на 1 ХЕ в среднем секретируется:
- на завтрак — 1,5—2,5 ед. инсулина;
- на обед 1,0—1,2 ед. инсулина;
- на ужин 1,1—1,3 ед. инсулина.
Одна единица инсулина снижает сахар крови у каждого по-разному. Из среднесуточной дозы инсулина величина пищевого инсулина составляет примерно 50—60 % (20—30 ед.), а на долю базального инсулина приходится 40—50 %.
Методы инсулинотерапии
[править | править код]Принципы инсулинотерапии (ИТ)
[править | править код]Использование комбинации инсулина короткого действия (ИКД) и инсулина продлённого действия:
- Среднесуточная доза (ССД) инсулина должна быть максимально близка к физиологической секреции.
- При распределении инсулина в течение суток 2/3 ССД должно вводиться утром, днем и ранним вечером и 1/3 — поздним вечером и на ночь.
В течение суток ИКД распределяют следующим образом:
- перед завтраком — 35 %;
- перед обедом — 25 %;
- перед ужином — 30 %;
- на ночь — 10 % от суточной дозы инсулина.
При необходимости в 5—6 часов утра — 4—6 ед. ИКД. Не следует в одной инъекции вводить более 14—16 ед. В случае, если необходимо ввести большую дозу, лучше увеличить количество инъекций, сократив интервалы введения.
Коррекция дозы инсулина
[править | править код]Важную роль в подборе дозы инсулина короткого действия играет расчёт суточных колебаний инсулинопотребности. В связи с физиологическими особенностями организма потребность инсулина для усвоения одной хлебной единицы изменяется в течение суток и может составлять от 0,5 до 4 единиц инсулина на одну ХЕ. Для определения данных показателей необходимо произвести измерения уровня глюкозы крови после основных приёмов пищи, знать количество хлебных единиц съеденных в это время и дозу инсулина короткого действия поставленную на это количество хлебных единиц. Рассчитывается соотношение количества хлебных единиц и количества единиц инсулина. Если уровень глюкозы крови после еды выше нормы, то на следующие сутки доза инсулина увеличивается на 1—2 единицы и рассчитывается, насколько изменился уровень гликемии на 1 единицу инсулина при том же количестве углеводов в данный приём пищи.[3]
Знание индивидуальной инсулинопотребности является необходимым условием для полноценной компенсации углеводного обмена при лечении диабета с помощью интенсифицированной инсулинотерапии. Благодаря знанию индивидуальной потребности инсулина на 1 хлебную единицу, больной может эффективно и безопасно для себя корректировать величину дозы инсулинов короткого действия в зависимости от приёма пищи.[3]
Коррекция доз инсулина по уровню гликемии. Для коррекции доз вводимого инсулина короткого действия Форш рекомендовал на каждые 0,28 ммоль/л сахара крови, превышающего 8,25 ммоль/л, дополнительно вводить 1 ед. Следовательно, на каждый «лишний» 1 ммоль/л глюкозы требуется дополнительно ввести 2—3 ед. инсулина
Коррекция доз инсулина по глюкозурии в настоящее время используется довольно редко в связи с наличием более совершенных способов контроля компенсации углеводного обмена. Для успешной компенсации углеводного обмена в отсутствие глюкометра больной должен уметь рассчитывать инсулинопотребность.
За сутки в промежутках между инъекциями инсулина собирать 4 порции мочи:
- между завтраком и обедом (предварительно, до завтрака, больной должен опорожнить мочевой пузырь);
- между обедом и ужином;
- между ужином и 22 часами;
- от 22 часов и до завтрака.
В каждой порции учитывают диурез, определяют % содержания глюкозы и рассчитывают количество глюкозы в граммах. При выявлении глюкозурии для её устранения на каждые 4—5 г глюкозы дополнительно вводят 1 ед. инсулина. На следующий день после сбора мочи доза вводимого инсулина увеличивается. После достижения компенсации или приближения к ней больной должен быть переведен на комбинацию инсулинов короткого действия и пролонгированных инсулинов. В настоящее время данный способ оценки компенсации углеводного обмена практически не используется, в связи с его низкой точностью, и появлением более эффективных методов самоконтроля.
Наиболее адекватным методом самоконтроля является определение уровня содержания глюкозы в крови. С помощью стационарных или индивидуальных глюкометров.
Виды инсулинотерапии
[править | править код]Традиционная инсулинотерапия. (комбинированная)
[править | править код]Существует метод комбинированной инсулинотерапии, когда в одной инъекции вводится смесь инсулинов короткой и средней или длинной продолжительности действия. Данный метод применяется при лабильном течении сахарного диабета. Преимущество его заключается в том, что он позволяет сократить число инъекций инсулина до 1—3 в сутки. Недостатком является невозможность полноценно имитировать физиологическую секрецию инсулина и, как следствие, невозможность полноценной компенсации углеводного обмена.[1]
При традиционной инсулинотерапии 1 или 2 раза в сутки вводятся препараты, содержащие одновременно инсулины короткого действия и пролонгированные инсулины. Также ранее допускалось смешивание инсулинов короткого и продленного действия в одном шприце; в настоящее время подобное делать не рекомендуется. При этом на долю ИСД приходится 2/3 ССД, а ИКД — 1/3 ССД.
Преимущества:
- простота введения;
- легкость понимания сути лечения больными, их родственниками, медицинским персоналом;
- отсутствие необходимости частого контроля гликемии. Достаточно контролировать гликемию 2—3 раза в неделю, а при невозможности самоконтроля — 1 раз в неделю;
- лечение можно проводить под контролем глюкозурического профиля.
Недостатки:
- необходимость жесткого соблюдения диеты в соответствии с подобранной дозой инсулина;
- необходимость жесткого соблюдения распорядка режима дня, сна, отдыха, физических нагрузок;
- обязательный 5—6-разовый прием пищи, в строго определенное время привязанный к введению инсулина;
- невозможность поддержания гликемии в пределах физиологических колебаний;
постоянная гиперинсулинемия, сопровождающая традиционную инсулинотерапию, повышает риск развития гипокалиемий, артериальной гипертонии, атеросклероза.
Традиционная инсулинотерапия показана пожилым людям, если они не могут усвоить требования интенсифицированной инсулинотерапии, лицам с психическими расстройствами, низким образовательным уровнем, больным, нуждающимся в постороннем уходе, недисциплинированным больным.
Расчет доз инсулина при традиционной инсулинотерапии:
- предварительно определяют среднесуточную дозу инсулина;
- распределяют среднесуточную дозу инсулина по времени суток: 2/3 перед завтраком и 1/3 перед ужином. Из них на долю инсулинов короткого действия должно приходиться 30—40 %, инсулинов длительного действия — 60—70 % от среднесуточной дозы.
Интенсифицированная инсулинотерапии
[править | править код]При отсутствии ожирения и сильных эмоциональных нагрузок инсулин назначается в дозе 0,5—1 единица на 1 килограмм массы тела в сутки. Введение инсулина призвано имитировать физиологическую секрецию в связи с этим выдвигаются следующие требования:[1][2]
- доза инсулина должна быть достаточна для утилизации поступающей в организм глюкозы;
- введённые инсулины должны имитировать базальную секрецию поджелудочной железы;
- введённые инсулины должны имитировать послеедовые пики секреции инсулина.
В связи с этим существует так называемая интенсифицированная инсулинотерапия. Суточная доза инсулина делится между инсулинами продлённого и короткого действия. Продлённые инсулины вводятся, как правило, утром и вечером и имитируют базальную секрецию поджелудочной железы. Инсулины короткого действия вводятся после каждого приёма пищи, содержащей углеводы, доза может меняться в зависимости от хлебных единиц, съеденных в данный приём пищи.[1]
Основные принципы интенсифицированной инсулинотерапии:
- потребность в базальном инсулине обеспечивается двумя инъекциями ИСД, который вводят утром и вечером, или одной инъекцией т. н. ультрадлинных препаратов, обычно на ночь. Суммарная доза ИСД составляет не более 40—50 % от среднесуточной дозы инсулина, 2/3 от суммарной дозы пролонгированного инсулина вводится перед завтраком, 1/3 — перед ужином;
- пищевая — болюсная секреция инсулина имитируется введением инсулинов короткого действия. Необходимые дозы инсулинов короткого действия рассчитываются с учетом планируемого для приема на завтрак, обед и ужин количества ХЕ и уровня гликемии перед приемом пищи ИИТ предусматривает обязательный контроль гликемии перед каждым приемом пищи, через 2 часа после приема пищи и на ночь. То есть больной должен проводить контроль гликемии 7 раз в день.
Преимущества:
- имитация физиологической секреции инсулина (базальной стимулированной);
- возможность более свободного режима жизни и распорядка дня у больного, больной может использовать «либерализованную» диету изменяя время приемов пищи, набор продуктов по своему желанию;
- более высокое качество жизни больного;
- эффективный контроль метаболических расстройств, обеспечивающий предупреждение развития поздних осложнений;
- необходимость обучения больных по проблеме СД, вопросам его компенсации, подсчету ХЕ, умению подбора доз И вырабатывает мотивацию, понимание необходимости хорошей компенсации, профилактики осложнений СД.
Недостатки:
- необходимость постоянного самоконтроля гликемии — до 7 раз в сутки;
- необходимость обучения больных в школах больных СД, изменения ими образа жизни;
- дополнительные затраты на обучение и средства самоконтроля;
- склонность к гипогликемиям, особенно в первые месяцы ИИТ.
Обязательными условиями возможности применения ИИТ являются достаточный интеллект больного, способность обучиться и реализовать приобретенные навыки на практике и возможность приобретения средств самоконтроля.
ИИТ показана:
- при СД1 практически всем больным, а при впервые выявленном СД обязательна;
- при беременности — перевод на ИИТ на весь период беременности, если до беременности больная велась на ТИТ;
- при гестационном СД, в случае неэффективности диеты и ДИФН.
Схема ведения больного при применении ИИТ:
- расчет суточного калоража;
- расчет планируемого для употребления на день количества углеводов в ХЕ, белков и жиров — в граммах. Хотя больной находится на «либерализованной» диете, он не должен съедать за сутки углеводов больше расчетной дозы в ХЕ. Не рекомендуется на 1 прием более 8 ХЕ.
Расчет суммарной дозы базального инсулина проводится любым из вышеуказанных способов. Расчет суммарного пищевого (стимулированного) инсулина проводится исходя из количества ХЕ, которое больной планирует для употребления в течение дня.
Более простые модифицированные методики ИИТ:
- 25 % среднесуточной дозы инсулина вводят перед ужином или в 22 часа в виде пролонгированных инсулинов. Инсулины короткого действия (составляет 75 % среднесуточной дозы) распределяют следующим образом: 40 % перед завтраком, по 30 % — перед обедом и ужином;
- 30 % среднесуточной дозы вводят в виде пролонгированных инсулинов, из них 2/3 дозы перед завтраком, 1/3 перед ужином;
- 70 % среднесуточная дозы вводят в виде инсулинов короткого действия, из них 40 % дозы перед завтраком, 30 % перед обедом, 30 % перед ужином или на ночь.
В дальнейшем показана коррекция доз инсулина в зависимости от состояния углеводного обмена, диеты, уровня физических нагрузок.
Способы введения инсулина
[править | править код]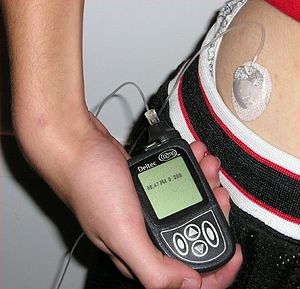
Инсулин вводится подкожно, с помощью инсулинового шприца, шприц-ручки или специальной помпы-дозатора. В настоящее время в России наиболее распространён способ введения инсулина с помощью шприц-ручек. Это связано с бо́льшим удобством, менее выраженным дискомфортом и простотой введения по сравнению с обычными инсулиновыми шприцами. Шприц-ручка позволяет быстро и практически безболезненно ввести необходимую дозу инсулина.
Метод введения инсулина с помощью инсулиновой помпы более распространён в США и странах Западной Европы, но и там он доступен только небольшой части больных — в среднем 2—5 %. Это связано с рядом объективных трудностей, которые в значительной степени нивелируют достоинства данного способа введения инсулина.[4]
К достоинствам данного метода относится более точная имитация физиологической секреции инсулина (препараты инсулина поступают в кровь в течение всего дня), возможность более точного контроля гликемии, отсутствие необходимости самостоятельно вводить инсулин (количество введённого инсулина контролируется помпой), также значительно снижается риск возникновения острых и отдалённых осложнений сахарного диабета. К недостаткам относится сложность устройства, проблемы с его фиксацией на теле, осложнения от постоянного нахождения подающей смесь иглы в теле. Также определённую сложность представляет подбор индивидуального режима работы аппарата. Данный метод введения инсулина считается наиболее перспективным; число людей, использующих инсулиновые помпы, постепенно увеличивается.[4].
Перспективные методы
[править | править код]Основная проблема традиционной инсулинотерапии заключается в низком терапевтическим индексе инсулина, что приводит к высокому риску гипогликемии при передозировке. Как следствие, при разработке новых методов инсулинотерапии уделяется внимание средствам создания постоянной концентрации инсулина в крови и способам автоматического введения инсулина в ответ на повышение уровня глюкозы[5].
Предложен инсулиновый пластырь, покрытый микроскопическими иглами, в каждой из которых находится контейнер с инсулином и глюкозоксидазой. Иголки на пластыре вонзаются в кожу на небольшую глубину, чтобы достичь капилляров и выбрасывать инсулин в ответ на изменение уровня глюкозы в крови. Метод опробован на мышах[6].
Примечания
[править | править код]- ↑ 1 2 3 4 5 6 7 8 Клиническая эндокринология. Руководство / Под ред. Н. Т. Старковой. — 3-е изд., перераб. и доп.. — СПб.: Питер, 2002. — С. 263—270. — 576 с. — («Спутник Врача»). — 4000 экз. — ISBN 5-272-00314-4.
- ↑ 1 2 3 4 Питер Дж. Уоткинс. Сахарный диабет = ABC of Diabetes / М. И. Балаболкина. — 2. — Москва: Бином, 2006. — P. 34—40. — 134 p. — 3000 экз. — ISBN 5-9518-0156-7.
- ↑ 1 2 IX. Интенсивная инсулинотерапия. Дата обращения: 8 августа 2009. Архивировано из оригинала 18 августа 2011 года.
- ↑ 1 2 Питер Дж. Уоткинс. Сахарный диабет = ABC of Diabetes / М. И. Балаболкина. — 2. — Москва: Бином, 2006. — P. 38—46. — 134 p. — 3000 экз. — ISBN 5-9518-0156-7.
- ↑ Alexander N. Zaykov, John P. Mayer, and Richard D. DiMarchi. Pursuit of a perfect insulin (англ.) // Nat. Rev. Drug Discov. — 2016. — Vol. 15. — P. 425—439. — doi:10.1038/nrd.2015.36.
- ↑ Jicheng Yu, Yuqi Zhang, Yanqi Ye, Rocco DiSanto, Wujin Sun, Davis Ranson, Frances S. Ligler, John B. Buse, and Zhen Gu. Microneedle-array patches loaded with hypoxia-sensitive vesicles provide fast glucose-responsive insulin delivery (англ.) // PNAS. — Vol. 112. — P. 8260—8265. — doi:10.1073/pnas.1505405112. Архивировано 27 июня 2015 года.
Литература
[править | править код]- Рубин А. Л. Диабет для «чайников» = Diabetes For Dummies. — 2-е изд. — М.: «Диалектика», 2006. — С. 496. — ISBN 0-7645-6820-5.