Чесотка
| Чесотка | |
|---|---|
 Чесоточный ход | |
| МКБ-11 | 1G04 |
| МКБ-10 | B86 |
| МКБ-10-КМ | B86 |
| МКБ-9 | 133.0 |
| МКБ-9-КМ | 133.0[1][2] |
| DiseasesDB | 11841 |
| MedlinePlus | 000830 |
| eMedicine | derm/382 emerg/517 ped/2047 |
| MeSH | D012532 |
Чесо́тка (лат. scabies) — заразное кожное заболевание (акародерматит), вызываемое чесоточным клещом Sarcoptes scabiei. Передаётся от человека к человеку в результате продолжительного прямого контакта кожа—кожа[3].
Самки чесоточных клещей роют в верхних слоях кожи ходы и откладывают там яйца. Спустя 4—6 недель после заражения у носителя возникает аллергическая реакция, проявляющаяся в виде зуда и папуловезикулёзной сыпи, часто с присоединением вторичных гнойничковых элементов вследствие инфицирования при расчёсывании. Лечение чесотки проводят при помощи инсектицидов.
Является одним из самых распространённых дерматологических заболеваний: предполагается, что чесоткой страдает более 200 миллионов человек. Болезнь наиболее распространена в тропических странах, главным образом среди детей и стариков[4]. Это заболевание внесено в группу забытых (пренебрегаемых) болезней.
История заболевания[править | править код]
Первые описания чесотки выполнены более 2500 лет назад[5]. Чесотка описана в Ветхом Завете и в трудах Аристотеля. В древней Греции чесотку относили к группе кожных заболеваний объединённых термином «псора». В древнем Риме чесотку называли «скабиес», это название сохранилось до наших дней. В средневековых трактатах выдвигались предположения о паразитарной природе чесотки. Достоверные доказательства роли чесоточных клещей в развитии заболевания появляются только после создания оптического микроскопа. В 1687 г. итальянский врач Джован Козимо Бономо и аптекарь Дьячинто Честони впервые описали связь между чесоточными клещами и типичными кожными симптомами, развивающимися вслед за заражением. Именно они впервые установили, что болезнь может быть вызвана микроскопическим организмом[6].
Полное и достоверное описание этиологии и патогенеза дал в 1844 г. немецкий дерматолог Фердинанд Гебра. Это руководство было в 1876 году переведено на русский язык А. Г. Полотебновым[7].
Эпидемиология[править | править код]
Точных сведений о глобальной эпидемиологической картине чесотки не существует[8][9]. Известны два относительно достоверных статистических отчёта по Эдинбургу (за 1815—2000 гг.) и по Дании (1900—1970 гг.). Согласно этим данным примерно 5 % пациентов с кожными заболеваниями имели чесотку за весь период наблюдений. Резкие скачки заболеваемости наблюдались в военное время, когда чесотка поражала до 30 % населения.
Существуют теории о волнообразном характере заболеваемости чесоткой с периодичностью в 7-30 лет. Однако эти теории подвергаются серьёзной критике[10]. Имеются данные о циклическом возрастании агрессивности чесоточного клеща вследствие развития его устойчивости к ряду скабицидов. Также отмечаются всплески заболеваемости в периоды войн, стихийных бедствий, голода и других социальных явлений, ведущих к ухудшению бытовых условий, питания и гигиены, и скученности людей.
Для заболеваемости чесоткой характерна сезонность. В России это осень-зима. Те же данные получены по результатам 20-летнего наблюдения в армии Израиля[11]. Сезонность заболевания объясняется отчасти биологическими особенностями самих клещей, плодовитость которых достигает максимума в сентябре-декабре, а также тем фактом, что прохладные условия способствуют лучшей выживаемости зудней во внешней среде. Кроме того, холод способствует скученности людей и снижению потоотделения (с потом выделяются противомикробные пептиды, к которым отчасти чувствительны и чесоточные клещи).[12] В странах Западной Африки пиковая заболеваемость также отмечена в холодные и засушливые сезоны. Там же, где выраженной климатической сезонности не наблюдается, заболеваемость чесоткой распределена равномерно в течение года (Бангладеш, Гамбия, Бразилия)[13][14][15][16].
Чесотка может протекать как эпидемически, так и эндемически. Спорадические вспышки характерны для индустриально развитых стран, где заболевание локализуется в основном в организованных коллективах, объединённых общими спальнями (воинские казармы, интернаты, детские дома, общежития, тюрьмы, лечебные учреждения и т. п.) или в асоциальных слоях общества. Коллективы, члены которых объединяются только в дневное время (группы в детских дошкольных учреждениях, классы в средних и высших учебных заведениях, трудовые коллективы), эпидемиологической опасности, как правило, не представляют. Общий уровень заболеваемости в таких странах невысок. По данным Англии и Уэлса за 1994—2003 гг. отмечена заболеваемость на уровне 351 случай на 100 тыс. человек в год у мужчин и 437 — у женщин[17]. В России ежегодная заболеваемость, судя по реализации скабицидных средств в аптечной сети, превышает миллион случаев.[1].
Однако в ряде стран заболеваемость намного выше и может достигать 40-80 %. Особенно много больных среди народов Субсахарной Африки и аборигенов Австралии и Новой Зеландии[18][19], что, вероятно, связано с особенностями их иммунитета и строением рогового слоя кожи.
В целом на конец XX в. чесоткой страдали около 300 млн человек (5 % населения планеты)[12].
В мире чесоткой больше болеют дети младшего возраста, что связано с отсутствием у них иммунитета к возбудителю и с более частыми прямыми контактами с кожей больных[12]. В России ситуация несколько иная. Основной риск составляет юношеская возрастная группа, которая, образуя всего десятую часть населения, берёт на себя до 25 % всей заболеваемости. Второе место традиционно занимает школьный возраст, третье — дошкольный, четвёртое — зрелый. Существенно, что при чесотке распределение заболеваемости по социальным группам согласуется с возрастным. Наибольшая заболеваемость у студентов, ниже — у школьников и дошкольников.[2] Такая ситуация объясняется особенностями сексуальной активности и развития противозудневого иммунитета в различных возрастных группах.
Пути передачи[править | править код]
Заражение чесоткой почти всегда происходит при продолжительном прямом контакте кожа—кожа[3]. Преобладает половой путь передачи. Дети нередко заражаются, когда спят в одной постели с больными родителями. В скученных коллективах реализуются и другие прямые кожные контакты (контактный спорт, возня детей, частые и крепкие рукопожатия и т. п.). Хотя ряд руководств продолжает воспроизводить устаревшие сведения о передаче чесотки через бытовые предметы (предметы обихода, постельные принадлежности и т. п.), специалисты сходятся на мнении, что такой путь заражения крайне маловероятен.[12] Исключением являются случаи норвежской чесотки, когда на теле больного обитает до нескольких миллионов клещей (в типичных случаях это 10-20 клещей).
Ключевой эксперимент, доказавший, что в передаче чесотки доминирующую роль играет прямой контакт с кожей больного, был выполнен в 1940 г. в Великобритании под руководством Mellanby. Из 272 попыток заразить добровольцев, укладывая их в постель, с которой только что поднимались больные с выраженной чесоткой, только 4 попытки привели к заболеванию[20].
Такие особенности передачи паразитоза объясняются следующими данными о его биологии:
- чесоточный клещ неактивен днём; самки выбираются на поверхность только в поздневечернее и ночное время суток;
- клещу необходимо около 30 мин для проникновения в кожу хозяина;
- во внешней среде клещ быстро погибает (при 21 °С и влажности 40-80 % паразит гибнет через 24-36 часов), чем теплее и суше, тем быстрее; активность клещ утрачивает ещё раньше[21][22].
В настоящее время всё больше руководств и медицинских обзоров включают чесотку наряду с фтириазом в список заболеваний, передающихся половым путём[23][24], хотя для передачи этих паразитозов имеет значение не столько сам коитус, сколько длительное соприкосновение телами в постели.
Биология и жизненный цикл чесоточного клеща[править | править код]

Возбудителем чесотки является чесоточный клещ — облигатный паразит человека. Для паразита характерен половой диморфизм: самки вдвое крупнее самцов, достигают 0,3-0,5 мм. Ротовые органы несколько выступают вперёд, по бокам имеется 2 пары передних ножек с присосками, 2 задние пары ножек располагаются на брюшной поверхности, у самок снабжены длинными щетинками, у самцов на 4 паре ножек вместо щетинок присоски. Яйца клеща имеют овальную форму, личинка, вышедшая из яйца, имеет овоидную форму и 3 пары ножек (4 пара отсутствует), размер её не превышает 0,15 на 0,1 мм[25].
Спаривание клещей происходит на поверхности кожи. Сразу после спаривания самцы погибают. Оплодотворённая самка формирует в роговом слое кожи чесоточный ход, в котором откладывает по 2-4 яйца за ночь. Кератин кожи клещи растворяют с помощью специальных протеолитических ферментов, содержащихся в их слюне (образующимся лизатом они и питаются). Самцы формируют короткие боковые ответвления в чесоточном ходе самки. Продолжительность жизни самки не превышает 4-6 недель. Личинки вылупляются через 2-4 дня и сразу начинают формировать ходы в самом верхнем слое кожи. Ещё через 3-4 дня личинки линяют и превращаются в протонимф, которые в свою очередь линяют через 2-5 дней в телеонимфу. Телеонимфа развивается во взрослого самца или самку через 5-6 дней. Итого формирование взрослого клеща происходит за 10-14 дней.
Заразным клещ может быть на любой стадии развития, однако чаще от человека к человеку чесотка передаётся с оплодотворёнными взрослыми самками.
Клещи не активны в дневное время. Самка начинает «рыть» ход (по 2-3 мм в день) вечером; тогда же усиливается зуд у больных типичными формами чесотки. Ночью самки выходят на поверхность кожи для спаривания и перемещения на другие участки тела (на поверхности тёплой кожи клещи перемещаются со скоростью 2,5 см в минуту[26]. Тогда же возникает наиболее благоприятная ситуация для заражения.
Патогенез[править | править код]
Клиническая картина при чесотке обусловлена иммунно-аллергической реакцией организма хозяина на продукты жизнедеятельности клеща, поэтому вся симптоматика развивается только после сенсибилизации больного. Этим объясняется длительный бессимптомный период (до 4 недель), предшествующий появлению первых признаков заболевания, при первичном заражении. В случаях же повторного заражения реакция на возбудителя может развиться в течение суток[27]. Развитием защитного иммунитета объясняется и трудность повторного заражения в эксперименте, а также тот факт, что при повторном заражении на теле больного обнаруживается значительно меньшее количество клещей[28].
Зуд при чесотке обусловлен в основном аллергической реакцией IV типа (гиперчувствительностью замедленного типа) на слюну, яйца и экскременты клещей. Расчёсы, вызванные зудом, нередко ведут к присоединению бактериальной флоры (стафилококков и стрептококков) с развитием гнойничков (пиодермии). Таким образом, сыпь при чесотке приобретает полиморфность.
Интересно, что те же аллергены обнаружены и в бытовой пыли, населённой микроскопическими бытовыми клещиками, которые также питаются эпителием человека, составляющим основу домашней пыли[29][30].
При выраженном поражении клещами повышается уровень интерлейкина-4[31]. У больных также наблюдается Th2-тип иммунного ответа, что связано с повышением у них сывороточных IgE и IgG в комбинации с эозинофилией. Однако этот выраженный гуморальный иммунный ответ не обладает значительным защитным действием[32]. При чесотке более значим клеточный иммунный ответ, который изучен на гистологическом уровне: клещей окружает воспалительный инфильтрат, состоящий из эозинофилов, лимфоцитов, гистиоцитов и небольшого количества нейтрофилов.
При норвежской форме чесотки наблюдается выраженный гиперкератоз, а в участках воспалительного инфильтрата обнаруживается большое количество клещей (до нескольких миллионов на теле одного больного). Норвежская чесотка возникает у больных, не ощущающих выраженного зуда, либо не способных совершать расчёсы. Такие состояния встречаются при иммунодефицитах, когда иммунная реакция на клещей вяла (СПИД, регулярный приём глюкокортикостероидных и других иммуносупрессивных препаратов), при нарушении периферической чувствительности (проказа, сирингомиелия, параличи, спинная сухотка), конституциональных аномалиях ороговения, а также у немощных больных (старческое слабоумие, малоумие, ограниченная подвижность и т. п.).
При длительном существовании инфильтрата формируется так называемая скабиозная лимфоплазия в форме узелков (нодулярная чесотка), когда инфильтраты становятся очень плотными и распределяются вокруг подкожных сосудов и в жировой клетчатке, напоминая элементы при лимфоме или псевдолимфоме.
Клиника[править | править код]
Характерным, но не обязательным клиническим симптомом при чесотке являются кожный зуд, усиливающийся в вечернее время. На коже формируется эритематозная папуловезикулёзная сыпь, при расчёсывании присоединяются гнойничковые элементы и образуются корки с формированием полиморфных высыпаний. Патогномоничным признаком является наличие чесоточных ходов.
Как только самка клеща попадает на кожу человека, она незамедлительно начинает «рыть» ход в роговом слое кожи со скоростью 0,5-5 мм в сутки. В результате на поверхности кожи при внимательном рассмотрении можно обнаружить слегка возвышающиеся над поверхностью кожи линии белесовато-серого цвета, размерами от 1 мм до 1 см. Передний слепой конец хода различим по наличию в нём клеща, который виден сквозь эпидермис в виде тёмной точки[7].
Чесоточные ходы становятся видимыми через несколько дней при формировании перитоннельной реакции организма хозяина. Чаще чесоточные ходы можно обнаружить в межпальцевых промежутках, на внутренней стороне запястий и на коже полового члена . Иногда чесоточные ходы обнаружить не удаётся (чесотка без ходов).
Первичная сыпь представлена мелкими эритематозными папулами, которые могут быть рассеянными или множественными, сливными. Со временем папулы могут преобразовываться в везикулярную (пузырьки), редко буллёзную (пемфигоидная) сыпь. Выраженность сыпи не коррелирует с количеством паразитов, а обусловлена аллергической реакцией на продукты их жизнедеятельности.
Сыпь распределяется чаще всего (в порядке убывания) в межпальцевых промежутках кистей, на сгибательной стороне запястий, у мужчин быстро переходит с кистей на пенис и мошонку. Затем поражаются локти, стопы, подмышки, зоны под грудью у женщин, пупочная область, линия пояса, ягодицы. В итоге задействоваться может всё тело, кроме лица и волосистой части головы (хотя у детей до 3 лет поражаются и эти области).
Наличие зуда, первичной сыпи и чесоточных ходов является основным клиническим симптомокомплексом типичной формы чесотки.
Папулы и везикулы часто развиваются во вторичные чесоточные элементы: экскориации (расчёсы), экзематозные элементы, вторичные гнойничковые высыпания и корки. Первичные и вторичные элементы при этом сосуществуют на одном больном.
В отечественной дерматологии принято выделять характерные эпонимические симптомы, облегчающие постановку диагноза:
- симптом Арди — пустулы и гнойные корочки на локтях и в их окружности;
- симптом Горчакова — там же кровянистые корочки;
- симптом Михаэлиса — кровянистые корочки и импетигинозные высыпания в межъягодичной складке с переходом на крестец;
- симптом Сезари — обнаружение чесоточных ходов в виде лёгкого возвышения при их пальпации.
Расчёсы нередко приводят к выраженному бактериальному инфицированию первичных элементов с развитием пиодермии, которая в редких случаях может вести к постстрептококковому гломерулонефриту и возможно к ревматическому поражению сердца[33][34][35][36]. Иногда пиодермия при чесотке сопровождается возникновением фурункулов, эктимы и абсцессов, сопровождающихся лимфаденитом и лимфангитом. У ряда больных развивается микробная экзема или аллергический дерматит, которые наряду с пиодермией, в отечественной дерматологии относят к осложнённым формам чесотки. Осложнения чесотки в виде дерматита и пиодермии возникают примерно у 50 % больных[7].
При чесотке описаны и другие осложнения: импетиго, пиогенная пневмония, септицемия, панариций, рожистое воспаление, орхоэпидидимит, внутренние абсцессы, регионарный лимфаденит.
У детей, особенно грудных, наряду с папуловезикулами и чесоточными ходами имеется везикулоуртикарная сыпь, развиваются мокнутия, возникают паронихии и онихии. У детей в первые 6 мес. жизни клиническая картина чесотки часто напоминает крапивницу и характеризуется большим количеством расчёсанных и покрытых в центре кровянистой корочкой волдырей, локализующихся на коже лица, спины, ягодиц. Позже превалирует мелкая везикулёзная сыпь, иногда пузыри (пемфигоидная форма). В отдельных случаях чесотка у детей напоминает острую экзему, сопровождается интенсивным зудом не только в местах локализации клещей, но и на отдалённых участках кожи. В связи с этим нередко отмечаются нарушение сна, чаще наблюдаются осложнения в виде аллергического дерматита, пиодермии типа импетиго. Могут возникать лимфадениты и лимфангиты, наблюдаются лейкоцитоз и лимфоцитоз, эозинофилия, ускорение СОЭ, альбуминурия. У грудных детей может развиться сепсис. В последние годы у детей отмечается рост случаев атипичной чесотки со стёртыми формами.
Примерно у 7 % больных формируется нодулярная (узелковая) чесотка[37], при которой формируются синюшно-багровые или коричневатые округлые уплотнения кожи 2-20 мм в диам., которые могут сохраняться на протяжении нескольких недель даже при отсутствии в них паразитов. По сути эти уплотнения представляют собой особый вариант чесоточного хода в виде лентикулярной папулы[38]. Причиной возникновения таких элементов является особая предрасположенность кожи отвечать на воздействие раздражителя реактивной гиперплазией лимфоидной ткани в местах наибольшего её скопления. Она преобладает на мошонке, половом члене, ягодицах, локтях, в переднеподмышечной области, иногда узелки формируются в перианальной области. Нодулярную чесотку называют также скабиозной лимфоплазией. Поскольку живых клещей в узелках нет, их образование объясняется выраженной иммунно-аллергической реакцией организма хозяина на продукты их жизнедеятельности. В случаях реинвазии наблюдается рецидив скабиозной лимфоплазии на старых местах уже без наличия хода. Узелки сопровождаются сильным зудом и в ряде случаев для их лечения применяют кортикостероидные инъекции[37].
К нетипичным формам чесотки относят также норвежскую чесотку, чесотку «чистоплотных» (чесотку «инкогнито») и псевдосаркоптоз.
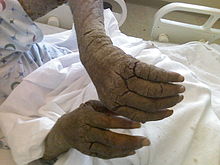
Норвежская (корковая, крустозная) чесотка была впервые описана норвежскими врачами Беком и Даниэльссеном (С. W. Boeck, D. С. Danielssen) в 1848 г.[39]. Норвежская чесотка развивается чаще у лиц с предрасполагающими расстройствами иммунитета или чувствительности кожи (см. Патогенез), однако в примерно 40 % случаев наблюдается у людей, не относящимся к группам риска, что предполагает возможную генетическую предрасположенность у таких больных. У 58 % больных норвежской чесоткой наблюдается эозинофилия, повышение уровня IgE (в среднем в 17 раз) выявляется в 96 % случаев.[40]. Клинически норвежская чесотка выглядит как псориазоформный дерматит с акральным распределением и наличием вариабельных белёсых чешуек. Обычно также вовлекаются и подногтевые зоны с развитием выраженного гиперкератоза, ведущего к утолщению и дистрофии ногтевой пластинки. В ряде случаев при норвежской чесотке преимущественно поражаются области скальпа, лица, шеи и ягодиц. Около половины больных норвежской чесоткой совершенно не чувствуют зуда[41]. В связи с тем, что при норвежской чесотке на теле больного может существовать более миллиона живых паразитов (при типичных формах количество клещей в среднем составляет 15 особей), такая форма болезни является исключительно заразной[42].
Чесотка «чистоплотных» или чесотка «инкогнито» выявляется у лиц, часто моющихся в быту или по роду своей производственной деятельности. При этом большая часть популяции чесоточного клеща механически удаляется с тела больного. Клиника заболевания соответствуют типичной чесотке при минимальной выраженности проявлений. Осложнения нередко маскируют истинную клиническую картину чесотки. Наиболее распространёнными являются пиодермия и дерматит, реже встречаются микробная экзема и крапивница.
Псевдосаркоптозом называют заболевание, возникающее у человека при заражении чесоточными клещами (S. scabiei отличных от var. homonis) от других млекопитающих (чаще собак). Для заболевания характерен короткий инкубационный период, отсутствие чесоточных ходов (клещи не размножаются на несвойственном хозяине), уртикарные папулы на открытых участках кожного покрова. От человека к человеку заболевание не передаётся (см. Псевдосаркоптоз).
Диагностика[править | править код]
Диагноз чесотки ставится на основании клинических проявлений, эпидемиологических данных, данных лабораторных методов обследования. Подтверждение диагноза лабораторно особенно важно при стёртой клинической картине. Существуют следующие методы лабораторного подтверждения заболевания[43]:
- Традиционное извлечение клеща иглой из слепого конца чесоточного хода, с последующей микроскопией возбудителя. Данный метод малоэффективен при исследовании старых полуразрушенных папул.
- Метод тонких срезов участков рогового слоя эпидермиса в области чесоточного хода при микроскопии позволяет выявить не только клеща, но и его яйца.
- Метод послойного соскабливания из области слепого конца чесоточного хода до появления крови. С последующей микроскопией материала.
- Метод щелочного препарирования кожи, с нанесением на кожу щелочного раствора, с последующей аспирацией мацерированой кожи и микроскопией.
В каждом случае, когда пациент предъявляет жалобы на кожный зуд, следует в первую очередь исключать чесотку, особенно если зуд возник и у других членов семьи или организованного коллектива.
Обнаружение чесоточных ходов достоверно подтверждает диагноз. Для полного подтверждения диагноза рекомендуется вскрыть чесоточный ход скальпелем, покрытым маслянистым веществом, осторожно процарапывая лезвием роговой слой кожи вдоль чесоточного хода. Полученные соскобы помещаются на предметное стекло и микроскопируются. Лучшие результаты получают при соскобах «свежих», не расчёсанных чесоточных ходов на межпальцевых промежутках рук. Хотя этот метод обладает 100 % специфичностью, его чувствительность невысока.
Хлорид калия позволяет растворить кератин, способствуя лучшему обнаружению клещей и яиц, однако при этом растворяются экскременты клещей, которые также имеют диагностическую ценность[источник не указан 2753 дня].
Чесоточные ходы легче обнаружить, если прокрасить кожу йодной настойкой — ходы визуализируются в виде полосок коричневого цвета на фоне окрашенной в светло-коричневый цвет здоровой кожи. За рубежом для этих целей используют чернила.
Видеодерматоскоп при увеличении в 600 раз позволяет обнаружить чесоточные ходы почти во всех случаях[44].
В связи с тем, что клещей удаётся обнаружить не всегда, ряд авторов предлагает следующий практический подход для диагностики: диагноз чесотки устанавливается при наличии папуловезикулёзной сыпи, пустулёзных элементов и кожного зуда (особенно усиливающегося в ночное время), а также при положительном семейном анамнезе[14].
Лечение[править | править код]
Лечение больных чесоткой направлено на уничтожение возбудителя с помощью акарицидных препаратов (скабицидов).
Опыт показывает, что при чесотке не бывает рецидивов, причинами возобновления заболевания являются реинвазия от непролеченных контактных лиц в очаге или вне его, недолеченность больного в связи с несоблюдением схем лечения, частичная обработка кожного покрова, сокращение продолжительности курса терапии.
- Лечение надо проводить исключительно под руководством врача.
- Лечение всех больных, проживающих вместе, должно проводиться одновременно.
- Необходимо чётко придерживаться схемы обработок, расписанной в инструкции к препарату или как назначит врач.
- Препарат наносится на всё тело, кроме лица и волосистой части головы, а у детей до 3 лет обрабатывать надо и эти участки.
- Важно коротко подстричь ногти и густо наносить препарат под ними (при расчёсывании под ногтями скапливаются яйца зудней).
- Втирание любого препарата осуществляется руками, что обусловлено высокой численностью чесоточных ходов на кистях. Если промежность и пах густо покрыты волосами, препарат лучше втирать щёткой.
- Лечение необходимо проводить в вечернее время, что связано с ночной активностью возбудителя.
- Мытьё больного рекомендуется проводить перед началом и по окончании курса лечения, при необходимости больной может смывать препарат каждое утро, при этом экспозиция его на коже должна быть не менее 12 часов, включая весь ночной период.
- Смена нательного и постельного белья проводится по окончании курса терапии.
- Детям, школьникам, солдатам и т. п. желателен 10-дневный карантин.
- Через 2 недели рекомендован повторный осмотр врача, для решения вопроса о повторном курсе лечения.
В РФ в соответствии с СанПиН 3.2.1333-03 все члены семьи заболевшего чесоткой лица живущие с больными в одном помещении подлежат профилактическому лечению. Если в организованном коллективе одновременно зарегистрировано более трёх случаев чесотки, профилактическое лечение проводят всему коллективу. Дети и школьники не допускаются в организованные детские коллективы и школы на период лечения[45].
Доказательных клинических испытаний по сравнительной эффективности скабицидных препаратов в настоящее время мало. Поэтому в разных странах предпочтения по препаратам варьируют[46].
Так, в США, Великобритании и Австралии в большинстве случаев применяется крем с 5 % перметрином. В развивающихся странах и в России основным средством является недорогая водно-мыльная суспензия или мазь бензилбензоата (10 % или 25 %, в РФ 20 %)[47]. В значительно меньшей степени в мире используются моносульфирам (25 %), малатион (5 %), линдан (0,3-1 %), кротамион (10 %)[48][49]. В последние годы большой популярностью в России пользуется французский препарат Спрегаль[50]. В беднейших странах до сих пор применяют серную мазь.[49][51] Новым революционным препаратом для лечения эктопаразитов (особенно норвежских форм чесотки) стал ивермектин[52][53].
Краткая характеристика отдельных препаратов:
1) Бензилбензоат в медицинской практике впервые появился в составе Перуанского бальзама. Сегодня его используют в виде различных лекарственных форм, приготовленных ex tempore или промышленным путём. В России это водно-мыльная суспензия и эмульсионная мазь, за рубежом — мыльно-спиртовые растворы, масляные взвеси, водные растворы с добавлением ДДТ и анестезина. Экспериментально доказано, что после однократной обработки бензилбензоатом гибнут все активные стадии клеща. Однако яйца выживают. С учётом максимального срока пребывания личинок в яйце (58 часов) предложена этиологически обоснованная схема лечения бензилбензоатом: водно-мыльную суспензию или мазь тщательно втирают руками один раз в день на ночь в первый и четвёртый дни курса. Мытьё и смену нательного и постельного белья рекомендуют на 5-й день. Второй и третий дни курса с успехом используют для лечения сопутствующих чесотке осложнений. Для гибели активных стадий клещей и эмбрионов достаточно 8-10-часовой экспозиции препарата. В связи с этим утром больным можно помыться. Общая эффективность (излечение) при стандартной схеме не превышает 50 %, поэтому курсы часто приходится повторять через 10 дней. Из частых побочных эффектов можно назвать местное раздражение кожи с чувством жжения[54][3].
2) Пиретрины и пиретроиды. Активным компонентом здесь являются пиретрины. Именно они входят в пластины, спирали и фумигаторы против гнуса, в инсектицидные спреи. Эффективны они и в качестве скабицидов. В большинстве развитых стран пиретроид перметрин является предпочтительным препаратом для лечения чесотки благодаря его низкой токсичности и высокой скабицидной активности[55][56]. В США перметрин используется для лечения чесотки с 1989 г. По Кохрановским данным перметрин является самым эффективным противочесоточным средством для наружного применения[46]. Он убивает и активные формы клеща, и яйца, поэтому часто достаточно однократного его применения (более 95 % излечения[57]).
В России препарат перметрина зарегистрирован под названием «Медифокс» (5 % и 20 %), однако качество его значительно уступает зарубежному перметрину (5 %). Поэтому протокол лечения (Приказ МЗ 24.04.2003 г. № 162) другой. Медифокс наносится на кожу всего туловища в 1-й, 2 и 3-й дни лечения. Используется постоянная концентрация и доза перметрина: 0,4 % водная эмульсия, приготавливаемая ex tempore путём добавления 8 мл 5 % концентрата перметрина к 100 мл кипячёной воды комнатной температуры. Препарат отменяется по окончании курса лечения, а также в случае возникновения аллергической реакции, контактного дерматита.
Синтетический пиретроид входит и в состав Спрегаля. Спрегаль — комбинированный французский препарат. Действующим началом является эсдепалетрин — нейротоксический яд, нарушающий катионный обмен мембран нервных клеток членистоногих. Второй компонент — пиперонил бутоксид — усиливает действие эсдепалетрина. Препаратом опрыскивают на ночь всю поверхность тела, кроме лица и волосистой части головы, с расстояния 20-30 см от поверхности кожи. Особенно тщательно Спрегаль втирают в места излюбленной локализации чесоточных ходов (кисти, запястья, стопы, локти). При локализации высыпаний на лице их обрабатывают ватным тампоном, смоченным препаратом. Следует избегать попадания препарата на слизистые оболочки. При лечении детей салфеткой закрываются рот и нос. Спустя 12 часов необходимо тщательно вымыться с мылом.
3) Линдан в РФ зарегистрирован как Якутин (фирма «Мерк», Германия), в продаже почти не встречается[58]. В мире его используют широко, поскольку препарат недорог. Однако с 70-х накопилось немало данных о его нейротоксических побочных эффектах (в связи с этим с 2001 г. запрещён к применению в качестве пестицида на территории ЕС), поэтому назначать линдан следует с осторожностью, при отсутствии альтернатив[12].
Меры по безопасному применению линдана:
- нельзя наносить сразу после приёма ванны/душа;
- наносится не более чем на 6 ч.;
- нельзя повторно наносить препарат через короткие промежутки времени;
- необходимо следить, чтобы дети не обсасывали пальцы;
- с исключительной осторожностью применяется у новорождённых, беременных, при выраженных расчёсах и экскориативных изменениях кожи (как при экземе, ихтиозе, псориазе), у пациентов с судорожными расстройствами и другими неврологическими заболеваниями.[12]
4) Кротамион в РФ зарегистрирован как Юракс (фирма «Бристол-Майерс Сквибб», США), который также малопопулярен[58]. По данным рандомизированных клинических испытаний по эффективности сильно уступает Перметрину[59]. Из побочных эффектов возможны непродолжительная эритема и конъюнктивит.[12]
5) Серная мазь (5-10 %). В настоящее время в развитых странах больше не используется из-за неприятного запаха, прокрашивания одежды, раздражающего действия на кожу и слизистые, чрескожное всасывание с потенциальным воздействием на почки. Однако в Африке и беднейших странах Юж. Америки серную мазь по-прежнему применяют благодаря её дешевизне[12]. До сих пор серную мазь назначают в России, на Украине и в Белоруссии. Схема применения: взрослым 20 % концентрация, детям − 10 %, мазь втирают по всей коже ежедневно на ночь в течение 5-7 дней. На шестой или восьмой день больной моется и меняет нательное и постельное бельё.
6) Ивермектин — комплекс действующих веществ из сравнительно новой противопаразитарной группы авермектинов, используемый в различных препаратах в качестве противочесоточного. Выпускаются препараты в виде мазей для наружного применения, а также 1 % раствор для инъекций (вводится подкожно. Многие годы его применяют для успешного лечения гельминтозов (особенно филяриозов). Убивает он и многих наружных паразитов (зудней, демодекса, вшей и др.). Побочные эффекты незначительны и редки. Тератогенного и генотоксического действия не отмечено.
Ивермектин — синтетическое производное авермектина (макролитический лактон). Он парализует паразита, связываясь с его специфическим нейротрансмиттерным рецептором, что нарушает функционирование периферических моторных синапсов. На биохимическом уровне блокируются глутамат-зависимые анионные каналы и ГАМК-зависимые хлоридные каналы). Препарат исключительно эффективен: при однократном применении излечиваются 70 % больных, а при повторной дозе через 2 недели — более 95 %. Сравнительные клинические исследования показывают, что по эффективности ивермектин не уступает или превосходит линдан[60][61], бензилбензоат[62][63] и перметрин[57].
Однако для лечения чесотки людей он одобрен пока только во Франции, Бразилии и ещё в нескольких странах. В то же время практически повсеместно, включая США, он рекомендован как препарат выбора для лечения норвежской чесотки (200мкг/кг двукратно)[64][65][66]. Во многих странах ивермектин придерживают в резерве для лечения самых сложных форм чесотки, чтобы избежать выработки массовой резистентности клещей к препарату. Случаи резистентности описаны во многих странах, где препарат применяется широко и бесконтрольно, в том числе в сельском хозяйстве[4].
В связи с наличием побочных эффектов у многих скабицидов ведётся активный поиск более безопасных альтернатив[67]. Масла ряда растений показали впечатляющий эффект как in vitro, так и в полевых испытаниях. Например, масло чайного дерева (Melaleuca alternifolia) продемонстрировало высокий скабицидный эффект in vitro[68], а паста, приготовленная из экстрактов нима (Azadirachta indica) и турмерика (Curcuma longa), привела к излечению 790 (97 %) пациентов с чесоткой в одном из пилотных испытаний[69]. Клинические испытания в Нигерии выявили очень высокий скабицидный эффект у масла кустарника Lippia multiflora[70].
После полного истребления клещей зуд и отдельные элементы сыпи могут сохраняться в течение ещё нескольких недель (особенно долго персистируют узелки), что обусловлено иммуно-аллергической природой чесоточной сыпи. Для облегчения таких симптомов врач может назначить противозудные, антигистаминные и кортикостероидные препараты. При присоединении бактериальной флоры могут назначаться препараты на основе антибиотиков, например неомицина и бацитрацина (Банеоцин)[71].
Примечание по лечению беременных: В США и Европе беременных не рекомендуют лечить препаратами типа Спрегаля, ограниченно назначают бензилбензоат, назначается без ограничений только перметрин[12]. В России наоборот — беременным назначают преимущественно бензилбензоат и Спрегаль, тогда как перметрин (медифокс), согласно отечественным инструкциям, противопоказан.
Профилактика[править | править код]
Объём профилактических мероприятий определяется в зависимости от эпидемиологической ситуации. При обнаружении чесотки заполняется форма экстренного извещения, и извещаются органы СЭС по месту жительства больного[72].
Лица из одного очага лечатся совместно с целью профилактики повторного заражения. Все лица, контактировавшие с поражёнными, проводят однократную профилактическую обработку кожных покровов противоклещевыми препаратами[72].
После лечения больного многие руководства рекомендуют обработку всех вещей и белья, с которыми контактировал больной (специальные спреи, стирка в горячей воде). В соответствии с данными по выживаемости чесоточных клещей во внешней среде, а также в связи с крайне низкой вероятностью передачи чесотки через бытовые предметы (непрямой контактный путь передачи), данные рекомендации обсуждаются в каждом конкретном случае.[12] Новейшие руководства не рекомендуют обрабатывать матрасы, мягкую мебель и ковры; постельное и нижнее бельё следует простирать в горячей воде, если с момента его использования прошло менее 48 часов.[66]
Примечание: Вопреки распространённому заблуждению чесотка не связана с низким уровнем гигиены. Чесоточный клещ не восприимчив к воде или мылу. При ежедневном приёме душа/ванны количество клещей и вероятность заражения не снижаются[73].
Прогноз[править | править код]
В случае сохранного иммунного статуса заболевание не представляет непосредственной угрозы для жизни. Своевременное адекватное лечение позволяет полностью устранить симптомы и последствия заболевания. Трудоспособность полностью восстанавливается.
В редких случаях, наблюдаемых в основном в беднейших странах, осложнённая чесотка может приводить к постстрептококковому гломерулонефриту и возможно к ревматическому поражению сердца (см. раздел «Клиника»).
У детей чесотка может осложняться тяжёлой пиодермией и сепсисом, вплоть до смерти больного[74]. Прогноз при норвежской чесотке сомнительный, лечение малоэффективно, нередки случаи смерти, наступающей вследствие интоксикации больного, нарушения сердечной деятельности, острой почечной недостаточности.
Заражение от животных[править | править код]
Другие млекопитающие (собаки, кошки, копытные, домашний скот и др.) могут быть инфицированы различными разновидностями клеща Sarcoptes scabiei, которые могут передаваться людям. При этом возникает картина, сходная с локализованной кожной чесоткой, вызываемой человеческим вариантом зудня (S. scabiei var. hominis). Однако все прочие разновидности клеща не способны завершить полный жизненный цикл на коже человека, поэтому такая чесотка непродолжительна и не требует лечения скабицидами[51][75].
См. в разделе «Клиника» о псевдосаркоптозе.
Примечания[править | править код]
- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29 — 2018-06-29 — 2018.
- ↑ 1 2 Scabies. Дата обращения: 27 октября 2017. Архивировано 23 декабря 2011 года.
- ↑ Источник. Дата обращения: 15 мая 2019. Архивировано 18 мая 2015 года.
- ↑ Van Hee R. Jeremy Thriverius (1504—1554): humanist doctor, born 500 years ago. Rev Med Brux. 2005 Sep-Oct;26(5):475-8.
- ↑ Ramos-e-Silva M. Giovan Cosimo Bonomo (1663—1696): discoverer of the etiology of scabies. Int J Dermatol1998; 37: 625-30.
- ↑ 1 2 3 Кожные и венерические болезни. Руководство для врачей / Скрипкин Ю. К. — М.: Медицина, 2002 год. — Т. 1. — С. 457—458. — 576 с. — ISBN 5-225-02856-x.
- ↑ Savin JA. Scabies in Edinburgh from 1815 to 2000. J Soc Med 2005; 98: 124-9.
- ↑ Christophersen J. The epidemiology of scabies in. Denmark, 1900—1975. Arch Dermatol 1978; 114: 747-50.
- ↑ Burkhart CG. Scabies: an epidemiologic reassessment. Ann Intern Med. 1983;98:498-503
- ↑ Mimouni D; Ankol O E; Davidovitch N; Gdalevich M; Zangvil E; Grotto I. Seasonality trends of scabies in a young adult population: a 20-year follow-up. The British journal of dermatology 2003;149(1):157-9.
- ↑ 1 2 3 4 5 6 7 8 9 10 Ulrich R Hengge,Bart J Currie,Gerold Jäger,Omar Lupi,Robert A Schwartz. The Lancet Infectious Diseases 1 December 2006; Volume 6, Issue 12:769-79.
- ↑ Kristensen JK. Scabies and Pyoderma in Lilongwe, Malawi. Prevalence and seasonal fluctuation. Int J Dermatol 1991; 30: 699—702.
- ↑ 1 2 Heukelbach J, Wilcke T, Winter B, Feldmeier H. Epidemiology and morbidity of scabies and pediculosis capitis in resource-poor communities in Brazil. Br J Dermatol 2005; 153: 150—156.
- ↑ Stanton B, Khanam S, Nazrul H, Nurani S, Khair T. Scabies in urban Bangladesh. J Trop Med Hyg 1987; 90: 219—226.
- ↑ Porter MJ. Seasonal change and its effect on the prevalence of infectious skin disease in a Gambian village. Trans R Soc Trop Med Hyg 1979; 74: 162—168.
- ↑ Pannell R S; Fleming D M; Cross K W. The incidence of molluscum contagiosum, scabies and lichen planus. Epidemiology and infection 2005;133(6):985-91.
- ↑ Currie BJ, Connors C, Krause V. Scabies programs in Aboriginal communities. Med J Aust 1994; 161: 637.
- ↑ Terry BC, Kanjah F, Sahr F, Kortequee S, Dukulay I, Gbakima AA. Sarcoptes scabiei infestation among children in a displacement camp in Sierra Leone. Public Health 2001; 115: 208—211.
- ↑ Mellanby K. The transmission of scabies. Br Med J 1941; 2: 405—406.
- ↑ Arlian LG. Biology, host relations, and epidemiology of Sarcoptes scabiei. Annu Rev Entomol 1989; 34: 139—161.
- ↑ Arlian LG, Runyan RA, Achar S, Estes SA. Survival and infectivity of Sarcoptes scabiei var. canis and var. hominis. J Am Acad Dermatol 1984; 11: 210—215.
- ↑ ВОЗ: Глобальная стратегия профилактики инфекций, передаваемых половым путём, и борьбы с ними, 2006—2015 гг., стр. 7. Дата обращения: 15 января 2010. Архивировано 21 июля 2009 года.
- ↑ http://whqlibdoc.who.int/publications/2003/9241546263.pdf/WHO (недоступная ссылка): GUIDELINES FOR THE MANAGEMENT OF SEXUALLY TRANSMITTED INFECTIONS
- ↑ Кожные и венерические болезни. Руководство для врачей / Скрипкин Ю. К. — М.: Медицина, 2002 год. — Т. 1. — С. 458—460. — 576 с. — ISBN 5-225-02856-x.
- ↑ Haag M L; Brozena S J; Fenske N A. Attack of the scabies: what to do when an outbreak occurs. Geriatrics 1993;48(10):45-6
- ↑ Mellanby K. The development of symptoms, parasitic infection and immunity in human scabies. Parasitology 1944; 35:197-206.
- ↑ Lalli PN, Morgan MS, Arlian LG. 2004. Skewed Th1/Th2 immune response to Sarcoptes scabiei . J Parasitology. 90:711-14.
- ↑ Falk, E.S., Dale, S., Bolle, R. and Haneberg, B., 1981. Antigens common to scabies and house dust mites. Allergy 36, pp. 233-38
- ↑ Arlian LG, Rapp CM, Morgan MS. Cross-antigenicity between the scabies mite, Sarcoptes scabiei, and the house dust mite, Dermatophagoides pteronyssinus. J. Invest. Dermatol 1991. 96:349-54
- ↑ Walton SF, Holt DC, Currie BJ, Kemp DJ. Scabies: new future for a neglected disease. Adv Parasitol 2004;57:309-76.
- ↑ Roberts LJ, Huffman SE, Walton SF, Currie BJ. Crusted scabies. clinical and immunological findings in seventy-eight patients and a review of literature. J Infect 2005; 50: 375-81.
- ↑ Svartman M, Potter EV, Poon-King T, Earle DP. Streptococcal infection of scabetic lesions related to acute glomerulonephritis in Trinidad. J Lab Clin Med 1973; 81: 182—193.
- ↑ Berrios X. Reflexiones sobre un brote epidémico de glomerulonefritis aguda postestreptocócica (Epidemic outbreak of acute post-streptococcal glomerulonephritis). Rev Chil Pediatr 1990; 61: 109—112.
- ↑ Whittle HC, Abdullahi MT, Fakunle F, Parry EH, Rajkovic AD. Scabies, pyoderma and nephritis in Zaria, Nigeria. A clinical and epidemiological study. Trans R Soc Trop Med Hyg 1973; 67: 349—363.
- ↑ Currie B, Brewster DR. Rheumatic fever in Aboriginal children. J Paediatr Child Health 2002; 38: 223—225.
- ↑ 1 2 Chosidow O. Scabies and pediculosis. Lancet 2000;355:819-826
- ↑ Фицпатрик Т., Джонсон Р., Вулф М., Сюрмонд Д. Дерматология. Атлас-справочник. М. Практика. 1999. — с. 850-6.
- ↑ Sweitzer SE, Winer LH. Norwegian scabies. Arch Dermatol Syph 1941;43:648-81.
- ↑ Roberts LJ, Huffam SE, Walton SF, Currie BJ. Crusted scabies: clinical and immunological findings in seventy-eight patients and a review of the literature. J Infect 2005; 50: 375—381.
- ↑ O’Donnell BF, O’Loughlin S, Powell FC. Management of crusted scabies. Int J Dermatol 1990;29:258-66.
- ↑ Currie B, Huffam S, O’Brien D, Walton S: Ivermectin for scabies. Lancet 1997;350:1551. 31.
- ↑ Кожные и венерические болезни. Руководство для врачей / Скрипкин Ю. К. — М.: Медицина, 2002 год. — Т. 1. — С. 468. — 576 с. — ISBN 5-225-02856-x.
- ↑ Micali G, Lacarrubba F, Lo Guzzo G. Scraping versus videodermatoscopy for the diagnosis of scabies: a comparative study. Acta Derm Venereol 2000; 79: 396.
- ↑ Санитарно-эпидемиологические правила и нормативы СанПиН 3.2.1333-03 «Профилактика паразитарных болезней на территории Российской Федерации». Дата обращения: 20 марта 2018. Архивировано 17 февраля 2020 года.
- ↑ 1 2 Walker GJ, Johnstone PW. Interventions for treating scabies. Cochrane Database Syst Rev 2000
- ↑ Johnston G, Sladden M. Scabies: diagnosis and treatment. BMJ 2005; 331: 619—622.
- ↑ Bigby M. A systematic review of the treatment of scabies. Arch Dermatol 2000; 136: 387—389.
- ↑ 1 2 Roos TC, Alam M, Roos S, Merk HF, Bickers DR. Pharmacotherapy of ectoparasitic infections. Drugs 2001; 61: 1067—1088.
- ↑ Спрегаль в лечении чесотки. Дата обращения: 14 января 2010. Архивировано 26 ноября 2016 года.
- ↑ 1 2 Burgess IF. Sarcoptes scabiei and scabies. Adv Parasitol 1994; 33: 235—292.
- ↑ Burkhart KM, Burkhart CN, Burkhart CG. Our scabies treatment is archaic, but ivermectin has arrived. Int J Dermatol 1998; 37: 76-77.
- ↑ del Giudice P, Chosidow O, Caumes E. Ivermectin in dermatology. J Drugs Dermatol 2003; 2: 13-21.
- ↑ Heukelbach Jörg; Feldmeier Hermann Scabies. Lancet 2006;367(9524):1769
- ↑ Franz TJ, Lehman PA, Franz SF, Guin JD. Comparative percutaneous absorption of lindane and permethrin. Arch Dermatol 1996; 132: 901—905.
- ↑ Tomalik-Scharte D, Lazar A, Meins J, et al. Dermal absorption of permethrin following topical administration. Eur J Clin Pharmacol. 2005; 61: 399—404.
- ↑ 1 2 Usha V, Gopalakrishnan Nair TV. A comparative study of oral ivermectin and topical permethrin cream in the treatment of scabies. J Am Acad Dermatol 2000; 42: 236—240.
- ↑ 1 2 см. электронные базы данных по аптечным сетям
- ↑ Taplin D, Meinking TL, Chen JA, Sanchez R. Comparison of crotamiton 10 % cream (Eurax) and permethrin 5 % cream (Elimite) for the treatment of scabies in children. Pediatr Dermatol. 1990 Mar;7(1):67-73.
- ↑ Madan V, Jaskiran K, Gupta U, Gupta DK. Oral ivermectin in scabies patients: a comparison with 1 % topical lindane lotion. J Dermatol 2001; 28: 481—484.
- ↑ Chouela EN, Abeldano AM, Pellerano G, et al. Equivalent therapeutic efficacy and safety of ivermectin and lindane in the treatment of human scabies. Arch Dermatol 1999; 135: 651—655.
- ↑ Glaziou P, Cartel JL, Alzieu P, Briot C, Moulia-Pelat JP, Martin PM. Comparison of ivermectin and benzyl benzoate for treatment of scabies. Trop Med Parasitol 1993; 44: 331—332.
- ↑ Brooks PA, Grace RF. Ivermectin is better than benzyl benzoate for childhood scabies in developing countries. J Paediatr Child Health 2002; 38: 401—404.
- ↑ Alberici F, Pagani L, Ratti G, Viale P. Ivermectin alone or in combination with benzyl benzoate in the treatment of human immunodeficiency virus-associated scabies. Br J Dermatol 2000; 142: 969—972.
- ↑ Leppard B, Naburi AE. The use of ivermectin in controlling an outbreak of scabies in a prison. Br J Dermatol 2000; 143: 520—523.
- ↑ 1 2 Cecil Medicine, 23rd Edition. 2008; Saunders. USA. pp. 2438—2439
- ↑ Heukelbach J, Feldmeier H. Ectoparasites—the underestimated realm. Lancet 2004; 363: 889—891.
- ↑ Walton SF, McKinnon M, Pizzutto S, Dougall A, Williams E, Currie BJ. Acaricidal activity of Melaleuca alternifolia tea tree oil: in vitro sensitivity of sarcoptes scabiei var hominis to terpinen-4-ol. Arch Dermatol 2004; 140: 563—566.
- ↑ Charles V, Charles SX. The use and efficacy of Azadirachta indica ADR ‘Neem’ and Curcuma longa ‘Turmeric’ in scabies. A pilot study. Trop Geogr Med 1992; 44: 178—181.
- ↑ Oladimeji FA, Orafidiya OO, Ogunniyi TA, Adewunmi TA. Pediculocidal and scabicidal properties of Lippia multiflora essential oil. J Ethnopharmacol 2000; 72: 305—311.
- ↑ Зорин А. Н. Клинический опыт применения препарата Банеоцин в терапии инфекционных поражений, кожи // II Клиническая дерматология и венерология. — 2005. — № 1. — С. 65—67.
- ↑ 1 2 Кожные и венерические болезни. Руководство для врачей / Скрипкин Ю. К. — М.: Медицина, 2002 год. — Т. 1. — С. 470. — 576 с. — ISBN 5-225-02856-x.
- ↑ Mellanby K. Epidemiology of scabies. In: Orkin M, Maibach HI, eds. Cutaneous infestations and insect bites. New York: Marcel Dekker, 1985: 71-74.
- ↑ Современные подходы к лечению чесотки Архивная копия от 14 августа 2010 на Wayback Machine на сайте www.dermatolog4you.ru.
- ↑ Chakrabarti A. Some epidemiological aspects of animal scabies in human population. Int J Zoonoses 1985; 12: 39-52.
Литература[править | править код]
- Соколова Т. В., Федоровская Р. Ф., Ланге А. Б. Чесотка. — М.: Медицина, 1989. — 176 с. — 50 000 экз. — ISBN 5-225-01576-X. (обл.)