Ацетат цинка
| Ацетат цинка | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Ацетат цинка |
| Традиционные названия | Цинк уксуснокислый |
| Хим. формула | C4H6O4Zn |
| Рац. формула | (CH3COO)2Zn |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса |
219,50 (дигидрат) 183,48 (ангидрат) г/моль |
| Плотность | 1,735 г/см³ (дигидрат) |
| Термические свойства | |
| Температура | |
| • плавления | 237 °C (дигидрат при 100 °C) |
| Химические свойства | |
| Растворимость | |
| • в воде | 43 г/100 мл (20 °C, дигидрат) |
| Структура | |
| Гибридизация | тетраэдр |
| Координационная геометрия | октаэдр (дигидрат) |
| Классификация | |
| Рег. номер CAS | 557-34-6 |
| PubChem | 11192 |
| Рег. номер EINECS | 209-170-2 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E650 |
| RTECS | ZG8750000 |
| ChEBI | 62984 |
| Номер ООН | H2ZEY72PME |
| ChemSpider | 10719 |
| Безопасность | |
| Фразы риска (R) | R22 R36 R50/53 |
| Фразы безопасности (S) | S26 S60 S61 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацета́т ци́нка — химическое соединение, цинковая соль уксусной кислоты. Образует кристаллогидраты —обычно в виде дигидрата Zn(CH 3 CO 2 ) 2 · 2H 2 O, также может быть получен в виде безводной формы при особых условиях реакции. Используется в качестве пищевой добавки ( E650[1]). Категорируется, как усилитель вкуса и аромата[1].
Свойства[править | править код]
При нормальных условиях и гидрат и безводная форма ацетата цинка представляет собой бесцветные кристаллы, растворимые в воде и многих органических растворителях (например, в этаноле, метаноле, ацетоне, анилине, пиридине)[1][2]. Дигидрат ацетата цинка имеет слабый запах уксусной кислоты[2].
Получение[править | править код]
Как и любые соли уксусной кислоты, ацетат цинка можно получить растворением оксида, гидроксида или некоторых солей цинка в уксусной кислоте. Известен простой[3] способ получения ацетата цинка взаимодействием оксида цинка с уксусной кислотой[4][5].
- 2CH3COOH + ZnO = Zn(CH3COO)2 + H2O
На этой реакции основан запатентованный способ получения дигидрата ацетата цинка[6]. Безводный ацетат цинка нельзя получить данным способом, даже если использовать безводную уксусную кислоту[3].
Гидратированный ацетат цинка может быть получен и множеством других способов[7], например, путём растворения гидроксокарбоната (основная соль цинка и угольной кислоты) либо гидроксида цинка в уксусной кислоте[7]. При этом реакция происходит эффективнее при взаимодействии с разбавленными растворами уксусной кислоты и при нагревании.
- 4CH3COOH + Zn2(CO3)(OH)2 = 2Zn(CH3COO)2 + 3H2O + CO2↑
- 2CH3COOH + Zn(OH)2 = Zn(CH3COO)2 + 2H2O
Обработка нитрата цинка уксусным ангидридом является альтернативным путем получения безводного ацетата цинка[8].
Для нужд электроники, волоконной оптики, атомной энергетики— запатентован россиянами способ получения высокочистого безводного ацетата цинка, основанный на реакции диэтилцинка, в качестве цинксодержащего соединения, с уксусной кислотой[3].
Химические свойства[править | править код]
Химические свойства ацетата цинка характерны для ацетатов.
Как и все растворимые соли, ацетат цинка диссоциирует в водных растворах.
При воздействии более сильных кислот выделяется уксусная кислота, а цинк образует соль более сильной кислоты. В реакции ацетата цинка с серной кислотой образуется уксусная кислота и сульфат цинка.
- Zn(CH3COO)2 + H2SO4 = 2CH3COOH + ZnSO4
При температуре ацетат цинка разлагается с образованием ацетона и карбоната цинка.
- Zn(CH3COO)2 = C3H6O + ZnCO3
Из-за этой реакции ацетат цинка нельзя хранить или сушить вблизи открытого огня.
Замещение цинка в ацетате металлами, стоящими левее цинка в электрохимическом ряду активности металлов, влияет на коррозионную стойкость. Так соприкосновение ацетата цинка и алюминия не рекомендуется[9].
- 3Zn(CH3COO)2 + 2Al = 2Al(CH3COO)3 + 3Zn
Взаимодействие ацетата цинка с сильными основаниями приводит, по реакции обмена, к образованию гидроксида цинка и соответствующей соли-ацетата. Эта реакция является качественной реакцией на ацетат цинка в части определения ионов цинка по белому осадку гидроксида цинка, который растворяется при дальнейшем воздействии щёлочью[10].
Zn(CH3COO)2 + 2NaOH = 2CH3COONa + Zn(OH)2
Структура[править | править код]
В безводном ацетате цинка цинк координируется с 4-мя атомами кислорода, образуя тетраэдрическую форму, затем эти тетраэдрические полиэдры соединяются между собой ацетатными лигандами, образуя полимерную структуру[11][12][13].
В дигидрате ацетата цинка цинк координируется с 8-ю атомами кислорода, образуя октаэдрическую форму, при этом обе ацетатные группы являются бидентатными лигандами[14][15].
Ацетат цинка, основной[править | править код]
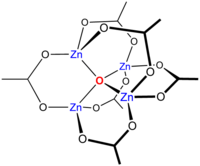
Нагрев ацетата цинка Zn(CH3CO2)2 в вакууме ведёт к потере уксусного ангидрида, оставляя осадок ацетата цинка основного (оксид ацетата цинка, оксиацетат цинка, оксид-гексаацетата цинка ) с формулой Zn4O(CH3CO2)6. Этот кластер имеет тетраэдрическую структуру с оксидным лигандом в центре.
Молекула соединения напоминает соответствующую ацетатную бериллиевую соль, но с бо́льшим межатомным расстоянием, так длина связи Zn-O ~1.97 Å, против ~1.63 Å для оксида-гексаацетата бериллия (Be4O(OAc)6)[16].
Оксид-гексаацетата цинка (Ацетат цинка основной) является распространенным предшественником Металл-органических каркасных структур.
Применение[править | править код]
Пищевое и медицинское применение[править | править код]
Ацетат цинка входит в список разрешенных к применению пищевых добавок как пищевая добавка E650.
Ацетат цинка может быть использован как:
- препарат для лечения дефицита цинка в организме,
- препарат для ингибирования усвоения меди при Болезни Вильсона — Коновалова,
- препарат в смеси с антибиотиком, например эритромицином, для лечения акне; мазь против зуда; противогрибковое средство,
- вяжущее средства в мазях, лосьонах,
- компонент зубных цементов,
- освежитель дыхания[17][18] и ингибитор налёта[19] в жевательной резинке,
- компонент пастилок для лечения назофарингита.
Ацетат цинка особенно показан в виде примеси в пастилках[20][21]. Мета-анализ показал, что три повышенные дозы препарата снижают длительность назофарингита на 42 %[22].
Хотя пастилки с ацетатом цинка укорачивают длительность назофарингита, многие цинковые пастилки на рынке США имеют либо слишком низкое содержание цинка, либо ингредиенты, связывающие ионы цинка, например лимонную кислоту[23]. Так что, выигрыш от высоких доз активного цинка в тестовом изучении может и не проявляться при обыденном применении потребителями.
Промышленное применение[править | править код]
В промышленности ацетат цинка применяется как:
- протрава для придания грибковой устойчивости древесине, протрава при окрашивании тканей
- цинкосодержащее вещество для производства других солей цинка (см. Категория:Соли цинка),
- реагент в производстве полимеров, этилацетата, этилена,
- катализатор в органическом синтезе,
- аналитический реактив,
- поверхностный ингибитор в водяных трубопроводах первого контура атомных электростанций,
- цинксодержащее вещество для получения в золь-гель процессе слоев прозрачного полупроводника — оксида цинка.
Литература[править | править код]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Химическая энциклопедия / Редкол.: И. Л. Кнунянц и другие. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
Примечания[править | править код]
- ↑ 1 2 3 Е650 - ацетат цинка(Е650). https://prodobavki.com. Дата обращения: 6 октября 2022. Архивировано 6 октября 2022 года.
- ↑ 1 2 ГОСТ 5823-78. https://files.stroyinf.ru. Дата обращения: 6 октября 2022. Архивировано 6 октября 2022 года.
- ↑ 1 2 3 Способ получения высокочистого безводного ацетата цинка. https://findpatent.ru. Дата обращения: 5 октября 2022. Архивировано 5 октября 2022 года.
- ↑ Цинк ацетат. https://himmax.ru. Дата обращения: 6 октября 2022. Архивировано 6 октября 2022 года.
- ↑ Ю. В. Карякин, И. И. Ангелов. Чистые химические вещества. — 4-е изд. — М.: Химия, 1974. — С. 403. — 408 с. — ISBN 978-5-458-45265-6. Архивировано 5 октября 2022 года.
- ↑ Способ получения двухводного ацетата цинка. Дата обращения: 5 октября 2022. Архивировано 5 октября 2022 года.
- ↑ 1 2 Ацетат цинка. https://ru.crystalls.info. Дата обращения: 5 октября 2022. Архивировано 5 октября 2022 года.
- ↑ O. F. Wagenknecht; R. Juza (1963). "Zinc Acetate". In G. Brauer (ed.). Handbook of Preparative Inorganic Chemistry, 2nd Ed. Vol. 2pages=1087. NY,NY: Academic Press.
- ↑ Таблица коррозионной стойкости. Среда: Ацетат цинка. Материал: алюминий. https://fluid-line.ru. Дата обращения: 6 октября 2022. Архивировано 6 октября 2022 года.
- ↑ Цинк. Химия цинка и его соединений. Качественные реакции. https://chemege.ru. Дата обращения: 6 октября 2022. Архивировано 6 октября 2022 года.
- ↑ Capilla, A. V.; Aranda, R. A. (1979). "Anhydrous Zinc(II) Acetate (CH3-COO)2Zn". Crystal Structure Communications. 8: 795–797.
- ↑ W. Clegg, I. R. Little and B. P. Straughan. Monoclinic anhydrous zinc(II) acetate (англ.) // Acta Crystallographica. — 1986. — Vol. C42. — P. 1701-1703. — doi:10.1107/S010827018609087X. Архивировано 7 октября 2022 года.
- ↑ H. He. A new monoclinic polymorph of anhydrous zinc acetate (англ.) // Acta Crystallographica. — 2006. — Vol. E62. — P. 3291-3292. — doi:10.1107/S1600536806046678. Архивировано 7 октября 2022 года.
- ↑ J. N. van Niekerk, F. R. L. Schoening and J. H. Talbot. The crystal structure of zinc acetate dihydrate, Zn(CH3COO)2·2H2O (неопр.) // Acta Cryst.. — 1953. — Т. 6, № 8. — С. 720—723. — doi:10.1107/S0365110X53002015.
- ↑ Ishioka, T.; Murata, A.; Kitagawa, Y.; Nakamura, K. T. Zinc(II) Acetate Dihydrate (англ.) // Acta Crystallographica. — 1997. — Vol. C53. — P. 1029-1031. — doi:10.1107/S0108270197004484. Архивировано 7 октября 2022 года.
- ↑ Koyama, H.; Saito, Y. The Crystal Structure of Zinc Oxyacetate, Zn4O(CH3COO)6 (англ.) // Bull. Chem. Soc. Japan : journal. — 1954. — Vol. 27, no. 2. — P. 112—114. — doi:10.1246/bcsj.27.112.
- ↑ Espacenet — Bibliographic data
- ↑ Espacenet — Bibliographic data
- ↑ Giertsen E., Svatun B., Saxton A. Plaque inhibition by hexetidine and zinc (неопр.) // Scand J Dent Res. — 1987. — February (т. 95, № 1). — С. 49—54. — PMID 3470899.
- ↑ Eby GA (2004) Zinc lozenges: cold cure or candy? Solution chemistry determinations. Biosci Rep 24:23-39 Архивировано 29 октября 2013 года.
- ↑ Eby GA (2010) Zinc lozenges as cure for the common cold. Med Hypotheses 74:482-92. Дата обращения: 20 февраля 2014. Архивировано 18 сентября 2017 года.
- ↑ Hemilä H (2011) Zinc lozenges may shorten the duration of colds: a systematic review. Open Respir Med J 5:51-8 Архивная копия от 30 ноября 2017 на Wayback Machine Refs with links: http://www.mv.helsinki.fi/home/hemila/Zn/TORMJ.htm Архивная копия от 29 октября 2013 на Wayback Machine
- ↑ Eby G (2009) Zinc Lozenges as a Common Cold Treatment. Дата обращения: 20 февраля 2014. Архивировано 29 октября 2013 года.