Диэтиленгликоль
| Диэтиленгликоль | |
|---|---|
 | |
| Общие | |
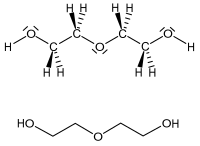
| Систематическое наименование |
2-[2-гидроксиэтокси]этанол |
| Сокращения | ДЭГ |
| Традиционные названия | дигликоль |
| Хим. формула | C4H10O3 |
| Физические свойства | |
| Молярная масса | 106,12 г/моль |
| Плотность | 1,118 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -7.8 °C |
| • кипения | 244-245 °C |
| • разложения | 343 °C |
| • вспышки | 124 °C |
| Энтальпия | |
| • образования | -626.8 кДж/моль |
| Классификация | |
| Рег. номер CAS | 111-46-6 |
| PubChem | 8117 |
| Рег. номер EINECS | 203-872-2 |
| SMILES | |
| InChI | |
| ChEBI | 46807 |
| ChemSpider | 13835180 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Диэтиленгликоль, двуэтиленовый спирт (дигликоль), ДЭГ — химическое соединение, представитель двухатомных спиртов.
Физические свойства[править | править код]
Диэтиленгликоль является прозрачной вязкой жидкостью. Гигроскопичен, обладает сладковатым вкусом. Растворим в воде, низших спиртах, ацетоне, анилине, феноле и хлороформе. Ограниченно растворим в бензоле, диэтиловом эфире и четырёххлористом углероде. Плохо растворим в минеральных и растительных маслах.
Химические свойства[править | править код]
Наличие в молекуле диэтиленгликоля двух спиртовых групп приводит к образованию внутри- и межмолекулярных водородных связей — с другими веществами, содержащими электроотрицательный атом (вода, амины).
Может быть использован в качестве топлива для портативных горелок. Горит пламенем, практически не имеющим цвета, при этом выделяется большое количество теплоты — 2376,39 кДж/моль:
Диэтиленгликоль склонен к автоокислению. Автоокисление значительно ускоряется при наличии примесей пероксидных соединений (пероксиды, гидропероксиды) и замедляется при добавлении ингибиторов (хиноны, гидрохиноны). Окисляясь, диэтиленгликоль приобретает желтоватую окраску.
Диэтиленгликоль проявляет свойства как гликолей, так и простых эфиров. С карбоновыми кислотами, их ангидридами и хлорангидридами образует сложные моно- и диэфиры, с альдегидами и кетонами в присутствии катализатора — фосфорной кислоты — соответствующие циклические ацетали.
Дегидрирование диэтиленгликоля на катализаторе (медь, цинк-медь-хром) приводит к 1,4-диоксан-2-ону. Дегидрирование на щелочных катализаторах даёт 1,4-диоксан. При оксиэтилировании при 150‒200оС в присутствии щелочных катализаторов образуется полиэтиленгликоль.
Реагирует с фосгеном, образующиеся продукты являются очень реакционноспособными. Для бис-хлоруглекислого эфира дигликоля возможна реакция с аллиловым спиртом в присутствии щелочи.
Физиологическое значение[править | править код]
Диэтиленгликоль относится к умеренно-опасным веществам (Класс опасности 3)[1]. При попадании в организм вызывает общетоксическое действие, в первую очередь поражает почки и печень[2]. ПДК диэтиленгликоля в воздухе рабочей зоны составляет 10 мг/м3. Однако его ингаляционное воздействие невелико из-за низкой упругости паров.
Производные[править | править код]
Диглим[3] (диметиловый эфир дигликоля) — является хорошим растворителем, устойчивым к основаниям
Получение[править | править код]
Промышленный синтез диэтиленгликоля заключается в следующих процессах:
- Оксиэтилирование этиленгликоля
- Синтез этиленгликоля из этиленоксида (как побочный продукт)
Применение[править | править код]
Диэтиленгликоль является сырьём в промышленном получении сложных эфиров, полиуретанов, олигоэфиракрилатов. Он служит пластификатором, эффективным экстрагентом ароматических веществ в процессах риформинга. Диэтиленгликоль используется как осушитель газов, в качестве основного компонента антифризов, гидравлических и гидротормозных жидкостей, как растворитель нитратов целлюлозы и полиэфирных смол.
Примечания[править | править код]
- ↑ name=https://docs.cntd.ru_Diglycol (недоступная ссылка)
- ↑ ГОСТ 10136-77. Диэтиленгликоль. Технические условия. Дата обращения: 30 августа 2009. Архивировано 22 июня 2010 года.
- ↑ Diglyme (англ.). Дата обращения: 18 ноября 2020. Архивировано 11 ноября 2020 года.
Ссылки[править | править код]
- ГОСТ 10136-77. Диэтиленгликоль. Технические условия. Дата обращения: 31 мая 2013.
Литература[править | править код]
- Кнунянц И. Л. и др. т.2 Даффа-Меди // Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
