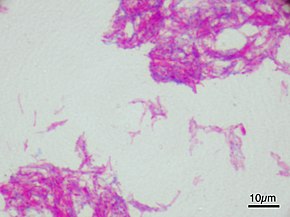
БЦЖ
| Вакцина для профилактики туберкулёза | |
|---|---|
| Vaccinum ad prophylaxim tuberculosis | |
 | |
| Химическое соединение | |
| DrugBank | DB12768 |
| Состав | |
| Действующее вещество | |
| живая аттенуированная культура Mycobacterium bovis | |
| Классификация | |
| Фармакол. группа | Вакцины, сыворотки, фаги и анатоксины |
| АТХ | J07AN01 |
| Лекарственные формы | |
| лиофилизат для приготовления суспензии | |
| Способы введения | |
| внутрикожно | |
| Другие названия | |
| Вакцина туберкулёзная БЦЖ живая, БЦЖ, БЦЖ-М, вакцина туберкулёзная для щадящей первичной иммунизации (БЦЖ-М), вакцина туберкулёзная (БЦЖ) | |

БЦЖ (сокр. от Баци́лла Кальме́та — Гере́на, фр. Bacillus Calmette—Guérin, BCG) — вакцина против туберкулёза, приготовленная из штамма ослабленной живой бычьей туберкулёзной палочки (Mycobacterium bovis), которая практически утратила вирулентность для человека, будучи специально выращенной в искусственной среде.
БЦЖ — исторически первая живая бактериальная вакцина для человека (Calmette и Guerin, 1921)[1].
БЦЖ — единственная доступная на 2018 год противотуберкулёзная вакцина[2]. Эта вакцина относительно безопасна, недорога и требует лишь одной инъекции. Несмотря на недостатки, вакцинация БЦЖ в большинстве эндемичных стран рассматривается в качестве жизнесберегающего и важного элемента стандартных мер по борьбе с туберкулёзом[3].
Помимо туберкулёза, вакцина БЦЖ обладает доказанной эффективностью в борьбе с проказой и, по неполным данным, защищает от язвы Бурули и других нетуберкулёзных микобактериозов[4]. Кроме того, она используется при лечении рака мочевого пузыря[5].
Описание[править | править код]
Вакцина БЦЖ представляет собой бычий тип микобактерии, аттенуированный (ослабленный в процессе селекции) штамм, не представляющий опасности для человека. По состоянию на 2018 год в мире создано больше 10 штаммов БЦЖ, все они созданы на основе ослабленного штамма M. bovis, выведенного Кальметом и Гереном в 1913 году[4].
Для предотвращения дальнейшего отклонения от первоначальной БЦЖ с 1956 года ВОЗ хранит лиофилизированные посевные серии вакцинных штаммов. В плане эффективности ни один штамм БЦЖ не обладает явными преимуществами перед другими штаммами и не существует глобального консенсуса относительно того, какой штамм БЦЖ является оптимальным для общего использования[6]. На 2004 год 90% вакцинаций БЦЖ в мире приходятся на штаммы[7]:
- Pasteur 1173 Р2 (Франция);
- Danish 1331 (Дания);
- Glaxo 1077 (производный от датского, изготовлен фирмой «Глаксо»);
- Tokyo 172-1 (Япония);
- БЦЖ-1 (Россия);
- Moreau RDJ.
Штаммы обладают различной реактогенностью. Pasteur 1173 Р2 и Danish 1331 индуцируют больше побочных реакций, чем Glaxo 1077, Tokyo 172-1 или Moreau RDJ. Дозы у каждой вакцины также различаются, у разных вакцин одна доза содержит от 50 тыс. до 3 млн. бактериальных тел[7].
В России и странах СНГ известны[8]:
- БЦЖ и БЦЖ-М, содержат выведенный З. А. Лебедевой штамм;
- датская вакцина, их несколько штаммов.
Препараты российских вакцин БЦЖ и БЦЖ-М представляют собой живые микобактерии вакцинного штамма (субштамма) BCG-1 Russia, лиофилизированные в 1,5% растворе глутамината натрия. Вакцина БЦЖ-М — препарат с уменьшенным вдвое весовым содержанием микобактерий БЦЖ в прививочной дозе (0,025 мг[9] против 0,05 мг в БЦЖ[10]), в основном за счёт убитых клеток[источник не указан 1260 дней]. Живые микобактерии штамма BCG-1, размножаясь в организме привитого, способствует развитию длительного специфического иммунитета к туберкулёзу. Российский субштамм обладает высокой иммуногенностью (высокими защитными свойствами), а приготовленная из него вакцина обладает невысокой реактогенностъю, вызывая не более 0,06% поствакцинальных лимфаденитов[11].
В целом, вакцина БЦЖ обладает неплохими защитными свойствами, но её эффективность неоднородна в разных возрастных группах[12].
Вакцина БЦЖ обладает доказанным защитным действием в отношении туберкулёзного менингита и диссеминированного туберкулёза среди детей. Она не предотвращает первичного инфицирования и, что более важно, не предотвращает реактивацию латентной лёгочной инфекции, являющейся основным источником бациллярного распространения среди населения[2].
Вакцина эффективна не только для предотвращения туберкулёза. Для атипичных форм микобактериозов, вызываемых микобактериями группы MAC (см. Микобактерии § Микобактерии avium-комплекса (MAC)) известно, что показатель заболеваемости в Швеции в период с 1975 по 1985 среди вакцинированных детей был в 5,9 раза ниже, чем среди невакцинированных (на 100 тыс. детей младше 5 лет: у невакцинированных 26,8 случая заболевания, у вакцинированных — 4,6)[13][14].
Отмечены случаи поствакцинальных осложнений.
История[править | править код]
В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Французский микробиолог Альбер Кальмет (фр. Albert Calmette) и ветеринар Камиль Герен (фр. Camille Guérin) работали в 1908 году в Институте Пастера в Лилле. Их работа охватывала получение культур туберкулёзной палочки и исследования различных питательных сред. При этом они выяснили, что на питательной среде на основе глицерина, желчи и картофеля вырастают туберкулёзные палочки наименьшей вирулентности. С этого момента они изменили ход исследования, чтобы выяснить, нельзя ли посредством повторяющегося культивирования вырастить ослабленный штамм для производства вакцины.
Исследования продлились до 1919 года, когда вакцина с невирулентными бактериями не вызвала туберкулёз у подопытных животных.
В 1919 году Кальмет и Герен перешли в Институт Пастера в Париже, где в 1921 году создали вакцину БЦЖ для применения на людях[15].
Общественное признание вакцины проходило с трудом, в частности, из-за случавшихся трагедий. В 1930 году в Любеке 240 новорождённых привили в 10-дневном возрасте. Все они заболели туберкулёзом, 72 из них умерли. Расследование показало, что вакцина была заражена вирулентным штаммом, который хранился в том же инкубаторе. Вину возложили на директора больницы, которого приговорили к 2 годам лишения свободы за халатность, повлёкшую смерть[16].
В 1925 году Кальмет передал профессору Л. А. Тарасевичу в Москву штамм БЦЖ, который был в нашей стране зарегистрирован как БЦЖ-1. В СССР началось экспериментальное и клиническое изучение вакцины БЦЖ-1. Через 3 года удалось систематизировать результаты, которые показали, что вакцинация эффективна: смертность от туберкулёза в группах вакцинированных детей в окружении бактериовыделителей была меньше, чем среди невакцинированных. В 1928 году было рекомендовано вакцинировать БЦЖ новорождённых из очагов туберкулёзной инфекции.
В 1928 году вакцина была принята Лигой Наций. Однако из-за противников вакцинации она не была широко распространена вплоть до окончания Второй мировой войны. С 1945 по 1948 год в Восточной Европе было привито 8 миллионов детей[источник не указан 1480 дней].
С середины 1950-х годов вакцинация новорождённых в городах и сельской местности стала обязательной. Вакцина БЦЖ обеспечивала определённую защиту детей перед туберкулёзом, особенно такими его формами, как милиарная и туберкулёзный менингит. До 1962 года вакцину БЦЖ у новорождённых применяли перорально, реже использовали накожный метод. С 1962 года для вакцинации и ревакцинации применяют более эффективный внутрикожный метод введения этой вакцины. В 1985 году для вакцинации новорождённых с отягощённым постнатальным периодом предложена вакцина БЦЖ-М, которая позволяет уменьшить антигенную нагрузку вакцинируемых.
С 2006 года несколько стран прекратили использование БЦЖ для массовой вакцинации ввиду радикального «снижения первичной заболеваемости туберкулёзом». США и Нидерланды никогда не использовали БЦЖ массово.
В 2018 году в ЮАР прошла вторую фазу клинических испытаний новая противотуберкулёзная вакцина H4:IC31, при этом она показала меньшую эффективность в сравнении с БЦЖ[17][18][19]
В начале 2020 эпидемиологи, изучающие COVID-19, заметили, что в странах, где население прививается вакциной БЦЖ, наблюдается относительно низкий уровень заболеваемости и смертности от коронавирусной инфекции[20][21]. Часть исследователей, обнаруживших корреляцию, отмечают при этом, что официальная статистика, которую они взяли в качестве исходных данных, может быть недостоверной, и что без клинических исследований нельзя утверждать, что вакцинация БЦЖ хоть как-то влияет на заболеваемость COVID-19[21]. Другие специалисты не согласны с оптимизмом части эпидемиологов, при этом они отмечают, что корреляция ещё не означает причинно-следственную связь, и призывают не делать поспешных выводов[22].
Рекомендации, показания и противопоказания[править | править код]
В 2018 году ВОЗ рекомендует[23]:
- В странах с высоким бременем туберкулёза все дети грудного возраста должны получить одну дозу вакцины БЦЖ как можно раньше после рождения, причём все здоровые новорождённые должны быть вакцинированы БЦЖ даже в ВИЧ-эндемичных районах.
- В странах с низким бременем туберкулёза вакцинация БЦЖ может быть ограничена новорождёнными и младенцами из выявленных групп высокого риска или детьми старшего возраста с отрицательными кожным тестом и анализом выявления гамма-интерферона (англ. IGRA).
- Вакцинация БЦЖ взрослых обычно не рекомендуется, но может проводиться для туберкулин-отрицательных лиц, имеющих неизбежный контакт с больным, инфицированным Mycobacterium tuberculosis с МЛУ (множественной лекарственной устойчивостью).
- В странах с низким уровнем туберкулёза проводить вакцинацию мигрантов из стран с высоким бременем туберкулёза не рекомендуется, но рекомендуется их вакцинировать перед возвращением домой, если они не были вакцинированы ранее.
- Ревакцинация БЦЖ не рекомендуется даже при отрицательных результатах тестов на туберкулёз.
- У младенцев, контактировавших после рождения с больным лёгочным туберкулёзом с положительным мазком мокроты, вакцинацию БЦЖ следует отложить до завершения шестимесячного профилактического курса лечения изониазидом.
- Младенцы и дети с клиническими проявлениями заражения ВИЧ и с другими формами иммунодефицита не должны подвергаться вакцинации БЦЖ.
- Прививка БЦЖ противопоказана:
- Людям с индивидуальной непереносимостью;
- Беременным и кормящим женщинам;
- Людям с иммунодефицитом и инфицированным ВИЧ за исключением тех, кто проходит лечение (антиретровирусную терапию) и чей организм иммунологически стабилен — им прививка БЦЖ показана.
- Путешественникам с отрицательным результатом тестов на туберкулёз, не прошедшим вакцинацию ранее, рекомендуется пройти вакцинацию БЦЖ перед посещением страны с высоким бременем туберкулёза.
- Для младенцев со сниженным весом (менее 2,5 кг) и родившихся недоношенными (меньше 31 недели) прививка БЦЖ ставится при стабильности клинического состояния и здоровья или может быть отложена до достижения нормальных показателей развития. Доза прививки при этом устанавливается индивидуально, ревакцинация не требуется.
- Младенцы, родившиеся у больных активной формой туберкулёза матерей, подтверждённой бактериологическими тестами, должны быть привиты обычной дозой БЦЖ после обследования, доказавшего отсутствие заболевания.
- В странах с высокой распространённостью ВИЧ-инфекции польза от прививки новорожденных БЦЖ перевешивает риск, связанный с прививкой, поэтому в таких популяциях ВОЗ рекомендует прививать младенцев, родившихся как от женщин с неизвестным статусом ВИЧ, так и от ВИЧ-инфицированных женщин, у которых нет клинических проявлений ВИЧ. В случае клинических проявлений ВИЧ прививка должна быть отложена на полгода для проведения профилактической анти-ВИЧ терапии.
Соблюдение рекомендации прививать детей, родившихся от женщин с неизвестным статусом ВИЧ, в России приводит к 1 % осложнений вакцинации БЦЖ (у ВИЧ-инфицированных младенцев)[24].
Показания[править | править код]
Показания к вакцинации БЦЖ по позиции ВОЗ 2008 года[25].
- всем детям грудного возраста, проживающим в высокоэндемичных по туберкулёзу районах за исключением противопоказаний;
- детям особого риска возникновения туберкулёзной инфекции, проживающим в низкоэндемичных по туберкулёзу районах;
- лицам, подвергающимся воздействию M.tuberculosis с множественной лекарственной резистентностью.
- Показания к применению отечественных вакцин БЦЖ и БЦЖ-М
Противопоказания[править | править код]
Противопоказания к вакцинации БЦЖ по позиции ВОЗ 2008 года[25].
- лицам с нарушениями иммунитета: с установленным или подозреваемым врожденным иммунодефицитом, раком, ВИЧ-инфицированным с клиническими проявлениями;
- пациентам, проходящим терапию препаратами, подавляющими иммунитет;
- беременным.
Противопоказание против проведения вакцинации БЦЖ беременных — условное: нет исследований, обосновывающих отвод от вакцинации для беременных. Это общая позиция ВОЗ — не прививать беременных живыми вакцинами[28].
Российские противопоказания вакцинации[править | править код]
К вакцинацией БЦЖ в России имеются следующие противопоказания[26]:
- для вакцинации:
- Недоношенность новорождённого — масса тела при рождении менее 2500 г.
- Внутриутробная гипотрофия III—IV степени.
- Острые заболевания. Вакцинация откладывается до окончания острых проявлений заболевания.
- Обострения хронических заболеваний. Вакцинация откладывается до окончания обострения.
- ВИЧ-инфекция у матери новорождённого, следует воздержаться от введения ему БЦЖ до возраста 18 месяцев, когда будет уточнён ВИЧ-статус младенца.
- Первичное иммунодефицитное состояние, злокачественные новообразования.
- При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 месяцев после окончания лечения.
- Генерализованная инфекция БЦЖ, выявленная у других детей в семье.
- для ревакцинации:
- Острые инфекционные и неинфекционные заболевания, обострения хронических и аллергических заболеваний. Прививка проводится через месяц после выздоровления или ремиссии.
- Иммунодефицитные состояния, злокачественные заболевания крови и новообразования.
При лечении иммунодепрессантами и лучевой терапии ревакцинацию проводят не ранее, чем через 6 месяцев после окончания лечения.
- Больные и ранее болевшие туберкулёзом, а также инфицированные микобактериями.
- Положительная и сомнительная реакция Манту с двумя туберкулиновыми единицами ППД-Л.
- Осложнённые реакции на предыдущее введение вакцины БЦЖ.
- При контакте с инфекционными больными прививки проводят по окончании срока карантина (по прошествии максимального срока инкубационного периода).
- Дети, имеющие противопоказания к вакцинации вакциной БЦЖ, прививаются вакциной БЦЖ-М с соблюдением инструкции к этой вакцине.
- При временном отводе от прививки требуется наблюдение за пациентом и привитие его после снятия противопоказаний (выздоровления, окончания карантина и пр.). В случае необходимости проводят соответствующие клинико−лабораторные обследования.
Противопоказания к вакцине БЦЖ-М[27]:
- Недоношенность новорождённого — масса тела при рождении менее 2000 г.
- Острые заболевания. Вакцинация откладывается до окончания острых проявлений заболевания и обострения хронических заболеваний.
- Первичное иммунодефицитное состояние, злокачественные новообразования. При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 месяцев после окончания лечения.
- Генерализованная инфекция БЦЖ, выявленная у других детей в семье.
- ВИЧ-инфекция у ребёнка с клиническими проявлениями вторичных заболеваний.
- ВИЧ-инфекция у матери новорождённого, не получавшей во время беременности антиретровирусную терапию.
- Временно освобождённые от прививок должны быть взяты под наблюдение и учёт и привиты после полного выздоровления или снятия противопоказаний. В случае необходимости проводят соответствующие клинико−лабораторные обследования.
Вопреки распространённому мнению, вакцинация от гепатита B не является противопоказанием для одновременного (в тот же день) введения вакцины БЦЖ[29].
Эффективность[править | править код]
Систематический обзор двенадцати когортных исследований показал эффективность прививки в защите от туберкулёза от 44 до 99 % за исключением одного исследования. В этом единственном исследовании описана неэффективность вакцинации, причём в нём нет данных о том, привилась введённая вакцина или нет (был ли у вакцинированных рубец на месте введения вакцины), поэтому, возможно, пациентам ввели неэффективную (испортившуюся) вакцину, при хранении которой не соблюдался температурный режим[30].
Эффективность защиты вакциной БЦЖ зависит от возраста[31]:
- у новорождённых составляет в среднем 82 %, у них прививка в пять раз снижает риск генерализованного туберкулёза и менингита;
- у туберкулин-отрицательных детей школьного возраста эффективность по лёгочной форме туберкулёза составляет 64 %, поскольку у детей старше 10 лет чаще возникает вторичный туберкулёз, а не первичный.
Большой разброс результатов исследования эффективности[править | править код]
Наиболее противоречивым аспектом БЦЖ является её непостоянная эффективность, обнаруженная в различных клинических исследованиях. Эффективность БЦЖ, похоже, сильно зависит от географического местоположения. Клинические исследования, проведённые в Великобритании, последовательно доказали защитный эффект от 60 % до 80 %[32]. Однако исследования, проведённые в некоторых других странах, не выявили защитного эффекта совсем. В целом, эффективность БЦЖ, похоже, падает с приближением к экватору[33].
Первое большое клиническое исследование, оценивающее эффективность БЦЖ, было проведено с 1956 по 1963 годы и включало почти 60 000 школьников, привитых БЦЖ, в возрасте 14—15 лет. Это исследование показало 84-процентную эффективность до 5 лет по прошествии иммунизации[34]. Однако исследование органов здравоохранения в США в Джорджии и Алабаме, опубликованное в 1966, показало эффективность на уровне 14 %[35].
Последующее исследование, проведённое в южной Индии и опубликованное в 1979 году («Чинглепутское исследование») показало отсутствие защитного эффекта[36]. По тщательности и охвату это было, пожалуй, самое серьёзное контролируемое рандомизированное исследование со слепым контролем. 260 тысяч детей были случайным образом разделены на 2 группы, первая из которых получала вакцину БЦЖ, а вторая — плацебо. Наблюдение за вакцинированными обеих групп продолжалось 7 с половиной лет. В результате, исследователи констатировали, что заболеваемость туберкулёзом в группе привитой вакциной оказалась слегка выше, чем в равной по размеру плацебо-группе[37][38].
Исследование, проведённое на американских индейцах, привитых в 1930-х годах нашло доказательства защиты по прошествии 60 лет с лишь слегка пониженной эффективностью[39].
Вакцина БЦЖ обладает наибольшей эффективностью против диссеминированного туберкулёза и туберкулёза мозга[40].
Причины изменчивой эффективности[править | править код]
Причины различной эффективности БЦЖ в различных странах трудно понять. Были предположены следующие причины, но ни одна не была доказана научно:
- Генетические различия штаммов БЦЖ Существуют генетические различия в штаммах БЦЖ, использованных в различных странах, и это может объяснять различающуюся эффективность[41].
- Генетические различия в популяциях Различия в построении генома в различных популяциях могут объяснять различия в эффективности. В исследованиях БЦЖ в Бирмингеме, опубликованных в 1988 году, проверяли детей, рождённых в семьях выходцев из Индии, где была зарегистрирована нулевая эффективность вакцины. Исследование показало 64 % защитный эффект, сходный со среднебританскими показателями, таким образом, опровергая гипотезу генетических различий прививаемых[42].
- Взаимовлияние нетуберкулёзных микобактерий Одна из гипотез состоит в том, что присутствие в окружающей среде других микобактерий, нежели M. tuberculosis, способно вызвать иммунный ответ в исследуемой популяции. Преобладание окружающих микобактерий увеличивается с приближением к экватору. Суть гипотезы в том, что БЦЖ не в состоянии вызвать дополнительную защитную реакцию, потому что такое население уже имеет природную иммунную реакцию на микобактерии. Обладает ли эта иммунная реакция действительными защитными свойствами против туберкулёза, вопрос спорный. Гипотеза была впервые выдвинута Палмером и Лонгом (Palmer and Long)[43].
- Взаимовлияние с паразитическими инфекциями Другая гипотеза состоит в том, что параллельные паразитические инфекции меняют иммунный ответ к БЦЖ, снижая её эффективность. Реакция Т-хелперов-1 необходима для эффективной иммунизации против возбудителя туберкулёза. Суть данной гипотезы в том, что одновременное заражение различными паразитами производит параллельную реакцию Т-хелперов-2, что притупляет эффективность БЦЖ[44].
Применение[править | править код]
Основное использование БЦЖ — это вакцинация против туберкулёза. Рекомендуется вводить внутрикожно. Вакцинация БЦЖ может давать ложноположительную реакцию на пробу Манту, но особо яркая реакция обычно указывает на болезнь, за исключением случаев аллергии. Не влияет на результаты анализа выявления гамма-интерферона (IGRA).
Частота и возраст вакцинации БЦЖ различается от страны к стране.
В России официальная рекомендация — вводить вакцину новорождённым на 3−5 день жизни, в результате в Москве новорождённые, выписанные из роддомов на 2 и 3 день, не получают вакцину в роддомах, при том, что существующая рекомендация ВОЗ — вакцинировать новорождённых сразу после рождения или как можно раньше[29].
Способ введения БЦЖ[править | править код]
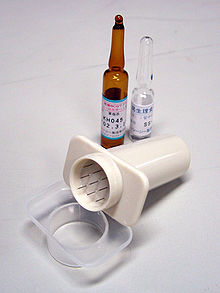
Туберкулиновая проба обязательна перед вакцинацией БЦЖ во всех случаях, кроме прививания новорождённых. Реакция на эту пробу является противопоказанием к прививке. Если прививка делается человеку с положительной туберкулиновой пробой, высок риск сильного местного воспаления и рубцевания. Существует неправильное представление[источник не указан 1480 дней], что БЦЖ не делается при положительной реакции на туберкулиновую пробу, потому что «иммунитет уже имеется».
БЦЖ вводится внутрикожно в месте прикрепления дельтовидной мышцы[источник не указан 1480 дней].
Подходы к вакцинации БЦЖ в разных странах[править | править код]
Вакцинация БЦЖ применяется во всех без исключения странах. В зависимости от эпидемиологической ситуации по туберкулёзу в конкретной стране либо массово вакцинируют новрожденных (более 150 стран), либо выборочно: новорожденных и взрослых из групп риска или индивидуальным показаниям. Некоторые страны после официальной отмены всеобщей неонатальной вакцинации ввели её вновь, реагируя либо на нарастание заболеваемости, либо на запросы населения[45].
- СССР и Россия. В СССР была принята всеохватная вакцинация новорождённых в родильных домах с 1962. Данная практика сохраняется и в России. Кроме того, проводится регулярная ревакцинация.
- Великобритания ввела поголовную иммунизацию в 1953 году. До 2005 года предписывалось прививать всех школьников в возрасте 13 лет и новорождённых из групп риска. БЦЖ также проводилась лицам, имевшим контакт с туберкулёзными больными. Пик случаев заболевания приходится на подростковый возраст и молодых людей, а исследования Совета по медицинским исследованиям Великобритании MRC показывают, что значимый иммунитет сохраняется максимально в течение 15 лет. Прививка БЦЖ проводилась в годы наибольшей заболеваемости лёгочным туберкулёзом. Всеобщая иммунизация была прекращена по причине падения соотношения расходы/эффективность: в то время как в 1953 году 94 ребёнка должны были быть привиты, чтобы предотвратить один случай туберкулёза, к 1988 году годовая заболеваемость туберкулёзом в Великобритании упала так, что надо было бы привить 12000 детей, чтобы предотвратить один случай туберкулёза[источник не указан 1924 дня]. В настоящее время в Великобритании прививаются люди с факторами риска: дети, родившиеся в странах, где уровень заболеваемости туберкулёзом превышает 40 случаев на 100 тыс. населения, прибывшие из таких стран, чьи родители жили в таких странах, контактирующие с больными туберкулёзом. Кроме того, прививка рекомендована тем, кто выезжает в страны с высоким уровнем туберкулёза на более чем три месяца[46].
- Индия ввела всеохватную иммунизацию БЦЖ в 1948 году первой из неевропейских стран[47].
- Бразилия ввела всеохватную иммунизацию БЦЖ в 1967—1968 годах и проводит её по настоящее время. Согласно бразильским законам, работники здравоохранения получают ревакцинацию БЦЖ[источник не указан 1924 дня].
- Германия. В ФРГ массовая иммунизация проводилась с 1950-х годов до мая 1975 года (Западная Германия)[48][49] и до 1998 года (Восточная Германия). В 1998 году в рекомендациях Постоянной комиссии по прививкам Института Роберта Коха всеобщая вакцинация БЦЖ уже не рекомендована. В качестве обоснования отмены приведены: хорошая эпидемиологическая ситуация, отсутствие надёжно доказанной эффективности вакцины БЦЖ и серьёзные побочные эффекты[50].
На 2018 год вакцинация против туберкулёза проводится выборочно, обоснования те же: благоприятная эпидемиологическая ситуация, эффективность защиты у прививки 50—80 %, побочные эффекты[51]. - Другие страны. В Сингапуре и Малайзии БЦЖ прививалась новорождённым, ревакцинация делалась в 12-летнем возрасте. С 2001 года в Сингапуре и Малайзии схема была изменена на однократную при рождении[источник не указан 1924 дня].
Вакцинация в странах ЕС[править | править код]
По состоянию на 2005 год вакцинация БЦЖ применяется во всех 28 странах Европейского союза, из них в семи странах она не поголовная — вакцинируются дети из групп риска, причём в двух странах из этих семи решение о вакцинации принимается по индивидуальным показаниям риска туберкулёза[52].
На 2005 год массово вакцинируют младенцев до года:
На 2005 год массово вакцинируют взрослых и детей старше года:
На 2005 год вакцинируют детей из групп риска или по индивидуальным показаниям, а также граждан, планирующих посетить регионы с высоким бременем туберкулёза:
Прочее применение[править | править код]
- Проказа: БЦЖ обладает полным защитным эффектом против проказы в 26 % случаев[53].
- Язва Бурули: По сообщениям 2001 года, БЦЖ может защищать от язвы Бурули или задерживать её развитие[54]. В 2015 году опубликовано исследование, не обнаружившее влияние БЦЖ на течение болезни при язве Бурули[55].
- Иммунотерапия рака: БЦЖ используется в лечении поверхностных форм рака мочевого пузыря, механизм действия неясен, предположительно, местный иммунный ответ, вызванный БЦЖ, помогает организму бороться с раковыми клетками[56][57][58]. БЦЖ также применяется для иммунотерапии рака кишечника[59] и для лечения болезни Бека (саркоида) у лошадей.
Побочные действия[править | править код]
Противотуберкулёзная вакцина БЦЖ — препарат из живой культуры микобактерий, поэтому избежать поствакцинальных осложнений полностью не удаётся. Осложнения при вакцинации БЦЖ известны давно и сопровождают её с начала массового применения вакцины[60].
Среди побочных действий вакцины БЦЖ выделяют лёгкие, наблюдающиеся практически у всех пациентов: папула (проходит за 2—4 недели), лёгкие изъязвления (длятся 1—2 месяца) и шрам (заживает 2—5 месяцев)[61].
Более тяжёлые, уже считающиеся осложнениями, побочные действия делятся на локальные (длятся до 6 месяцев) и систематические[61].
Побочные действия вакцинирования БЦЖ зависят от штамма, количества микробных тел в дозе и от соблюдения техники введения вакцины. Последнее критически важно: когда из-за нарушения техники введения вакцина вводится не внутрикожно, а подкожно, возникает специфическое осложнение «холодный абсцесс»[60]. В случае, если холодный абсцесс не был обнаружен своевременно, возможно его самопроизвольное вскрытие с образованием язвы[62]. Холодный абсцесс не представляет опасности для здоровья ребёнка, но вызывает тревогу у родителей[60].
Холодный абсцесс — это наиболее частое осложнение. При этом все (суммарно) локальные осложнения возникают по всему миру в 1 случае из диапазона от тысячи до 10 тысяч доз вакцины[61].
Наиболее тяжёлое осложнение — генерализованная БЦЖ-инфекция — возникает в России с частотой 1,56—4,29 на 1 млн доз, а у ВИЧ-инфицированных его частота составляет 1 %, поэтому некоторые специалисты не рекомендуют вакцинировать БЦЖ детей, рождённых у матерей с неизвестным ВИЧ-статусом до проверки ВИЧ-статуса младенца[60]. В целом по миру генерализованная БЦЖ-инфекция встречается реже — 1 случай на 230—640 тыс. доз, из них случаев БЦЖ-инфекции у иммунодефицитных пациентов (как ВИЧ, так и с другими иммунодефицитами) встречается один случай на 640 000 доз вакцины[61]. Несмотря на риск, в странах с высоким бременем туберкулёза (Россия к ним относится) ВОЗ рекомендует вакцинировать детей от матерей с неизвестным статусом ВИЧ, поскольку риск туберкулёза при отсутствии вакцинации перевешивает риск развития генерализованной БЦЖ-инфекции[61][23].
В случае отложенной прививки после отрицательного результата пробы Манту можно попасть в «ложноотрицательное окно», когда организм уже инфицирован, но проба ещё не даёт реакцию, сделать прививку БЦЖ и тем самым спровоцировать заболевание[63].
В России распространён миф о том, что якобы БЦЖ сама вызывает туберкулёз. Это не соответствует действительности. БЦЖ действительно несовершенна и не защищает от вторичных форм туберкулёза, а у детей с врождёнными дефектами иммунной системы может вызвать осложнения вплоть до смертельного исхода, но дети с такими тяжёлыми формами иммунной недостаточности не выживают и при отказе от вакцинации БЦЖ[64].
Антивакцинаторство против БЦЖ[править | править код]
Противники вакцинации распространяют дезинформацию о вакцине БЦЖ. В частности, они утверждают, что якобы БЦЖ вызывает туберкулёз и якобы во всех цивилизованных странах её отменили. В действительности вакцинация БЦЖ применяется во всех без исключения странах, но по-разному, в зависимости от эпидемиологической обстановки в каждой стране (среди населения России заболеваемость туберкулёзом — 100 случаев на 100 тыс. чел., в США — 4, в Канаде — 1). По состоянию на 2009 год в 150 странах вакцинация БЦЖ всеобщая неонатальная, в 30 из них также проводится ревакцинация; а ещё в 31 странах применяется избирательная вакцинация групп населения с повышенным риском инфицирования туберкулёзом. Также в странах с высокой заболеваемостью ревакцинируют детей старшего возраста с отрицательным туберкулиновым тестом. Чехия, Словакия и Иордания после официальной отмены всеобщей вакцинации были вынуждены снова её ввести из-за увеличения заболеваемости туберкулёзом. В Норвегии была возобновлена вакцинация БЦЖ по запросам населения[45].
Влияние на другие инфекционные заболевания[править | править код]
Вакцинация БЦЖ, проведённая в первые дни после рождения, на протяжении неонатального периода защищает младенцев не только от туберкулёза, но и от других инфекционных заболеваний. В условиях высокой смертности приоритетное введение БЦЖ в первый день жизни может иметь значительные преимущества для общественного здравоохранения за счет снижения общей инфекционной заболеваемости и смертности, например, в Уганде[65].
Коронавирусная инфекция COVID-19[править | править код]
Есть наблюдение, что в странах и регионах, где проводилась массовая вакцинация БЦЖ, заболевших выявляется меньше. Авторы исследования отмечают, что это предварительное исследование, и что замеченная корреляция может быть вызвана неучтёнными факторами, а также может быть ошибочной, например, из-за недостоверности исходных данных, вызванных ограниченным тестированием и публикацией неполных статистических данных в рассмотренных странах[20]. Это исследование вызвало оптимистичные заявления некоторых эпидемиологов[21], которые породили критику: учёные поясняют, что корреляция ещё не означает причинно-следственную связь, исходное исследование имеет недостатки дизайна и делать какие-то выводы не только рано, но опасно[22]. В эпидемиологических исследованиях на основе статистических данных предварительно показано, что смертность от COVID-19 в странах, где применяется вакцинация БЦЖ, существенно ниже, чем в странах, где её не применяют. Одни исследователи сообщают про разницу в 5,8 раз[66], другие — более, чем в 9 раз (4,28 против 40 смертей на миллион жителей). Эти исследования предварительные, предпринимаются попытки начать достоверное исследование по критериям доказательной медицины[67]. Одно исследование показало схожее соотношение положительных тестов на SARS-CoV-2 среди вакцинированных и невакцинированных в детском возрасте взрослых людей, что говорит не в пользу гипотезы о возможном защитном эффекте против COVID-19 прививки, сделанной в детском возрасте[68].
В 2020 году начались клинические испытания, призванные выявить профилактический эффект вакцины БЦЖ против COVID-19[69]: в мае 2020 года — на людях работоспособного возраста в США с плановым сроком завершения в ноябре 2021 года, у медицинских работников в Австралии[70] и Нидерландах[71], плановые сроки их завершения — март 2022[70] и октябрь 2020[71], соответственно.
См. также[править | править код]
- ГамТБвак
- Туберкулиновая проба
- Квантеферон
- Первичный туберкулёзный комплекс
- Всемирная организация здравоохранения
Примечания[править | править код]
- ↑ Прививка от Лиги наций Архивная копия от 27 декабря 2021 на Wayback Machine 2017
- ↑ 1 2 WHO position paper – February 2018, p. 84.
- ↑ Позиция ВОЗ – Май 2008, с. 8.
- ↑ 1 2 WHO position paper – February 2018, p. 83.
- ↑ Позиция ВОЗ – Май 2008, с. 2.
- ↑ Позиция ВОЗ – Май 2008, с. 9.
- ↑ 1 2 Information Sheet — WHO, p. 1.
- ↑ Белозёрова, 1:04:59.
- ↑ Вакцина туберкулезная для щадящей первичной иммунизации (БЦЖ-М) (Vaccinum tuberculosis (BCG-M) cryodesiccatum), инструкция, лиофилизат для приготовления суспензии для... Дата обращения: 3 ноября 2021. Архивировано 4 апреля 2016 года.
- ↑ Вакцина туберкулезная (БЦЖ) (Vaccinum tuberculosis (BCG)), инструкция, лиофилизат для приготовления суспензии для внутрикожного введения, 0.05 мг/доза — Энциклопедия лекарств РЛС. Дата обращения: 3 ноября 2021. Архивировано 20 июля 2021 года.
- ↑ Фтизиатрия: национальное руководство, 2007, с. 478−479.
- ↑ Белозёрова, 1:05:35−1:05:45.
- ↑ Оттен Т. Ф., Васильев А. В. Микобактериоз. — СПб.: Медицинская пресса, 2005. — С. 134.
- ↑ Romanus V. Atypical mycobacteria in extrapulmonary disease among children. Incidence in Sweden from 1969 to 1990, related to changing BCG-vaccination coverage : [англ.] / Romanus V., Hallander H. O., Olinder-Nielsen A. M. … [et al.] // Tuberculosis and Lung Disease. — 1995. — Vol. 76, no. 4 (August). — С. 300−310. — ISSN 1027-3719. — PMID 7579311.
- ↑ Fine, P. E. M. Issues relating to the use of BCG in immunisation programmes : [англ.] / P. E. M. Fine, I. A. M. Carneiro, J. B. Milstein … [et al.]. — Geneva : WHO, 1999.
- ↑ Rosenthal, S. R. BCG vaccination against tuberculosis : [англ.]. — Boston : Little, Brown & Co., 1957.
- ↑ Новая вакцина от туберкулёза впервые прошла клинические испытания. РИА Новости (19 февраля 2018). Дата обращения: 13 июля 2018. Архивировано 13 июля 2018 года.
- ↑ Светлана Маслова. Вторая фаза клинических исследований доказывает эффективность новой вакцины, а также пользу существующий вакцины БЦЖ против туберкулёза. Хайтек+ (12 июля 2018). Дата обращения: 13 июля 2018. Архивировано 13 июля 2018 года.
- ↑ Elisa Nemes. Prevention of M. tuberculosis Infection with H4:IC31 Vaccine or BCG Revaccination : [англ.] / Elisa Nemes, Hennie Geldenhuys, Virginie Rozot … [et al.] // New England Journal of Medicine. — 2018. — No. 379 (12 July). — P. 138−149. — doi:10.1056/NEJMoa1714021. — PMID 29996082. — PMC 5937161.
- ↑ 1 2 Aaron Miller, Mac Josh Reandelar, Kimberly Fasciglione, Violeta Roumenova, Yan Li, Gonzalo H Otazu. Correlation between universal BCG vaccination policy and reduced morbidity and mortality for COVID-19: an epidemiological study (англ.) // medRxiv. — 2020-03-28. — P. 2020.03.24.20042937. — doi:10.1101/2020.03.24.20042937. Архивировано 30 января 2021 года.
- ↑ 1 2 3 Sruthijith, K. K. BCG vaccination policies make a ten times difference in Covid-19 incidence, mortality : New study : [англ.] // Economic Times. — 2020. — 3 April.
Sruthijith, K. K. BCG vaccination policies make a ten times difference in Covid-19 incidence, mortality : New study : [англ.] // Uro Today. — 2020. — 6 April. - ↑ 1 2 Emily MacLean. Universal BCG vaccination and protection against COVID-19: critique of an ecological study (англ.). Nature Research Microbiology Community (1 апреля 2020). Дата обращения: 2 апреля 2020. Архивировано 7 апреля 2020 года.
- ↑ 1 2 WHO position paper – February 2018.
- ↑ Белозёрова, 01:14:49−01:15:05.
- ↑ 1 2 Позиция ВОЗ – Май 2008, с. 2,93—95.
- ↑ 1 2 БЦЖ: Инструкция по применению.
- ↑ 1 2 БЦЖ-М: Инструкция по применению.
- ↑ Белозёрова, 01:14:09−01:14:19.
- ↑ 1 2 Белозёрова, 01:09:31−01:10:27.
- ↑ Белозёрова, 01:07:24−01:07:57.
- ↑ Белозёрова, 01:07:58−01:08:57.
- ↑ P. E. M. Fine PhD, Prof. Variation in protection by BCG: implications of and for heterologous immunity (англ.) // The LANCET : journal. — 1995. — Vol. 346. — P. 1339—1345.
- ↑ Colditz G. A., Brewer T. F., Berkey C. S., et al. Efficacy of BCG Vaccine in the Prevention of Tuberculosis (англ.) // JAMA : journal. — 1994. — Vol. 271. — P. 698—702.
- ↑ Hart P. D., Sutherland I. BCG and vole bacillus vaccines in the prevention of tuberculosis in adolescence and early adult life. Final Report of the Medical Research Council (англ.) // Brit Med J : journal. — 1977. — Vol. 2. — P. 293—295.
- ↑ Comstock G. W., Palmer C. E. Long-term results of BCG in the southern United States (англ.) // Am Rev Resp Dis : journal. — 1966. — Vol. 93, no. 2. — P. 171—183.
- ↑ Fifteen year follow up of trial of BCG vaccines in south India for tuberculosis prevention. Tuberculosis Research Centre (ICMR), Chennai. — PubMed — NCBI. Дата обращения: 29 апреля 2017. Архивировано 23 января 2019 года.
- ↑ Indian Council of Medical Research in collaboration with WHO. Trial of BCG vaccines in South India for tuberculosis prevention // Indian J Med Res. — 1979. — № 70. — С. 349—363.
- ↑ Editorial. BCG: Bad news from India (англ.) // The Lancet : журнал. — Elsevier, 1980. — No. January 12. — P. 73—74.
- ↑ Aronson N. E., Santosham M., Comstock G. W., et al. Long-term efficacy of BCG vaccine in American Indians and Alaska Natives: A 60-year follow-up study (англ.) // JAMA : journal. — 2004. — Vol. 291, no. 17. — P. 2086—2091.
- ↑ Rodrigues L. C., Diwan V. K., Wheeler J. G. Protective Effect of BCG against Tuberculous Meningitis and Miliary Tuberculosis: A Meta-Analysis (англ.) // Int J Epidemiol : journal. — 1993. — Vol. 22. — P. 1154—1158.
- ↑ Brosch R., Gordon S.V., Garnier T., Eiglmeier K., et al. Genome plasticity of BCG and impact on vaccine efficacy (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2007. — doi:10.1073/pnas.0700869104.
- ↑ Packe G. E., Innes J. A. Protective effect of BCG vaccination in infant Asians: a case-control study (англ.) // Arch Dis Child : journal. — 1988. — Vol. 63. — P. 277—281.
- ↑ Palmer C. E., Long M. W. Effects of infection with atypical mycobacteria on BCG vaccination and tuberculosis (англ.) // Am Rev Respir Dis : journal. — 1966. — P. 553—568.
- ↑ Rook G. A. W., Dheda K., Zumla A. Do successful tuberculosis vaccines need to be immunoregulatory rather than merely Th1-boosting? (англ.) // Vaccine : journal. — Elsevier, 2005. — Vol. 23, no. 17—18. — P. 2115—2120. — doi:10.1016/j.vaccine.2005.01.069.
- ↑ 1 2 Мац, Александр Наумович. Врачам об антипрививочном движении и его вымыслах в СМИ // Педиатрическая фармакология : журн. — 2009. — Т. 6, № 6. — С. 12—35.
- ↑ Tuberculosis. The disease, its treatment and prevention (англ.) (pdf). NHS (2018). Дата обращения: 19 января 2019. Архивировано 19 января 2019 года. Overview. Tuberculosis (TB) (англ.). NHS. Дата обращения: 19 января 2019. Архивировано 19 января 2019 года.
- ↑ Mahler H. T., Mohamed Ali P. Review of mass B.C.G. project in India // Indian Journal of Tuberculosis. — 1955. — Т. 2, № 3. — С. 108—116. Архивировано 13 февраля 2007 года.
- ↑ Weekly Epidem. Rec. Архивная копия от 18 декабря 2020 на Wayback Machine, 1980, Jan 4, No.1, P. 1—3.
- ↑ ten Dam H. G., Hitze K. L. Does BCG vaccination protect the newborn and young infants? (англ.) // Bull World Health Organ.. — 1980. — Vol. 58, iss. 1. — P. 37—41. — PMID 6991146.
- ↑ Mitteilung der Ständigen Impfkommission (STIKO) am Robert Koch-Institut / Stand: März 1998 : [нем.] // Epidemiologisches Bulletin. — Berlin : Robert Koch–Institut Bundesinstitut für Infektionskrankheiten und nicht übertragbare Krankheiten, 1998. — № 15 (17 April). — S. 109, 114. — ISSN 1430–0265.
- ↑ Tuberkulose-Impfung in Deutschland? Welche Möglichkeiten gibt es, wenn die Impfung für einen Auslandsaufenthalt gefordert wird? (нем.). Robert Koch Institut (3 января 2018). — FAQ о прививке против туберкулёза в Германии. Как сделать прививку для поездки за границу? Дата обращения: 19 января 2019. Архивировано 17 января 2021 года.
- ↑ 1 2 3 4 Infuso, A. Table 1. — In: European survey of BCG vaccination policies and surveillance in children, 2005 : [англ.] / A. Infuso, D. Falzon // Eurosurveillance : J.. — 2006. — Vol. 604, no. 11. — ISSN 1560-7917. — doi:10.2807/esm.11.03.00604-en.
- ↑ Setia MS. The role of BCG in prevention of leprosy : A meta-analysis / Setia MS, Steinmaus C, Ho CS … [и др.] // The Lancet. Infectional Diseases. — Vol. 6, no. 3. — P. 162–70. — doi:10.1016/S1473-3099(06)70412-1. — PMID 16500597.
- ↑ Audrey Tanghe. Protective efficacy of a DNA vaccine encoding antigen 85A from Mycobacterium bovis BCG against Buruli ulcer : [арх. 20 января 2019] / Audrey Tanghe, Jean Content, Jean-Paul Van Vooren … [и др.] // Infection and Immunity. — 2001. — Vol. 69, no. 9 (сентябрь). — P. 5403–11. — doi:10.1128/IAI.69.9.5403-5411.2001. — PMID 11500410. — PMC 98650.
- ↑ Richard Odame Phillips. Effectiveness of Routine BCG Vaccination on Buruli Ulcer Disease : A Case-Control Study in the Democratic Republic of Congo, Ghana and Togo : [англ.] : [арх. 21 февраля 2022] / Richard Odame Phillips, Delphin Mavinga Phanzu, Marcus Beissner … [et al.] // PLoS Neglected Tropical Diseases : J.. — 2015. — Vol. 9, no. 1 (8 January). — doi:10.1371/journal.pntd.0003457. — PMID 25569674. — PMC 4287572.
- ↑ Steg A. Systemic bacillus Calmette-Guerin infection in patients treated by intravesical BCG therapy for superficial bladder cancer : [англ.] / Steg A, Leleu C, Debré B … [et al.] // Progress in clinical and biological research : J.. — 1989. — Vol. 310. — P. 325−34. — PMID 2672020.
- ↑ Lamm DL. A randomized trial of intravesical doxorubicin and immunotherapy with bacille Calmette-Guerin for transitional-cell carcinoma of the bladder : [англ.] / Lamm DL, Blumenstein BA, Crawford ED // New England Journal of Medicine. — 1991. — Vol. 325, no. 17 (24 October). — P. 1205–9. — doi:10.1056/NEJM199110243251703. — PMID 1922207.
- ↑ Frank Liaw. Systemic BCG‐osis following intravesical BCG instillation for bladder carcinoma : [англ.] : pdf / Frank Liaw, Yan Yu Tan, David Hendry // Clinical Case Reports : J.. — 2017. — Vol. 5, no. 10 (October). — P. 1569−1572. — doi:10.1002/ccr3.1129. — PMID 29026546. — PMC 5628231.
- ↑ Mosolits S. Towards therapeutic vaccines for colorectal carcinoma : a review of clinical trials : [англ.] / Mosolits S, Nilsson B, Mellstedt H. // Expert Review of Vaccines. — 2005. — Vol. 4, no. 3 (June). — P. 329–50. — doi:10.1586/14760584.4.3.329. — PMID 16026248.
- ↑ 1 2 3 4 Белозёрова, 01:06:29−01:07:24.
- ↑ 1 2 3 4 5 WHO. WHO Information Sheet. Observed rate of vaccine reactions Bacille Calmette Guerin (BCG) Vaccine. WHO (апрель 2012). Дата обращения: 7 апреля 2017. Архивировано 24 июля 2017 года.
- ↑ Перельман, 2007.
- ↑ Белозёрова, 01:16:05−01:16:20.
- ↑ Факты и мифы. Вакцинация: мифы и реальность. Специалисты о прививках. Национальная ассоциация специалистов по контролю инфекций, связанных с оказанием медицинской помощи (НАСКИ). — «Миф 11. Вакцина БЦЖ не только не защищает от туберкулёза, но и сама его вызывает и способствует нарастанию заболеваемости, поэтому БЦЖ-вакцинацию отменили во всех цивилизованных странах. Факты. Эта дезинформация весьма популярна в России в связи с довольно высокой заболеваемостью туберкулёзом лёгких.» Дата обращения: 31 декабря 2018. Архивировано 3 января 2019 года.
- ↑ Prentice, S. BCG-induced non-specific effects on heterologous infectious disease in Ugandan neonates : an investigator-blind randomised controlled trial : [англ.] / S. Prentice, B. Nassanga, E. L. Webb … [et al.] // The Lancet : журн. — 2021. — doi:10.1016/S1473-3099(20)30653-8.
- ↑ Differential COVID-19-attributable mortality and BCG vaccine use in countries Архивная копия от 15 апреля 2020 на Wayback Machine — [Препринт, рецензирование не пройдено, достоверность низкая.]
- ↑ DOI: 10.13140/RG.2.2.35948.10880 — [Препринт, рецензирование не пройдено, достоверность низкая.]
- ↑ Uri Hamiel, Eran Kozer, Ilan Youngster. SARS-CoV-2 Rates in BCG-Vaccinated and Unvaccinated Young Adults (англ.) // JAMA. — 2020. — 13 May. — doi:10.1001/jama.2020.8189. Архивировано 12 ноября 2020 года.
- ↑ Clinical trials of BCG for Covid19. Clinical Trials. US National Institute of Health. Дата обращения: 31 марта 2020. Архивировано 10 апреля 2020 года.
- ↑ 1 2 BCG Vaccination to Protect Healthcare Workers Against COVID-19 (BRACE). Clinical Trials. US National Institute of Health. Дата обращения: 14 апреля 2020. Архивировано 11 апреля 2020 года.
- ↑ 1 2 Reducing Health Care Workers Absenteeism in Covid-19 Pandemic Through BCG Vaccine (BCG-CORONA). Clinical Trials. US National Institute of Health. Дата обращения: 14 апреля 2020. Архивировано 12 апреля 2020 года.
Литература[править | править код]
- Фтизиатрия : национальное руководство : Подготовлено под эгидой Российского общества фтизиатров и Ассоциации медицинских обществ по качеству / Под ред. М. И. Перельмана. — М. : ГЭОТАР-Медиа, 2007. — Глава 30: Патогенетическая терапия: БЦЖ-терапия. Глава 32: Специфическая профилактика. — С. 461, 478−485. — 512 с. — (Национальные руководства). — 2000 экз. — ББК 55.4. — УДК 616-0015(G). — ISBN 978-5-9704-0497-3.
- Вакцина БЦЖ. Документ по позиции ВОЗ (pdf). ВОЗ. ВОЗ (8 мая 2008). Дата обращения: 20 декабря 2018.
- BCG vaccines. // WHO position paper – February 2018 (англ.) (pdf). WHO. ВОЗ. — Вакцина БЦЖ. Документ по позиции Всемирной организации здравоохранения. Февраль 2018. Дата обращения: 20 декабря 2018.
- ВОЗ. Information Sheet Observed Rate of Vaccine Reactions Bacille Calmette–Guerin (BCG) Vaccine (англ.) (pdf). Сайт Всемирной Организации Здравоохранения (апрель 2012). — [Информационный листок ВОЗ о наблюдаемой частоте реакций на вакцину БЦЖ]. Дата обращения: 23 декабря 2018.
- Министерство здравоохранения Российской Федерации. Вакцина туберкулёзная БЦЖ живая. Фармакопейная статья (doc). Министерство здравоохранения Российской Федерации. — ФС.3.3.1.0018.15. Дата обращения: 20 декабря 2018.
- Перельман, М. И. Фтизиатрия. — М. : ГЭОТАР-Медиа, 2007. — Гл. 32. — (Консультант врача). — ISBN 978-5-9704-1234-3.
- Чистович, А. Н. Патологическая анатомия и патогенез туберкулёза. — 2-е изд. — М. : Медицина, 1973. — С. 18−20. — 175 с.
Ссылки[править | править код]
- Белозёрова Анна Сергеевна, фтизиатр, рентгенолог. Туберкулёз — просто и понятно на YouTube — Клиника «Рассвет», 2018.
- Immunization, Vaccines and Biologicals. BCG position paper (англ.). WHO. ВОЗ. — Документы о позиции Всемирной организации здравоохранения по вакцине БЦЖ. Дата обращения: 20 декабря 2018.
- CDC. Fact Sheets. BCG Vaccine (англ.). Centers for Disease Control and Prevention. U. S. Department of Health & Human Services (4 мая 2016). — [Лист «Факты о вакцине БЦЖ», опубликованный Центрами по контролю и профилактике заболеваний США]. Дата обращения: 23 декабря 2018.
- Вакцина туберкулёзная БЦЖ. Инструкция по медицинскому применению. Микроген. АО «НПО „Микроген“». Дата обращения: 29 декабря 2018.
- Вакцина туберкулёзная для щадящей первичной иммунизации БЦЖ-М. Инструкция по медицинскому применению. Микроген. АО «НПО „Микроген“». Дата обращения: 29 декабря 2018.