Вирус иммунодефицита человека
| Вирус иммунодефицита человека | ||||||
|---|---|---|---|---|---|---|
![Стилизованное изображение сечения ВИЧ[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ea/Human_Immunodeficency_Virus_-_stylized_rendering.jpg/275px-Human_Immunodeficency_Virus_-_stylized_rendering.jpg) Стилизованное изображение сечения ВИЧ[1] | ||||||
| Научная классификация | ||||||
|
Реалм: Царство: Pararnavirae Тип: Artverviricota Класс: Порядок: Семейство: Подсемейство: Род: Группа: Primate lentivirus group |
||||||
| Международное научное название | ||||||
| Primate lentivirus group | ||||||
| Виды | ||||||
|
||||||
| Группа по Балтимору | ||||||
| VI: оцРНК-ОТ-вирусы | ||||||
| ||||||
Ви́рус иммунодефици́та челове́ка (ВИЧ) — ретровирус из рода лентивирусов, вызывающий медленно прогрессирующее[3] заболевание — ВИЧ-инфекцию[4][5].
Вирус поражает клетки иммунной системы, имеющие на своей поверхности рецепторы CD4: Т-хелперы, моноциты, макрофаги, клетки Лангерганса[6], дендритные клетки, клетки микроглии[7]. В результате работа иммунной системы угнетается и развивается синдром приобретённого иммунного дефицита (СПИД), организм больного теряет возможность защищаться от инфекций и опухолей, возникают вторичные оппортунистические заболевания, которые не характерны для людей с нормальным иммунным статусом[8][9][10][11][12][13].
Лечение ВИЧ-инфекции заключается в приёме антиретровирусной терапии, которая позволяет ВИЧ-положительным людям вести нормальный образ жизни, а её качество и продолжительность может не отличаться при должной терапии от таковых у ВИЧ-отрицательных людей[14][15]. При приёме указанной терапии человек достигает неопределяемой вирусной нагрузки, вследствие чего не способен передать инфекцию другим людям, в том числе при незащищённом половом акте[16][17][18][19], также терапия позволяет ВИЧ-положительным родителям естественным путём зачать и родить здорового ребёнка[20]. В отсутствие приёма терапии прогрессирующая ВИЧ-инфекция способна привести к оппортунистическим заболеваниям.
Открытие ВИЧ[править | править код]


В 1981 году появились первые три научные статьи о необычных случаях развития пневмоцистной пневмонии и саркомы Капоши у гомосексуальных мужчин[23][24]. До этого оба заболевания встречались редко и были характерны для совершенно разных групп пациентов: саркомой Капоши в основном болели пожилые мужчины средиземноморского происхождения, а пневмоцистной пневмонией — пациенты с лейкозом после интенсивной химиотерапии. Появление этих заболеваний, свидетельствующих о тяжёлом иммунодефицитном состоянии, у молодых людей, не входящих в соответствующие группы риска, наблюдалось впервые[24]. Затем обнаружили такие же симптомы среди наркопотребителей, больных гемофилией A[25], и гаитян[26][27]. Наиболее значимым было обнаружение снижения соотношения CD4+/CD8+-клеток в результате относительного и/или абсолютного уменьшения количества CD4+-лимфоцитов в сочетании с увеличением количества CD8+-лимфоцитов[24][28][29].
В июле 1982 года для обозначения этого состояния был предложен термин синдром приобретённого иммунного дефицита (СПИД, AIDS)[30]. В сентябре 1982 года СПИДу было дано полноценное определение как нозологической форме на основании наблюдения ряда оппортунистических инфекций у четырёх групп пациентов, указанных выше[24][31].
В период с 1981 по 1984 год вышло несколько работ, связывающих вероятность развития СПИДа с анальным сексом или с влиянием наркотиков[32][33][34][35][36][37]. Параллельно велись работы над гипотезой о возможной инфекционной природе СПИДа.
Вирус иммунодефицита человека был открыт в 1983 году в двух лабораториях, работавших независимо друг от друга: в Институте Пастера во Франции под руководством Люка Монтанье и в Национальном институте рака в США под руководством Роберта Галло. Результаты исследований, в которых из тканей пациентов с симптомами СПИДа впервые удалось выделить новый ретровирус, были опубликованы 20 мая 1983 года в журнале Science[38][39]. В этих же работах выделенный из больных СПИДом вирус был впервые успешно размножен в культивируемых Т-лимфоцитах. Французская группа исследователей показала, что серологически этот вирус отличается от HTLV-I, и назвала его LAV («вирус, ассоциированный с лимфаденопатией»), а американская группа назвала его HTLV-III, ошибочно отнеся к группе HTLV-вирусов. Исследователи выдвинули предположение, что вирус может вызывать синдром приобретённого иммунного дефицита[24].
В 1986 году было доказано, что вирусы, открытые в 1983 французскими и американскими исследователями, генетически идентичны. Первоначальные названия вирусов были упразднены и предложено одно общее название — вирус иммунодефицита человека[40]. В 2008 году Люк Монтанье и Франсуаза Барр-Синусси были удостоены Нобелевской премии в области физиологии или медицины «за открытие вируса иммунодефицита человека»[41].
ВИЧ-инфекция[править | править код]
Инфицирование[править | править код]
Вирус может передаваться через прямой контакт повреждённой или неповреждённой слизистой оболочки или повреждённой кожи здорового человека с биологическими жидкостями заражённого человека: кровью, предсеменной жидкостью (выделяющейся на протяжении всего полового акта), спермой, секретом влагалища, грудным молоком. Передача вируса может происходить при незащищённом анальном, вагинальном или оральном сексе[42][43].
Интактная, неповреждённая кожа является эффективным барьером для инфекции, так как в коже отсутствуют клетки, которые могут быть заражены ВИЧ. Для успешной инфекции требуется прямой контакт с кровеносной системой или с мембранами клеток слизистых оболочек. Слизистые оболочки половых органов и прямой кишки часто получают незначительные повреждения при половом акте, через которые вирус может проникать в кровь. Такие повреждения чаще возникают при наличии заболеваний, передающихся половым путём, например, в случае герпеса. Поэтому особенно опасной формой полового акта для принимающего партнёра является незащищённый анальный секс, так как при этой форме возникает наибольшее число мелких и крупных повреждений[44][45]. С другой стороны, заражение возможно и в случае неповреждённой слизистой оболочки, так как слизистая содержит значительное количество дендритных клеток (в том числе, клеток Лангерганса), которые могут играть роль «переносчиков» вирусных частиц в лимфатические узлы.
Передача вируса происходит с большей вероятностью при использовании заражённых игл и шприцев (особенно потребителями инъекционных наркотиков), а также при переливании крови (в случае нарушения медицинским персоналом установленных процедур проверки донорской крови)[46]. Также передача вируса может произойти между матерью и ребёнком во время беременности, родов (заражение через кровь матери)[47][48] и при грудном вскармливании (причём как от заражённой матери к здоровому ребёнку через грудное молоко, так и от заражённого ребёнка к здоровой матери через покусывание груди во время кормления)[49].
Вирус не передаётся воздушно-капельным путём, бытовым путём, при соприкосновении с неповреждённой кожей, через укусы большинства кровососущих насекомых[50] (исключение составляют мухи-жигалки)[нет в источнике (обс.)], слёзы[51] и слюну (из-за того, что концентрация вирионов ВИЧ в этих жидкостях ниже инфицирующей дозы, а также из-за того, что слюна — агрессивная среда, разрушающая своими ферментами вирионы ВИЧ)[51].
Вирус не стоек во внешней среде, быстро погибает под прямыми солнечными лучами; при температуре выше 57⁰C, и практически моментально при 100⁰C; также вирус очень чувствителен к кислотности (он может выжить только при pH от 7 до 8), щелочным и солёным средам[52].
Болезнь[править | править код]

В течение болезни выделяют три стадии: острую инфекцию, латентный период и терминальную стадию (СПИД) (см. иллюстрацию). В ходе развития ВИЧ-инфекции у одного и того же человека в результате мутаций возникают новые штаммы вируса, которые различаются по скорости воспроизведения и способности инфицировать[8][9]. Размножившись, вирусные частицы высвобождаются из поражённых клеток и внедряются в новые — цикл развития повторяется. Инфицированные вирусом Т-хелперы постепенно гибнут из-за разрушения вирусом, апоптоза или уничтожения Т-киллерами. В процессе развития ВИЧ-инфекции количество CD3-CD4 лимфоцитов снижается настолько, что организм уже не может противостоять возбудителям оппортунистических инфекций, которые неопасны или мало опасны для здоровых людей с нормально функционирующей иммунной системой. Причины снижения могут быть различными:
1 — перераспределение пролимфоцитов в сторону CD3-CD8 или естественных киллеров, вызываемое, например, герпесом 4го типа
2 — комплиментарность gp120 и рецептора CD4 — вызывает аутоимунную реакцию, выработку антител, разрушающих CD3-CD4 лимфоцит (наличие данного белка необходимо определять с учётом погрешности тест систем)
3 — сопутствующими заболеваниями, угнетающими костный мозг или органы кроветворения (тимус, лимфатическую систему).
Согласно сведениям об исследованиях данной проблемы, только около 4 % CD3-CD4 лимфоцитов поражается вирусом.
Причем необходимо понимать, что CD3-CD4 и CD3-CD8 лимфоциты это постоянно вырабатываемые организмом клетки из пролимфоцитов, организм сам регулирует какой пролимфоцит станет CD4, CD8 или естественным киллером.
На терминальной стадии (СПИД) ослабленный организм поражают бактериальные, грибковые, вирусные и протозойные инфекции, а также опухоли[11][12][13]. В отсутствие антиретровирусной терапии смерть пациента наступает не в результате размножения вируса в CD4+-клетках, а по причине развития оппортунистических заболеваний (вторичных по отношению к ВИЧ-инфекции).
Эпидемиология[править | править код]
По данным на 2011 год, в мире за всё время ВИЧ-инфекцией заболели 60 миллионов человек, из них: 25 миллионов умерли, а 35 миллионов живут с ВИЧ-инфекцией[54]. Более двух третей из них проживают в Африке к югу от пустыни Сахара[55]. Эпидемия началась здесь в конце 1970-х — начале 1980-х. Затем эпидемия перекинулась в США, Западную Европу и страны Южной Африки. Сегодня, за исключением стран Африки, быстрее всего вирус распространяется в Центральной Азии и Восточной Европе (в том числе в России). Эпидемическая ситуация в этих регионах сдерживалась до конца 1990-х, затем с 1999 по 2002 годы количество инфицированных почти утроилось — в основном за счёт инъекционных наркоманов. Значительно ниже среднего ВИЧ-инфекция распространена в Восточной Азии, Северной Африке и на Ближнем Востоке. В масштабе планеты эпидемическая ситуация стабилизировалась, количество новых случаев ВИЧ-инфекции снизилось с 3,5 миллиона в 1997 году до 2,7 миллиона в 2007 году[55]. По данным на конец 2016 года, в России 848 тысяч человек живут с ВИЧ-инфекцией, за период с 1986 по 2016 год умерло от разных причин 220 тысяч ВИЧ-инфицированных граждан России[56] (подробнее см. Статистика заболеваемости и смертности по России).
Диагностика[править | править код]
Анализ крови позволяет обнаружить антитела к белкам вируса (ИФА), реакцию антител на белки вируса (вестерн-блот), РНК вируса (ОТ-ПЦР)[57]. Определение вирусной нагрузки (подсчёт количества копий РНК вируса в миллилитре плазмы крови) позволяет судить о стадии заболевания и эффективности лечения[58][59].
Обязательная проверка донорской крови в развитых странах в значительной степени сократила возможность передачи вируса при её использовании. Тестирование на ВИЧ беременных женщин позволяет своевременно начать приём лекарств и родить здорового ребёнка.
Существует мнение, что принудительное тестирование населения бесперспективно с точки зрения сдерживания эпидемии[60] и нарушает права человека[61]. В России проведение теста без согласия человека является незаконным[62], однако существуют ситуации, в которых предоставление результатов тестирования на ВИЧ является обязательным, но не насильственным (донорство, трудоустройство медицинских работников, для иностранных граждан, получающих разрешение на пребывание в РФ, в местах лишения свободы при наличии клинических показаний)[63].
Лечение[править | править код]
На 2022 год известно о четырёх случаях излечения от вируса. Три из них в медицинской литературе фигурируют под прозвищами «Берлинский», «Лондонский» и «Сан-Паулский» пациенты, эффект в их случаях был достигнут при помощи пересадки костного мозга (донорские клетки содержали мутацию CCR5-Δ32, делающую их невосприимчивыми к ВИЧ)[64][65][66]. В начале 2022 года стало известно[67] о четвёртом человеке, который излечился от ВИЧ, на этот раз с помощью трансплантации клеток пуповинной крови, содержащих мутацию CCR5-Δ32[67]. В марте 2023 года в журнале Cell вышла статья, описывающая данный случай[68].
Из 35 миллионов человек, живущих с ВИЧ-инфекцией, часть остаётся в живых благодаря антиретровирусной терапии. В случае отсутствия антиретровирусной терапии ВИЧ-инфекции, смерть наступает в среднем через 9—11 лет после заражения[8][10]. При проведении антиретровирусной терапии продолжительность жизни пациента составляет 70—80 лет[69][70][71]. Антиретровирусные препараты мешают ВИЧ размножаться в клетках иммунной системы человека, блокируя внедрение вирионов в клетки и нарушая на разных этапах процесс сборки новых вирионов. Своевременно начатое лечение антиретровирусными препаратами в сотни раз снижает риск развития СПИДа и последующей смерти[72][73][74]. Антиретровирусные препараты у части пациентов вызывают побочные эффекты, в некоторых случаях даже требующие сменить схему лечения (набор принимаемых лекарств).
Терапию назначают при снижении иммунитета и/или высокой вирусной нагрузке. Если число CD4+-лимфоцитов велико и вирусная нагрузка низкая, терапию не назначают. После назначения терапии лекарства нужно принимать ежедневно в одно и то же время и пожизненно, что создаёт неудобства для пациентов. Кроме того, следует учитывать высокую стоимость месячного курса лекарств. В 2014 году необходимые лекарства получали менее половины из 9,5 млн человек, нуждающихся в противовирусной терапии[75].
Также все беременные женщины с ВИЧ-инфекцией должны начинать незамедлительную АРВТ для предотвращения передачи ВИЧ плоду[76].
Согласно рекомендациям ВОЗ, АРВТ следует незамедлительно начинать всем ВИЧ-инфицированным детям до полутора лет[77]. Начало терапии у детей, получивших ВИЧ от матери, в течение 3 месяцев после родов снижает смертность на 75 %[78]. В отсутствие лечения треть ВИЧ-инфицированных детей умирает в течение первого года жизни и 50 % — в течение второго года. Если диагностика ВИЧ невозможна, лечение следует начинать в возрасте 9 месяцев, либо ранее, в случае появления симптомов[79].
По состоянию на февраль 2016 года было объявлено, что группе немецких учёных удалось полностью удалить тип ВИЧ-1 из живых клеток. Испытания проводились на клетках человека, вживлённых подопытным мышам. Испытания на людях должны проводиться в ближайшее время[80][81][82].
В 2018 году Администрацией по контролю над продуктами и лекарствами (FDA) был одобрен ибализумаб (ibalizumab-uiyk) для применения в терапии пациентов с мультирезистентным ВИЧ-1. Препарат представляет собой моноклональное антитело, которое связывается с CD4 рецепторами T-клеток и подавляет процесс проникновения вируса в клетку человека. Ибализумаб может применяться в терапии с другими антиретровирусными лекарствами. По результатам клинических исследований с участием 40 пациентов, ранее прошедших лечение более чем 10 различными антиретровирусными агентами, вирусная нагрузка снизилась у большинства испытуемых через одну неделю после введения первой дозы препарата. Через 24 недели терапии вирусологическая супрессия была достигнута у 43 % участников клинических испытаний[83].
ВИЧ в 2019 году вносили в список десяти основных проблем здравоохранения, которые требуют особого внимания ВОЗ[84].
Классификация[править | править код]
Вирус иммунодефицита человека относят к семейству ретровирусов (Retroviridae), роду лентивирусов (Lentivirus). Название Lentivirus происходит от латинского слова lente — медленный. Такое название отражает одну из особенностей вирусов этой группы, а именно — медленную и неодинаковую скорость развития инфекционного процесса в макроорганизме. Для лентивирусов также характерен длительный инкубационный период[85].
Для вируса иммунодефицита человека характерна высокая частота генетических изменений, возникающих в процессе самовоспроизведения. Частота возникновения ошибок у ВИЧ составляет 10−3 — 10−4 ошибок на геном на цикл репликации, что на несколько порядков больше аналогичной величины у эукариот. Размер генома ВИЧ составляет примерно 104 нуклеотидов. Из этого следует, что практически каждый дочерний геном хотя бы на один нуклеотид отличается от своего предшественника. В современной классификации различают два основных вида ВИЧ — ВИЧ-1 и ВИЧ-2. Предполагается, что эти вирусы возникли в результате независимой передачи людям SIV (вируса иммунодефицита обезьян) от шимпанзе и мангабеев соответственно[86].
И ВИЧ-1, и ВИЧ-2 способны вызывать серьёзный иммунодефицит, однако клиническое течение болезни несколько различается. Известно, что ВИЧ-2 менее патогенен и передаётся с меньшей вероятностью, чем ВИЧ-1. Вероятно, это связано с тем, что ВИЧ-2-инфекция характеризуется более низким числом вирусных частиц на миллилитр крови. Отмечено, что инфекция ВИЧ-2 обеспечивает носителю небольшую защиту от заражения ВИЧ-1. Однако описаны случаи двойной инфекции, причём заражение может происходить в любом порядке. Инфекция ВИЧ-2 реже заканчивается развитием СПИДа. Есть сведения о несколько большей частоте развития саркомы Капоши, кандидоза ротовой полости и хронической лихорадки при ВИЧ-1/СПИДе. При ВИЧ-2/СПИДе чаще развивается энцефалит, хроническая или бактериальная диарея, серьёзные цитомегаловирусные инфекции и холангит[86]. К роду Lentivirus также относят виды, вызывающие схожие заболевания у обезьян, кошек, лошадей, овец и т. д.[8][87][88]
ВИЧ-1[править | править код]
ВИЧ-1 описан в 1983 году и является наиболее распространённым и патогенным видом ВИЧ[89]. Глобальная эпидемия ВИЧ-инфекции главным образом обусловлена распространением ВИЧ-1. В подавляющем большинстве случаев, если не оговорено иначе, под ВИЧ подразумевают ВИЧ-1[90].
Вид ВИЧ-1 классифицируют на главную группу М и несколько побочных групп. Считается, что группы M, N, O, P образовались в результате независимых случаев передачи SIV от обезьяны к человеку, и последующей мутации вируса до ВИЧ[91].
- Вирусы группы М (англ. main — основная) являются причиной более 90 % случаев ВИЧ-инфекции. Группу М классифицируют на несколько клад, называемых подтипами, также обозначаемых буквами:
- подтип A широко распространён, например, в Западной Африке и России[92];
- подтип B доминирует в Европе, Северной Америке, Южной Америке, Японии, Таиланде, Австралии[93];
- подтип C преобладает в Южной и Восточной Африке, Индии, Непале, некоторых частях Китая[93];
- подтип D обнаружен только в Восточной и Центральной Африке[93];
- подтип E не был выявлен в нерекомбинантном виде, лишь совместно с подтипом А как CRF01_AE в Юго-Восточной Азии[93];
- подтип F выявлен в Центральной Африке, Южной Америке и Восточной Европе[94];
- подтип G и рекомбинантная форма CRF02_AG выявлены в Африке и Центральной Европе[94];
- подтип H обнаружен только в Центральной Африке[94];
- подтип I был предложен для описания штамма-продукта множественной рекомбинации CRF04_cpx нескольких подтипов[95];
- подтип J распространён в Северной, Центральной и Западной Африке и странах Карибского бассейна[96];
- подтип K обнаружен только в Конго и Камеруне[94].
- подтип L обнаружен в Конго[97].
- Группа O (англ. outlier — непохожий) обнаружена в Центральной Африке и Западной Африке. Наиболее распространена в Камеруне, где в 1997 году более 2 % пациентов были заражены вирусом группы О[98] (около 100 000 человек, по данным на 2013 год)[99]. Вирусы этой группы не определялись ранними версиями тест-систем на ВИЧ-1; современные тесты определяют вирусы и группы О, и группы N[100].
- Группа N (англ. non-M, non-O — ни M, ни O) обозначает штаммы не М и не О, описана в 1998 году и обнаружена только в Камеруне. С 2006 года выявлены лишь 10 заражений вирусами группы N[101].
- Группа P — в 2009 году была определена нуклеотидная последовательность РНК ВИЧ, значительно сходная с вирусом иммунодефицита обезьян, описанным у горилл (SIVgor), но не с SIV, характерным для шимпанзе (SIVcpz). Вирус был выделен из образцов, полученных от женщины камерунского происхождения, проживающей во Франции[102][103][104].
ВИЧ-2[править | править код]
ВИЧ-2 идентифицирован в 1986 году[105], генетически очень близок к T-лимфотропному вирусу SIV, и в меньшей степени к вирусу ВИЧ-1. Геномы ВИЧ-1 и ВИЧ-2 имеют гомологию консервативных генов gag и pol около 60 %, и до 45 % для генов белков оболочки[106]. По состоянию на 2010 год, описано 8 групп ВИЧ-2, лишь группы A и B являются эпидемическими. Вирусы группы А распространены в Западной Африке, Анголе, Мозамбик, Бразилии, Индии и мало распространены в США и Европе[107][108]. Вирусы группы В распространены в Западной Африке[109][110].
Строение вириона[править | править код]

Вирионы ВИЧ имеют вид сферических частиц, диаметр которых составляет около 100—120 нанометров[111]. Это приблизительно в 60 раз меньше диаметра эритроцита[112]. В состав зрелых вирионов входит несколько тысяч белковых молекул различных типов.
Капсид зрелого вириона, состоящий из примерно 2000 молекул белка р24, имеет форму усечённого конуса[113].
Внутри капсида находится белково-нуклеиновый комплекс: две нити вирусной РНК, прочно связанные с белком нуклеокапсида p7, ферменты (обратная транскриптаза, протеаза, интеграза)[113]. С капсидом также ассоциированы белки Nef и Vif (7—20 молекул Vif на вирион). Внутри вириона (и, вероятнее всего, за пределами капсида) обнаружен белок Vpr[42]:8-11. Кроме того, с капсидом ВИЧ-1 (но не ВИЧ-2) связаны около 200 копий клеточного фермента пептидилпролилизомеразы A[англ.] (циклофилин А), необходимого для сборки вириона[114].
Капсид окружён оболочкой, образованной примерно 2000 молекул матриксного белка p17[113]. Матриксная оболочка, в свою очередь, окружена двуслойной липидной мембраной, являющейся наружной оболочкой вируса. Она образована молекулами фосфолипидов, захваченными вирусом во время его отпочковывания от клетки, в которой он сформировался[115]. В липидную мембрану встроены 72 гликопротеиновых комплекса Env, каждый из которых образован тремя молекулами трансмембранного гликопротеина gp41 (TM), служащего «якорем» комплекса, и тремя молекулами поверхностного гликопротеина gp120 (SU)[114]. С помощью белка gp120 вирус присоединяется к рецептору CD4 и корецептору, находящимся на поверхности Т-лимфоцитов человека. Стехиометрическое соотношение p24:gp120 в вирионе составляет 60—100:1[42]:11. При формировании наружной оболочки вируса также происходит захват некоторого количества мембранных белков клетки, в том числе человеческих лейкоцитарных антигенов (HLA) классов I и II и молекул адгезии[113][116].
Белки вириона интенсивно изучаются, поскольку являются мишенями разрабатываемых лекарств и вакцины против ВИЧ.
Функции важных структурных белков ВИЧ-1[113][116]
| Сокращение | Описание | Функции |
|---|---|---|
| gp41 (TM, transmembrane) | Трансмембранный гликопротеин массой 41 кДа | Располагается во внешнем слое липидной мембраны, играет роль «якоря», удерживающего молекулы белка gp120 |
| gp120 (SU, surface) | Гликопротеин массой 120 кДа | Наружный белок вириона. Нековалентно связан с трансмембранным белком gp41. С одной молекулой gp41 связаны 3—5 молекул gp120. Способен связывать рецептор CD4. Играет важную роль в процессе проникновения вируса в клетку. |
| p24 (CA, capsid) | Белок массой 24 кДа | Образует капсид вируса |
| p17 (MA, matrix) | Матриксный белок массой 17 кДа | Около двух тысяч молекул этого белка образуют слой толщиной 5—7 нм, располагающийся между внешней оболочкой и капсидом вируса. |
| p7 (NC, nucleocapsid) | Нуклеокапсидный белок массой 7 кДа | Входит в состав капсида вируса. Образует комплекс с вирусной РНК. |
Геном и кодируемые белки[править | править код]
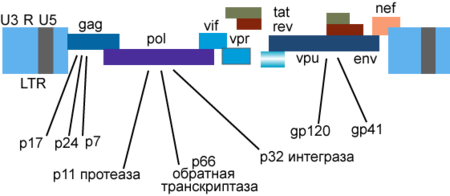
Генетический материал ВИЧ представлен двумя копиями положительно-смысловой (+)РНК[114]. Геном ВИЧ-1 имеет длину 9000 нуклеотидов. Концы генома представлены длинными концевыми повторами, которые управляют продукцией новых вирусов и могут активироваться и белками вируса, и белками инфицированной клетки.
9 генов ВИЧ-1 кодируют, по крайней мере, 15 белков[117]. Ген pol кодирует ферменты: обратную транскриптазу (RT), интегразу (IN) и протеазу (PR). Ген gag кодирует полипротеин Gag/p55, расщепляемый вирусной протеазой до структурных белков p6, p7, p17, p24. Ген env кодирует белок gp160, расщепляемый клеточной эндопротеазой фурином на структурные белки gp41 и gp120[42]:8-12. Другие шесть генов — tat, rev, nef, vif, vpr, vpu (vpx у ВИЧ-2) — кодируют белки, отвечающие за способность ВИЧ-1 инфицировать клетки и производить новые копии вируса. Репликация ВИЧ-1 in vitro возможна без генов nef, vif, vpr, vpu, однако их продукты необходимы для полноценной инфекции in vivo[118][119][120].
Gag[править | править код]
Полипротеин-предшественник Gag/p55 синтезируется с полноразмерной геномной РНК (которая в данном случае служит в качестве мРНК) в процессе стандартной кэп-зависимой трансляции, но возможна и IRES-зависимая трансляция. Предшественники функциональных белков располагаются в составе полипротеина Gag/p55 в следующем порядке: p17…p24…p2…p7…p1…p6[42]:8 (р1 и р2 — соединительные пептиды; другие продукты расщепления Gag/p55 описаны выше). Нерасщеплённый протеазой Gag/p55 содержит три основных домена: домен мембранной локализации (М, membrane targeting), домен взаимодействия (I, interaction) и «поздний» домен (L, late). Домен М, расположенный внутри области p17/МА, миристилируется (присоединяются остатки миристиновой кислоты) и направляет Gag/p55 к плазматической мембране. Домен I, находящийся внутри области p7NC (NC, nucleocapsid), отвечает за межмолекулярные взаимодействия отдельных мономеров Gag/p55. Домен L, также локализованный в области p7NC, опосредует отпочковывание вирионов от плазматической мембраны; в этом процессе участвует также р6 область полипротеина Gag/p55[42]:8[121].
Vpu[править | править код]
Двумя важными функциями белка Vpu являются: 1) разрушение клеточного рецептора CD4 в эндоплазматическом ретикулуме путём привлечения убиквитинлигазных комплексов и 2) стимуляция выделения дочерних вирионов из клетки путём инактивации интерферон-индуцируемого трансмембранного белка CD317/BST-2, получившего также название «tetherin» за его способность подавлять выделение вновь образовавшихся дочерних вирионов посредством их удержания на поверхности клетки[118][119][122][123][124][125].
Vpr[править | править код]
Белок Vpr необходим для репликации вируса в неделящихся клетках, в том числе макрофагах. Этот белок, наряду с другими клеточными и вирусными белками, активирует транскрипцию с использованием длинных концевых повторов генома ВИЧ в качестве промоторов. Белок Vpr играет важную роль в переносе вирусной ДНК в ядро и вызывает задержку деления клетки в периоде G2[126].
Vif[править | править код]
Белок Vif играет важную роль в поддержке репликации вируса. Vif индуцирует убиквитинилирование и деградацию клеточного антивирусного белка APOBEC3G, который вызывает деаминирование ДНК, приводящее к мутационным заменам G на A в вирусной ДНК, синтезируемой в ходе обратной транскрипции. Штаммы, лишённые Vif, не реплицируются в CD4+-лимфоцитах, некоторых линиях T-лимфоцитов и макрофагах. Эти штаммы способны проникать в клетки-мишени и начинать обратную транскрипцию, однако синтез вирусной ДНК остаётся незавершённым[126].
Nef[править | править код]
Белок Nef выполняет несколько функций. Он подавляет экспрессию молекул CD4 и HLA классов I и II на поверхности инфицированных клеток, и тем самым позволяет вирусу ускользать от атаки цитотоксических T-лимфоцитов и от распознавания CD4+-лимфоцитами. Белок Nef может также угнетать активацию T-лимфоцитов, связывая различные белки-компоненты систем внутриклеточной передачи сигнала[126].
У инфицированных вирусом иммунодефицита макак-резусов активная репликация вируса и прогрессирование болезни возможны только при интактном гене nef. Делеции гена nef были обнаружены в штаммах ВИЧ, выделенных у группы австралийцев с длительным непрогрессирующим течением инфекции[127]. Однако у части из них со временем появились признаки прогрессирования инфекции, в том числе снижение числа CD4+-лимфоцитов. Таким образом, хотя делеции гена nef и могут замедлять репликацию вируса, это не гарантирует полной невозможности прогрессирования заболевания[128].
Tat и Rev[править | править код]
Регуляторные белки Tat (транс-активатор) и Rev накапливаются в ядре клетки и связывают определённые участки вирусной РНК. Белок Tat имеет молекулярную массу около 14-15 кДа, связывает вторичную структуру геномной РНК вблизи 5'-нетранслируемой области[126][129], активирует обратную транскрипцию геномной РНК ВИЧ, синтез вирусных мРНК, необходим для репликации вируса почти во всех культурах клеток, регулирует выход вирионов из заражённых клеток[126][129], нуждается в клеточном кофакторе — циклине T1. Белок Rev регулирует экспрессию белков вириона, связывает мРНК гена env в области RRE (англ. Rev response element) интрона, разделяющего экзоны генов Tat и Rev[126][129].
Белки Tat и Rev стимулируют транскрипцию провирусной ДНК и транспорт РНК из ядра в цитоплазму, а также необходимы для трансляции. Белок Rev обеспечивает также транспорт компонентов вируса из ядра и переключение синтеза регуляторных белков вируса на синтез структурных[126].
Жизненный цикл[править | править код]
До проникновения в клетку-мишень[править | править код]
После попадания вирионов ВИЧ на поверхность и внутрь организма, вирусные частицы оказываются в различных по своей агрессивности биологических жидкостях. Слюна и желудочный сок содержат ферменты, которые в бо́льшей степени разрушают вирионы ВИЧ, чем другие биологические жидкости (это не относится к младенцам первых месяцев жизни, у которых ещё не вырабатываются соответствующие ферменты пищеварения, из-за чего младенцы могут быть заражены через грудное молоко). Вирионы ВИЧ проникают в кровеносную и лимфатическую систему организма и перемещаются по организму в потоке крови и лимфы. Оказавшись рядом с CD4-клеткой, вирионы ВИЧ присоединяются к рецептору CD4 на её плазматической мембране[130].
Проникновение в клетку и обратная транскрипция[править | править код]
| Механизм слияния вириона ВИЧ и плазматической мембраны Т-лимфоцита человека     |
Вирусный гликопротеин gp120 прочно связывает рецептор CD4. В результате такого взаимодействия gp120 претерпевает конформационные изменения, которые позволяют ему также связать молекулу корецептора CXCR4 или CCR5 (экспрессируемых на поверхности Т-лимфоцитов, макрофагов, дендритных клеток и микроглии)[131][132]. В зависимости от способности связывать эти корецепторы, ВИЧ классифицируют на R5-тропные (связывают только корецептор CCR5), X4-тропные (связывают только корецептор CXCR4) и R5X4-тропные (могут взаимодействовать с обоими корецепторами) варианты[131]. При заражении, в основном, передаются R5-тропные и R5X4-тропные варианты[133]. Препараты, блокирующие корецепторы, могут быть эффективны против ВИЧ[134].
После описанных событий вирусный белок gp41 проникает в мембрану клетки и подвергается значительным конформационным изменениям, вследствие которых мембрана клетки и мембрана вириона ВИЧ сближаются друг с другом и затем сливаются. Вирусный белок gp41 очень важен для слияния мембран, поэтому его рассматривают в качестве мишени для разработки противовирусных препаратов.
После слияния мембран содержимое вириона проникает внутрь клетки. Внутри клетки вирусная РНК высвобождается из капсида. Затем под действием обратной транскриптазы происходит обратная транскрипция — процесс синтеза ДНК на основании информации в одноцепочечной геномной РНК вируса[135]. Большая часть лекарственных препаратов, одобренных для применения при ВИЧ-инфекции, направлена на нарушение работы обратной транскриптазы[8].
Транспорт вирусной ДНК в ядро и интеграция в геном[править | править код]
После завершения обратной транскрипции в CD4+-лимфоците вирусный геном представлен невстроенной ДНК. Для встраивания вирусной ДНК в геном клетки-хозяина и для образования новых вирусов необходима активация T-лимфоцитов. Активация CD4+-лимфоцитов происходит при их контакте с антигенпредставляющими клетками в лимфоидной ткани. Наличие вирусов на поверхности фолликулярных дендритных клеток и присутствие провоспалительных цитокинов (ИЛ-1, ИЛ-6 и ФНОα) способствуют размножению ВИЧ в инфицированных клетках. Именно поэтому лимфоидная ткань служит самой благоприятной средой для репликации ВИЧ[136].
Синтезированная вирусная ДНК транспортируется внутрь ядра клетки в составе пре-интеграционного комплекса, в который также входят белки ВИЧ p17/MA, Nef и интеграза[137]. Далее вирусная ДНК встраивается в хромосому активированного T-лимфоцита под действием интегразы. Несколько препаратов, ингибирующих интегразу, широко используются в современной комплексной антиретровирусной терапии. Вирусная ДНК, встроившаяся в хромосому клетки, называется провирусом[8].
Транскрипция, сплайсинг, транспорт РНК из ядра в цитоплазму и трансляция[править | править код]
В ядре клеточная РНК-полимераза синтезирует предшественник вирусных информационных РНК (мРНК), длина которого равна длине геномной РНК ВИЧ-1. Этот предшественник мРНК подвергается 5'-концевому кэпированию и 3'-концевому полиаденилированию. Кроме того, предшественник мРНК подвергается сплайсингу, в результате которого образуются более 40 разных мРНК, которые можно разделить на 3 класса[138]:
- несплайсированная РНК длиной около 9.3 kb — далее используется в качестве мРНК для синтеза белков Gag и Gag-Pol, а также в качестве геномной РНК;
- не полностью сплайсированные РНК размером около 4 kb — используются как мРНК для синтеза белков Vif, Vpr, Tat, Vpu и Env;
- полностью сплайсированные РНК размером около 2 kb — используются как мРНК для синтеза белков Vpr, Tat, Rev и Nef.
На ранней стадии экспрессии генов, в отсутствие белка Rev, несплайсированная и не полностью сплайсированные РНК ВИЧ-1 нестабильны и быстро разрушаются в ядре. В то же время полностью сплайсированные мРНК ВИЧ-1 являются стабильными и транспортируются из ядра в цитоплазму[138]. В цитоплазме с помощью рибосом происходит процесс трансляции — биосинтез белка из аминокислот по заданной матрице на основе генетической информации, содержащейся в мРНК. Синтезированный в цитоплазме белок Rev транспортируется в ядро, где связывается с областью RRE несплайсированной и не полностью сплайсированных РНК, что стабилизирует эти РНК. Кроме того, Rev взаимодействует с клеточным белком CRM1 (экспортин 1), и это взаимодействие стимулирует транспорт несплайсированной и не полностью сплайсированных РНК из ядра в цитоплазму, где происходит синтез закодированных в них белков[138].
Сборка и отпочковывание вирионов[править | править код]
Геномная РНК вируса, а также вирусные белки транспортируются к местам сборки вирионов — к мембране. Вирионы первоначально формируются из полипротеинов-предшественников структурных белков и ферментов и на этой стадии не являются инфекционными. В ходе созревания вирусной частицы вирусная протеаза расщепляет белки-предшественники до функциональных компонентов[8]. Несколько одобренных противовирусных препаратов ингибируют работу протеазы и препятствуют формированию зрелых вирионов[8].
Новые вирусные частицы отпочковываются от поверхности клетки, захватывая часть её мембраны, и выходят в кровяное русло, а клетка хозяина, несущая рецептор CD4, погибает[139][140]. Недавние исследования показали, что процесс отпочковывания вирионов может быть более сложным, чем считалось ранее. Так было обнаружено, что благодаря взаимодействию белка Gag с компонентами клетки вирионы накапливаются в особых внутриклеточных мультивезикулярных тельцах, которые обычно служат для экспорта белков. Таким образом вирусные частицы высвобождаются из клетки, эксплуатируя её собственную систему транспорта макромолекул[8].
Распространение по организму[править | править код]
Только что выделившийся из заражённого лимфоцита вирион ВИЧ в плазме крови живёт в среднем около 8 часов[130]. Продолжительность полужизни (время, за которое погибает 50 % вирионов ВИЧ) в плазме крови составляет примерно 6 часов[130]. В остальных средах продолжительность полужизни вирионов ВИЧ на порядки меньше[141].
В период острой фазы ВИЧ-инфекции отсутствие специфического иммунного ответа позволяет вирусу активно реплицироваться и достигать высоких концентраций в крови. Вирус заселяет органы лимфатической системы, CD4+-лимфоциты, макрофаги, а также другие клетки: альвеолярные макрофаги лёгких, клетки Лангерганса, фолликулярные дендритные клетки лимфатических узлов, клетки олигодендроглии и астроциты мозга и эпителиальные клетки кишки[142][143]. В лимфоидной ткани ВИЧ размножается на протяжении всего заболевания, поражая макрофаги, активированные и покоящиеся CD4+-лимфоциты и фолликулярные дендритные клетки[144][145]. Количество клеток, содержащих провирусную ДНК, в лимфоидной ткани в 5—10 раз выше, чем среди клеток крови, а репликация ВИЧ в лимфоидной ткани на 1—2 порядка выше, чем в крови. Основным клеточным резервуаром ВИЧ являются CD4+-Т-лимфоциты иммунологической памяти[146].
Для активации CD8+-лимфоцитов и образования антиген-специфических цитотоксических T-лимфоцитов необходима презентация пептидного антигена в комплексе с человеческим лейкоцитарным антигеном класса I. Дендритные клетки, необходимые для начала первичных антиген-специфичных реакций, захватывают антигены, перерабатывают и переносят их на свою поверхность, где эти антигены в комплексе с дополнительными стимулирующими молекулами активируют T-лимфоциты. Заражённые клетки часто не выделяют дополнительных стимулирующих молекул и поэтому не способны вызвать активацию достаточного числа B- и T-лимфоцитов, функция которых зависит от дендритных клеток[136].
На 2023 год ВИЧ-инфекция до сих пор остаётся неизлечимым заболеванием, так как геном вируса интегрируется в хромосомы клеток и может реактивироваться даже после курса антиретровирусной терапии. В настоящее время идёт поиск безопасных способов редактирования генома человека и исключения из него провирусной ДНК[147][148]. В 2014 году был предложен метод удаления генома ВИЧ-1 из заражённых клеток при помощи системы CRISPR/Cas9. С помощью этого метода исследователям удалось вырезать фрагмент провирусной ДНК, заключённый между 5'- и 3'-концевыми LTR-областями из хромосом заражённых клеток в культуре. Кроме того, этот метод оказался также эффективным для профилактики заражения неинфицированных клеток. Описанный подход может привести к разработке способа полного избавления от ВИЧ-инфекции[149][150].
Происхождение[править | править код]

HIV — вирус иммунодефицита человека
SIV — вирус иммунодефицита обезьян
Методом молекулярной филогении показано, что вирус иммунодефицита человека образовался в конце XIX или в начале XX века[151][152][153][154][155], скорее всего в 1920-х гг[156].
Оба типа вируса иммунодефицита человека ВИЧ-1 и ВИЧ-2 возникли в Западной и Центральной Африке южнее Сахары и передались от обезьян к людям. ВИЧ-1 возник на юге Камеруна в результате эволюции эндемичного вируса иммунодефицита обезьян SIV-cpz, который заражает черномордых шимпанзе (Pan troglodytes troglodytes)[157][158]. ВИЧ-1, как полагают, перешёл видовой барьер, по крайней мере, трижды и породил три группы вирусов: M, N и О[159].
ВИЧ-2 возник на территории Западной Африки (от южного Сенегала до запада Берега Слоновой Кости) в результате эволюции вируса иммунодефицита обезьян SIV-smm, который заражает тёмно-коричневых мангабеев (Cercocebus atys), представителя мартышкообразных узконосых обезьян[160].
Существует доказательство того, что охотники на диких животных (обезьян) или поставщики мяса в Западной и Центральной Африке подвергаются заражению вирусом иммунодефицита обезьян, причём вероятность заражения коррелирует с частотой взаимодействия с обезьянами и их мясом[161]. Однако вирус иммунодефицита обезьян — слабый вирус, и, как правило, подавляется иммунной системой человека в течение недели после заражения. Считается, что необходимо несколько передач вируса от человека к человеку в быстрой последовательности, чтобы вирусу хватило времени мутировать в ВИЧ[162]. Хотя передача вируса иммунодефицита обезьян от человека к человеку происходит редко, определённые социальные факторы могут существенно влиять на частоту заражений. Предполагают, что условия для распространения вируса были неблагоприятны в Африке до XX века. Сопоставление периодов ускоренной эволюции ВИЧ с социо-экономическими изменениями позволяет делать предположения о природе факторов, ускоривших распространение ВИО и ВИЧ.
Генетические исследования показывают, что последний общий предок ВИЧ-1 группы М существовал около 1910 года[163]. Сторонники этой даты связывают распространение ВИЧ с развитием колониализма в Африке и ростом больших городов. Эти факторы привели к таким социальным изменениям в обществе, как увеличение частоты беспорядочных половых связей, распространение проституции и заболеваний, передающихся половым путём (ЗППП)[164]. ЗППП, такие как сифилис, могут сопровождаться генитальными язвами. Исследования показывают, что вероятность передачи ВИЧ во время вагинального полового акта, достаточно низкая при обычных условиях, может быть увеличена в десятки, если не в сотни раз, если один из партнёров страдает от генитальных язв. О степени распространённости ЗППП в колониальных городах в начале 1900-х можно судить по следующим цифрам: в 1928 году по меньшей мере 45 % жительниц восточного Леопольдвиля (ныне — Киншаса, ранний центр распространения ВИЧ группы М) были проституированными женщинами, а в 1933 году около 15 % всех жителей этого же города были заражены одной из форм сифилиса. Ретроспективный анализ показал, что начало эпидемии ВИЧ-инфекции в Киншасе совпало с пиком эпидемии генитальных язв в середине 1930-х годов[164].
Альтернативная точка зрения гласит, что основным фактором, способствовавшим адаптации ВИЧ к людям и его распространению, была небезопасная медицинская практика в Африке в годы после Второй мировой войны, такая как использование нестерильных многоразовых шприцев при массовых вакцинациях, инъекциях антибиотиков и противомалярийных средств[110][165][166].
В результате ретроанализа образцов крови, взятых после Второй мировой войны, зафиксирован самый ранний документальный случай наличия ВИЧ в организме человека, кровь у которого взяли в 1959 году[167]. Вирус, возможно, присутствовал в Соединённых Штатах уже в 1966 году[168], но подавляющее большинство случаев заражения ВИЧ, идентифицированных за пределами тропической Африки, можно проследить до одного неустановленного человека, который заразился ВИЧ на Гаити, а затем перенёс инфекцию в США около 1969 года[169].
Мутация CCR5-Δ32[править | править код]
Естественная устойчивость к ВИЧ[править | править код]
Описаны случаи устойчивости людей к ВИЧ. Проникновение вируса в клетку иммунной системы связано с его взаимодействием с поверхностным рецептором, белком CCR5. Делеция (утеря участка гена) CCR5-дельта32 приводит к невосприимчивости её носителя к ВИЧ. Предполагается, что эта мутация возникла примерно две с половиной тысячи лет назад и со временем распространилась в Европе. Сейчас к ВИЧ фактически устойчив в среднем 1 % жителей Европы, 10—15 % европейцев имеют частичную сопротивляемость к ВИЧ[170]. 0,1-0,3 % русского населения почти невосприимчивы к ВИЧ[171]. Учёные Ливерпульского университета объясняют распространение мутации гена CCR5 тем, что она усиливает сопротивляемость к бубонной чуме. Эпидемия «чёрной смерти» 1347 года (а в Скандинавии ещё и 1711 года) способствовала увеличению частоты этого генотипа в Европе.
Мутация в гене CCR2 также уменьшает шанс проникновения ВИЧ в клетку и приводит к задержке развития СПИДа. Существует небольшой процент ВИЧ-положительных людей (около 10 %), у которых СПИД не развивается в течение долгого времени. Их называют нонпрогрессорами (nonprogressors)[172][173].
Важный клеточный компонент защиты против ВИЧ — антивирусный белок APOBEC3G, который вызывает деаминирование ДНК, приводящее к мутационным заменам G на A в вирусной ДНК, синтезируемой в ходе обратной транскрипции. APOBEC3G инактивируется белком Vif ВИЧ-1, который вызывает его убиквитинилирование и деградацию[174].
Обнаружено, что одним из главных элементов антивирусной защиты человека и других приматов является белок TRIM5a, способный распознавать капсид вирусных частиц и препятствовать размножению вируса в клетке. TRIM5a человека и шимпанзе несколько отличаются друг от друга и эффективны против разных вирусов: этот белок защищает шимпанзе от ВИЧ и родственных ему вирусов, а человека — от вируса PtERV1[175]. Обезьяны Нового Света, за исключением мирикины, которая имеет химерный ген TRIM5-CypA, устойчивостью к ВИЧ не обладают[176].
Другой важный элемент антивирусной защиты — интерферон-индуцируемый трансмембранный белок CD317/BST-2 (англ. bone marrow stromal antigen 2)[122][123][177]. CD317 — трансмембранный белок 2-го типа с необычной топологией: он имеет трансмембранный домен рядом с N-концом и гликозилфосфатидилинозитол (GPI) на С-конце, между которыми расположен внеклеточный домен[178]. Показано, что CD317 непосредственно взаимодействует со зрелыми дочерними вирионами, «привязывая» их к поверхности клетки[179]. Для объяснения механизма такого «привязывания» предложено несколько альтернативных моделей, которые, тем не менее, сходятся в следующем: молекулы CD317 формируют параллельный гомодимер; один или два гомодимера связываются одновременно с одним вирионом и клеточной мембраной. При этом с мембраной вириона взаимодействуют либо оба мембранных «якоря» (трансмембранный домен и GPI) одной из молекул CD317, либо один из них[179]. Спектр активности CD317 включает, по крайней мере, четыре семейства вирусов: ретровирусы, филовирусы, аренавирусы и герпесвирусы[177]. Активность данного клеточного фактора ингибируется белками Vpu ВИЧ-1, Env ВИЧ-2 и SIV, Nef SIV, гликопротеином оболочки вируса Эбола и белком К5 герпесвируса саркомы Капоши[118][119][124][125][177][180][181]. Обнаружен кофактор белка CD317 — клеточный белок ВСА2 (Breast cancer-associated gene 2; Rabring7, ZNF364, RNF115) — Е3-убиквитинлигаза класса RING. BCA2 усиливает интернализацию вирионов ВИЧ-1, «привязанных» белком CD317 к поверхности клетки, в CD63+ внутриклеточные везикулы с их последующим разрушением в лизосомах[182].
См. также[править | править код]
- Тимоти Рэй Браун («Берлинский пациент») — первый человек, который вылечился от ВИЧ/СПИДа.
- Роберт Рейфорд («нулевой пациент») — первая зарегистрированная жертва ВИЧ/СПИДа в Северной Америке.
- Арвид Ноэ — первая зарегистрированная жертва ВИЧ/СПИДа в Европе.
- Грете Раск — одна из первых жертв ВИЧ/СПИДа в Европе.
- Гаэтан Дюга — канадский бортпроводник, внёсший значительный вклад в распространение вируса в Северной Америке и ранее ошибочно идентифицировавшийся как «нулевой пациент».
Примечания[править | править код]
- ↑ James E. Rickman. Human genes may predict AIDS progression rate (англ.). Los Alamos National Laboratory News Bulletin (14 июля 2003). Архивировано 23 марта 2004 года.
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ Медпортал. ВИЧ-инфекция и СПИД. Дата обращения: 24 января 2015. Архивировано 20 января 2015 года.
- ↑ Weiss R.A. How does HIV cause AIDS? (англ.) // Science. — 1993. — May (vol. 260, no. 5112). — P. 1273—1279. — doi:10.1126/science.8493571. — . — PMID 8493571.
- ↑ Douek D.C., Roederer M., Koup R.A. Emerging Concepts in the Immunopathogenesis of AIDS (англ.) // Annu. Rev. Med. : journal. — 2009. — Vol. 60. — P. 471—484. — doi:10.1146/annurev.med.60.041807.123549. — PMID 18947296. — PMC 2716400.
- ↑ Kawamura T., Kurtz S. E., Blauvelt A., Shimada S. The role of Langerhans cells in the sexual transmission of HIV. (англ.) // Journal of dermatological science. — 2005. — Vol. 40, no. 3. — P. 147—155. — doi:10.1016/j.jdermsci.2005.08.009. — PMID 16226431.
- ↑ Kramer-Hämmerle S., Rothenaigner I., Wolff H., Bell J. E., Brack-Werner R. Cells of the central nervous system as targets and reservoirs of the human immunodeficiency virus. (англ.) // Virus research. — 2005. — Vol. 111, no. 2. — P. 194—213. — doi:10.1016/j.virusres.2005.04.009. — PMID 15885841.
- ↑ 1 2 3 4 5 6 7 8 9 NIAID/NIH: The Relationship Between the Human Immunodeficiency Virus and the Acquired Immunodeficiency Syndrome. Дата обращения: 11 июля 2014. Архивировано 10 сентября 2016 года.
- ↑ 1 2 Alimonti J.B., Ball T.B., Fowke K.R. Mechanisms of CD4+ T lymphocyte cell death in human immunodeficiency virus infection and AIDS. (англ.) // Journal of General Virology[англ.] : journal. — Microbiology Society[англ.], 2003. — Vol. 84, no. 7. — P. 1649—1661. — doi:10.1099/vir.0.19110-0. — PMID 12810858.
- ↑ 1 2 UNAIDS, WHO. 2007 AIDS epidemic update (англ.) (PDF) 10 (декабрь 2007). Дата обращения: 12 марта 2008. Архивировано 27 мая 2008 года.
- ↑ 1 2 Holmes C.B., Losina E., Walensky R.P., Yazdanpanah Y., Freedberg K.A. Review of human immunodeficiency virus type 1-related opportunistic infections in sub-Saharan Africa (англ.) // Clin. Infect. Dis. : journal. — 2003. — Vol. 36, no. 5. — P. 656‐662. — doi:10.1086/367655. — PMID 12594648.
- ↑ 1 2 Guss D.A. The acquired immune deficiency syndrome: an overview for the emergency physician, Part 1 (англ.) // J. Emerg. Med. : journal. — 1994. — Vol. 12, no. 3. — P. 375—384. — doi:10.1016/0736-4679(94)90281-X. — PMID 8040596.
- ↑ 1 2 Guss D.A. The acquired immune deficiency syndrome: an overview for the emergency physician, Part 2 (англ.) // J. Emerg. Med. : journal. — 1994. — Vol. 12, no. 4. — P. 491—497. — doi:10.1016/0736-4679 (94)90346-8. — PMID 7963396.
- ↑ Роксби, Филиппа (2017-05-11). "Почему сейчас люди с ВИЧ живут столько же, сколько и здоровые". BBC News Русская служба. Архивировано 13 апреля 2019. Дата обращения: 25 июня 2020.
- ↑ ВИЧ больше не убивает. Газета.Ru. Дата обращения: 25 июня 2020. Архивировано 13 апреля 2019 года.
- ↑ «Неопределяемый = не передающий». SpidCenter. Дата обращения: 27 января 2021. Архивировано 1 декабря 2020 года.
- ↑ Главная (рус.). NO STIGMA. Дата обращения: 27 января 2021. Архивировано 13 апреля 2019 года.
- ↑ Медработники должны рассказывать о тезисе «U = U» всем ВИЧ+. life4me.plus. Дата обращения: 27 января 2021. Архивировано 13 апреля 2019 года.
- ↑ Центр СПИД - НЕОПРЕДЕЛЯЕМЫЙ = НЕ ПЕРЕДАЮЩИЙ. www.hiv-spb.ru. Дата обращения: 27 января 2021. Архивировано 22 апреля 2021 года.
- ↑ ВИЧ и беременность: что нужно знать, как правильно реагировать и где получить поддержку (рус.). НЭН. Дата обращения: 27 января 2021. Архивировано 14 апреля 2019 года.
- ↑ Public Health Image Library Архивная копия от 25 июля 2014 на Wayback Machine Scanning electron micrograph of HIV-1 virions budding from a cultured lymphocyte. See PHIL 10000 for a colorized view of this image, and PHIL 14270, for a black and white version, both viewed at a lower magnigication
- ↑ Department of Health and Human Services. Centers for Disease Control and Prevention’s Public Health Image Library (PHIL), image #948.Проверено 27 июля 2012.
- ↑ Pneumocystis pneumonia--Los Angeles. (англ.) // MMWR. Morbidity and mortality weekly report. — 1981. — Vol. 30, no. 21. — P. 250—252. — PMID 6265753.
- ↑ 1 2 3 4 5 History of AIDS Up to 1986 (англ.). AVERT. Дата обращения: 21 июля 2014. Архивировано 7 октября 2015 года.
- ↑ Pneumocystis carinii pneumonia among persons with hemophilia A (англ.) // MMWR Morb. Mortal. Wkly. Rep. : journal. — 1982. — July (vol. 31, no. 27). — P. 365—367. — PMID 6815443. Архивировано 5 августа 2012 года.
- ↑ Opportunistic infections and Kaposi's sarcoma among Haitians in the United States (англ.) // MMWR Morb. Mortal. Wkly. Rep. : journal. — 1982. — July (vol. 31, no. 26). — P. 353—354. — PMID 6811853. Архивировано 20 сентября 2011 года.
- ↑ Cohen J. HIV/AIDS: Latin America & Caribbean. HAITI: making headway under hellacious circumstances (англ.) // Science : journal. — 2006. — Vol. 313, no. 5786. — P. 470—473. — doi:10.1126/science.313.5786.470b. — PMID 16873641.
- ↑ Centers for Disease Control (CDC). Persistent, generalized lymphadenopathy among homosexual males (англ.) // MMWR Morb Mortal Wkly Rep. : journal. — 1982. — Vol. 31, no. 19. — P. 249—251. — PMID 6808340. Архивировано 18 октября 2011 года.
- ↑ Barré-Sinoussi F., Chermann J.C., Rey F., Nugeyre M.T., Chamaret S., Gruest J., Dauguet C., Axler-Blin C., Vézinet-Brun F., Rouzioux C., Rozenbaum W., Montagnier L;. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS) (англ.) // Science : journal. — 1983. — Vol. 220, no. 4599. — P. 868—871. — doi:10.1126/science.6189183. — . — PMID 6189183.
- ↑ The history of AIDS 1981—1986 (англ.). AVERT. Дата обращения: 21 июля 2014. Архивировано 10 февраля 2009 года.
- ↑ Update on acquired immune deficiency syndrome (AIDS)--United States. (англ.) // MMWR. Morbidity and mortality weekly report. — 1982. — Vol. 31, no. 37. — P. 507—508. — PMID 6815471.
- ↑ Gottlieb M. S., Schroff R., Schanker H. M., Weisman J. D., Fan P. T., Wolf R. A., Saxon A. Pneumocystis carinii pneumonia and mucosal candidiasis in previously healthy homosexual men: evidence of a new acquired cellular immunodeficiency. (англ.) // The New England journal of medicine. — 1981. — Vol. 305, no. 24. — P. 1425—1431. — doi:10.1056/NEJM198112103052401. — PMID 6272109.
- ↑ Durack D. T. Opportunistic infections and Kaposi's sarcoma in homosexual men. (англ.) // The New England journal of medicine. — 1981. — Vol. 305, no. 24. — P. 1465—1467. — doi:10.1056/NEJM198112103052408. — PMID 6272112.
- ↑ Goedert J. J., Neuland C. Y., Wallen W. C., Greene M. H., Mann D. L., Murray C., Strong D. M., Fraumeni J. F. Jr., Blattner W. A. Amyl nitrite may alter T lymphocytes in homosexual men. (англ.) // Lancet. — 1982. — Vol. 1, no. 8269. — P. 412—416. — PMID 6121088.
- ↑ Jaffe H. W., Choi K., Thomas P. A., Haverkos H. W., Auerbach D. M., Guinan M. E., Rogers M. F., Spira T. J., Darrow W. W., Kramer M. A., Friedman S. M., Monroe J. M., Friedman-Kien A. E., Laubenstein L. J., Marmor M., Safai B., Dritz S. K., Crispi S. J., Fannin S. L., Orkwis J. P., Kelter A., Rushing W. R., Thacker S. B., Curran J. W. National case-control study of Kaposi's sarcoma and Pneumocystis carinii pneumonia in homosexual men: Part 1. Epidemiologic results. (англ.) // Annals of internal medicine. — 1983. — Vol. 99, no. 2. — P. 145—151. — PMID 6603806.
- ↑ Mathur-Wagh U., Enlow R. W., Spigland I., Winchester R. J., Sacks H. S., Rorat E., Yancovitz S. R., Klein M. J., William D. C., Mildvan D. Longitudinal study of persistent generalised lymphadenopathy in homosexual men: relation to acquired immunodeficiency syndrome. (англ.) // Lancet. — 1984. — Vol. 1, no. 8385. — P. 1033—1038. — PMID 6143974.
- ↑ Newell G. R., Adams S. C., Mansell P. W., Hersh E. M. Toxicity, immunosuppressive effects and carcinogenic potential of volatile nitrites: possible relationship to Kaposi's sarcoma. (англ.) // Pharmacotherapy. — 1984. — Vol. 4, no. 5. — P. 284—291. — PMID 6150466.
- ↑ Barré-Sinoussi F., Chermann J. C., Rey F., Nugeyre M. T., Chamaret S., Gruest J., Dauguet C., Axler-Blin C., Vézinet-Brun F., Rouzioux C., Rozenbaum W., Montagnier L. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS). (англ.) // Science (New York, N.Y.). — 1983. — Vol. 220, no. 4599. — P. 868—871. — PMID 6189183.
- ↑ Gallo R. C., Sarin P. S., Gelmann E. P., Robert-Guroff M., Richardson E., Kalyanaraman V. S., Mann D., Sidhu G. D., Stahl R. E., Zolla-Pazner S., Leibowitch J., Popovic M. Isolation of human T-cell leukemia virus in acquired immune deficiency syndrome (AIDS). (англ.) // Science (New York, N.Y.). — 1983. — Vol. 220, no. 4599. — P. 865—867. — PMID 6601823.
- ↑ Coffin J., Haase A., Levy J. A., Montagnier L., Oroszlan S., Teich N., Temin H., Toyoshima K., Varmus H., Vogt P. What to call the AIDS virus? (англ.) // Nature. — 1986. — Vol. 321, no. 6065. — P. 10. — PMID 3010128.
- ↑ The Nobel Prize in Physiology or Medicine 2008 Press Release (англ.). — «Harald zur Hausen, Françoise Barré-Sinoussi, Luc Montagnier». Дата обращения: 21 июля 2014. Архивировано 10 августа 2018 года.
- ↑ 1 2 3 4 5 6 Levy J.A. HIV and the pathogenesis of AIDS. — USA: American Society for Microbiology, 2007. — ISBN 978-1-55581-393-2.
- ↑ Rothenberg R. B., Scarlett M., del Rio C., Reznik D., O'Daniels C. Oral transmission of HIV. (англ.) // AIDS (London, England). — 1998. — Vol. 12, no. 16. — P. 2095—2105. — PMID 9833850.
- ↑ Begay O., Jean-Pierre N., Abraham C. J., Chudolij A., Seidor S., Rodriguez A., Ford B. E., Henderson M., Katz D., Zydowsky T., Robbiani M., Fernández-Romero J. A. Identification of personal lubricants that can cause rectal epithelial cell damage and enhance HIV type 1 replication in vitro. (англ.) // AIDS research and human retroviruses. — 2011. — Vol. 27, no. 9. — P. 1019—1024. — doi:10.1089/AID.2010.0252. — PMID 21309617.
- ↑ James Wilton. From exposure to infection: The biology of HIV transmission (англ.). Дата обращения: 10 сентября 2014. Архивировано из оригинала 10 сентября 2014 года.
- ↑ Jpnh G Bartlett. [hopkons-hivguide.org Карманный справочник. Лечение ВИЧ-инфекции и СПИДа у взрослых]. — Медицинская школа Университета Джонса Хопкинса, 2008. — 138 с.
- ↑ Cooper E. R., Charurat M., Mofenson L., Hanson I. C., Pitt J., Diaz C., Hayani K., Handelsman E., Smeriglio V., Hoff R., Blattner W. Combination antiretroviral strategies for the treatment of pregnant HIV-1-infected women and prevention of perinatal HIV-1 transmission. (англ.) // Journal of acquired immune deficiency syndromes (1999). — 2002. — Vol. 29, no. 5. — P. 484—494. — PMID 11981365.
- ↑ Recommendations for Use of Antiretroviral Drugs in Pregnant HIV-1-Infected Women for Maternal Health and Interventions to Reduce Perinatal HIV-1 Transmission in the United States (англ.). AIDSinfo.nih.gov (12 октября 2006). Дата обращения: 21 июля 2014. Архивировано из оригинала 22 апреля 2006 года.
- ↑ Всемирная организация здравоохранения. HIV transmission through breastfeeding. A review of available evidence. — 2007. — ISBN 9789241596596. Архивировано 21 января 2022 года.
- ↑ Kerr C. Bloodsucking fly blamed for transmitting HIV. (англ.) // The Lancet infectious diseases. — 2002. — Vol. 2, no. 5. — P. 265. — PMID 12062985.Цитата: «Most bloodsucking insects are not capable of transmitting HIV because they inject saliva and ingest blood through different routes»
- ↑ 1 2 CDC. HIV Transmission (англ.). Дата обращения: 21 июля 2014. Архивировано 4 февраля 2005 года. Centers for Disease Control and Prevention. HIV and Its Transmission (англ.). The Center for HIV Law and Policy. — Разоблачение мифов о передаче ВИЧ бытовым путём, при поцелуях, укусах, через слюну, слёзы и др. Дата обращения: 21 июля 2014. Архивировано 4 марта 2016 года. aids.gov. HOW DO YOU GET HIV OR AIDS? (англ.). U.S. Department of Health & Human Services. Дата обращения: 21 июля 2014. Архивировано 14 мая 2017 года. Baron S., Poast J., Cloyd M. W. Why is HIV rarely transmitted by oral secretions? Saliva can disrupt orally shed, infected leukocytes. (англ.) // Archives of internal medicine. — 1999. — Vol. 159, no. 3. — P. 303—310. — PMID 9989543.
- ↑ «Устойчивость вируса ВИЧ во внешней среде» O-spide.ru Официальный интернет-портал Минздрава России о профилактике ВИЧ/СПИД. Дата обращения: 18 июля 2020. Архивировано 19 июля 2020 года.
- ↑ Приведено согласно Figure 1, опубликованной в Pantaleo, G et al. New concepts in the immunopathogenesis of human immunodeficiency virus infection (англ.) // New England Journal of Medicine : journal. — 1993. — 4 February (vol. 328, no. 5). — P. 327—335. — PMID 8093551., также доступна Figure 4 в The relationship between the human immunodeficiency virus and the acquired immunodeficiency syndrome (англ.). US National Institute of Allergy and Infectious Diseases. Дата обращения: 3 ноября 2009. Архивировано из оригинала 30 ноября 2009 года. Дополнительная информация опубликована в Piutak, M et al. High levels of HIV-1 in plasma during all stages of infection determined by competitive PCR (англ.) // Science : journal. — 1993. — 19 March (vol. 259, no. 510). — P. 1749—1754. — PMID 8096089.
- ↑ Борьба со СПИД в России: как остановить болезнь? РИА Новости (30 ноября 2011). Дата обращения: 16 июня 2013. Архивировано 16 июня 2013 года.
- ↑ 1 2 UNAIDS World AIDS Day Report 2011 (англ.). UNAIDS World AIDS (2011). Дата обращения: 16 июня 2013. Архивировано 16 июня 2013 года.
- ↑ Федеральный центр СПИД: Справка ВИЧ-инфекция в Российской Федерации в 2014 г. Дата обращения: 23 июля 2015. Архивировано из оригинала 15 августа 2015 года.
- ↑ National HIV and STD Testing Resources (англ.). Centers for Disease Control and Prevention. Дата обращения: 21 июля 2014. (недоступная ссылка)
- ↑ aids.gov. Just Diagnosed with HIV AIDS: Understand Your Test Results: Viral Load (англ.). U.S. Department of Health & Human Services. Дата обращения: 21 июля 2014. Архивировано 13 мая 2017 года.
- ↑ WebMD Medical Reference from Healthwise. Human Immunodeficiency Virus (HIV) Test (англ.). Healthwise. Дата обращения: 21 июля 2014. Архивировано 11 ноября 2017 года.
- ↑ ВИЧ.рф тест на ВИЧ. Дата обращения: 12 сентября 2014. Архивировано 12 августа 2020 года.
- ↑ ВИЧ/СПИД: Тестирование и консультирование. Дата обращения: 12 сентября 2014. Архивировано 19 апреля 2018 года.
- ↑ Федеральный закон от 22 июля 1993 г. № 5487-1 "Основы законодательства Российской Федерации об охране здоровья граждан" 0. Российская газета. Дата обращения: 21 июля 2014. Архивировано 25 октября 2020 года.
- ↑ Тест на ВИЧ с точки зрения права. Николай Недзельский. Дата обращения: 21 июля 2014. Архивировано 7 февраля 2016 года.
- ↑ Kristina Allers, Gero Hütter, Jörg Hofmann, Christoph Loddenkemper, Kathrin Rieger, Eckhard Thiel, Thomas Schneider. Evidence for the cure of HIV infection by CCR5Δ32/Δ32 stem cell transplantation // Blood. — 2011-03-10. — Т. 117, вып. 10. — С. 2791–2799. — ISSN 1528-0020 0006-4971, 1528-0020. — doi:10.1182/blood-2010-09-309591.
- ↑ Jon Cohen. Has a second person with HIV been cured? (англ.). Science Mag (4 марта 2019). doi:10.1126/science.aax2247. Дата обращения: 10 июля 2020. Архивировано 8 июля 2020 года.
- ↑ Jon Cohen. An intriguing—but far from proven—HIV cure in the ‘São Paulo Patient’ (англ.). Science Mag (7 июля 2020). doi:10.1126/science.abd6947. Дата обращения: 10 июля 2020. Архивировано 10 июля 2020 года.
- ↑ 1 2 Анастасия Кузнецова–Фантони. Врачи сообщили о ремиссии у пациентки с ВИЧ после переливания пуповинной крови. N + 1 — главное издание о науке, технике и технологиях. Дата обращения: 17 марта 2023. Архивировано 16 марта 2023 года.
- ↑ Jingmei Hsu, Koen Van Besien, Marshall J. Glesby, Savita Pahwa, Anne Coletti, Meredith G. Warshaw, Larry Petz, Theodore B. Moore, Ya Hui Chen, Suresh Pallikkuth, Adit Dhummakupt, Ruth Cortado, Amanda Golner, Frederic Bone, Maria Baldo, Marcie Riches, John W. Mellors, Nicole H. Tobin, Renee Browning, Deborah Persaud, Yvonne Bryson, Patricia Anthony, Frederic Bone, Renee Browning, Yvonne Bryson, Anne Coletti, Marshall J. Glesby, Amanda Golner, Rohan Hazra, Jingmei Hsu, Ronald Mitsuyasu, Theodore B. Moore, Savita Pahwe, Deborah Persaud, Lawrence Petz, Nicole H. Tobin, Meredith G. Warshaw, Dwight Yin. HIV-1 remission and possible cure in a woman after haplo-cord blood transplant (англ.) // Cell. — 2023-03-16. — Т. 186, вып. 6. — С. 1115–1126.e8. — ISSN 1097-4172 0092-8674, 1097-4172. — doi:10.1016/j.cell.2023.02.030.
- ↑ aidsmap. Ожидаемая продолжительность жизни для некоторых групп ВИЧ-инфицированных лиц в США теперь значительно превосходит её средний показатель. Дата обращения: 26 января 2015. Архивировано из оригинала 7 марта 2015 года.
- ↑ Антиретровирусная терапия online. Продолжительность жизни людей с ВИЧ, получающих АРВТ в развитых странах. Дата обращения: 26 января 2015. Архивировано 27 мая 2020 года.
- ↑ US National Library of Medicine National Institutes of Health. Closing the Gap: Increases in Life Expectancy among Treated HIV-Positive Individuals in the United States and Canada. Дата обращения: 29 сентября 2017. Архивировано 27 мая 2020 года.
- ↑ Emery S., Neuhaus J. A., Phillips A. N., Babiker A., Cohen C. J., Gatell J. M., Girard P. M., Grund B., Law M., Losso M. H., Palfreeman A., Wood R. Major clinical outcomes in antiretroviral therapy (ART)-naive participants and in those not receiving ART at baseline in the SMART study. (англ.) // The Journal of infectious diseases. — 2008. — Vol. 197, no. 8. — P. 1133—1144. — doi:10.1086/586713. — PMID 18476292.
- ↑ Katzenstein D. A., Hammer S. M., Hughes M. D., Gundacker H., Jackson J. B., Fiscus S., Rasheed S., Elbeik T., Reichman R., Japour A., Merigan T. C., Hirsch M. S. The relation of virologic and immunologic markers to clinical outcomes after nucleoside therapy in HIV-infected adults with 200 to 500 CD4 cells per cubic millimeter. AIDS Clinical Trials Group Study 175 Virology Study Team. (англ.) // The New England journal of medicine. — 1996. — Vol. 335, no. 15. — P. 1091—1098. — doi:10.1056/NEJM199610103351502. — PMID 8813039.
- ↑ Sterne J. A., Hernán M. A., Ledergerber B., Tilling K., Weber R., Sendi P., Rickenbach M., Robins J. M., Egger M. Long-term effectiveness of potent antiretroviral therapy in preventing AIDS and death: a prospective cohort study. (англ.) // Lancet. — 2005. — Vol. 366, no. 9483. — P. 378—384. — doi:10.1016/S0140-6736(05)67022-5. — PMID 16054937.
- ↑ Starting, Monitoring & Switching HIV Treatment (англ.). AVERT. Дата обращения: 21 июля 2014. Архивировано 7 октября 2015 года.
- ↑ AIDSinfo. Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents (англ.). NIH. Дата обращения: 13 августа 2014. Архивировано из оригинала 1 ноября 2016 года.
- ↑ World Health Organization. Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection (англ.). Дата обращения: 13 августа 2014. Архивировано 11 апреля 2020 года.
- ↑ UNAIDS. Gap report (англ.). Дата обращения: 13 августа 2014. Архивировано 6 мая 2020 года.
- ↑ AVERT. HIV treatment children (англ.). Дата обращения: 13 августа 2014. Архивировано 23 сентября 2015 года.
- ↑ Janet Karpinski, Ilona Hauber, Jan Chemnitz et al. Directed evolution of a recombinase that excises the provirus of most HIV-1 primary isolates with high specificity (англ.) // Nature Biotechnology : journal. — Nature Publishing Group, 2016. — doi:10.1038/nbt.34.
- ↑ Немецким учёным удалось победить вирус иммунодефицита человека Архивная копия от 1 октября 2020 на Wayback Machine Новости высоких технологий (Дата обращения: 1 марта 2016)
- ↑ Janet Karpinski, Ilona Hauber, Jan Chemnitz et al.. Directed evolution of a recombinase that excises the provirus of most HIV-1 primary isolates with high specificity (англ.). Nature Biotechnology (22 февраля 2016). Дата обращения: 1 марта 2016. Архивировано 24 февраля 2016 года.
- ↑ В США одобрен препарат для лечения ВИЧ с новым механизмом действия. Дата обращения: 19 марта 2018. Архивировано 28 ноября 2020 года.
- ↑ Десять проблем здравоохранения, над которыми ВОЗ будет работать в 2019 году. ВОЗ (2019). Дата обращения: 29 марта 2019. Архивировано 19 апреля 2019 года.
- ↑ Kurth, R; Bannert, N. Retroviruses: Molecular Biology, Genomics and Pathogenesis. — Caister Academic Press, 2010. — ISBN 978-1-904455-55-4.
- ↑ 1 2 Nyamweya S., Hegedus A., Jaye A., Rowland-Jones S., Flanagan K. L., Macallan D. C. Comparing HIV-1 and HIV-2 infection: Lessons for viral immunopathogenesis. (англ.) // Reviews in medical virology. — 2013. — Vol. 23, no. 4. — P. 221—240. — doi:10.1002/rmv.1739. — PMID 23444290.
- ↑ Gelderblom H.R., Ozel M., Pauli G. Morphogenesis and morphology of HIV. Structure relations (англ.) // Arch. Virol. : journal. — 1989. — Vol. 106. — P. 1—13.
- ↑ Lentivirus (англ.). International Committee on Taxonomy of Viruses (ICTV). — Virus Taxonomy: 2013 Release. Дата обращения: 21 июля 2014. Архивировано из оригинала 29 июля 2014 года.
- ↑ Джон Бартлетт. Типы и подтипы ВИЧ // Клинические аспекты ВИЧ-инфекции. — 2009. Архив
- ↑ HIV Strains: Types, Groups and Subtypes (англ.). AVERT. Дата обращения: 21 июля 2014. Архивировано 24 сентября 2015 года.
- ↑ Sharp P. M., Hahn B. H. Origins of HIV and the AIDS pandemic. (англ.) // Cold Spring Harbor perspectives in medicine. — 2011. — Vol. 1, no. 1. — P. 006841. — doi:10.1101/cshperspect.a006841. — PMID 22229120.
- ↑ Bobkov A.F., Kazennova E.V., Selimova L.M., et al. Temporal trends in the HIV-1 epidemic in Russia: predominance of subtype A (англ.) // J. Med. Virol. : journal. — 2004. — October (vol. 74, no. 2). — P. 191—196. — doi:10.1002/jmv.20177. — PMID 15332265.
- ↑ 1 2 3 4 Goudsmit, Jaap. Viral Sex; The Nature of AIDS. Oxford University Press. New York, New York, 1997. Pg. 51-58. Retrieved May 25, 2008.
- ↑ 1 2 3 4 [1] Архивная копия от 15 февраля 2009 на Wayback Machine Introduction to HIV types, groups and subtypes. March 3, 2008. Retrieved May 25, 2008.
- ↑ Paraskevis D., Magiorkinis M., Vandamme A. M., Kostrikis L. G., Hatzakis A. Re-analysis of human immunodeficiency virus type 1 isolates from Cyprus and Greece, initially designated 'subtype I', reveals a unique complex A/G/H/K/? mosaic pattern. (англ.) // The Journal of general virology. — 2001. — Vol. 82, no. Pt 3. — P. 575—580. — PMID 11172098.
- ↑ Hemelaar J., Gouws E., Ghys P.D., Osmanov S. Global and regional distribution of HIV-1 genetic subtypes and recombinants in 2004. (англ.) // AIDS : journal. — 2006. — March (vol. 20, no. 16). — P. W13—23. — doi:10.1097/01.aids.0000247564.73009.bc. — PMID 17053344.
- ↑ First New HIV Strain in 19 Years Identified — Scientific American. Дата обращения: 12 июля 2021. Архивировано 15 ноября 2019 года.
- ↑ Peeters M., Gueye A., Mboup S., Bibollet-Ruche F., Ekaza E., Mulanga C., Ouedrago R., Gandji R., Mpele P., Dibanga G., Koumare B., Saidou M., Esu-Williams E., Lombart J.P., Badombena W., Luo N., Vanden Haesevelde M., Delaporte E. Geographical distribution of HIV-1 group O viruses in Africa (англ.) // AIDS : journal. — 1997. — March (vol. 11, no. 4). — P. 493—498. — doi:10.1097/00002030-199704000-00013. — PMID 9084797.
- ↑ Mourez T, Simon F, Plantier JC. Non-M variants of human immunodeficiency virus type 1. Clin Microbiol Rev. 2013 Jul;26(3):448-61
- ↑ AVERT.org. HIV Strains: Types, Groups and Subtypes (англ.). Дата обращения: 24 июля 2014. Архивировано 24 сентября 2015 года.
- ↑ Julie Yamaguchi, Ruthie Coffey, Ana Vallari, Charlotte Ngansop, Dora Mbanya, Nicaise Ndembi, Lazare Kaptué, Lutz G. Gürtler, Pierre Bodelle, Gerald Schochetman, Sushil G. Devare, Catherine A. Brennan. Identification of HIV Type 1 Group N Infections in a Husband and Wife in Cameroon: Viral Genome Sequences Provide Evidence for Horizontal Transmission (англ.) // AIDS Research and Human Retroviruses : journal. — 2006. — January (vol. 22, no. 1). — P. 83—92. — doi:10.1089/aid.2006.22.83. — PMID 16438650.
- ↑ Plantier J.C., Leoz M., Dickerson J.E., De Oliveira F., Cordonnier F., Lemée V., Damond F., Robertson D.L., Simon F. A new human immunodeficiency virus derived from gorillas (англ.) // Nature Medicine : journal. — 2009. — August (vol. 15, no. 8). — P. 871—872. — doi:10.1038/nm.2016. — PMID 19648927.
- ↑ "New HIV strain discovered". Associated Press. CBC News. 2009-08-03. Архивировано из оригинала 5 августа 2009. Дата обращения: 3 августа 2009.
- ↑ Donald G. McNeil, Jr. (2010-09-16). "Precursor to H.I.V. Was in Monkeys for Millennia". New York Times. Архивировано 11 декабря 2019. Дата обращения: 17 сентября 2010.
But P appears to have crossed over from a gorilla; it was discovered only last year, and in only one woman, who was from Cameroon, where lowland gorillas are hunted for meat.
- ↑ Clavel F., Guétard D., Brun-Vézinet F., Chamaret S., Rey M. A., Santos-Ferreira M. O., Laurent A. G., Dauguet C., Katlama C., Rouzioux C. Isolation of a new human retrovirus from West African patients with AIDS. (англ.) // Science (New York, N.Y.). — 1986. — Vol. 233, no. 4761. — P. 343—346. — PMID 2425430.
- ↑ Guyader M., Emerman M., Sonigo P., Clavel F., Montagnier L., Alizon M. Genome organization and transactivation of the human immunodeficiency virus type 2. (англ.) // Nature. — 1987. — Vol. 326, no. 6114. — P. 662—669. — doi:10.1038/326662a0. — PMID 3031510.
- ↑ HIV-2 Infection Surveillance--United States, 1987-2009. (англ.) // MMWR. Morbidity and mortality weekly report. — 2011. — Vol. 60, no. 29. — P. 985—988. — PMID 21796096. За 12 лет с 1988 по 2010 в США зарегистрированы лишь 242 случая ВИЧ-инфекции
- ↑ Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents (англ.). U.S. Department of Health and Human Services. — «Инфекция ВИЧ-2 эндемична в Западной Африке и имеет лишь ограниченное распространение за пределами этой зоны.» Дата обращения: 21 июля 2014. Архивировано из оригинала 1 декабря 2019 года.
- ↑ Santiago, M. L.; Range, F.; Keele, B. F.; Li, Y.; Bailes, E.; Bibollet-Ruche, F.; Fruteau, C.; Noe, R.; Peeters, M. Simian Immunodeficiency Virus Infection in Free-Ranging Sooty Mangabeys (Cercocebus atys atys) from the Taï Forest, Côte d'Ivoire: Implications for the Origin of Epidemic Human Immunodeficiency Virus Type 2 (англ.) // Journal of Virology : journal. — 2005. — Vol. 79, no. 19. — P. 12515—12527. — doi:10.1128/JVI.79.19.12515-12527.2005. — PMID 16160179. — PMC 1211554.
- ↑ 1 2 Marx P.A., Alcabes P.G., Drucker E. Serial human passage of simian immunodeficiency virus by unsterile injections and the emergence of epidemic human immunodeficiency virus in Africa (англ.) // Philos Trans R Soc Lond B Biol Sci : journal. — 2001. — Vol. 356, no. 1410. — P. 911—920. — doi:10.1098/rstb.2001.0867. — PMID 11405938. — PMC 1088484. Архивировано 29 марта 2016 года.
- ↑ McGovern S.L., Caselli E., Grigorieff N., Shoichet B.K. A common mechanism underlying promiscuous inhibitors from virtual and high-throughput screening (англ.) // Journal of Medical Chemistry : journal. — 2002. — Vol. 45, no. 8. — P. 1712—1722. — doi:10.1021/jm010533y. — PMID 11931626.
- ↑ Compared with overview in: Fisher, Bruce; Harvey, Richard P.; Champe, Pamela C. Lippincott's Illustrated Reviews: Microbiology (Lippincott's Illustrated Reviews Series). — Hagerstown, MD: Lippincott Williams & Wilkins, 2007. — ISBN 0-7817-8215-5. Page 3
- ↑ 1 2 3 4 5 6 Los Alamos National Laboratory. HIV Sequence Compendium 2008. — 2008. Архивировано 24 ноября 2017 года.
- ↑ 1 2 3 Turner B. G., Summers M. F. Structural biology of HIV. (англ.) // Journal of molecular biology. — 1999. — Vol. 285, no. 1. — P. 1—32. — doi:10.1006/jmbi.1998.2354. — PMID 9878383.
- ↑ Pudney J., Song M. J. Electron microscopic analysis of HIV-host cell interactions. (англ.) // Tissue & cell. — 1994. — Vol. 26, no. 4. — P. 539—550. — PMID 8091422.
- ↑ 1 2 Orentas R. J., Hildreth J. E. Association of host cell surface adhesion receptors and other membrane proteins with HIV and SIV. (англ.) // AIDS research and human retroviruses. — 1993. — Vol. 9, no. 11. — P. 1157—1165. — PMID 8312057.
- ↑ Fauci A. S. HIV and AIDS: 20 years of science. (англ.) // Nature medicine. — 2003. — Vol. 9, no. 7. — P. 839—843. — doi:10.1038/nm0703-839. — PMID 12835701.
- ↑ 1 2 3 Guatelli J. C. Interactions of viral protein U (Vpu) with cellular factors. (англ.) // Current topics in microbiology and immunology. — 2009. — Vol. 339. — P. 27—45. — doi:10.1007/978-3-642-02175-6_2. — PMID 20012522.
- ↑ 1 2 3 Nomaguchi M., Fujita M., Adachi A. Role of HIV-1 Vpu protein for virus spread and pathogenesis. (англ.) // Microbes and infection / Institut Pasteur. — 2008. — Vol. 10, no. 9. — P. 960—967. — doi:10.1016/j.micinf.2008.07.006. — PMID 18672082.
- ↑ Malim M. H., Emerman M. HIV-1 accessory proteins--ensuring viral survival in a hostile environment. (англ.) // Cell host & microbe. — 2008. — Vol. 3, no. 6. — P. 388—398. — doi:10.1016/j.chom.2008.04.008. — PMID 18541215.
- ↑ Ho S. K., Coman R. M., Bunger J. C., Rose S. L., O'Brien P., Munoz I., Dunn B. M., Sleasman J. W., Goodenow M. M. Drug-associated changes in amino acid residues in Gag p2, p7(NC), and p6(Gag)/p6(Pol) in human immunodeficiency virus type 1 (HIV-1) display a dominant effect on replicative fitness and drug response. (англ.) // Virology. — 2008. — Vol. 378, no. 2. — P. 272—281. — doi:10.1016/j.virol.2008.05.029. — PMID 18599104.
- ↑ 1 2 Neil S. J., Zang T., Bieniasz P. D. Tetherin inhibits retrovirus release and is antagonized by HIV-1 Vpu. (англ.) // Nature. — 2008. — Vol. 451, no. 7177. — P. 425—430. — doi:10.1038/nature06553. — PMID 18200009.
- ↑ 1 2 Van Damme N., Goff D., Katsura C., Jorgenson R. L., Mitchell R., Johnson M. C., Stephens E. B., Guatelli J. The interferon-induced protein BST-2 restricts HIV-1 release and is downregulated from the cell surface by the viral Vpu protein. (англ.) // Cell host & microbe. — 2008. — Vol. 3, no. 4. — P. 245—252. — doi:10.1016/j.chom.2008.03.001. — PMID 18342597.
- ↑ 1 2 Dubé M., Bego M. G., Paquay C., Cohen A. Modulation of HIV-1-host interaction: role of the Vpu accessory protein. (англ.) // Retrovirology. — 2010. — Vol. 7. — P. 114. — doi:10.1186/1742-4690-7-114. — PMID 21176220.
- ↑ 1 2 Ruiz A., Guatelli J. C., Stephens E. B. The Vpu protein: new concepts in virus release and CD4 down-modulation. (англ.) // Current HIV research. — 2010. — Vol. 8, no. 3. — P. 240—252. — PMID 20201792.
- ↑ 1 2 3 4 5 6 7 Votteler, J. and Schubert, U. (2008) Human Immunodeficiency Viruses: Molecular Biology. Encyclopedia of Virology. (3rd ed.) 517—525
- ↑ Rhodes D. I., Ashton L., Solomon A., Carr A., Cooper D., Kaldor J., Deacon N. Characterization of three nef-defective human immunodeficiency virus type 1 strains associated with long-term nonprogression. Australian Long-Term Nonprogressor Study Group. (англ.) // Journal of virology. — 2000. — Vol. 74, no. 22. — P. 10581—10588. — PMID 11044102.
- ↑ Gorry P. R., McPhee D. A., Verity E., Dyer W. B., Wesselingh S. L., Learmont J., Sullivan J. S., Roche M., Zaunders J. J., Gabuzda D., Crowe S. M., Mills J., Lewin S. R., Brew B. J., Cunningham A. L., Churchill M. J. Pathogenicity and immunogenicity of attenuated, nef-deleted HIV-1 strains in vivo. (англ.) // Retrovirology. — 2007. — Vol. 4. — P. 66. — doi:10.1186/1742-4690-4-66. — PMID 17888184.
- ↑ 1 2 3 Montagnier, Luc. (1999) Human Immunodeficiency Viruses (Retroviridae). Encyclopedia of Virology (2nd Ed.) 763—774
- ↑ 1 2 3 HIV-1 dynamics in vivo: virion clearance rate, infected cell life-span, and viral generation time (англ.). Science. 1996 Mar 15;271(5255):1582-6.. Дата обращения: 23 августа 2014. Архивировано из оригинала 5 марта 2016 года., PMID 8599114
- ↑ 1 2 Coakley E., Petropoulos C. J., Whitcomb J. M. Assessing chemokine co-receptor usage in HIV. (англ.) // Current opinion in infectious diseases. — 2005. — Vol. 18, no. 1. — P. 9—15. — PMID 15647694.
- ↑ Myszka D. G., Sweet R. W., Hensley P., Brigham-Burke M., Kwong P. D., Hendrickson W. A., Wyatt R., Sodroski J., Doyle M. L. Energetics of the HIV gp120-CD4 binding reaction. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2000. — Vol. 97, no. 16. — P. 9026—9031. — PMID 10922058.
- ↑ Wilen CB, Tilton JC, Doms RW. HIV: cell binding and entry. Cold Spring Harb Perspect Med. 2012 Aug 1;2(8)
- ↑ Информация о ВИЧ на сайте NIAID (англ.). Дата обращения: 7 августа 2014. Архивировано 10 сентября 2016 года.
- ↑ Размножение вируса иммунодефицита человека в клетке (недоступная ссылка)
- ↑ 1 2 Патогенез ВИЧ-инфекции. Архивная копия от 24 сентября 2015 на Wayback Machine
- ↑ Levy J.A. HIV and the pathogenesis of AIDS. — p. 110, 111, 160, 161 — USA: American Society for Microbiology, 2007. — ISBN 978-1-55581-393-2
- ↑ 1 2 3 Karn J., Stoltzfus C. M. Transcriptional and posttranscriptional regulation of HIV-1 gene expression. (англ.) // Cold Spring Harbor perspectives in medicine. — 2012. — Vol. 2, no. 2. — P. 006916. — doi:10.1101/cshperspect.a006916. — PMID 22355797.
- ↑ John Hopkins AIDS Servise Жизненный цикл ВИЧ-инфекции Архивная копия от 8 июля 2007 на Wayback Machine
- ↑ Perelson A. S., Neumann A. U., Markowitz M., Leonard J. M., Ho D. D. HIV-1 dynamics in vivo: virion clearance rate, infected cell life-span, and viral generation time. (англ.) // Science (New York, N.Y.). — 1996. — Vol. 271, no. 5255. — P. 1582—1586. — PMID 8599114.
- ↑ Survival outside the body Архивная копия от 29 декабря 2015 на Wayback Machine / HIV transmission & testing, NAM Publications (англ.)
- ↑ ВИЧ-инфекция Под ред. Ю. В. Лобзина, С. С. Козлова, А. Н. Ускова, 2000 год. (недоступная ссылка)
- ↑ Meng G., Wei X., Wu X., Sellers M. T., Decker J. M., Moldoveanu Z., Orenstein J. M., Graham M. F., Kappes J. C., Mestecky J., Shaw G. M., Smith P. D. Primary intestinal epithelial cells selectively transfer R5 HIV-1 to CCR5+ cells. (англ.) // Nature medicine. — 2002. — Vol. 8, no. 2. — P. 150—156. — doi:10.1038/nm0202-150. — PMID 11821899.
- ↑ Burton G. F., Keele B. F., Estes J. D., Thacker T. C., Gartner S. Follicular dendritic cell contributions to HIV pathogenesis. (англ.) // Seminars in immunology. — 2002. — Vol. 14, no. 4. — P. 275—284. — PMID 12163303.
- ↑ Blauvelt A., Asada H., Saville M. W., Klaus-Kovtun V., Altman D. J., Yarchoan R., Katz S. I. Productive infection of dendritic cells by HIV-1 and their ability to capture virus are mediated through separate pathways. (англ.) // The Journal of clinical investigation. — 1997. — Vol. 100, no. 8. — P. 2043—2053. — doi:10.1172/JCI119737. — PMID 9329969.
- ↑ Siliciano RF, Greene WC. «HIV latency». Cold Spring Harb Perspect Med. 2011 Sep;1(1): a007096. doi: 10.1101/cshperspect.a007096
- ↑ Генетический ластик для ВИЧ. Фонд развития межсекторного социального партнёрства. Дата обращения: 21 июля 2014. Архивировано 25 сентября 2020 года.
- ↑ Ye L., Wang J., Beyer A. I., Teque F., Cradick T. J., Qi Z., Chang J. C., Bao G., Muench M. O., Yu J., Levy J. A., Kan Y. W. Seamless modification of wild-type induced pluripotent stem cells to the natural CCR5Δ32 mutation confers resistance to HIV infection. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2014. — Vol. 111, no. 26. — P. 9591—9596. — doi:10.1073/pnas.1407473111. — PMID 24927590.
- ↑ Hu W., Kaminski R., Yang F., Zhang Y., Cosentino L., Li F., Luo B., Alvarez-Carbonell D., Garcia-Mesa Y., Karn J., Mo X., Khalili K. RNA-directed gene editing specifically eradicates latent and prevents new HIV-1 infection. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2014. — Vol. 111, no. 31. — P. 11461—11466. — doi:10.1073/pnas.1405186111. — PMID 25049410.
- ↑ Кирилл Стасевич. Клетки человека избавили от ВИЧ. Наука и жизнь. nkj.ru (25 июля 2014). Дата обращения: 27 июля 2014. Архивировано 8 августа 2020 года.
- ↑ Gao F., Bailes E., Robertson D.L., et al. Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes (англ.) // Nature : journal. — 1999. — Vol. 397, no. 6718. — P. 436—441. — doi:10.1038/17130. — PMID 9989410.
- ↑ Worobey M., Gemmel M., Teuwen D.E., et al. Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960 (англ.) // Nature : journal. — 2008. — October (vol. 455, no. 7213). — P. 661—664. — doi:10.1038/nature07390. — PMID 18833279. Архивировано 16 августа 2010 года.
- ↑ Salemi, M.; Strimmer, K; Hall, WW; Duffy, M; Delaporte, E; Mboup, S; Peeters, M; Vandamme, A.M. Dating the common ancestor of SIVcpz and HIV-1 group M and the origin of HIV-1 subtypes by using a new method to uncover clock-like molecular evolution (англ.) // The FASEB Journal[англ.] : journal. — Federation of American Societies for Experimental Biology[англ.], 2000. — Vol. 15, no. 2. — P. 276—278. — doi:10.1096/fj.00-0449fje. — PMID 11156935.
- ↑ Korber, B.; Muldoon, M; Theiler, J; Gao, F; Gupta, R; Lapedes, A; Hahn, BH; Wolinsky, S; Bhattacharya, T. Timing the Ancestor of the HIV-1 Pandemic Strains (англ.) // Science. — 2000. — Vol. 288, no. 5472. — P. 1789—1796. — doi:10.1126/science.288.5472.1789. — . — PMID 10846155.
- ↑ Worobey M., Gemmel M., Teuwen D.E., et al. Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960 (англ.) // Nature : journal. — 2008. — October (vol. 455, no. 7213). — P. 661—664. — doi:10.1038/nature07390. — . — PMID 18833279.
- ↑ Lenta.ru: Наука и техника: Наука: Учёные определили место и время рождения ВИЧ. Дата обращения: 3 октября 2014. Архивировано 3 октября 2014 года.
- ↑ Gao F., Bailes E., Robertson D.L., et al. Origin of HIV-1 in the chimpanzee Pan troglodytes troglodytes (англ.) // Nature : journal. — 1999. — February (vol. 397, no. 6718). — P. 436—441. — doi:10.1038/17130. — . — PMID 9989410.
- ↑ Keele, B. F., van Heuverswyn, F., Li, Y. Y., Bailes, E., Takehisa, J., Santiago, M. L., Bibollet-Ruche, F., Chen, Y., Wain, L. V., Liegois, F., Loul, S., Mpoudi Ngole, E., Bienvenue, Y., Delaporte, E., Brookfield, J. F. Y., Sharp, P. M., Shaw, G. M., Peeters, M., and Hahn, B. H. Chimpanzee Reservoirs of Pandemic and Nonpandemic HIV-1 (англ.) // Science : journal. — 2006. — 28 July (vol. 313, no. 5786). — P. 523—526. — doi:10.1126/science.1126531. — . — PMID 16728595. — PMC 2442710.
- ↑ Sharp, P. M.; Bailes, E.; Chaudhuri, R. R.; Rodenburg, C. M.; Santiago, M. O.; Hahn, B. H. The origins of acquired immune deficiency syndrome viruses: where and when? (англ.) // Philosophical Transactions of the Royal Society B: Biological Sciences : journal. — 2001. — Vol. 356, no. 1410. — P. 867—876. — doi:10.1098/rstb.2001.0863. — PMID 11405934. — PMC 1088480. Архивировано 25 октября 2007 года. Архивированная копия. Дата обращения: 4 февраля 2012. Архивировано из оригинала 25 октября 2007 года.
- ↑ Reeves, J. D. and Doms, R. W. Human Immunodeficiency Virus Type 2 (англ.) // Journal of General Virology[англ.]. — Microbiology Society[англ.], 2002. — Vol. 83, no. Pt 6. — P. 1253—1265. — doi:10.1099/vir.0.18253-0. — PMID 12029140.
- ↑ Kalish M.L., Wolfe N.D., Ndongmo C.D., McNicholl J., Robbins K.E., et al. Central African hunters exposed to simian immunodeficiency virus (англ.) // Emerg Infect Dis : journal. — 2005. — Vol. 11, no. 12. — P. 1928—1930. — PMID 16485481.
- ↑ Marx P.A., Alcabes P.G., Drucker E. Serial human passage of simian immunodeficiency virus by unsterile injections and the emergence of epidemic human immunodeficiency virus in Africa (англ.) // Philos Trans R Soc Lond B Biol Sci : journal. — 2001. — Vol. 356, no. 1410. — P. 911—920. — doi:10.1098/rstb.2001.0867. — PMID 11405938. — PMC 1088484. Архивировано 17 сентября 2013 года.
- ↑ Worobey, Michael; Gemmel, Marlea; Teuwen, Dirk E.; Haselkorn, Tamara; Kunstman, Kevin; Bunce, Michael; Muyembe, Jean-Jacques; Kabongo, Jean-Marie M.; Kalengayi, Raphaël M. Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960 (англ.) // Nature : journal. — 2008. — Vol. 455, no. 7213. — P. 661—664. — doi:10.1038/nature07390. — . — PMID 18833279. Архивировано 13 января 2012 года. Архивированная копия. Дата обращения: 4 февраля 2012. Архивировано из оригинала 13 января 2012 года.
- ↑ 1 2 Sousa, João Dinis de; Müller, Viktor; Lemey, Philippe; Vandamme, Anne-Mieke; Vandamme, Anne-Mieke. High GUD Incidence in the Early 20th Century Created a Particularly Permissive Time Window for the Origin and Initial Spread of Epidemic HIV Strains (англ.) // PLOS One : journal / Martin, Darren P.. — Public Library of Science, 2010. — Vol. 5, no. 4. — P. e9936. — doi:10.1371/journal.pone.0009936. — PMID 20376191. — PMC 2848574. Архивировано 10 октября 2012 года.
- ↑ Chitnis, Amit; Rawls, Diana; Moore, Jim. Origin of HIV Type 1 in Colonial French Equatorial Africa? (англ.) // AIDS Research and Human Retroviruses : journal. — 2000. — Vol. 16, no. 1. — P. 5—8. — doi:10.1089/088922200309548. — PMID 10628811.
- ↑ Donald G. McNeil, Jr. (2010-09-16). "Precursor to H.I.V. Was in Monkeys for Millennia". New York Times. Архивировано 11 декабря 2019. Дата обращения: 17 сентября 2010.
Dr. Marx believes that the crucial event was the introduction into Africa of millions of inexpensive, mass-produced syringes in the 1950s. ... suspect that the growth of colonial cities is to blame. Before 1910, no Central African town had more than 10,000 people. But urban migration rose, increasing sexual contacts and leading to red-light districts.
- ↑ Zhu, T., Korber, B. T., Nahmias, A. J., Hooper, E., Sharp, P. M. and Ho, D. D. An African HIV-1 Sequence from 1959 and Implications for the Origin of the epidemic (англ.) // Nature : journal. — 1998. — Vol. 391, no. 6667. — P. 594—597. — doi:10.1038/35400. — . — PMID 9468138. Архивировано 27 сентября 2011 года.
- ↑ Kolata, Gina (1987-10-28). "Boy's 1969 Death Suggests AIDS Invaded U.S. Several Times". The New York Times. Архивировано 11 февраля 2009. Дата обращения: 11 февраля 2009.
- ↑ The emergence of HIV/AIDS in the Americas and beyond (англ.). Архивировано из оригинала 28 марта 2012 года.
- ↑ Randy Dotinga. Genetic HIV Resistance Deciphered (англ.). WIRED.com // Condé Nast. Дата обращения: 21 июля 2014. Архивировано 8 февраля 2017 года.
- ↑ Кузнецов, Даниил. Прививка или смерть : [арх. 20 декабря 2018] // Популярная механика : журн.. — 2018. — № 9.
- ↑ Kaur G., Mehra N. Genetic determinants of HIV-1 infection and progression to AIDS: susceptibility to HIV infection. (англ.) // Tissue antigens. — 2009. — Vol. 73, no. 4. — P. 289—301. — doi:10.1111/j.1399-0039.2009.01220.x. — PMID 19317737.
- ↑ Chinen J., Shearer W. T. Molecular virology and immunology of HIV infection. (англ.) // The Journal of allergy and clinical immunology. — 2002. — Vol. 110, no. 2. — P. 189—198. — PMID 12170257.
- ↑ Sheehy AM, Gaddis NC, Choi JD, Malim MH (2002) Isolation of a human gene that inhibits HIV-1 infection and is suppressed by the viral Vif protein. Nature. 2002 Aug 8;418 (6898):646-650.
- ↑ Kaiser, Shariser. Restriction of an Extinct Retrovirus by the Human TRIM5α Antiviral Protein (англ.) // Science : journal. — 2007. — 22 June (vol. 316, no. 5832). — P. 1756—1758. Архивировано 13 июля 2007 года.
- ↑ Sayah D. M., Sokolskaja E., Berthoux L., Luban J. Cyclophilin A retrotransposition into TRIM5 explains owl monkey resistance to HIV-1. (англ.) // Nature. — 2004. — Vol. 430, no. 6999. — P. 569—573. — doi:10.1038/nature02777. — PMID 15243629.
- ↑ 1 2 3 Tokarev A., Skasko M., Fitzpatrick K., Guatelli J. Antiviral activity of the interferon-induced cellular protein BST-2/tetherin. (англ.) // AIDS research and human retroviruses. — 2009. — Vol. 25, no. 12. — P. 1197—1210. — doi:10.1089/aid.2009.0253. — PMID 19929170.
- ↑ Kupzig S., Korolchuk V., Rollason R., Sugden A., Wilde A., Banting G. Bst-2/HM1.24 is a raft-associated apical membrane protein with an unusual topology. (англ.) // Traffic (Copenhagen, Denmark). — 2003. — Vol. 4, no. 10. — P. 694—709. — PMID 12956872.
- ↑ 1 2 Perez-Caballero D., Zang T., Ebrahimi A., McNatt M. W., Gregory D. A., Johnson M. C., Bieniasz P. D. Tetherin inhibits HIV-1 release by directly tethering virions to cells. (англ.) // Cell. — 2009. — Vol. 139, no. 3. — P. 499—511. — doi:10.1016/j.cell.2009.08.039. — PMID 19879838.
- ↑ Douglas J. L., Gustin J. K., Viswanathan K., Mansouri M., Moses A. V., Früh K. The great escape: viral strategies to counter BST-2/tetherin. (англ.) // PLoS pathogens. — 2010. — Vol. 6, no. 5. — P. e1000913. — doi:10.1371/journal.ppat.1000913. — PMID 20485522.
- ↑ Evans D. T., Serra-Moreno R., Singh R. K., Guatelli J. C. BST-2/tetherin: a new component of the innate immune response to enveloped viruses. (англ.) // Trends in microbiology. — 2010. — Vol. 18, no. 9. — P. 388—396. — doi:10.1016/j.tim.2010.06.010. — PMID 20688520.
- ↑ Miyakawa K., Ryo A., Murakami T., Ohba K., Yamaoka S., Fukuda M., Guatelli J., Yamamoto N. BCA2/Rabring7 promotes tetherin-dependent HIV-1 restriction. (англ.) // PLoS pathogens. — 2009. — Vol. 5, no. 12. — P. e1000700. — doi:10.1371/journal.ppat.1000700. — PMID 20019814.
Литература[править | править код]
- ВИЧ 2014/2015
- Санитарные правила СП 3.1.5.2826-10 Профилактика ВИЧ-инфекции
- Методические рекомендации МР 3.1.0087-14 Профилактика заражения ВИЧ
- Леви Д. Э. ВИЧ и патогенез СПИДа / Джей Э. Леви; Пер. 3-го изд. с англ. Е. А. Монастырской; Под ред. Г. А. Игнатьевой ; Лаб. изучения опухолеродных вирусов и вирусов иммунодефицита человека, Мед. отделение и Научно-исслед. институт рака Калифорнийского университета, Мед. шк. Университета Калифорнии, Сан-Франциско, Калифорния. — М.: Научный Мир, 2010. — 736 с. — ISBN 978-5-91522-198-6.
- Малый В. П. ВИЧ/СПИД: (вирус иммунодефицита человека, синдром приобретённого иммунодефицита). — М.: Эксмо, 2009. — 672 с. — (Новейший медицинский справочник). — ISBN 978-5-699-31017-3.
- Покровский В. В. (редактор). ВИЧ-инфекция и СПИД: Национальное руководство. — М.: ГЭОТАР-Медиа, 2013. — 608 с. — ISBN 978-5-9704-2442-1.
- Bushman F.D., Nabel G.J., Swanstrom R. (Editors). HIV: From biology to prevention and treatment. — Cold Spring Harbor, New York, USA: Cold Spring Harbor Laboratory Press, 2012. — 572 с. — ISBN 978-193611340-8.
- Levy J.A. HIV and the pathogenesis of AIDS. — Third edition. — ASM Press, 2007. — 644 с. — ISBN 978-1-55581-393-2.
- Pancino G., Silvestri G., Fowke K. (Editors). Models of protection against HIV/SIV: Avoiding AIDS in humans and monkeys. — UK-USA-Canada: Academic Press, 2012. — 345 с. — ISBN 978-0-12-387715-4.
- Pepin J. The origins of AIDS. — New York, USA: Cambridge University Press, 2011. — 293 с. — ISBN 978-0-52118637-7.
- Prasad V.R., Kalpana G.V. (Editors). HIV protocols. — Humana Press, 2009. — 457 с. — ISBN 978-1-58829-859-1.
- Sax P.E., Cohen C.J., Kuritzkes D.R. (Editors). HIV essentials. — Jones and Bartlett Learning, 2012. — 248 с. — ISBN 978-1-4496-5092-6.
- Spearman P., Freed E.O. (Editors). HIV interactions with host cell proteins. — Springer, 2009. — 204 с. — ISBN 978-3-642-02174-9.
- Weeks B.B., Alcamo I.E. AIDS: The biological basis. — USA - Canada - UK: Jones and Bartlett Publishers, 2010. — 360 с. — ISBN 978-0-7637-6324-4.
Ссылки[править | править код]
- ВИЧ на curlie.org
- Второй в мире пациент полностью излечился от ВИЧ // Вести.ру, 11 марта 2020
Эта статья входит в число хороших статей русскоязычного раздела Википедии. |