Нитрат железа(II)
| Нитрат железа(II) | |
|---|---|
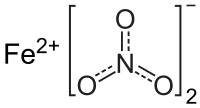 | |
| Общие | |
| Систематическое наименование |
Нитрат железа(II) |
| Хим. формула | FeN2O6 |
| Рац. формула | Fe(NO3)2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | |
| Термические свойства | |
| Температура | |
| • плавления | (гексагидрат) 60,5 °C |
| Классификация | |
| Рег. номер CAS | 14013-86-6 |
| PubChem | 9815404 |
| SMILES | |
| InChI | |
| ChemSpider | 7991154 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Нитрáт желéза(II) — соль азотной кислоты и двухвалентного железа.
Физические свойства[править | править код]
 |
Нитрат железа(II) существует в основном в виде кристаллогидратов Fe(NO3)2·6H2O и Fe(NO3)2·9H2O.
Гексагидрат нитрата железа(II) Fe(NO3)2·6H2O — светло-зелёные кристаллы с ромбической кристаллической решеткой. Хорошо растворяется в воде, причем растворимость растёт вместе с повышением температуры. В равновесии с насыщенным водным раствором существует в интервале от −12 до 60,5 °C и концентрации раствора в пределах 39—69,5 %. При более низких температурах и концентрациях растворов устойчив нонагидрат нитрата железа(II) Fe(NO3)2·9H2O.
График растворимости представлен на рисунке.
Особые точки:
| Состояние | Температура, °С | Концентрация, % |
| Лёд + Fe(NO3)2·9H2O | −28 | (35) |
| Fe(NO3)2·9H2O + Fe(NO3)2·6H2O | ~(−12) | (39) |
| Fe(NO3)2·6H2O | 60,5 | 62,5 |
Безводный нитрат железа(II) и его кристаллогидраты неустойчивы, поэтому легко окисляются на воздухе.
Получение[править | править код]
Нитрат железа(II) образуется при растворении железа в разбавленной азотной кислоте на холоде:
В чистом состоянии его лучше получать обменной реакцией сульфата железа(II) с нитратом свинца(II):
Химические свойства[править | править код]
Проявляет восстановительные свойства. Гидролиз практически не проявляется.
- Водный раствор нитрата железа(II) разлагается при кипячении с образованием основного нитрата железа(III):
- Реагирует с щелочами с образованием гидроксида железа(II):
- С растворимыми карбонатами дает белый карбонат железа(II):
- Восстанавливается до металлического железа при действии более активного металла (см. Электрохимический ряд активности металлов):
- Взаимодействует с гексацианоферратом(III) калия (красной кровяной солью) с образованием тёмно-синего осадка гексацианоферрата(II) железа(III)-калия (берлинская лазурь):
- При термическом разложении образуется оксид железа(III), а не оксид железа(II):
Литература[править | править код]
- Волков А.И., Жарский И.М. Большой химический справочник / А.И.Волков, И.М.Жарский. - Мн.: Современная школа, 2005. - 608 с.
- Г.Реми. Курс неорганической химии. 2 том - М.: Издательство иностранной литературы, 1963. - 920 с.
- Киргинцев А.Н., Трушникова Л.Н., Лаврентьева В.Г. Растворимость неорганических веществ в воде. Справочник. Изд-во "Химия", Л., 1972, стр. 248, табл. 87, рис. 589.
- Гринвуд Н. Химия элементов: в 2 томах. / Н.Гринвуд, А.Эрншо; пер. с англ. - М.: БИНОМ. Лаборатория знаний, 2011. - (Лучший зарубежный учебник)
- Химическая технология неорганических веществ: В 2 кн. Кн. 2. Учебное пособие/Т.Г. Ахметов, Р.Т. Порфирьева, Л.Г. Гайсин и др.; Под ред. Т.Г. Ахметова. - М.: Высш. шк., 2002 - 688 с.: ил.
В статье не хватает ссылок на источники (см. рекомендации по поиску). |







![{\displaystyle {\mathsf {Fe(NO_{3})_{2}+K_{3}[Fe(CN)_{6}]\ \rightarrow \ KFe[Fe(CN)_{6}]\downarrow +2KNO_{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a80afb1ff22749afcc38d3ba8d5df8dc2b8dcedf)

